Påvisning av nøytraliseringsfølsomme epitoper i antigener vist på viruslignende partikkelbaserte vaksiner ved hjelp av en fangstanalyse
Summary
Her presenterer vi en protokoll for å oppdage nøytraliseringsepiller på antigen-viser viruslignende partikler (VLPer). Immunoprecipitation av det humane immunsviktviruset (HIV)-avledede VLPer utføres ved hjelp av konvoluttglykoproteiner-spesifikke monoklonale antistoffer kombinert med protein G-konjugerte magnetiske perler. Fangede VLPer blir deretter utsatt for SDS-PAGE og vestlig blot-analyse ved hjelp av viral kjerneprotein Gag-spesifikke antistoffer.
Abstract
Den viruslignende partikkelen (VLP) fangeanalyse er en immunoprecipitation metode, kjent som en ‘pull-down analyse’ som brukes til å rense og isolere antigen-displaying VLPs. Overflate antigen-spesifikke antistoffer er koblet til, og dermed immobilisert på en solid og uoppløselig matrise som perler. På grunn av deres høye affinitet til målantigenet, kan disse antistoffene fange VLPer dekorert med konjakkantigenet forankret i membrankonvolutten til VLPene. Denne protokollen beskriver bindingen av antigenspesifikke antistoffer mot protein A- eller G-konjugede magnetiske perler. I vår studie undersøkes humant immunsviktvirus (HIV)-avledede VLPer dannet av det gruppespesifikke antigenet (Gag) viral kjerneforløperprotein p55 Gag og viser konvoluttglykoproteinene (Env) av HIV. VIP-ene fanges opp ved hjelp av bredt nøytraliserende antistoffer (bNAbs) rettet mot nøytraliseringsfølsomme epitoper i Env. VLP-fangstanalysen som er skissert her representerer en sensitiv og lett å utføre metode for å demonstrere at (i) VLPene er dekorert med det respektive målantigenet, (ii) overflateantigenet beholdt sin strukturelle integritet som demonstrert ved epitopspesifikk binding av bNAbs som brukes i analysen og (iii) den strukturelle integriteten til VLPene avslørt ved påvisning av Gag-proteiner i en påfølgende vestlig blotanalyse. Følgelig letter bruken av bNAbs for immunoprecipitation en prediksjon av om VLP-vaksiner vil kunne fremkalle en nøytraliserende B-cellerespons hos vaksinerte mennesker. Vi forventer at denne protokollen vil gi andre forskere en verdifull og grei eksperimentell tilnærming for å undersøke potensielle VLP-baserte vaksiner.
Introduction
Viruslignende partikler (VLPer) ligner den opprinnelige viruspartikkelstrukturen mens de mangler viral genom, og gir dermed en høy sikkerhetsprofil1,2. VIP-er representerer en individuell klasse vaksiner som i økende grad utvikles på grunn av deres høye immunogenisitet3,4,5,6,7. Dette er spesielt tilfelle for membran-innhyllede VLPer, noe som gjør det mulig å vise ikke bare homologe virale overflateantigener, men også heterologe antigener som tumorantigener8,9,10. Figur 1 gir en eksemplarisk oversikt over strukturen til en innhyllet antigen-dekorert VLP. Under utviklingsprosessen av VLP-baserte vaksiner er analyser uunnværlige, noe som muliggjør analyse av det respektive målantigenet som vises på VLP-overflaten. Slike analyser bør være medvirkende til å belyse sammensetningen av en partikkelvaksine: (i) Er VLPene dekorert med det respektive overflateantigenet? (ii) Har overflateantigenet beholdt sin opprinnelige struktur som demonstrert ved epitopgjenkjenning av nøytraliserende antistoffer (bNAbs) og (iii) kan VLPs strukturelle integritet bekreftes på grunn av påvisning av det virale proteinmedierende VLP-formasjonen?
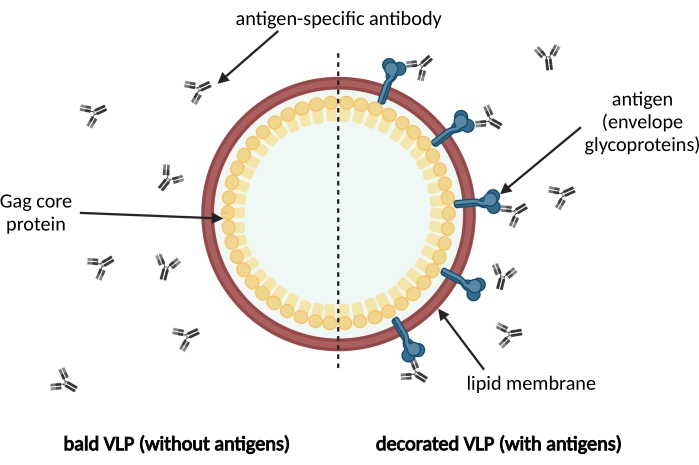
Figur 1: Skjematisk illustrasjon av en membran-innhylset VLP. VLPer dannes av umodne forløper Gag kjerneproteiner og er omgitt av en lipidmembran avledet fra vertscellen. Antigenene, for eksempel konvoluttglykoproteiner, er innlemmet i lipidmembranen og vises på overflaten av VLP (til høyre). Antigenspesifikke antistoffer gjenkjenner antigenet. Til venstre vises en skallet VLP uten antigendekorasjon. Klikk her for å se en større versjon av denne figuren.
Spesielt VLPer dannet av viral gruppespesifikk antigen (Gag) kjerneforløperprotein p55 av human immunsviktvirus type 1 (HIV-1) er foretrukne stillaser for antigenvisning i vaksineutvikling som mange antistoffer, og ELISA-sett er tilgjengelige, noe som muliggjør kvantifisering av disse VLPene11,12. HIV-1-konvoluttglykoproteinene (Env), nemlig transmembranproteinet gp41 (gp41-TM) og den oppløselige overflateenheten gp120 (gp120-SU) som danner heterodimere, er innlemmet i membrankonvolutten av partikler og er avgjørende målantigener for utvikling av vaksiner mot HIV-infeksjon13,14,15 . Visning av nøytraliseringsfølsomme epitoper i disse målantigenene er en forutsetning for å fremkalle en bredt nøytraliserende antistoffrespons hos vaksiner. Foruten en T-cellerespons rettet mot Gag-proteinene, regnes dette som en viktig korrelasjon av beskyttelse mot HIV-infeksjon16. Følgelig, og ved design og produksjon av VIP-er dekorert med målantigenkandidater, representerer den påfølgende analysen av kvaliteten på de viste antigenene et kritisk skritt i prosessen med vaksineutvikling.
Immunoprecipitation (IP) er en mye brukt teknikk for påvisning av proteinproteininteraksjoner og rensing av proteinkomplekser i liten skala17. Barret et al. først rapportert om utviklingen av IP i 1960, men denne metoden har blitt stadig ytterligere forbedret. IP muliggjør fangst og isolering av et målantigen (byttedyr) fra en løsning ved å bruke et antigenspesifikt antistoff (agn) immobilisert ved kobling til perler18,19. I denne protokollen demonstrerer vi en variasjon av den klassiske IP-applikasjonen ved hjelp av membrankonvolverte p55 Gag-dannede VLPer som byttedyr og bNAbs som gjenkjenner nøytraliseringsfølsomme epitoper i konvoluttproteinene som vises på overflaten av VLPene som agnproteiner. Den vellykkede anvendelsen av denne VLP-fangstanalysen letter forutsigelsen av om de testede antigenpositive VIP-ene vil kunne fremkalle en nøytraliserende B-cellerespons hos vaksinerte mennesker. Slike immunogene egenskaper hos VLP-baserte vaksinekandidater blir ofte demonstrert i små dyremodeller20,21,22.
For å vurdere kvaliteten på den nyutviklede VLP-vaksinekandidaten har VLP-fangstanalyser blitt brukt med hell5,23,24. Antallet publiserte metoder er imidlertid begrenset. VLP-fangstanalysen som presenteres her starter med immobilisering av Env-spesifikke bNAbs på protein G-konjugerte perler, som binder seg til Fc-regionen av pattedyr-avledede antistoffer. Typiske matriser for immobilisering av det valgte antistoffet er agarose eller magnetiske perler. Magnetiske perler er imidlertid gunstige for bruksområder med høy gjennomstrømning25. I neste trinn fanges VLPer som viser målantigenet av bNAb-belagte perler. De dannede immunkompleksene som består av Env-positive VIP-er og immobiliserte bNAbs, er lett beriket ved hjelp av en magnet. De isolerte immunkompleksene blir unngått i det siste trinnet. Deretter kan VLPene karakteriseres biokjemisk. Her utførte vi vestlig blotanalyse ved hjelp av p55 Gag virale kjerneproteinspesifikke antistoffer for å demonstrere at det utfelte målet Env antigener ikke bare inneholdt nøytraliseringsfølsomme epitoper, men ble også vist på Gag-dannede VLPer. Videre øker påvisning av viral kjerne Gag-proteiner følsomheten til fangstanalysen siden Gag-proteiner er mer rikelig enn Env i en VLP. I HIV-1 er Env-proteiner bare til stede på et enkelt- eller tosifret tall26, mens mer enn 3500 Gag-molekyler utgjør kjernen i en partikkel27.
Sammenlignet med andre teknikker for undersøkelse av proteinproteininteraksjoner28,29, gir VLP-fangstanalysen en alternativ metode for forskningslaboratorier som ikke har tilgang til dyre analytiske instrumenter. For eksempel kan transmisjonselektronmikroskopianalyse (TEM), overflateplasmonresonansspektroskopi (SPR) og nanopartikkelsporingsanalyse (NTA) være kostnadskrevende. Fangstanalysen som presenteres her, tillater også senere subjeksjon av fanget antigenpositive VLP-prøver for ytterligere proteinkarakterisering, for eksempel ved bruk av henholdsvis geleelektroforese, immunoblotting, elektronmikroskopi og massespektrometri (MS). Tatt i betraktning at den opprinnelige strukturen til målantigenet er bevart under VLP-fangstanalysen, kan også ytelsen til en innfødt SIDE og påfølgende immunoblottingsteknikker brukes.
VLP-fangstanalysen representerer en brukervennlig og sensitiv metode for å undersøke dekorasjonen av VIP-er med målantigener som eksponerer nøytraliseringsfølsomme epitoper, og dermed deres nytte som fremtidige vaksinekandidater.
Protocol
Representative Results
Discussion
Før VLP-fangstanalysen evaluerer du dannelsen av VIP-er og uttrykket for målantigenet i VLP-produsentens cellelinjer. Instrumentelle metoder er strømningscytometrisk analyse av celleoverflateuttrykket til antigenet, samt antigen- og viral kjerneproteinspesifikk ELISA av CFSN og pelleterte VLPer.
Kritiske trinn i VLP-fangstanalysen er belegget av perlene med fangstantistoffer – her bNAbs – og den påfølgende fangsten av de antigenpositive VLPene av de antistoffbelagte perlene. Vellykket belegg av perlene med antistoffer avhenger av valget av det konjugede immunglobulin (Ig)-bindende proteinet. Donorartene så vel som Ig-klassen av antistoffene bestemmer om protein G- eller protein A-konjuged perler er å foretrekke. For de fleste arter og Ig-klasser er protein G den første av valg33. Som et alternativ til protein A / G-konjugerte perler, er streptavidinperler for belegget med biotinylerte antistoffer tilgjengelige. Perler kan også kombineres med antistoffer.
Fangsten av VLP-ene ved antistoffbelagte perler avhenger av grundig blanding, tilstrekkelig inkubasjonstid, antigenoverflod og affinitet av fangstantistoffet. Vår erfaring er at grundig blanding av de antistoffbelagte perlene med VLP-prøvene best oppnås ved bruk av volumer >500 μL i 1,5 ml rør under rotasjon i minst 2 timer ved romtemperatur eller 4 °C. Et annet potensielt hinder er den for lave mengden VLPer i utvalget. For antistoffer som sterkt binder målantigenet, tillater VLP-innganger så lave som 15 ng Gag-protein vanligvis lett påvisbare mengder av de virale kjerneproteinene som bruker vestlig blotanalyse. Imidlertid krever lavaffinitetsantistoffer høyere inngangsmengder, for eksempel 100 ng Gag-protein, for å oppnå avgjørende resultater (figur 3, bNAb 3).
Noen overflateantigener er utsatt for protease nedbrytning. Her anbefaler vi tilsetning av proteasehemmere til VLP-prøvene og inkubasjon ved 4 °C. Ikke-spesifikk vedheft av vertscelleproteiner og VIP-er til perlebundne antistoffer observeres sjelden og bør utelukkes ved å bruke passende negative kontroller, som vi demonstrerte her ved hjelp av mock og skallede VLP-prøver og isotype kontrollantistoffer. Strategier for å redusere ikke-spesifikk binding inkluderer utvidede vasketrinn og tilsetning av kasein i vaskebufferen34. Videre kan fangstanalysen også forbedres ved å bestemme det optimale forholdet mellom antistoff og antigenvisning av VLP-mengde.
I det siste trinnet i VLP-fangstanalysen beskriver vi elution av immunkompleksene fra perlene ved å koke i å redusere Laemmli-bufferen. I løpet av dette trinnet demonteres VIP-ene, og fangstantistoffene og målantigenene skilles fra perlene. Spesielt må donorartene til det primære antistoffet som brukes i den påfølgende vestlige blotanalysen avvike fra donoren til fangstantistoffet for å unngå utilsiktet deteksjon av fangstantistoffet av sekundær anti-donor IgG HRP-konjugede antistoffer.
VLP-fangstanalysen som presenteres her, gir en brukervennlig og sensitiv metode for å oppdage nøytraliseringsfølsomme epitoper i strukturelle intakte målantigener som vises på VLP-overflater. Fangstanalysen muliggjør imidlertid ikke direkte epitop-kvantifisering. ELISA utført med bNAbs er medvirkende til dette formålet og bør gjennomføres parallelt, spesielt hvis undersøkte VLPer er ment å brukes i prekliniske studier som benytter dyremodeller35. Dette er avgjørende, da mengden antigen direkte kan korrelere med fremkalling av en nøytraliserende antistoffrespons hos immuniserte dyr, som vist for porcin circovirus type 2 (PCV2) vaksiner36.
En ideell vaksine bør resultere i fremføring av bNAbs rettet mot nøytraliseringsfølsomme epitoper på virionoverflaten. Analysen av disse epitopene, spesielt med henvisning til deres fulle strukturelle integritet på partikkelvaksineoverflaten, er avgjørende for å identifisere potensielle vaksinekandidater. Dette er ikke bare tilfelle for HIV-avledede VIP-er, men også for mange andre VLP-vaksiner i utvikling37. Fremtredende VLP-baserte vaksiner er for eksempel avledet fra ikke-innkapslede eller kapslede foreldrevirus som humant papillomavirus (HPV). I motsetning til HIV-1-partikler, som dannes av bare ett strukturelt kjerneprotein, nemlig p55 Gag, og omsluttet av membranen som stammer fra VLP-produsentcellen, består HPV-partikler av bare ett eller to strukturelle kjerneproteiner38,39. På samme måte og som presentert her for innkapslede VIP-er, kan VLP-fangstanalysen også gjelde for påvisning av nøytraliseringssensitive epitoper av ikke-innkapslede VIP-er.
Som et alternativ til fangstanalysen kan VLP-prøver direkte bli utsatt for innfødt SIDE etterfulgt av vestlig blotanalyse ved hjelp av bNAbs og passende sekundære antistoffer koblet til HRP40. Men og for analyse av HIV Env-dekorerte VIP-er er denne analysen mindre følsom, da bare et lavt antall antigenproteiner per VLP kan forventes. I motsetning til dette letter fangstanalysen deteksjonen av kjerneproteinene rikelig i store mengder per VLP, når det gjelder HIV-avledede VLPer, danner mer enn 3500 Gag-proteiner en VLP27. Dette muliggjør svært sensitiv indirekte deteksjon av epitoper i Env som vises selv ved lave tettheter på VIP-er.
Antallet veletablerte metoder for å undersøke nøytraliseringsfølsomme epitoper i overflateantigener av VLPer er begrenset. Merking av antigenene som vises på VLPene er mulig med epitopspesifikke antistoff-fluoroforkonjugater og påfølgende deteksjon ved nanopartikkelsporingsanalyse (NTA), noe som muliggjør deteksjon og kvantifisering av VLPer. Denne metoden er også vellykket utviklet og optimalisert for eksosomer som presenterer celleoverflatemarkører41. Også overflateplasmon resonans (SPR) spektroskopi gjør det mulig å analysere interaksjoner mellom ukonjugerte nøytraliserende antistoffer og cognate epitoper presentert på VLPs. Selv om de ikke er egnet for høyere gjennomstrømningsanalyse, kan VIP-er også merkes med bNAbs koblet til gullpartikler og påfølgende transmisjonselektronmikroskopisk (TEM)-undersøkelse42.
Til slutt gir VLP-fangstanalysen noen betydelige fordeler: (i) Vurdering av nøytraliseringsfølsomme epitoper på overflaten av VIP-er, (ii) sensitiv og indirekte deteksjon av antigener selv når den vises ved lave tettheter på VIP-er, og (iii) metoden krever ikke kostnadsintensivt analytisk utstyr.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av et stipend fra det tyske føderale utdannings- og forskningsdepartementet, finansieringsprogrammet Forschung an Fachhochschulen, kontraktsnummer 13FH767IA6 og 13FH242PX6 til JS. Figur 1 og 2 ble opprettet med BioRender.com.
Materials
| 1.5 mL reaction tubes | Eppendorf | ||
| 10x PBS | gibco | 70011044 | |
| 4%–15% Mini-PROTEAN TGX stain-free protein gels | BioRad | 4568085 | |
| Antibodies (bnAbs) | Polymun Scientic | ||
| Isotype control antibody | invitrogen (Thermo Fisher Scientific) | 02-7102 | |
| Chemidoc XRS+ imaging system | BioRad | 1708265 | |
| Chicken anti-rabbit IgG HRP-coupled | Life technologies | A15987 | 1:5000 in TBS-T + 2 % (w/v) powdered milk |
| Dynabeads Protein G Immunoprecipitation Kit | invitrogen (Thermo Fisher Scientific) | 10007D | includes buffers and washing solutions |
| FreeStyle 293-F cells | invitrogen (Thermo Fisher Scientific) | R790-07 | |
| FreeStyle 293 Expression Medium | invitrogen (Thermo Fisher Scientific) | 12338026 | |
| Gel blotting papers | Whatman | GB005 | |
| Glycine | Carl Roth | 0079 | blotting buffer |
| Magnetic separation rack | New England Biolabs | S1509S | for 12 x 1.5 mL or 6 x 1.5 mL tubes |
| Methanol | Carl Roth | 4627 | blotting buffer |
| Mini-PROTEAN Tetra Cell electrophoresis system | BioRad | ||
| Optima XE-90 ultracentrifuge | Beckman Coulter | ||
| PageRuler prestained protein ladder | Thermo Scientific | 26616 | |
| Polyvinylidene fluoride (PVDF) syringe filters, 0.45 µm | Carl Roth | KC89.1 | |
| Powdered milk | Carl Roth | T145 | blocking buffer |
| PVDF transfermembrane, 0.45 µm | Carl Roth | T830.1 | |
| QuickTiter HIV p24 ELISA | Cell Biolabs | VPK-108-H | |
| Rabbit polyclonal to HIV1 p55 + p24 + p17 | abcam | ab63917 | 1:2000 in TBS-T + 2 % (w/v) powdered milk |
| Rotator | Heidolph | REAX2 | |
| ROTI Load 1 (laemmli buffer) | Carl Roth | K929.1 | 4x concentrated reducing protein gel loading buffer |
| ROTIPHORESE 10x SDS-PAGE | Carl Roth | 3060 | |
| Sodium chloride | Carl Roth | 3957 | TBS-T buffer |
| SuperSignal West Pico PLUS chemiluminescent substrate | Thermo Scientific | 34579 | |
| SW28 rotor | Beckman Coulter | ||
| Thermomixer | Cel Media | basic | |
| Trans-Blot Turbo | BioRad | ||
| Trehalose dihydrate | Carl Roth | 8897.2 | |
| TRIS | Carl Roth | 5429 | blotting buffer |
| TRIS hydrochloride | Carl Roth | 9090 | TBS-T buffer |
| Tween-20 | Carl Roth | 9127 | TBS-T buffer |
| Ultra Clear centrifuge tubes | Beckman Coulter | 344058 |
References
- Roldão, A., Mellado, M. C. M., Castilho, L. R., Carrondo, M. J. T., Alves, P. M. Virus-like particles in vaccine development. Expert Review of Vaccines. 9 (10), 1149-1176 (2010).
- Noad, R., Roy, P. Virus-like particles as immunogens. Trends in Microbiology. 11 (9), 438-444 (2003).
- Qian, C., et al. Recent progress on the versatility of virus-like particles. Vaccines. 8 (1), 139 (2020).
- Zabel, F., Kündig, T. M., Bachmann, M. F. Virus-induced humoral immunity: On how B cell responses are initiated. Current Opinion in Virology. 3 (3), 357-362 (2013).
- Garg, H., Mehmetoglu-Gurbuz, T., Joshi, A. Virus Like Particles (VLP) as multivalent vaccine candidate against Chikungunya, Japanese Encephalitis, Yellow Fever and Zika Virus. Scientific Reports. 10 (1), 4017 (2020).
- Hodgins, B., Pillet, S., Landry, N., Ward, B. J. A plant-derived VLP influenza vaccine elicits a balanced immune response even in very old mice with co-morbidities. PLoS ONE. 14 (1), 0210009 (2019).
- Lai, C. C., et al. Process development for pandemic influenza VLP vaccine production using a baculovirus expression system. Journal of Biological Engineering. 13, 78 (2019).
- Caldeira, J. C., Perrine, M., Pericle, F., Cavallo, F. Virus-like particles as an immunogenic platform for cancer vaccines. Viruses. 12 (5), 488 (2020).
- Nika, L., et al. An HER2-displaying virus-like particle vaccine protects from challenge with mammary carcinoma cells in a mouse model. Vaccines. 7 (2), 41 (2019).
- Mohsen, M. O., Zha, L., Cabral-Miranda, G., Bachmann, M. F. Major findings and recent advances in virus-like particle (VLP)-based vaccines. Seminars in Immunology. 34, 123-132 (2017).
- Fontana, D., Garay, E., Cevera, L., Kratje, R., Prieto, C., Gòdia, F. Chimeric VLPs based on hiv-1 gag and a fusion rabies glycoprotein induce specific antibodies against rabies and foot-and-mouth disease virus. Vaccines. 9 (3), 251 (2021).
- Cervera, L., et al. Production of HIV-1-based virus-like particles for vaccination: achievements and limits. Applied Microbiology and Biotechnology. 103 (18), 7367-7384 (2019).
- Gonelli, C. A., King, H. A. D., Mackenzie, C., Sonza, S., Center, R. J., Purcell, D. F. J. Immunogenicity of HIV-1-based virus-like particles with increased incorporation and stability of membrane-bound env. Vaccines. 9 (3), 1-36 (2021).
- Trkola, A. HIV not as simple as one, two, three. Nature. 568, 321-322 (2019).
- Berman, P. W., et al. Protection of chimpanzees from infection by HIV-1 after vaccination with recombinant glycoprotein gp120 but not gp160. Nature. 345 (6276), 622-625 (1990).
- Barouch, D. H. Challenges in the development of an HIV-1 vaccine. Nature. 455 (7213), 613-619 (2008).
- DeCaprio, J., Kohl, T. O. Immunoprecipitation. Cold Spring Harbor Protocols. 2020 (11), 449-461 (2020).
- Barret, B., Wood, P. A., Volwiler, W. Quantitation of gamma globulins in human serum by immunoprecipitation. Journal of Laboratory and Clinical Medicine. 55, 605-615 (1960).
- Kaboord, B., Perr, M. Isolation of proteins and protein complexes by immunoprecipitation. Methods in Molecular Biology. 424, 349-364 (2008).
- Lee, S. H., Chu, K. B., Kang, H. J., Quan, F. S. Virus-like particles containing multiple antigenic proteins of Toxoplasma gondii induce memory T cell and B cell responses. PLoS ONE. 14 (8), 0220865 (2019).
- Lee, Y. T., et al. Intranasal vaccination with M2e5x virus-like particles induces humoral and cellular immune responses conferring cross-protection against heterosubtypic influenza viruses. PLoS ONE. 13 (1), 0190868 (2018).
- Wang, J., et al. Large-scale manufacture of VP2 VLP vaccine against porcine parvovirus in Escherichia coli with high-density fermentation. Applied Microbiology and Biotechnology. 104 (9), 3847-3857 (2020).
- Swenson, D. L., et al. Generation of Marburg virus-like particles by co-expression of glycoprotein and matrix protein. FEMS Immunology and Medical Microbiology. 40 (1), 27-31 (2004).
- Latham, T., Galarza, J. M. Formation of wild-type and chimeric influenza virus-like particles following simultaneous expression of only four structural proteins. Journal of Virology. 75 (13), 6154-6165 (2001).
- Doyle, J., Ray, M., Ouyang, A., Benton, B., Bell, P. A. Abstract 4877: High throughput proteomic applications using protein A/G magnetic beads. Association for Cancer Research (AACR) 102nd Annual Meeting. 20, 4877 (2011).
- Zhu, P., et al. Electron tomography analysis of envelope glycoprotein trimers on HIV and simian immunodeficiency virus virions. Proceedings of the National Academy of Sciences of the United States of America. 100 (26), 15812-15817 (2003).
- Lavado-García, J., Jorge, I., Boix-Besora, A., Vázquez, J., Gòdia, F., Cervera, L. Characterization of HIV-1 virus-like particles and determination of Gag stoichiometry for different production platforms. Biotechnology and Bioengineering. 118 (7), 2660-2675 (2021).
- Miura, K. An overview of current methods to confirm protein-protein interactions. Protein & Peptide Letters. 25 (8), 728-733 (2018).
- Rao, V. S., Srinivas, K., Sujini, G. N., Kumar, G. N. Advances in molecular techniques to study diversity. Plant Biotechnology, Volume 1: Principles, Techniques, and Applications. , 341-365 (2017).
- Rosengarten, J. F., Schatz, S., Wolf, T., Barbe, S., Stitz, J. Components of a HIV-1 vaccine mediate virus-like particle (VLP)-formation and display of envelope proteins exposing broadly neutralizing epitopes. Virology. , 41-48 (2022).
- JoVE, Grundlegende Methoden in der Zell- und Molekularbiologie. Separating Protein with SDS-PAGE. JoVE Science Education Database. , (2021).
- Eslami, A., Lujan, J. Western blotting: sample preparation to detection. Journal of Visualized Experiments: JoVE. (44), e2359 (2010).
- Sheng, S., Kong, F. Separation of antigens and antibodies by immunoaffinity chromatography. Pharmaceutical Biology. 50 (8), 1038-1044 (2012).
- Guzzo, C., et al. Virion incorporation of integrin 47 facilitates HIV-1 infection and intestinal homing. Science Immunology. 2 (11), (2017).
- Wei, M., et al. Bacteria expressed hepatitis E virus capsid proteins maintain virion-like epitopes. Vaccine. 32 (24), 2859-2865 (2014).
- Jin, J., Park, C., Cho, S. H., Chung, J. The level of decoy epitope in PCV2 vaccine affects the neutralizing activity of sera in the immunized animals. Biochemical and Biophysical Research Communications. 496 (3), 846-851 (2018).
- Zhang, X., et al. Lessons learned from successful human vaccines: Delineating key epitopes by dissecting the capsid proteins. Human Vaccines and Immunotherapeutics. 11 (5), 1277-1292 (2015).
- DiGiuseppe, S., Bienkowska-Haba, M., Guion, L. G. M., Keiffer, T. R., Sapp, M. Human papillomavirus major capsid protein L1 remains associated with the incoming viral genome throughout the entry process. Journal of Virology. 91 (16), 00537 (2017).
- Wang, J. W., Roden, R. B. S. L2, the minor capsid protein of papillomavirus. Virology. 445 (1-2), 175-186 (2013).
- Binley, J. M., et al. Profiling the specificity of neutralizing antibodies in a large panel of plasmas from patients chronically infected with human immunodeficiency virus type 1 subtypes B and C. Journal of Virology. 82 (23), 11651-11668 (2008).
- Thane, K. E., Davis, A. M., Hoffman, A. M. Improved methods for fluorescent labeling and detection of single extracellular vesicles using nanoparticle tracking analysis. Scientific Reports. 9 (1), 12295 (2019).
- Mulder, A. M., et al. Toolbox for non-intrusive structural and functional analysis of recombinant VLP based vaccines: A case study with hepatitis B vaccine. PLoS ONE. 7 (4), 0033235 (2012).

