Dypvev tre-foton fluorescens mikroskopi i intakt mus og sebrafisk hjerne
Summary
Tre-foton mikroskopi muliggjør fluorescensavbildning med høy kontrast dypt i levende biologisk vev, som mus- og sebrafiskhjerner, med høy romlig oppløsning.
Abstract
Multifotonmikroskopiteknikker, for eksempel tofotonmikroskopi (14:00) og trefotonmikroskopi (15:00), er kraftige verktøy for dypvevs in vivo-avbildning med subcellulær oppløsning. 15:00 har to store fordeler for dypvevsavbildning over 14:00 som har blitt mye brukt i biologilaboratorier: (i) lengre dempingslengde i spredningsvev ved å bruke ~ 1300 nm eller ~ 1700 nm eksitasjonslaser; (ii) mindre bakgrunnsfluorescensgenerering på grunn av høyere ordens ikke-lineær eksitasjon. Som et resultat tillater 15:00 strukturell og funksjonell avbildning med høy kontrast dypt inne i spredningsvev som intakt musehjerne fra kortikale lag til hippocampus og hele forebrain av voksen sebrafisk.
I dag er laserkilder som er egnet for 15:00 kommersielt tilgjengelige, noe som muliggjør konvertering av et eksisterende to-foton (2P) bildebehandlingssystem til et tre-foton (3P) system. I tillegg er flere kommersielle 3P-mikroskoper tilgjengelige, noe som gjør denne teknikken lett tilgjengelig for biologiforskningslaboratorier. Dette dokumentet viser optimaliseringen av et typisk 3PM-oppsett, spesielt rettet mot biologigrupper som allerede har et 2P-oppsett, og demonstrerer intravital 3D-avbildning i intakt mus og voksne sebrafiskhjerner. Denne protokollen dekker den fullstendige eksperimentelle prosedyren for 3P-avbildning, inkludert mikroskopjustering, prechirping av ~ 1300 og ~ 1700 nm laserpulser, dyreforberedelse og intravital 3P fluorescensavbildning dypt i voksne sebrafisk og musehjerner.
Introduction
I life science har multifotonmikroskopiteknikker (MPM), som 14:00 og 15:00, vært kraftige verktøy for dyp in vivo-avbildning med høy romlig oppløsning og høy kontrast i spredningsvev. I tillegg forårsaker disse metodene mindre fotobleaching sammenlignet med en-foton konfikal mikroskopi 1,2,3,4. 15:00 er fordelaktig for dypere vevsavbildning sammenlignet med 14:00 på grunn av to hovedtrekk: (i) ansettelse av lengre bølgelengdeeksitasjon (~ 1300 nm eller ~ 1700 nm) reduserer vevsspredning, og (ii) eksitasjonsprosessen med høyere rekkefølge (dvs. fluorescenssignalet avhenger av kuben til eksitasjonskraften i 15:00 i stedet for kvadratet av eksitasjonskraften i 14:00) som undertrykker uønsket bakgrunnsfluorescens3 . Følgelig muliggjør 3PM høykontrastavbildning i dypere områder i levende vev som hippocampus i en intakt voksen musehjerne 3,5,6,7,8,9,10,11 og hele forebrain av voksen sebrafisk12, inkludert Ca 2+ aktivitetsregistrering og flerfargede observasjoner. Videre har høykontrastbilder blitt oppnådd med 15:00 gjennom de intakte hodeskallene av mus og voksen sebrafisk12,13.
I dag er eksitasjonslaserkilder egnet for 3P-eksitasjon (3PE) ved ~ 1300 og ~ 1700 nm kommersielt tilgjengelige. Siden laserskanningssystemet i hovedsak er det samme for 14:00 og 15:00, er det mulig å konvertere et eksisterende 2P-oppsett til et 3P-oppsett i biologilaboratorier med installasjon av en kommersielt tilgjengelig laser for 3PE. 3P-fluorescenssignalet er avhengig av lasereffekten, pulsvarigheten, laserrepetisjonshastigheten og den numeriske blenderåpningen (NA) til objektivlinsen. Forutsatt at et diffraksjonsbegrenset fokus (dvs. den bakre blenderåpningen til objektivlinsen er overfylt av eksitasjonsstrålen), beskriver Eq (1) den tidsgjennomsnittte fluorescensfotonfluksen fra brennvidden som følge av 3PE.
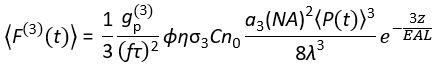 (1)
(1)
Der f er laserrepetisjonshastigheten, er τ laserpulsvarigheten (full bredde ved halv maksimum), φ er systemets oppsamlingseffektivitet, η er fluorescens kvanteeffektiviteten, σ3 er absorpsjonskrysssnittet, C er fluoroforonsentrasjonen, n0 er den reflekterende indeksen til prøvemediet (f.eks. vann), λ er eksitasjonsbølgelengden i vakuum, vakuum , NA er den numeriske blenderåpningen til objektivet, en3 er den romlige integrasjonskonstanten til brennviddet, 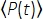 er den tidsgjennomsnittte eksitasjonsfotonfluksen (fotoner/ s) under objektivet, z er bildedybden, og EAL er den effektive dempingslengden14. Her har vi antatt at EAL (vanligvis > 100 μm) er mye større enn mikroskopets aksiale oppløsning (vanligvis < 10 μm). Under paraksial tilnærming er en3 lik 28,114. gp(3) er 3rd-order temporal sammenheng av eksitasjonskilden, og gp(3) er henholdsvis 0,41 og 0,51 for hyperbolsk-sekant-kvadred pulser og gaussiske pulser. Innsamlingseffektiviteten φ kan estimeres ved å vurdere fluorescenssamlingen ved objektivet, overføringen av objektivlinsen, reflektiviteten til det dikroiske speilet, overføringen av filtrene og detektorens deteksjonseffektivitet (f.eks. fotomultiplikatorrør eller PMT). Siden 3P-fluorescensintensiteten er svært avhengig av ulike parametere, kreves optimalisering av 3P-oppsettet for å maksimere 3P-fluorescenssignalene.
er den tidsgjennomsnittte eksitasjonsfotonfluksen (fotoner/ s) under objektivet, z er bildedybden, og EAL er den effektive dempingslengden14. Her har vi antatt at EAL (vanligvis > 100 μm) er mye større enn mikroskopets aksiale oppløsning (vanligvis < 10 μm). Under paraksial tilnærming er en3 lik 28,114. gp(3) er 3rd-order temporal sammenheng av eksitasjonskilden, og gp(3) er henholdsvis 0,41 og 0,51 for hyperbolsk-sekant-kvadred pulser og gaussiske pulser. Innsamlingseffektiviteten φ kan estimeres ved å vurdere fluorescenssamlingen ved objektivet, overføringen av objektivlinsen, reflektiviteten til det dikroiske speilet, overføringen av filtrene og detektorens deteksjonseffektivitet (f.eks. fotomultiplikatorrør eller PMT). Siden 3P-fluorescensintensiteten er svært avhengig av ulike parametere, kreves optimalisering av 3P-oppsettet for å maksimere 3P-fluorescenssignalene.
Denne protokollen illustrerer optimaliseringsprosessen til et typisk 3P-oppsett, som vil være nyttig spesielt for biologilaboratorier som har et 2P-oppsett og planlegger å utvide sin evne til 3P-avbildning eller opprettholde sitt kommersielle 3P-oppsett med optimal ytelse. Denne videoartikkelen demonstrerer også dypvevs 3P-avbildning i levende dyrehjerner. Den første delen tar for seg optimalisering av et typisk 3P-oppsett med en kommersielt tilgjengelig laserkilde og multifotonmikroskop. Den andre og tredje delen beskriver sebrafisk og muspreparat, henholdsvis for 3PM av nevronale strukturer og aktiviteter. Musekraniotomioperasjonen har tidligere blitt rapportert i protokollpapirer samt 15,16,17. Den fjerde delen demonstrerer intravital 3P-avbildning i sebrafisk og musehjerner.
Protocol
Representative Results
Discussion
Denne protokollen forklarer trinnvise prosedyrer for å sette opp 3P-avbildning med et kommersielt mikroskop og laserkilde. Sammenlignet med 14:00, har 15:00 en fordel i applikasjoner som krever optisk tilgang i de dypere områdene som i musen hjernen hippocampus. Selv om 15:00 for det meste brukes i nevrovitenskap, kan 15:00 potensielt brukes i andre vev som lymfeknuter, bein og svulster for dypvevsobservasjon.
Det er viktig å kontrollere at bildesystemet fungerer nær skuddstøygrensen, noe som sikrer at deteksjons- og datainnsamlingselelektronikken bidrar med ubetydelig støy til bildet etter PMT-ene. Usikkerheten i antall fotoner som oppdages er fundamentalt begrenset av fotonskuddsstøy. Skuddstøybegrenset ytelse kan oppnås i et typisk multifotonmikroskop ved hjelp av en fotodetektor med høy forsterkning (f.eks. en PMT). Fotonskuddsstøy følger en Poisson statistisk fordeling, der standardavviket for fordelingen er lik kvadratroten av gjennomsnittet av fordelingen. Følg trinn 1.14 i protokolldelen for å kontrollere den begrensede ytelsen for skuddstøy.
For å unngå lysdemping ved H2O er det nyttig å bruke D2O til nedsenking, spesielt for ~ 1700 nm eksitasjon. Når D2O brukes, er det viktig å oppdatere D2O hver ~10 min eller bruke et stort volum D2O for å unngå D2O/ H2O utveksling under bildebehandling. Man kan også forsegle D2O fra rommiljøet3. Hvis en objektiv linse med lang arbeidsavstand (WD) (f.eks. WD ved 4 mm eller lenger) brukes til avbildning, kan nedsenkningsvæsketykkelsen overstige 2-3 mm. Den økte tykkelsen gjør H2O absorpsjon ikke ubetydelig selv ved ~ 1300 nm21. Derfor kan D2O være nødvendig selv for 1300 nm 3PM når du bruker en lang WD objektiv.
Ettersom 3P-fluorescensintensiteten avhenger av kuben til eksitasjonspulsenergien i fokus (Eq. (1)), er det spesielt viktig å stille inn riktig lasereffekt for å oppnå tilstrekkelige 3P fluorescenssignaler samtidig som termisk og ikke-lineær skade i levende vev unngås. Den gjennomsnittlige lasereffekten bør holdes under terskelen for termisk skade. I musehjernen, for eksempel for å unngå termisk vevsskade, bør den gjennomsnittlige kraften på musens hjerneoverflate holdes på eller under ~ 100 mW for ~ 1300 nm eksitasjon på en dybde på 1 mm og med et synsfelt (FOV) på 230 μm x 230 μm21. På samme måte bør gjennomsnittseffekten på ~ 1700 nm holdes på eller under ~ 50 mW ved ~ 1 mm dybde og en FOV på ~ 230 μm x 230 μm (upubliserte data). Videre, for å unngå eksitasjonsmetning og potensiell ikke-lineær skade, bør eksitasjonspulsenergien holdes på 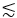 henholdsvis 2 nJ og
henholdsvis 2 nJ og 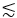 3 nJ for ~ 1300 nm og ~ 1700 nm eksitasjon, henholdsvis30.
3 nJ for ~ 1300 nm og ~ 1700 nm eksitasjon, henholdsvis30.
På grunn av lysabsorpsjon og spredning i vev, dempes pulsenergien i fokus til 1/e (~ 37%) etter penetrasjon av vev med 1 EAL. EAL varierer i forskjellige vev og med eksitasjonsbølgelengdene, for eksempel i neocortex av musehjernen, er EAL ~ 300 μm og ~ 400 μm ved ~ 1300 nm og ~ 1700 nm, henholdsvis 3,29 (figur 5). For å holde den samme pulsenergien i fokus (f.eks. 1 nJ/puls) på en dybde på n EALer, må overflatepulsenergien multipliseres med 1 nJ × en. For rask bildebehandling av strukturell og funksjonell dynamikk er en eksitasjonslaser med høy repetisjonshastighet (ved 1 MHz eller høyere) ønskelig å oppnå en høy bildefrekvens 5,6,7,10. Pulsenergibehovet og den gjennomsnittlige laserkraftgrensen begrenser imidlertid gjeldende repetisjonshastighet.
For eksempel, når vi ser for oss en moderat dyp region ved 4 EALer (dvs. ~ 1,2 mm i musebarken med 1300 nm eksitasjon), kreves ~ 55 nJ / puls på overflaten for å holde 1 nJ / puls i fokus. Når den gjennomsnittlige strømbegrensningen er 100 mW, kan vi bruke en laserrepetisjonshastighet på ~ 2 MHz. Men for å se dypere på en dybde på 7 EALer, kreves ~1100 nJ/puls på overflaten for å opprettholde 1 nJ/puls i fokus. Forutsatt at maksimal gjennomsnittlig effekt er 100 mW for å unngå termisk skade, bør laserrepetisjonshastigheten reduseres til 0,1 MHz for å oppnå en 1100 nJ / puls på overflaten. Tabell 1 oppsummerer typiske bildeforhold i musens hjernebark. Legg merke til at bildedybden i tabell 1 forutsetter at EAL er ensartet i hele musebarken.
Videre, på grunn av laserkraftbegrensningen i dypvev 15:00, eksisterer en avveining mellom bildefrekvensen og bildepikselstørrelsen, noe som er spesielt viktig for funksjonell bildebehandling som kalsiumavbildning. Den maksimale tilgjengelige laserrepetisjonshastigheten bestemmes på hver dybde basert på den nødvendige pulsenergien i fokus og den gjeldende gjennomsnittlige lasereffekten som beskrevet ovenfor, for eksempel 2 MHz på en dybde som tilsvarer ~ 4 EALer med 1300 nm eksitasjon. Generelt krever bildebehandling minst én puls per piksel. Følgelig bestemmes minimum tilgjengelig pikselboetid av laserrepetisjonshastigheten, for eksempel 0,5 μs / piksel med 2 MHz eksitasjon.
For å holde den høye romlige oppløsningen (~ 1 μm i laterale) i 3P-bilder, er det ideelt å sette 1 piksel til et område på ~ 1 μm2, for eksempel 256 x 256 piksler for en FOV på 250 x 250 μm2. For å utføre rask bildebehandling med en betydelig stor FOV (f.eks. 250 x 250 μm2 med 256 x 256 piksler), gir henholdsvis 0,5 MHz, 1 MHz og 2 MHz pulsrepetisjonshastigheter teoretisk maksimal bildefrekvens på henholdsvis ~ 7,6, ~ 15 og ~ 30 bilder / s. På samme måte er optimaliseringen av laserrepetisjonshastigheten viktig, avhengig av måldybden, skannehastigheten og FOV, for å bruke tilstrekkelig pulsenergi under terskelen for termisk skade. For å øke bildehastigheten kan en adaptiv eksitasjonskilde brukes til å konsentrere alle eksitasjonspulsene på nevronene (dvs. interesseregioner) ved å levere laserpulser på forespørsel til nevronene31.
15:00 er fordelaktig sammenlignet med 14:00 i dyp avbildning i levende vev og gjennom svært spredningsmedier som hodeskalle, bein og det hvite materielaget (dvs. den eksterne kapselen) i musehjernen. Jo lengre EAL og den ikke-lineære eksitasjonen med høyere rekkefølge av 3PE fordeler dypvevsavbildning. For eksempel, til bilde GCaMP6 i musebarken, er 2P fluorescenssignal med 920 nm eksitasjon høyere enn 3P fluorescenssignal med 1300 nm eksitasjon i grunne områder ved 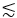 690 μm (dvs. ~ 2,3 EALer ved 1300 nm)21. På grunn av den lengre EAL på 1300 nm sammenlignet med 920 nm, gir 3PE imidlertid sterkere fluorescens enn 2P-eksitasjon (2PE) på en dybde på ~ 690 μm og dypere21. Denne dybden er definert som “signalovergangsdybde”, der fluorescenssignalstyrkene til 2PE og 3PE er identiske med samme repetisjonshastighet og samme maksimale tillatte gjennomsnittlige krefter21. Signalovergangsdybden avhenger av eksitasjonsbølgelengdene for 2PE og 3PE og fluoroforen.
690 μm (dvs. ~ 2,3 EALer ved 1300 nm)21. På grunn av den lengre EAL på 1300 nm sammenlignet med 920 nm, gir 3PE imidlertid sterkere fluorescens enn 2P-eksitasjon (2PE) på en dybde på ~ 690 μm og dypere21. Denne dybden er definert som “signalovergangsdybde”, der fluorescenssignalstyrkene til 2PE og 3PE er identiske med samme repetisjonshastighet og samme maksimale tillatte gjennomsnittlige krefter21. Signalovergangsdybden avhenger av eksitasjonsbølgelengdene for 2PE og 3PE og fluoroforen.
I praksis tillater 920 nm eksitasjon høyere gjennomsnittlig lasereffekt enn 1300 nm eksitasjon på grunn av mindre vannabsorpsjon. Den høyere gjennomsnittlige effekten til 2PE vil imidlertid bare presse signalets crossover-dybde med 0,9 EALer4. I tillegg, når prøven er tett merket, har 3PE den ekstra fordelen med mye høyere SBR. Derfor, selv før du når signalovergangslengden, kan 15:00 være bedre for bildebehandling enn 14:00. For eksempel, når du forestiller deg musen hjernen vaskulaturen, som har en volumfraksjon (dvs. merkingstetthet) på ~ 2%, 1300 nm 3PM med 100 mW eksitasjonskraft overgår 920 nm 2PM med 200 mW eksitasjonskraft i en dybde på ~ 700 μm for fluorescein.
15:00 har også en fordel når du ser gjennom et tynt, men svært spredningslag som kan forvrenge punktspredningsfunksjonen til eksitasjonsstrålen og generere en defokusbakgrunn4. For eksempel, gjennom den intakte skallen i musehjernen, lider 2PM-bilder av defokusbakgrunnen selv på den grunne dybden av <100 μm fra hjerneoverflaten13. En lignende defokusbakgrunn ble observert i 14:00 med 1280 nm eksitasjon gjennom det hvite stoffet i musehjernen32. Derfor, når vev er avbildet gjennom uklare lag, er 3PM å foretrekke fremfor 14:00 for høykontrastbilder uavhengig av merketettheten.
Vi rapporterte nylig en perle fantom og teoretisk analyse som viser at bildedybdegrensen på 15:00 er over 8 EALs33; 8 EALer tilsvarer ~3 mm med ~1700 nm eksitasjon i musebarken. Den tilgjengelige laseren har imidlertid ikke nok pulsenergi til å oppnå 8 EALer i musehjernen. Videreutvikling av sterkere lasere vil presse den nåværende bildedybdegrensen på 15:00.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av NSF DBI-1707312 Cornell NeuroNex Hub og NIH 1U01NS103516.
Materials
| 5% Povidone-iodine | Amazon | NDC 67818-155-32 | Aceptical cleaning of surgical areas |
| 70% Ethanol | Thermo Fisher Scientific | CAS 64-17-5 | Aceptical cleaning of surgical areas |
| Agarose | Sigma | A4718-256 | Preparing zebrafish chamber |
| Atropine | Cornell Veterinary Care | ||
| Bergamo II | Thorlabs | Multiphoton Imaging Microscope | |
| Bupivacaine | Cornell Veterinary Care | ||
| Dexamethasone | Cornell Veterinary Care | ||
| Donut shape glass (ID4.5, OD6.5) | Potomac Photonics | Cover glass used for craniotomy | |
| eye ointment (or topical ophthalmic ointment) | Puralube Vet Ointment | NDC 17033-211-38 | Used as a lubricant to prevent irritation or to relieve dryness of the eye during surgery and anesthesia |
| GaAsP Amplified PMT | Thorlabs | PMT2100 | PMT detector |
| Glucose | Cornell Veterinary Care | ||
| Glycopyrrolate | Cornell Veterinary Care | ||
| Heater (800 W) | Finnex | Aquarium heater for zebrafish water) | |
| Isoflurane USP 250 mL | Piramal | NDC 66794-0013-25 | For anesthesia of mice |
| Ketoprofen | Cornell Veterinary Care | ||
| Kimwipes | Kimtech | Laboratory tissue for preparing zebrafish | |
| Nanofil syringe (10 micrometer) with 36 G needle | WPI | NANOFIL + NF36BV | Syringe and needle for injection of pancuronium bromide |
| Optical Adhesive | Norland | NOA 68 | To stick round coverslip and donut shape glass together. |
| Pancuronium Bromide | Cornell Veterinary Care | ||
| Peristaltic Pump | Elemental Science | ESI MP2 | Water pump for zebrafish setup |
| Polyethylene tubing (I.D. 0.58 mm., O.D. 0.965 mm.) | Elemental Science | MP2 pump tubing | Tubing that goes in the mouth of the zebrafish |
| Round Cover Slip German Glass #1.5, 5 mm | Electron Microscopy Sciences | 7229605 | Cover glass used for craniotomy |
| Spirit-NOPA | Spectra Physics | Tunable Optical Parametric Amplifier | |
| SR400 | Stanford Research Systems | SR400 | Photon counter |
| Standard Photodiode Power Sensor | Thorlabs | S122C | Power detector |
| Sterilized phosphate buffered saline (PBS) | Millipore Sigma | SKU 806552-500ml | Used during mouse brain surgery |
| Surgical drape | Dynarex disposable towel drape | 4410 | For aceptical mouse surgery |
| Thin strip boxing wax | Corning Rubber Co., Inc. | Holding tubing in place in zebrafish chamber | |
| ThorImage | Thorlabs | Image acquisition software | |
| Tricaine (Ethyl-m-aminobenzoate methanesulfonate salt) | MP | 103106 | Zebrafish anesthesia and euthanasia |
| Tygon tubing (I.D. 1/16 in., O.D. 1/8 in.) | Tygon | Tubing for water flow for zebrafish preparation | |
| VaporGuard | VetEquip | 931401 | For recycling isoflurane |
| Vetbond tissue adhesive | 3M | 1469SB | To glue the glass window on the mouse skull, and to glue the laboratory tissue when preparing the fish. |
| XLPLN25XWMP2 | Olympus | Multiphoton Excitation Dedicated Objective |
References
- Denk, W., Strickler, J. H., Webb, W. W. Two-photon laser scanning fluorescence microscopy. Science. 248 (4951), 73-76 (1990).
- Helmchen, F., Denk, W. Deep tissue two-photon microscopy. Nature Methods. 2 (12), 932-940 (2005).
- Horton, N. G., et al. In vivo three-photon microscopy of subcortical structures within an intact mouse brain. Nature Photonics. 7 (3), 205-209 (2013).
- Wang, T., Xu, C. Three-photon neuronal imaging in deep mouse brain. Optica. 7 (8), 947-960 (2020).
- Ouzounov, D. G., et al. In vivo three-photon imaging of activity of GCaMP6-labeled neurons deep in intact mouse brain. Nature Methods. 14 (4), 388-390 (2017).
- Weisenburger, S., et al. Volumetric Ca2+ imaging in the mouse brain using hybrid multiplexed sculpted light microscopy. Cell. 177 (4), 1050-1066 (2019).
- Yildirim, M., Sugihara, H., So, P. T. C., Sur, M. Functional imaging of visual cortical layers and subplate in awake mice with optimized three-photon microscopy. Nature Communications. 10, 177 (2019).
- Takasaki, K., Abbasi-Asl, R., Waters, J. Superficial bound of the depth limit of two-photon imaging in mouse brain. eNeuro. 7 (1), (2020).
- Guesmi, K., et al. Dual-color deep-tissue three-photon microscopy with a multiband infrared laser. Light, Science & Applications. 7, 12 (2018).
- Hontani, Y., Xia, F., Xu, C. Multicolor three-photon fluorescence imaging with single-wavelength excitation deep in mouse brain. Science Advances. 7 (12), 3531 (2021).
- Liu, H., et al. In vivo deep-brain structural and hemodynamic multiphoton microscopy enabled by quantum dots. Nano Letters. 19 (8), 5260-5265 (2019).
- Chow, D. M., et al. Deep three-photon imaging of the brain in intact adult zebrafish. Nature Methods. 17 (6), 605-608 (2020).
- Wang, T., et al. Three-photon imaging of mouse brain structure and function through the intact skull. Nature Methods. 15 (10), 789-792 (2018).
- Xu, C., Webb, W. W. Multiphoton excitation of molecular fluorophores and nonlinear laser microscopy. Topics in Fluorescence Spectroscopy. 5. , 471-540 (2002).
- Mostany, R., Portera-Cailliau, C. A craniotomy surgery procedure for chronic brain imaging. Journal of Visualized Experiments: JoVE. (12), e680 (2008).
- Łukasiewicz, K., Robacha, M., Bożycki, &. #. 3. 2. 1. ;., Radwanska, K., Czajkowski, R. Simultaneous two-photon in vivo imaging of synaptic inputs and postsynaptic targets in the mouse retrosplenial cortex. Journal of Visualized Experiments: JoVE. (109), e53528 (2016).
- Kyweriga, M., Sun, J., Wang, S., Kline, R., Mohajerani, M. H. A large lateral craniotomy procedure for mesoscale wide-field optical imaging of brain activity. Journal of Visualized Experiments: JoVE. (123), e52642 (2017).
- Gordon, J. P., Martinez, O. E., Fork, R. L. Negative dispersion using pairs of prisms. Optics Letters. 9 (5), 150-152 (1984).
- Entenberg, D., et al. Setup and use of a two-laser multiphoton microscope for multichannel intravital fluorescence imaging. Nature Protocols. 6 (10), 1500-1520 (2011).
- Horton, N. G., Xu, C. Dispersion compensation in three-photon fluorescence microscopy at 1,700 nm. Biomedical Optics Express. 6 (4), 1392-1397 (2015).
- Wang, T., et al. Quantitative analysis of 1300-nm three-photon calcium imaging in the mouse brain. eLife. 9, 53205 (2020).
- Cheng, L. -. C., Horton, N. G., Wang, K., Chen, S. -. J., Xu, C. Measurements of multiphoton action cross sections for multiphoton microscopy. Biomedical Optics Express. 5 (10), 3427-3433 (2014).
- Huang, K. -. H., et al. A virtual reality system to analyze neural activity and behavior in adult zebrafish. Nature Methods. 17 (3), 343-351 (2020).
- Jacobson, G. A., Rupprecht, P., Friedrich, R. W. Experience-dependent plasticity of odor representations in the telencephalon of zebrafish. Current Biology. 28 (1), 1-14 (2018).
- Li, J., et al. Early development of functional spatial maps in the zebrafish olfactory bulb. Journal of Neuroscience. 25 (24), 5784-5795 (2005).
- Barbosa, J. S., et al. Live imaging of adult neural stem cell behavior in the intact and injured zebrafish brain. Science. 348 (6236), 789-793 (2015).
- Dray, N., et al. Large-scale live imaging of adult neural stem cells in their endogenous niche. Development. 142 (20), 3592-3600 (2015).
- Kobat, D., et al. Deep tissue multiphoton microscopy using longer wavelength excitation. Optics Express. 17 (16), 13354-13364 (2009).
- Wang, M., Wu, C., Sinefeld, D., Li, B., Xia, F., Xu, C. Comparing the effective attenuation lengths for long wavelength in vivo imaging of the mouse brain. Biomedical Optics Express. 9 (8), 3534-3543 (2018).
- Vogel, A., Noack, J., Hüttman, G., Paltauf, G. Mechanisms of femtosecond laser nanosurgery of cells and tissues. Applied Physics B. 81 (8), 1015-1047 (2005).
- Li, B., Wu, C., Wang, M., Charan, K., Xu, C. An adaptive excitation source for high-speed multiphoton microscopy. Nature Methods. 17 (2), 163-166 (2019).
- Kobat, D., Horton, N. G., Xu, C. In vivo two-photon microscopy to 1.6-mm depth in mouse cortex. Journal of Biomedical Optics. 16 (10), 106014 (2011).
- Akbari, N., Rebec, M. R., Xia, F., Xu, C. Imaging deeper than the transport mean free path with multiphoton microscopy. Biomedical Optics Express. 13, 452-463 (2022).

