Analyse af Parkinsons sygdom musemodel induceret af Adeno-associerede virale vektorer, der koder for humane α-synuclein
Summary
Dette arbejde analyserer vektordosis og eksponeringstid, der kræves for at inducere neuroinflammation, neurodegeneration og motorisk svækkelse i denne prækliniske model af Parkinsons sygdom. Disse vektorer, der koder for den humane α-synuclein, leveres i substantia nigra for at rekapitulere synucleinpatologien forbundet med Parkinsons sygdom.
Abstract
Parkinsons sygdom er en neurodegenerativ lidelse, der involverer døden af de dopaminerge neuroner i den nigrostriatale vej og følgelig det progressive tab af kontrol over frivillige bevægelser. Denne neurodegenerative proces udløses af aflejring af proteinaggregater i hjernen, som hovedsageligt består af α-synuclein. Flere undersøgelser har vist, at neuroinflammation er nødvendig for at udvikle neurodegeneration forbundet med Parkinsons sygdom. Især involverer den neuroinflammatoriske proces mikroglial aktivering såvel som infiltration af perifere T-celler i substantia nigra (SN). Dette arbejde analyserer en musemodel af Parkinsons sygdom, der rekapitulerer mikroglial aktivering, T-celleinfiltration i SN, neurodegeneration af nigrale dopaminerge neuroner og motorisk svækkelse. Denne musemodel af Parkinsons sygdom induceres af stereotaxisk levering af adeno-associerede virale vektorer, der koder for den humane vildtype α-synuclein (AAV-hαSyn) i SN. Den korrekte levering af virale vektorer i SN blev bekræftet ved hjælp af kontrolvektorer, der koder for grønt fluorescerende protein (GFP). Derefter blev det evalueret, hvordan dosis af AAV-hαSyn administreret i SN påvirkede omfanget af hαSyn-ekspression, tabet af nigrale dopaminerge neuroner og motorisk svækkelse. Desuden blev dynamikken i hαSyn-ekspression, mikroglial aktivering og T-celleinfiltration bestemt i hele sygdomsudviklingens forløb. Således giver denne undersøgelse kritiske tidspunkter, der kan være nyttige til at målrette synucleinpatologi og neuroinflammation i denne prækliniske model af Parkinsons sygdom.
Introduction
Efter Alzheimers sygdom er Parkinsons sygdom den næstmest udbredte neurodegenerative sygdom på verdensplan. De primære neuroner, der er berørt af Parkinsons sygdom, er dem i den nigrostriatale vej, som producerer dopamin og styrer frivillig bevægelse. Som følge heraf er det mest karakteristiske symptom forbundet med denne lidelse motorisk svækkelse. Denne patologi involverer også aflejring af proteinaggregater i hjernen, som hovedsageligt består af α-synuclein (αSyn)1, et cytosolisk protein forbundet med præsynaptiske terminaler. Beviser har vist, at dannelsen af patogene indeslutninger af αSyn udløses af fejlfoldning eller af nogle posttranslationelle modifikationer af dette protein2.
Især er der etableret et tæt forhold mellem αSyn-patologi og tabet af dopaminerge neuroner i den nigrostriatale vej i human Parkinsons sygdom og dyremodeller 3,4. At forstå, hvordan αSyn-aggregater genereres, og hvordan de inducerer neuronal død, repræsenterer en betydelig udfordring på området. En voksende gruppe undersøgelser har vist, at mitokondriel dysfunktion ved at øge oxidativt stress er en af de vigtigste årsager til dannelsen af αSyn-aggregater2. Faktisk risikerer flere gener forbundet med Parkinsons sygdom proteiner involveret i mitokondriefunktion, morfologi og dynamik 5,6. Derudover udgør lysosomal dysfunktion, som resulterer i akkumulering af dysfunktionelle mitokondrier og forkert foldet αSyn, en anden vigtig begivenhed, der fremmer dannelsen af αSyn-aggregater7.
Nye beviser har vist, at når αSyn-aggregater er deponeret i hjernen, stimulerer disse patogene proteiner vejafgiftslignende receptorer (TLR’er) på mikrogliaen, hvilket udløser mikroglial aktivering og et indledende inflammatorisk miljø i substantia nigra (SN) 8,9. Desuden indikerer beviserne, at αSyn-aggregater fanges og præsenteres af antigenpræsenterende celler til T-celler, hvilket inducerer et adaptivt immunrespons, der er specifikt for αSyn10,11. Disse αSyn-specifikke T-celler infiltrerer efterfølgende hjernen og genformuleres af aktiveret mikroglia, hvilket fremmer udskillelsen af neurotoksiske faktorer, der fremkalder neuronal død 9,10. Interessant nok har flere bevislinjer antydet, at αSyn-aggregater genereres først i det enteriske nervesystem og derefter transporteres gennem vagusnerven til hjernestammen12.
Flere dyremodeller af Parkinsons sygdom er blevet anvendt i mange år, herunder dem, der er induceret ved administration af neurotoksiske stoffer (dvs. 6-hydroxydopamin, paraquat, rotenon, 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridin) og dem, der involverer genetiske tilstande (dvs. mutant α-synuclein, mutant leucinrig gentagelseskinase 2)13 . På trods af modeller, der involverer neurotoksinduceret neurodegeneration, der replikerer nogle aspekter af Parkinsons sygdom, rekapitulerer ingen af dem alle de væsentlige aspekter af sygdommen eller er ikke progressive13. På den anden side, selv om genetiske musemodeller, der involverer ekspression af mutante versioner af leucinrig gentagelseskinase 2, mutante versioner af α-synuclein eller overekspression af human vildtype α-synuclein resulterer i motorisk svækkelse og i nogle tilfælde også udvikling af synukleinopati, reproducerer de ikke fremtrædende neurodegeneration af de nigrale dopaminerge neuroner, hvilket er et væsentligt aspekt af Parkinsons sygdom13, 14. En tredje slags dyremodel for neurodegeneration har formået at opfylde de fleste af de væsentlige aspekter af Parkinsons sygdom, den stereotaksiske levering af adeno-associerede virale vektorer (AAV’er), der koder for den humane α-synuclein (AAV-hαSyn)14,15. Det er vigtigt, at AAV’er tillader transduktion af neuroner med høj effektivitet og på lang sigt i pattedyrs voksne hjerne. Desuden har den stereotaksiske levering af AAV-hαSyn i SN vist sig at reproducere mange af de væsentlige aspekter af sygdommen, herunder αSyn-patologi, mikroglial aktivering, neurodegeneration og motorisk svækkelse 16,17,18,19,20. Denne undersøgelse præsenterer en analyse af, hvordan dosis af viral vektor og tiden efter viral vektorlevering påvirker omfanget af hαSyn-ekspression, neurodegeneration og neuroinflammation i den nigrostriatale vej samt graden af motorisk svækkelse i musemodellen for ensidig stereotaksisk levering af hαSyn i SN.
Protocol
Representative Results
Discussion
Musemodellen for neurodegeneration, der analyseres her, kan hjælpe med at studere mange kritiske aspekter involveret i patofysiologien af Parkinsons sygdom, herunder de mekanismer, der er involveret i αSynpatologi og mikroglial aktivering, inddragelsen af det perifere immunsystem i reguleringen af neuroinflammation og mekanismerne for neurodegeneration. Blandt de mekanismer, der er involveret i αSyn-patologi, er de subcellulære mekanismer forbundet med mitokondriel, lysosomal eller proteasomal dysfunktion i nærvær af en overdreven belastning af αSyn i de dopaminerge neuroner i SN2. Det er vigtigt at overveje, at ud over hαSyn-ekspressionen induceret af AAV-medieret transduktion bidrager den endogene mus αSyn også til belastningen af det samlede αSyn-udtryk. Transgene mus, der overudtrykker mus αSyn, udvikler lignende synucleinpatologi, neuropatologi og motorisk svækkelse som disse musemodeller baseret på overekspression af hαSyn32. Med hensyn til mikroglial aktivering kan den nuværende musemodel bruges til at undersøge, hvordan forskellige molekylære og cellulære aktører såsom cytokiner, neurotransmittere, astrocytter, neuroner, blod-hjerne-barrieren og T-celler kan regulere erhvervelsen af proinflammatoriske eller antiinflammatoriske funktionelle fænotyper 8,10,11 . Denne model udgør også et vigtigt redskab til at studere det perifere immunsystems rolle, herunder ikke kun T-celler, men også makrofager, monocytter og neutrofiler, på processerne for neuroinflammation og neurodegeneration af nigrale neuroner 11,33,34. Endelig repræsenterer denne musemodel også et værdifuldt system til at studere de cellulære og molekylære mekanismer for neurodegeneration in vivo, herunder dem, der induceres af interne cellulære processer, såsom oxidativ stress, energiunderskud og beskadigede organeller 2, eller dem, der udøves af eksterne aktører, såsom neurotoksiske faktorer produceret af mikrogliaceller, astrocytter og cytotoksiske T-celler8, 28,29,35.
En begrænsning af denne musemodel er undersøgelsen af, hvordan den patologiske aggregering af αSyn på ekstra-cerebrale steder kan udgøre de indledende faser i udviklingen af Parkinsons sygdom36. I denne henseende er der voksende beviser, der tyder på, at før neurodegenerationen af nigralneuroner og motorisk svækkelse begynder αSynpatologi i tarmslimhinden og det olfaktoriske epitel36 og sandsynligvis også det αSyn-specifikke T-cellerespons12. Bagefter ville αSyn-aggregater migrere gennem vagusnerven til hjernestammen, hvilket udløste neuroinflammation og neurodegeneration af dopaminerge neuroner12. Selvom AAV-hαSyn-modellen rekapitulerer de fleste aspekter af Parkinsons sygdom, er der ingen tydelig involvering af den patologiske aggregering af αSyn på ekstra-cerebrale steder i denne model. En alternativ model, der involverer hαSyn-patologi, der er egnet til at studere disse aspekter af Parkinsons sygdom, kan være transgene mus, der overudtrykker hαSyn under kontrol af Thy1-promotoren, Thy1-SNCA-modellen 37, hvor sygdomsudvikling er afhængig af tarmmikrobiotaen og involverer en tydelig gastrointestinal svækkelse38.
Selvom det er nyttigt til undersøgelsen af de forskellige processer, der er forbundet med patofysiologien af Parkinsons sygdom, involverer den nuværende musemodel kritiske trin, der skal kontrolleres minutiøst, herunder korrekt levering af de virale vektorer i de tilsvarende rumlige koordinater, den selektive ekspression af hαSyn i neuroner (hvilket afhænger af AAV-serotypen og vektorkonstruktionen), og den korrekte AAV-dosis og timing, før du analyserer Parkinsons fænotype. Analysen af den korrekte levering af de virale vektorer i SN er nødvendig, da brugen af de korrekte rumlige koordinater for SN muligvis ikke er nok, når nålen ikke er helt lige, hvilket undertiden er umærkeligt for det menneskelige øje. Desuden afhænger diffusionen af AAV-vektorerne af AAV-serotype39. Af disse grunde er det nødvendigt at udføre periodiske kvalitetskontroller, der kontrollerer den korrekte levering og diffusion af de injicerede AAV-GFP-vektorer efter observation af GFP i hjerneskiver, der indeholder SN-området.
Med hensyn til den selektive ekspression af hαSyn i neuroner kunne ekspressionen af hαSyn i princippet konstrueres til at blive kontrolleret af en promotor, der er selektiv for neuroner eller, endnu mere præcis, selektiv for dopaminerge neuroner, såsom brugen af TH-promotoren i AAV-vektorer til at inducere den selektive ekspression af gener i dopaminerge neuroner40 . Denne strategi virker imidlertid ikke, når det, der søges, er overekspression af genet af interesse. Af denne grund er det i den nuværende model vigtigt at anvende en stærk promotor (en promotor, der inducerer høj ekspression af downstream-genet) og AAV-serotyper med neuronal tropisme. I denne undersøgelse blev CBA-promotoren brugt som en stærk promotor til at inducere overekspression af hαSyn, og AAV5-serotypen blev anvendt til den virale vektor. Denne serotype er tidligere blevet brugt til at transducere muse- ogrotteneuroner 41,42. Her viste resultaterne, at 12 uger efter leveringen af AAV5-GFP i musens SN var den grønne fluorescens selektivt til stede på den ipsilaterale side af både SN og striatum (figur 1), hvilket indikerer den effektive transduktion af neuroner i den nigrostriatale vej.
Et andet kritisk aspekt af denne musemodel af Parkinsons sygdom er det tidspunkt, der kræves for at analysere en bestemt proces efter operationen. I denne henseende viser dette arbejde en kinetisk undersøgelse af forskellige processer involveret i patologien. Da vigtige tidspunkter ændrer sig med den dosis af virale genomer, der gives pr. mus, blev serotypen af AAV anvendt, eller endda med det anvendte parti AAV, først udført en dosis-respons-analyse af mængden af AAV-αSyn, der kræves for at inducere et signifikant tab af TH + neuroner og motorisk svækkelse. Tidligere undersøgelser har vist signifikant motorisk svækkelse og et tab af TH+ neuroner i den nigrostriatale vej efter 12 ugers AAV-αSyn-injektioner i mus i doser fra 6 x 108-3 x 1010 virale genomer pr. mus 16,17,30,31. Følgelig varierede dosis af AAV-hαSyn, der blev anvendt til at inducere hαSyn-ekspressionen i den nigrostriatale vej, tabet af TH+ neuroner og motorisk svækkelse hos mus fra 1 x 108-1 x 1010 virale genomer pr. Mus. For at kontrollere, at tabet af TH + neuroner og motorisk svækkelse blev induceret af overekspression af hαSyn i SN og ikke ved AAV-infektion af neuroner i SN, blev kontrolgrupper inkluderet, hvor AAV-kodning for et reportergen (AAV-eGFP) blev leveret ensidigt i SN af mus, og neurodegeneration og motorisk svækkelse blev bestemt. Resultaterne viste, at 1 x 1010 virale genomer pr. mus 12 uger efter stereotaksisk kirurgi var en korrekt dosis AAV5-hαSyn, da mus, der modtog denne virale belastning, viste signifikant hαSyn i den nigrostriatale vej (figur 2 og figur 3), tab af TH + neuroner (figur 4) og motorisk svækkelse (figur 5). I modsætning hertil var lavere doser af AAV5-hαSyn (1 x 108 virale genomer pr. mus og 1 x 109 virale genomer pr. mus) ikke stærke nok til at nå signifikante ændringer i alle disse parametre tilsammen (figur 2-4). Bemærk, at administrationen af AAV-GFP ved 1 x 1010 virale genomer pr. Mus inducerede en lav (~ 20%), men signifikant grad af tab af TH + neuroner af nigral dopaminerge neuroner (figur 4A, B). Dette resultat stemmer overens med tidligere observationer ved hjælp af denne model41 og er sandsynligvis konsekvensen af et lavt niveau af neuroinflammation induceret af administrationen af AAV-vektorer i SN. Ikke desto mindre var omfanget af tab af TH+-neuroner signifikant højere hos mus, der fik AAV5-hαSyn sammenlignet med dem, der fik samme dosis AAV-GFP (figur 4C). Det bemærkes, at kinetikken af hαSyn-ekspression ikke kun afhænger af effektiviteten af transduktion, men også af omfanget af AAV-diffusion39. Da AAV-diffusion afhænger af AAV-serotypen, kan de præcise nøgletidspunkter i denne dyremodel variere, når der anvendes en anden AAV-serotype, der er forskellig fra AAV5.
Derefter blev der udført en kinetisk analyse ved hjælp af 1 x 1010 virale genomer pr. Mus for at bestemme vigtige tidspunkter i denne musemodel. Da de nuværende beviser har vist nogle tidlige symptomer, der vises før motorisk svækkelse, hvilket ville muliggøre tidlig diagnose af Parkinsons sygdom43,44, forsøgte disse eksperimenter at finde det tidspunkt, hvor hαSyn-ekspression allerede var tydelig, men i mangel af motorisk svækkelse. Resultaterne viser, at starten på hαSyn-ekspression i SN var 5 uger efter den stereotaksiske levering af AAV-hαSyn (figur 6). Dette tidspunkt udgør et interessant tidsmæssigt punkt at begynde at administrere terapier, der er skræddersyet til at stoppe de neuroinflammatoriske og neurodegenerative processer. Andre vigtige tidspunkter, der blev bestemt her, var spidsbelastningstiderne for to kritiske hændelser forbundet med neuroinflammationsprocessen: det tidspunkt, hvor mikroglia når den maksimale grad af aktivering og tidspunktet for maksimal T-celleinfiltration i SN. Resultaterne viste en kurve med en tendens, der nåede to bølger af maksimal mikroglial aktivering, den første 10 uger efter operationen og den anden 15 uger efter operationen (figur 7). Den kinetiske analyse af T-celleinfiltration viste spidsbelastningstiden for Treg-infiltration i SN 11 uger efter stereotaksisk kirurgi (figur 8). Overraskende nok blev der ikke påvist nogen effektor T-celler (CD4 + Foxp3-), der infiltrerede SN i løbet af den analyserede tidsramme (uge 8-13 efter operationen). Alt i alt tyder disse resultater på en passende tidsramme for at begynde at administrere terapier rettet mod at stoppe processen med neuroinflammation og dæmpe T-celleinfiltration i SN ved hjælp af denne prækliniske model, som varierer mellem uge 5 efter operationen (begyndelsen af hαSyn overekspression) og uge 10 efter operationen (den første bølge af neuroinflammation og T-celleinfiltration) (figur 9).
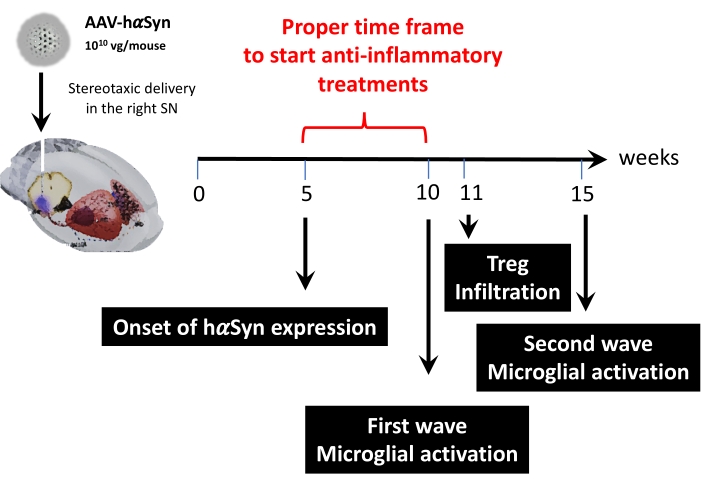
Figur 9: Oversigt over de vigtigste tidspunkter, der er fundet for denne dyremodel. Klik her for at se en større version af denne figur.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker Dr. Sebastián Valenzuela og Dr. Micaela Ricca for deres værdifulde veterinære bistand i vores dyreanlæg. Dette arbejde blev støttet af “Financiamiento Basal para Centros Científicos y Tecnológicos de Excelencia de ANID” Centro Ciencia & Vida, FB210008 (til Fundación Ciencia & Vida) og Geroscience Center for Brain Health and Metabolism, FONDAP-15150012. Dette arbejde blev også finansieret af tilskud FONDECYT-1210013 (til R.P.) og FONDECYT-1150766 (til F.C.) fra “Agencia Nacional de Investigación y Desarrollo de Chile (ANID)” og MJFF-10332.01 (til R.P.) og MJFF-17303 (til F.C.) fra Michael J Fox Foundation for Parkinson’s Research.
Materials
| ANIMALS AND ANIMAL FOOD | |||
| Foxp3-GFP C57BL/6 mice | The Jackson Laboratory (Bar Harbor, ME) | Stock No: 023800 | |
| Laboratory Rodent Diet | LabDiet | Rodent Diet 5001 | Standard Rodent diet |
| Wild-type C57BL/6 mice | The Jackson Laboratory (Bar Harbor, ME) | Stock No: 000664 | |
| VIRAL VECTORS | |||
| AAV5-CBA-αSyn | University of Iowa Viral Vector Core Facility | N/A | Stock concentration at 10E13 vg/mL |
| AAV5-CBA-eGFP | University of Iowa Viral Vector Core Facility | N/A | Stock concentration at 9.5 x 10E12 vg/mL |
| ANESTHETICS AND ANALGESICS | |||
| Isoflurane | Baxter | 218082 | 1% for stereotaxic surgery |
| Ketamine | Drag Pharma | CHE30 | 70 mg/Kg for stereotaxic surgery |
| Sevoflurane | Baxter | VE2L9117 | For before transcardial perfusion |
| Tramadol | Drag Pharma | DPH134 | 30 mg/Kg every 24 h |
| Xylazine | Centrovet | EHL40 | 9 mg/kg for stereotaxic surgery |
| EQUIPMENT | |||
| Beam test | Home made | N/A | horizontal beam 25 cm length and 3 cm width. The beam surface was covered by a metallic grid (1 cm2). |
| Cryostate | Leica | CM1520 | |
| Digital camera | Nikon | S2800 Coolpix | For recording the beam test performance |
| Microscope | Olympus | BX51 | Used for IHC analysis (section 4.4) |
| Microscope | Olympus | IX71 | Used for IF analysis (section 5.3) |
| Microscope | Leica | DMI8 | Used for IF analysis (section 5.7) |
| New Standard Stereotaxic, mouse | Stoelting, Wood Dale, IL, USA | 51500 | stereotaxic frame for surgery |
| Peristaltic Pump | Masterflex | C-flex L/S16 | |
| Power supply unit | Olympus | U-RFL-T | Used for IF analysis (section 5.3) |
| Surgical suture | Sylkam®, B Braun | C0760171 | |
| Syringe 100 U | BD | 324918 | For anesthesia before transcardial perfusion, 29G needle |
| Syringe RN 5uL SYR W/O NEEDLE | Hamilton | HA-7641-01 | For viral vector innoculation |
| BUFFERS AND REAGENTS | |||
| Aviden, Peroxidase Conjugate | Merck, Darmstadt, Germany | 189728 | |
| Bovine Serum Albumin | Merck, Darmstadt, Germany | 9048-46-8 | |
| Cryotrotection buffer | Home made | N/A | 20% glycerine and 2% DMSO in PBS |
| DAPI | Abcam | ab228549 | |
| Diaminobenzidine | Merck, Darmstadt, Germany | D8001 | |
| Fluoromount -G T | Electron Microscopy Science | 17984-25 | |
| Gelatin | Merck, Darmstadt, Germany | 104078 | |
| Normal goat serum | Jackson ImmunoResearch Laboratory | 5000121 | |
| Paraformaldehyde | Merck, Darmstadt, Germany | 104005 | |
| PBS | Home made | N/A | 0.125 M, pH 7.4 |
| Peroxidase inactivating buffer | Home made | N/A | 0.03% H2O2 in methanol |
| Triton X-100 | Sigma-Aldrich | 9036-19-5 | |
| Trizma Hydrochloride | Merck, Darmstadt, Germany | 1185-53-1 | |
| Tween 20 | Sigma-Aldrich | 822184 | |
| ANTIBODIES | |||
| Biotin-SP (long spacer) AffiniPure Goat Anti-Rabbit IgG (H+L) | Jackson ImmunoResearch Laboratory | 111065003 | |
| Goat anti-Rabbit IgG (H+L) Alexa Fluor 546 | ThermoFisher Scientific | A11010 | |
| Goat anti-Rabbit IgG (H+L) Alexa Fluor 647 | ThermoFisher Scientific | A21244 | |
| Goat anti-Rat IgG (H+L) Alexa Fluor 546 | ThermoFisher Scientific | A11081 | |
| Rabbit monoclonal anti-alpha-Synuclein | Abcam | ab138501 | |
| Rabbit monoclonal anti-Iba-1 | Abcam | EPR16588 | |
| Rabbit polyclonal anti-Tyrosine Hydroxylase | Millipore | AB152 | |
| Rat monoclonal anti-CD4 | Biolegend | 100402 | |
| SOFTWARES | |||
| GraphPad | Prism | 6.0 | Fos stats analysis |
| ImageJ | National Institute of Health | N/A | For image analysis |
| LAS X | Leica | N/A | For image capture with Leica microscope |
| ProgRes Capture Pro | Jenoptik | N/A | For image capture with Olympus microscope |
| VLC media player | VideoLAN Organization | N/A | For analysis of behavioural tests |
References
- Braak, H., et al. Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiology of Aging. 24 (2), 197-211 (2003).
- Lim, K. L., Zhang, C. W. Molecular events underlying Parkinson’s disease – An interwoven tapestry. Frontiers in Neurology. 4, 33 (2013).
- Abdelmotilib, H., et al. α-Synuclein fibril-induced inclusion spread in rats and mice correlates with dopaminergic neurodegeneration. Neurobiology of Disease. 105, 84-98 (2017).
- Mori, F., et al. Relationship among alpha-synuclein accumulation, dopamine synthesis, and neurodegeneration in Parkinson disease substantia nigra. The Journal of Neuropathology & Experimental Neurology. 65 (8), 808-815 (2006).
- Winklhofer, K. F., Haass, C. Mitochondrial dysfunction in Parkinson’s disease. Biochimica et Biophysica Acta. 1802 (1), 29-44 (2010).
- Vazquez-Velez, G. E., Zoghbi, H. Y. Parkinson’s disease genetics and pathophysiology. Annual Review of Neuroscience. 44, 87-108 (2021).
- Dehay, B., et al. Lysosomal impairment in Parkinson’s disease. Movement Disorders. 28 (6), 725-732 (2013).
- Gonzalez, H., Elgueta, D., Montoya, A., Pacheco, R. Neuroimmune regulation of microglial activity involved in neuroinflammation and neurodegenerative diseases. Journal of Neuroimmunology. 274 (1-2), 1-13 (2014).
- Pacheco, R. T-cell based immunotherapies for Parkinson’s disease. Exploration of Neuroprotective Therapy. 1 (2), 72-85 (2021).
- Gonzalez, H., Contreras, F., Pacheco, R. Regulation of the neurodegenerative process associated to Parkinson’s disease by CD4+ T-cells. Journal of Neuroimmune Pharmacology. 10 (4), 561-575 (2015).
- Gonzalez, H., Pacheco, R. T-cell-mediated regulation of neuroinflammation involved in neurodegenerative diseases. Journal of Neuroinflammation. 11 (1), 201 (2014).
- Campos-Acuna, J., Elgueta, D., Pacheco, R. T-cell-driven inflammation as a mediator of the gut-brain axis involved in Parkinson’s disease. Frontiers in Immunology. 10, 239 (2019).
- Blesa, J., Phani, S., Jackson-Lewis, V., Przedborski, S. Classic and new animal models of Parkinson’s disease. Journal of Biomedicine and Biotechnology. 2012, 845618 (2012).
- Ulusoy, A., Decressac, M., Kirik, D., Bjorklund, A. Viral vector-mediated overexpression of alpha-synuclein as a progressive model of Parkinson’s disease. Progress in Brain Research. 184, 89-111 (2010).
- Gomez-Benito, M., et al. Modeling Parkinson’s disease with the alpha-synuclein protein. Frontiers in Pharmacology. 11, 356 (2020).
- Song, L. K., et al. Targeted overexpression of alpha-synuclein by rAAV2/1 vectors induces progressive nigrostriatal degeneration and increases vulnerability to MPTP in mouse. PLoS One. 10 (6), 0131281 (2015).
- Theodore, S., Cao, S., McLean, P. J., Standaert, D. G. Targeted overexpression of human alpha-synuclein triggers microglial activation and an adaptive immune response in a mouse model of Parkinson disease. Journal of Neuropathology and Experimental Neurology. 67 (12), 1149-1158 (2008).
- Sanchez-Guajardo, V., Annibali, A., Jensen, P. H., Romero-Ramos, M. alpha-Synuclein vaccination prevents the accumulation of parkinson disease-like pathologic inclusions in striatum in association with regulatory T cell recruitment in a rat model. Journal of Neuropathology and Experimental Neurology. 72 (7), 624-645 (2013).
- Sanchez-Guajardo, V., Febbraro, F., Kirik, D., Romero-Ramos, M. Microglia acquire distinct activation profiles depending on the degree of alpha-synuclein neuropathology in a rAAV based model of Parkinson’s disease. PLoS One. 5 (1), 8784 (2010).
- Oliveras-Salva, M., et al. rAAV2/7 vector-mediated overexpression of alpha-synuclein in mouse substantia nigra induces protein aggregation and progressive dose-dependent neurodegeneration. Molecular Neurodegeneration. 8, 44 (2013).
- Cho, C., et al. Evaluating analgesic efficacy and administration route following craniotomy in mice using the grimace scale. Scientific Reports. 9 (1), 359 (2019).
- Flecknell, P. . Laboratory Animal Anaesthesia. 3rd Ed. , (2009).
- Bind, R. H., Minney, S. M., Rosenfeld, S., Hallock, R. M. The role of pheromonal responses in rodent behavior: Future directions for the development of laboratory protocols. Journal of the American Association for Laboratory Animal Science. 52 (2), 124-129 (2013).
- Paxinos, G., Franklin, K. B. J. . The Mouse Brain in Stereotaxic Coordinates. , (2001).
- Elgueta, D., et al. Dopamine receptor D3 expression is altered in CD4+ T-cells from Parkinson’s disease patients and its pharmacologic inhibition attenuates the motor impairment in a mouse model. Frontiers in Immunology. 10, 981 (2019).
- Gage, G. J., Kipke, D. R., Shain, W. Whole animal perfusion fixation for rodents. Journal of Visualized Experiments. (65), e3564 (2012).
- Fernandez-Suarez, D., et al. The monoacylglycerol lipase inhibitor JZL184 is neuroprotective and alters glial cell phenotype in the chronic MPTP mouse model. Neurobiology of Aging. 35 (11), 2603-2616 (2014).
- Elgueta, D., et al. Pharmacologic antagonism of dopamine receptor D3 attenuates neurodegeneration and motor impairment in a mouse model of Parkinson’s disease. Neuropharmacology. 113, 110-123 (2017).
- Montoya, A., et al. Dopamine receptor D3 signalling in astrocytes promotes neuroinflammation. Journal of Neuroinflammation. 16 (1), 258 (2019).
- Williams, G. P., et al. Targeting of the class II transactivator attenuates inflammation and neurodegeneration in an alpha-synuclein model of Parkinson’s disease. Journal of Neuroinflammation. 15 (1), 244 (2018).
- Benskey, M. J., et al. Silencing alpha synuclein in mature nigral neurons results in rapid neuroinflammation and subsequent toxicity. Frontiers in Molecular Neuroscience. 11, 36 (2018).
- Rieker, C., et al. Neuropathology in mice expressing mouse alpha-synuclein. PLoS One. 6 (9), 24834 (2011).
- Harms, A. S., et al. alpha-Synuclein fibrils recruit peripheral immune cells in the rat brain prior to neurodegeneration. Acta Neuropathologica Communications. 5 (1), 85 (2017).
- Williams, G. P., et al. CD4 T cells mediate brain inflammation and neurodegeneration in a mouse model of Parkinson disease. Brain. 144 (7), 2047-2059 (2021).
- Matheoud, D., et al. Intestinal infection triggers Parkinson’s disease-like symptoms in Pink1(-/-) mice. Nature. 571 (7766), 565-569 (2019).
- Jan, A., Goncalves, N. P., Vaegter, C. B., Jensen, P. H., Ferreira, N. The prion-like spreading of alpha-synuclein in Parkinson’s disease: Update on models and hypotheses. International Journal of Molecular Sciences. 22 (15), 8338 (2021).
- Chesselet, M. F., et al. A progressive mouse model of Parkinson’s disease: The Thy1-aSyn ("Line 61") mice. Neurotherapeutics. 9 (2), 297-314 (2012).
- Sampson, T. R., et al. Gut microbiota regulate motor deficits and neuroinflammation in a model of Parkinson’s disease. Cell. 167 (6), 1469-1480 (2016).
- Ciron, C., et al. Human alpha-iduronidase gene transfer mediated by adeno-associated virus types 1, 2, and 5 in the brain of nonhuman primates: Vector diffusion and biodistribution. Human Gene Therapy. 20 (4), 350-360 (2009).
- Ben-Shaanan, T. L., et al. Activation of the reward system boosts innate and adaptive immunity. Nature Medicine. 22 (8), 940-944 (2016).
- Albert, K., Voutilainen, M. H., Domanskyi, A., Airavaara, M. AAV vector-mediated gene delivery to substantia nigra dopamine neurons: Implications for gene therapy and disease models. Genes. 8 (2), 63 (2017).
- Bordia, T., Perez, X. A., Heiss, J., Zhang, D., Quik, M. Optogenetic activation of striatal cholinergic interneurons regulates L-dopa-induced dyskinesias. Neurobiology of Disease. 91, 47-58 (2016).
- Kim, A., et al. Upgraded methodology for the development of early diagnosis of Parkinson’s disease based on searching blood markers in patients and experimental models. Molecular Neurobiology. 56 (5), 3437-3450 (2018).
- Lei, H., et al. Parkinson’s disease diagnosis via joint learning from multiple modalities and relations. IEEE Journal of Biomedical and Health Informatics. 23 (4), 1437-1449 (2018).

