Analysera Parkinsons sjukdom musmodell inducerad av adenoassocierade virala vektorer som kodar för humant α-synuklein
Summary
Detta arbete analyserar vektordosen och exponeringstiden som krävs för att inducera neuroinflammation, neurodegeneration och motorisk försämring i denna prekliniska modell av Parkinsons sjukdom. Dessa vektorer som kodar för den mänskliga α-synuklein levereras till substantia nigra för att rekapitulera synukleinpatologin associerad med Parkinsons sjukdom.
Abstract
Parkinsons sjukdom är en neurodegenerativ sjukdom som involverar döden av de dopaminerga neuronerna i den nigrostriatala vägen och följaktligen den progressiva förlusten av kontroll över frivilliga rörelser. Denna neurodegenerativa process utlöses av avsättningen av proteinaggregat i hjärnan, vilka huvudsakligen består av α-synuklein. Flera studier har visat att neuroinflammation krävs för att utveckla neurodegenerationen i samband med Parkinsons sjukdom. I synnerhet involverar den neuroinflammatoriska processen mikroglial aktivering samt infiltration av perifera T-celler i substantia nigra (SN). Detta arbete analyserar en musmodell av Parkinsons sjukdom som rekapitulerar mikroglial aktivering, T-cellinfiltration i SN, neurodegeneration av nigral dopaminerga neuroner och motorisk försämring. Denna musmodell av Parkinsons sjukdom induceras av stereotaxisk leverans av adenoassocierade virusvektorer som kodar för den mänskliga vildtypen α-synuklein (AAV-hαSyn) i SN. Korrekt leverans av virala vektorer till SN bekräftades med hjälp av kontrollvektorer som kodar för grönt fluorescerande protein (GFP). Därefter utvärderades hur dosen av AAV-hαSyn administrerad i SN påverkade omfattningen av hαSyn-uttryck, förlusten av nigral dopaminerga neuroner och motorisk försämring. Dessutom bestämdes dynamiken i hαSyn-uttryck, mikroglial aktivering och T-cellinfiltration under hela sjukdomsutvecklingen. Således ger denna studie kritiska tidpunkter som kan vara användbara för att rikta in sig på synukleinpatologi och neuroinflammation i denna prekliniska modell av Parkinsons sjukdom.
Introduction
Efter Alzheimers sjukdom är Parkinsons sjukdom den näst vanligaste neurodegenerativa sjukdomen i världen. De primära nervcellerna som påverkas vid Parkinsons sjukdom är de av den nigrostriatala vägen, som producerar dopamin och kontrollerar frivillig rörelse. Som en konsekvens är det mest karakteristiska symptomet i samband med denna sjukdom motorisk försämring. Denna patologi innefattar också avsättning av proteinaggregat i hjärnan, som huvudsakligen består av α-synuklein (aSyn)1, ett cytosoliskt protein associerat med presynaptiska terminaler. Bevis har visat att genereringen av patogena inklusioner av αSyn utlöses av felveckning eller av vissa post-translationella modifieringar av detta protein2.
I synnerhet har ett nära samband etablerats mellan αSyn-patologi och förlusten av dopaminerga neuroner i den nigrostriatala vägen i human Parkinsons sjukdom och djurmodeller 3,4. Att förstå hur αSyn-aggregat genereras och hur de inducerar neuronal död utgör en betydande utmaning inom området. En växande grupp studier har visat att mitokondriell dysfunktion är en av de främsta orsakerna till genereringen av αSyn-aggregat2 genom att öka oxidativ stress. Faktum är att flera gener associerade med Parkinsons sjukdom riskerar proteiner som är involverade i mitokondriell funktion, morfologi och dynamik 5,6. Dessutom utgör lysosomal dysfunktion, som resulterar i ackumulering av dysfunktionella mitokondrier och felveckad αSyn, en annan viktig händelse som främjar genereringen av αSyn-aggregat7.
Nya bevis har indikerat att när αSyn-aggregat deponeras i hjärnan stimulerar dessa patogena proteiner tollliknande receptorer (TLR) på mikroglia, vilket utlöser mikroglial aktivering och en initial inflammatorisk miljö i substantia nigra (SN)8,9. Dessutom indikerar bevisen att αSyn-aggregat fångas upp och presenteras av antigenpresenterande celler till T-celler, vilket inducerar ett adaptivt immunsvar specifikt för αSyn10,11. Dessa αSyn-specifika T-celler infiltrerar därefter hjärnan och restimuleras av aktiverad mikroglia, vilket främjar utsöndringen av neurotoxiska faktorer som framkallar neuronal död 9,10. Intressant nog har flera bevislinjer föreslagit att αSyn-aggregat genereras först i det enteriska nervsystemet och sedan transporteras genom vagusnerven till hjärnstammen12.
Flera djurmodeller av Parkinsons sjukdom har använts i många år, inklusive de som induceras genom administrering av neurotoxiska ämnen (dvs. 6-hydroxidopin, parakvat, rotenon, 1-metyl-4-fenyl-1,2,3,6-tetrahydropyridin) och de som involverar genetiska tillstånd (dvs. mutant α-synuklein, mutant leucinrikt upprepat kinas 2)13 . Trots modeller som involverar neurotoxininducerad neurodegeneration som replikerar vissa aspekter av Parkinsons sjukdom, rekapitulerar ingen av dem alla väsentliga aspekter av sjukdomen eller är inte progressiva13. Å andra sidan, även om genetiska musmodeller som involverar uttryck av mutanta versioner av leucinrika upprepa kinas 2, mutanta versioner av α-synuklein eller överuttrycket av human vildtyp α-synuklein resulterar i motorisk försämring och i vissa fall också utvecklingen av synukleinopati, reproducerar de inte framträdande neurodegenerering av de nigrala dopaminerga neuronerna, vilket är en väsentlig aspekt av Parkinsons sjukdom13, 14. En tredje typ av djurmodell av neurodegeneration har lyckats uppfylla de flesta av de väsentliga aspekterna av Parkinsons sjukdom, stereotaxisk leverans av adenoassocierade virusvektorer (AAV) som kodar för den mänskliga α-synuklein (AAV-hαSyn)14,15. Viktigt är att AAV tillåter transduktion av neuroner med hög effekt och på lång sikt i den vuxna hjärnan hos däggdjur. Dessutom har stereotaxisk leverans av AAV-hαSyn i SN visat sig reproducera många av de väsentliga aspekterna av sjukdomen, inklusive αSyn-patologi, mikroglial aktivering, neurodegeneration och motorisk försämring 16,17,18,19,20. Denna studie presenterar en analys av hur dosen av viral vektor och tiden efter viral vektorleverans påverkar omfattningen av hαSyn-uttryck, neurodegeneration och neuroinflammation i den nigrostriatala vägen, liksom graden av motorisk försämring i musmodellen för ensidig stereotaxisk leverans av hαSyn i SN.
Protocol
Representative Results
Discussion
Musmodellen för neurodegeneration som analyseras här kan hjälpa till att studera många kritiska aspekter som är involverade i patofysiologin vid Parkinsons sjukdom, inklusive mekanismerna som är involverade i αSyn-patologi och mikroglial aktivering, involveringen av det perifera immunsystemet i regleringen av neuroinflammation och mekanismerna för neurodegeneration. Bland de mekanismer som är involverade i αSyn-patologi är de subcellulära mekanismerna associerade med mitokondriell, lysosomal eller proteasomal dysfunktion i närvaro av en överdriven belastning av αSyn i de dopaminerga neuronerna iSN2. Det är viktigt att tänka på att förutom hαSyn-uttrycket inducerat av AAV-medierad transduktion bidrar den endogena musen αSyn också till belastningen av totalt aSyn-uttryck. Transgena möss som överuttrycker mus αSyn utvecklar liknande synukleinpatologi, neuropatologi och motorisk försämring som dessa musmodeller baserat på överuttrycket av hαSyn32. När det gäller mikroglial aktivering kan den nuvarande musmodellen användas för att studera hur olika molekylära och cellulära spelare såsom cytokiner, neurotransmittorer, astrocyter, neuroner, blod-hjärnbarriären och T-celler kan reglera förvärvet av proinflammatoriska eller antiinflammatoriska funktionella fenotyper 8,10,11 . Denna modell utgör också ett viktigt verktyg för att studera det perifera immunsystemets roll, inklusive inte bara T-celler utan även makrofager, monocyter och neutrofiler, på processerna för neuroinflammation och neurodegenerering av nigralneuroner 11,33,34. Slutligen representerar denna musmodell också ett värdefullt system för att studera de cellulära och molekylära mekanismerna för neurodegeneration in vivo, inklusive de som induceras av interna cellulära processer, såsom oxidativ stress, energiunderskott och skadade organeller 2, eller de som utövas av externa aktörer, såsom neurotoxiska faktorer som produceras av mikrogliaceller, astrocyter och cytotoxiska T-celler8, 28,29,35.
En begränsning av denna musmodell är studien av hur den patologiska aggregeringen av αSyn på extra-cerebrala platser kan utgöra de inledande stadierna i utvecklingen av Parkinsons sjukdom36. I detta avseende finns det växande bevis som tyder på att αSyn-patologin börjar i tarmslemhinnan och luktepitelet36 och förmodligen det αSyn-specifika T-cellsvaret12 före neurodegenerationen av nigralneuroner och motorisk försämring. Efteråt skulle αSyn-aggregat migrera genom vagusnerven till hjärnstammen, vilket utlöser neuroinflammation och neurodegeneration av dopaminerga neuroner12. Även om AAV-hαSyn-modellen rekapitulerar de flesta aspekter av Parkinsons sjukdom, finns det ingen uppenbar inblandning av den patologiska aggregeringen av αSyn på extra-cerebrala platser i denna modell. En alternativ modell som involverar hαSyn-patologi som är lämplig för att studera dessa aspekter av Parkinsons sjukdom kan vara transgena möss som överuttrycker hαSyn under kontroll av Thy1-promotorn, Thy1-SNCA-modellen 37, där sjukdomsutvecklingen är beroende av tarmmikrobiotan och innebär en uppenbar gastrointestinal försämring38.
Även om det är till hjälp för studien av de olika processerna som är associerade med patofysiologin vid Parkinsons sjukdom, innebär den nuvarande musmodellen kritiska steg som bör kontrolleras noggrant, inklusive korrekt leverans av virusvektorerna i motsvarande rumsliga koordinater, det selektiva uttrycket av hαSyn i neuroner (vilket beror på AAV-serotypen och vektorkonstruktionen), och rätt AAV-dos och timing innan du analyserar den parkinsoniska fenotypen. Analysen av korrekt leverans av virusvektorerna i SN är nödvändig, eftersom användningen av de korrekta rumsliga koordinaterna för SN kanske inte räcker när nålen inte är helt rak, vilket ibland är omärkligt för det mänskliga ögat. Dessutom beror diffusionen av AAV-vektorerna på AAV-serotyp39. Av dessa skäl är det nödvändigt att utföra regelbundna kvalitetskontroller för att kontrollera korrekt leverans och diffusion av de injicerade AAV-GFP-vektorerna efter observation av GFP i hjärnskivor som innehåller SN-området.
När det gäller det selektiva uttrycket av hαSyn i neuroner kan uttrycket av hαSyn i princip konstrueras för att styras av en promotor selektiv för neuroner eller, ännu mer exakt, selektiv för dopaminerga neuroner, såsom användningen av TH-promotorn i AAV-vektorer för att inducera det selektiva uttrycket av gener i dopaminerga neuroner40 . Denna strategi fungerar dock inte när det som eftersträvas är överuttryck av genen av intresse. Av denna anledning är det i den nuvarande modellen viktigt att använda en stark promotor (en promotor som inducerar högt uttryck av nedströmsgenen) och AAV-serotyper med neuronal tropism. I denna studie användes CBA-promotorn som en stark promotor för att inducera överuttryck av hαSyn, och AAV5-serotypen användes för virusvektorn. Denna serotyp har använts tidigare för att transducera mus- och råttneuroner41,42. Här visade resultaten att 12 veckor efter leveransen av AAV5-GFP i SN hos möss var den gröna fluorescensen selektivt närvarande på ipsilateralsidan av både SN och striatum (Figur 1), vilket indikerar effektiv transduktion av neuroner i den nigrostriatala vägen.
En annan kritisk aspekt av denna musmodell av Parkinsons sjukdom är den tidpunkt som krävs för att analysera en viss process efter operationen. I detta avseende visar detta arbete en kinetisk studie av olika processer som är involverade i patologin. Eftersom viktiga tidpunkter förändras med dosen av virala genom som ges per mus, den serotyp av AAV som används, eller till och med med den sats AAV som används, utfördes först en dos-responsanalys av mängden AAV-αSyn som krävs för att inducera en signifikant förlust av TH + -neuroner och motorisk försämring. Tidigare studier har visat signifikant motorisk försämring och en förlust av TH+ neuroner i nigrostriatalvägen efter 12 veckors AAV-αSyn-injektioner hos möss i doser från 6 x 108–3 x 1010 virala genom per mus 16,17,30,31. Följaktligen varierade dosen av AAV-hαSyn som användes för att inducera hαSyn-uttrycket i den nigrostriatala vägen, förlusten av TH + -neuroner och motorisk försämring hos möss från 1 x 108–1 x 1010 virala genom per mus. För att kontrollera att förlusten av TH + -neuroner och motorisk försämring inducerades av överuttrycket av hαSyn i SN och inte av AAV-infektion av neuroner i SN, inkluderades kontrollgrupper där AAV-kodning för en reportergen (AAV-eGFP) levererades ensidigt i SN hos möss och neurodegeneration och motorisk försämring bestämdes. Resultaten visade att 1 x10 10 virusgenom per mus 12 veckor efter stereotaxisk kirurgi var en korrekt dos av AAV5-hαSyn, eftersom möss som fick denna virusbelastning visade signifikant hαSyn i den nigrostriatala vägen (figur 2 och figur 3), förlust av TH + -neuroner (figur 4) och motorisk försämring (figur 5). Däremot var lägre doser av AAV5-hαSyn (1 x 108 virala genom per mus och 1 x 109 virala genom per mus) inte tillräckligt starka för att nå signifikanta förändringar i alla dessa parametrar tillsammans (figur 2–4). Observera att administreringen av AAV-GFP vid 1 x 1010 virala genom per mus inducerade en låg (~ 20%), men signifikant grad av förlust av TH + -neuroner av nigral dopaminerga neuroner (Figur 4A, B). Detta resultat överensstämmer med tidigare observationer med denna modell41 och är förmodligen konsekvensen av en låg nivå av neuroinflammation inducerad av administrering av AAV-vektorer i SN. Ändå var omfattningen av förlusten av TH+ neuroner signifikant högre hos möss som fick AAV5-hαSyn jämfört med dem som fick samma dos av AAV-GFP (figur 4C). Observera att kinetiken för hαSyn-uttryck inte bara beror på transduktionens effektivitet utan också på omfattningen av AAV-diffusion39. Eftersom AAV-diffusion beror på AAV-serotypen kan de exakta nyckeltidpunkterna i denna djurmodell variera när man använder en annan AAV-serotyp som skiljer sig från AAV5.
Därefter genomfördes en kinetisk analys med 1 x 1010 virala genom per mus för att bestämma viktiga tidpunkter i denna musmodell. Eftersom nuvarande bevis har visat några tidiga symtom som uppträder före motorisk försämring, vilket skulle möjliggöra tidig diagnos av Parkinsons sjukdom43,44, försökte dessa experiment hitta den tidpunkt då hαSyn-uttrycket redan var uppenbart men i avsaknad av motorisk försämring. Resultaten visar att uppkomsten av hαSyn-uttryck i SN var 5 veckor efter stereotaxisk leverans av AAV-hαSyn (figur 6). Denna tidpunkt utgör en intressant tidspunkt för att börja administrera terapier skräddarsydda för att stoppa de neuroinflammatoriska och neurodegenerativa processerna. Andra viktiga tidpunkter som bestämdes här var topptiderna för två kritiska händelser associerade med neuroinflammationsprocessen: den tid då mikroglia når maximal aktiveringsgrad och tiden för maximal T-cellinfiltration i SN. Resultaten visade en kurva med en trend som nådde två vågor av maximal mikroglial aktivering, den första vid 10 veckor efter operationen och den andra vid 15 veckor efter operationen (figur 7). Den kinetiska analysen av T-cellsinfiltration visade topptiden för Treg-infiltration i SN vid 11 veckor efter stereotaxisk operation (figur 8). Överraskande nog upptäcktes inga effektor T-celler (CD4 + Foxp3-) som infiltrerade SN under den analyserade tidsramen (vecka 8–13 efter operationen). Sammantaget föreslår dessa resultat en lämplig tidsram för att börja administrera terapier inriktade på att stoppa processen med neuroinflammation och dämpa T-cellinfiltration i SN med hjälp av denna prekliniska modell, som sträcker sig mellan vecka 5 efter operationen (uppkomsten av hαSyn-överuttryck) och vecka 10 efter operationen (den första vågen av neuroinflammation och T-cellinfiltration) (Figur 9).
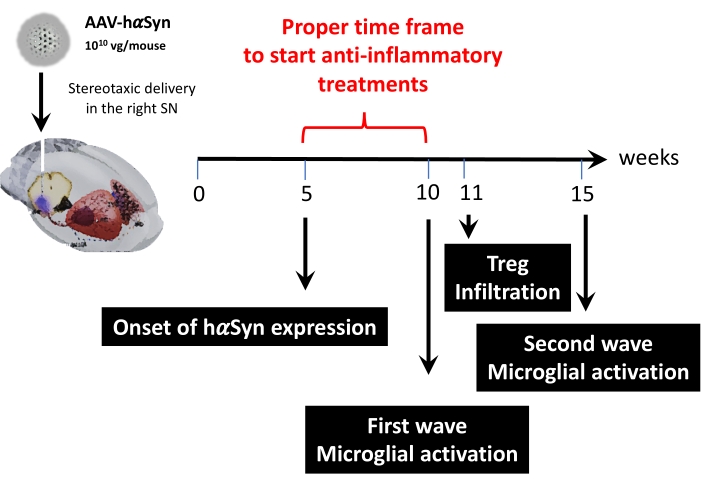
Figur 9: Sammanfattning av de viktigaste tidpunkterna som hittades för denna djurmodell.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi tackar Dr. Sebastián Valenzuela och Dr. Micaela Ricca för deras värdefulla veterinärhjälp i vår djuranläggning. Detta arbete stöddes av “Financiamiento Basal para Centros Científicos y Tecnológicos de Excelencia de ANID” Centro Ciencia & Vida, FB210008 (till Fundación Ciencia & Vida) och Geroscience Center for Brain Health and Metabolism, FONDAP-15150012. Detta arbete finansierades också av bidrag FONDECYT-1210013 (till R.P.) och FONDECYT-1150766 (till F.C.) från “Agencia Nacional de Investigación y Desarrollo de Chile (ANID)” och MJFF-10332.01 (till R.P.) och MJFF-17303 (till F.C.) från Michael J Fox Foundation for Parkinson’s Research.
Materials
| ANIMALS AND ANIMAL FOOD | |||
| Foxp3-GFP C57BL/6 mice | The Jackson Laboratory (Bar Harbor, ME) | Stock No: 023800 | |
| Laboratory Rodent Diet | LabDiet | Rodent Diet 5001 | Standard Rodent diet |
| Wild-type C57BL/6 mice | The Jackson Laboratory (Bar Harbor, ME) | Stock No: 000664 | |
| VIRAL VECTORS | |||
| AAV5-CBA-αSyn | University of Iowa Viral Vector Core Facility | N/A | Stock concentration at 10E13 vg/mL |
| AAV5-CBA-eGFP | University of Iowa Viral Vector Core Facility | N/A | Stock concentration at 9.5 x 10E12 vg/mL |
| ANESTHETICS AND ANALGESICS | |||
| Isoflurane | Baxter | 218082 | 1% for stereotaxic surgery |
| Ketamine | Drag Pharma | CHE30 | 70 mg/Kg for stereotaxic surgery |
| Sevoflurane | Baxter | VE2L9117 | For before transcardial perfusion |
| Tramadol | Drag Pharma | DPH134 | 30 mg/Kg every 24 h |
| Xylazine | Centrovet | EHL40 | 9 mg/kg for stereotaxic surgery |
| EQUIPMENT | |||
| Beam test | Home made | N/A | horizontal beam 25 cm length and 3 cm width. The beam surface was covered by a metallic grid (1 cm2). |
| Cryostate | Leica | CM1520 | |
| Digital camera | Nikon | S2800 Coolpix | For recording the beam test performance |
| Microscope | Olympus | BX51 | Used for IHC analysis (section 4.4) |
| Microscope | Olympus | IX71 | Used for IF analysis (section 5.3) |
| Microscope | Leica | DMI8 | Used for IF analysis (section 5.7) |
| New Standard Stereotaxic, mouse | Stoelting, Wood Dale, IL, USA | 51500 | stereotaxic frame for surgery |
| Peristaltic Pump | Masterflex | C-flex L/S16 | |
| Power supply unit | Olympus | U-RFL-T | Used for IF analysis (section 5.3) |
| Surgical suture | Sylkam®, B Braun | C0760171 | |
| Syringe 100 U | BD | 324918 | For anesthesia before transcardial perfusion, 29G needle |
| Syringe RN 5uL SYR W/O NEEDLE | Hamilton | HA-7641-01 | For viral vector innoculation |
| BUFFERS AND REAGENTS | |||
| Aviden, Peroxidase Conjugate | Merck, Darmstadt, Germany | 189728 | |
| Bovine Serum Albumin | Merck, Darmstadt, Germany | 9048-46-8 | |
| Cryotrotection buffer | Home made | N/A | 20% glycerine and 2% DMSO in PBS |
| DAPI | Abcam | ab228549 | |
| Diaminobenzidine | Merck, Darmstadt, Germany | D8001 | |
| Fluoromount -G T | Electron Microscopy Science | 17984-25 | |
| Gelatin | Merck, Darmstadt, Germany | 104078 | |
| Normal goat serum | Jackson ImmunoResearch Laboratory | 5000121 | |
| Paraformaldehyde | Merck, Darmstadt, Germany | 104005 | |
| PBS | Home made | N/A | 0.125 M, pH 7.4 |
| Peroxidase inactivating buffer | Home made | N/A | 0.03% H2O2 in methanol |
| Triton X-100 | Sigma-Aldrich | 9036-19-5 | |
| Trizma Hydrochloride | Merck, Darmstadt, Germany | 1185-53-1 | |
| Tween 20 | Sigma-Aldrich | 822184 | |
| ANTIBODIES | |||
| Biotin-SP (long spacer) AffiniPure Goat Anti-Rabbit IgG (H+L) | Jackson ImmunoResearch Laboratory | 111065003 | |
| Goat anti-Rabbit IgG (H+L) Alexa Fluor 546 | ThermoFisher Scientific | A11010 | |
| Goat anti-Rabbit IgG (H+L) Alexa Fluor 647 | ThermoFisher Scientific | A21244 | |
| Goat anti-Rat IgG (H+L) Alexa Fluor 546 | ThermoFisher Scientific | A11081 | |
| Rabbit monoclonal anti-alpha-Synuclein | Abcam | ab138501 | |
| Rabbit monoclonal anti-Iba-1 | Abcam | EPR16588 | |
| Rabbit polyclonal anti-Tyrosine Hydroxylase | Millipore | AB152 | |
| Rat monoclonal anti-CD4 | Biolegend | 100402 | |
| SOFTWARES | |||
| GraphPad | Prism | 6.0 | Fos stats analysis |
| ImageJ | National Institute of Health | N/A | For image analysis |
| LAS X | Leica | N/A | For image capture with Leica microscope |
| ProgRes Capture Pro | Jenoptik | N/A | For image capture with Olympus microscope |
| VLC media player | VideoLAN Organization | N/A | For analysis of behavioural tests |
References
- Braak, H., et al. Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiology of Aging. 24 (2), 197-211 (2003).
- Lim, K. L., Zhang, C. W. Molecular events underlying Parkinson’s disease – An interwoven tapestry. Frontiers in Neurology. 4, 33 (2013).
- Abdelmotilib, H., et al. α-Synuclein fibril-induced inclusion spread in rats and mice correlates with dopaminergic neurodegeneration. Neurobiology of Disease. 105, 84-98 (2017).
- Mori, F., et al. Relationship among alpha-synuclein accumulation, dopamine synthesis, and neurodegeneration in Parkinson disease substantia nigra. The Journal of Neuropathology & Experimental Neurology. 65 (8), 808-815 (2006).
- Winklhofer, K. F., Haass, C. Mitochondrial dysfunction in Parkinson’s disease. Biochimica et Biophysica Acta. 1802 (1), 29-44 (2010).
- Vazquez-Velez, G. E., Zoghbi, H. Y. Parkinson’s disease genetics and pathophysiology. Annual Review of Neuroscience. 44, 87-108 (2021).
- Dehay, B., et al. Lysosomal impairment in Parkinson’s disease. Movement Disorders. 28 (6), 725-732 (2013).
- Gonzalez, H., Elgueta, D., Montoya, A., Pacheco, R. Neuroimmune regulation of microglial activity involved in neuroinflammation and neurodegenerative diseases. Journal of Neuroimmunology. 274 (1-2), 1-13 (2014).
- Pacheco, R. T-cell based immunotherapies for Parkinson’s disease. Exploration of Neuroprotective Therapy. 1 (2), 72-85 (2021).
- Gonzalez, H., Contreras, F., Pacheco, R. Regulation of the neurodegenerative process associated to Parkinson’s disease by CD4+ T-cells. Journal of Neuroimmune Pharmacology. 10 (4), 561-575 (2015).
- Gonzalez, H., Pacheco, R. T-cell-mediated regulation of neuroinflammation involved in neurodegenerative diseases. Journal of Neuroinflammation. 11 (1), 201 (2014).
- Campos-Acuna, J., Elgueta, D., Pacheco, R. T-cell-driven inflammation as a mediator of the gut-brain axis involved in Parkinson’s disease. Frontiers in Immunology. 10, 239 (2019).
- Blesa, J., Phani, S., Jackson-Lewis, V., Przedborski, S. Classic and new animal models of Parkinson’s disease. Journal of Biomedicine and Biotechnology. 2012, 845618 (2012).
- Ulusoy, A., Decressac, M., Kirik, D., Bjorklund, A. Viral vector-mediated overexpression of alpha-synuclein as a progressive model of Parkinson’s disease. Progress in Brain Research. 184, 89-111 (2010).
- Gomez-Benito, M., et al. Modeling Parkinson’s disease with the alpha-synuclein protein. Frontiers in Pharmacology. 11, 356 (2020).
- Song, L. K., et al. Targeted overexpression of alpha-synuclein by rAAV2/1 vectors induces progressive nigrostriatal degeneration and increases vulnerability to MPTP in mouse. PLoS One. 10 (6), 0131281 (2015).
- Theodore, S., Cao, S., McLean, P. J., Standaert, D. G. Targeted overexpression of human alpha-synuclein triggers microglial activation and an adaptive immune response in a mouse model of Parkinson disease. Journal of Neuropathology and Experimental Neurology. 67 (12), 1149-1158 (2008).
- Sanchez-Guajardo, V., Annibali, A., Jensen, P. H., Romero-Ramos, M. alpha-Synuclein vaccination prevents the accumulation of parkinson disease-like pathologic inclusions in striatum in association with regulatory T cell recruitment in a rat model. Journal of Neuropathology and Experimental Neurology. 72 (7), 624-645 (2013).
- Sanchez-Guajardo, V., Febbraro, F., Kirik, D., Romero-Ramos, M. Microglia acquire distinct activation profiles depending on the degree of alpha-synuclein neuropathology in a rAAV based model of Parkinson’s disease. PLoS One. 5 (1), 8784 (2010).
- Oliveras-Salva, M., et al. rAAV2/7 vector-mediated overexpression of alpha-synuclein in mouse substantia nigra induces protein aggregation and progressive dose-dependent neurodegeneration. Molecular Neurodegeneration. 8, 44 (2013).
- Cho, C., et al. Evaluating analgesic efficacy and administration route following craniotomy in mice using the grimace scale. Scientific Reports. 9 (1), 359 (2019).
- Flecknell, P. . Laboratory Animal Anaesthesia. 3rd Ed. , (2009).
- Bind, R. H., Minney, S. M., Rosenfeld, S., Hallock, R. M. The role of pheromonal responses in rodent behavior: Future directions for the development of laboratory protocols. Journal of the American Association for Laboratory Animal Science. 52 (2), 124-129 (2013).
- Paxinos, G., Franklin, K. B. J. . The Mouse Brain in Stereotaxic Coordinates. , (2001).
- Elgueta, D., et al. Dopamine receptor D3 expression is altered in CD4+ T-cells from Parkinson’s disease patients and its pharmacologic inhibition attenuates the motor impairment in a mouse model. Frontiers in Immunology. 10, 981 (2019).
- Gage, G. J., Kipke, D. R., Shain, W. Whole animal perfusion fixation for rodents. Journal of Visualized Experiments. (65), e3564 (2012).
- Fernandez-Suarez, D., et al. The monoacylglycerol lipase inhibitor JZL184 is neuroprotective and alters glial cell phenotype in the chronic MPTP mouse model. Neurobiology of Aging. 35 (11), 2603-2616 (2014).
- Elgueta, D., et al. Pharmacologic antagonism of dopamine receptor D3 attenuates neurodegeneration and motor impairment in a mouse model of Parkinson’s disease. Neuropharmacology. 113, 110-123 (2017).
- Montoya, A., et al. Dopamine receptor D3 signalling in astrocytes promotes neuroinflammation. Journal of Neuroinflammation. 16 (1), 258 (2019).
- Williams, G. P., et al. Targeting of the class II transactivator attenuates inflammation and neurodegeneration in an alpha-synuclein model of Parkinson’s disease. Journal of Neuroinflammation. 15 (1), 244 (2018).
- Benskey, M. J., et al. Silencing alpha synuclein in mature nigral neurons results in rapid neuroinflammation and subsequent toxicity. Frontiers in Molecular Neuroscience. 11, 36 (2018).
- Rieker, C., et al. Neuropathology in mice expressing mouse alpha-synuclein. PLoS One. 6 (9), 24834 (2011).
- Harms, A. S., et al. alpha-Synuclein fibrils recruit peripheral immune cells in the rat brain prior to neurodegeneration. Acta Neuropathologica Communications. 5 (1), 85 (2017).
- Williams, G. P., et al. CD4 T cells mediate brain inflammation and neurodegeneration in a mouse model of Parkinson disease. Brain. 144 (7), 2047-2059 (2021).
- Matheoud, D., et al. Intestinal infection triggers Parkinson’s disease-like symptoms in Pink1(-/-) mice. Nature. 571 (7766), 565-569 (2019).
- Jan, A., Goncalves, N. P., Vaegter, C. B., Jensen, P. H., Ferreira, N. The prion-like spreading of alpha-synuclein in Parkinson’s disease: Update on models and hypotheses. International Journal of Molecular Sciences. 22 (15), 8338 (2021).
- Chesselet, M. F., et al. A progressive mouse model of Parkinson’s disease: The Thy1-aSyn ("Line 61") mice. Neurotherapeutics. 9 (2), 297-314 (2012).
- Sampson, T. R., et al. Gut microbiota regulate motor deficits and neuroinflammation in a model of Parkinson’s disease. Cell. 167 (6), 1469-1480 (2016).
- Ciron, C., et al. Human alpha-iduronidase gene transfer mediated by adeno-associated virus types 1, 2, and 5 in the brain of nonhuman primates: Vector diffusion and biodistribution. Human Gene Therapy. 20 (4), 350-360 (2009).
- Ben-Shaanan, T. L., et al. Activation of the reward system boosts innate and adaptive immunity. Nature Medicine. 22 (8), 940-944 (2016).
- Albert, K., Voutilainen, M. H., Domanskyi, A., Airavaara, M. AAV vector-mediated gene delivery to substantia nigra dopamine neurons: Implications for gene therapy and disease models. Genes. 8 (2), 63 (2017).
- Bordia, T., Perez, X. A., Heiss, J., Zhang, D., Quik, M. Optogenetic activation of striatal cholinergic interneurons regulates L-dopa-induced dyskinesias. Neurobiology of Disease. 91, 47-58 (2016).
- Kim, A., et al. Upgraded methodology for the development of early diagnosis of Parkinson’s disease based on searching blood markers in patients and experimental models. Molecular Neurobiology. 56 (5), 3437-3450 (2018).
- Lei, H., et al. Parkinson’s disease diagnosis via joint learning from multiple modalities and relations. IEEE Journal of Biomedical and Health Informatics. 23 (4), 1437-1449 (2018).

