Standardisering og vedlikehold av 3D-hundeorpatiske og intestinale organoidkulturer for bruk i biomedisinsk forskning
Summary
Eksperimentelle metoder for å høste voksne stamceller fra hundens tarm- og levervev for å etablere 3D organoidkulturer beskrives. Videre diskuteres laboratorieteknikkene for å sikre konsistent vekst og gi standard driftsprosedyrer for høsting, biobank og gjenopplive hundens tarm- og leverorganoidkulturer.
Abstract
Hunder utvikler komplekse multifaktorielle sykdommer analogt med mennesker, inkludert inflammatoriske sykdommer, metabolske sykdommer og kreft. Derfor representerer de relevante store dyremodeller med translasjonspotensialet til human medisin. Organoider er 3-dimensjonale (3D), selvmonterte strukturer avledet fra stamceller som etterligner mikroanatomi og fysiologi av deres opprinnelsesorgan. Disse translasjonelle in vitro-modellene kan brukes til stoffpermeabilitet og oppdagelsesapplikasjoner, toksikologivurdering og for å gi en mekanistisk forståelse av patofysiologien til multifaktorielle kroniske sykdommer. Videre kan hundeorganoider forbedre livene til følgesvenner, gi innspill på ulike områder av veterinærforskning og legge til rette for personlige behandlingsapplikasjoner i veterinærmedisin. En liten gruppe givere kan lage en biobank av organoidprøver, noe som reduserer behovet for kontinuerlig vevshøsting, da organoide cellelinjer kan underkultureres på ubestemt tid. Heri presenteres tre protokoller som fokuserer på kulturen av tarm- og levermusinorganoider avledet fra voksne stamceller. Canine Organoid Isolation Protocol skisserer metoder for å behandle vev og innebygging av celleisolering i en støttende matrise (solubilisert ekstracellulær membranmatrise). Canine Organoid Maintenance Protocol beskriver organoid vekst og vedlikehold, inkludert rengjøring og passivring sammen med passende tidspunkt for utvidelse. Organoid Harvesting and Biobanking Protocol beskriver måter å trekke ut, fryse og bevare organoider for videre analyse.
Introduction
Gnagere er den mest brukte dyremodellen for biomedisinsk og translasjonell forskning1. De er usedvanlig nyttige for å undersøke grunnleggende molekylær patogenese av sykdommene, selv om deres kliniske relevans for kroniske multifaktorielle sykdommer nylig har blitt stilt spørsmål ved2. Hundemodellen har flere fordeler i forhold til gnagere3,4. Hunder og mennesker deler likheter i metabolomikk og tarmmikrobiom som utviklet seg på grunn av forbruk av menneskelig diett gjennom ulike perioder av domesticering5,6,7. Likheter mellom hund og human gastrointestinal anatomi og fysiologi er et annet av eksemplene8.
I tillegg deler hunder ofte lignende miljøer og livsstil med sine eiere9. Jo lengre levetid for hunder i forhold til gnagere tillater den naturlige utviklingen av mange kroniske tilstander10. Inflammatorisk tarmsykdom eller metabolsk syndrom er eksempler på multifaktorielle kroniske sykdommer som deler viktige likheter mellom mennesker og hunder11,12. Prekliniske studier av hunder som involverer hunder med naturlig forekommende sykdommer, kan generere mer pålitelige data enn de som er oppnådd fra gnagermodeller13. For å minimere bruken av levende dyreforskning og overholde prinsippene til 3Rs (Reduce, Refine, Replace)14, har det imidlertid dukket opp alternativer til in vivo-testing ved hjelp av 3D in vitro hundeorganoider15.
Organoider er selvmonterte 3D stamcelleavledede strukturer som rekapitulerer fysiologien og mikroanatomien til deres opprinnelige organer16,17. Denne teknologien ble først beskrevet av Sato et al. i 200917 og tillot mer overførbare in vitro-studier i epitelceller enn det som tidligere var mulig ved hjelp av 2D kreftcellekulturer18,19,20. Organoider er nyttige in vitro-modeller i mange biomedisinske disipliner som i preklinisk toksikologiske21,22,23, absorpsjons- eller metabolismestudier24,25,26,27,28, samt i personlige medisinske tilnærminger29,30,31 . Den vellykkede kulturen av hund intestinale organoider har blitt beskrevet for første gang i 201912, mens leverorganoider avledet fra en hund først ble rapportert av Nantasanti et al. i 201532. Canine organoider har siden blitt vellykket brukt i studier som undersøker hundens kroniske enteropatier, gastrointestinale stromale svulster, kolorektal adenokarsinom12 og Wilsons sykdom33,34.
Mens voksne stamceller kan høstes via nekropsier, krever organoidteknologien ikke alltid ofre for dyrene. Endoskopiske og laparoskopiske biopsier, eller til og med fin nål aspirater av organer35, er en levedyktig kilde til voksne stamceller for epitelial organoid isolasjon12. Utbredt bruk av slike ikke-invasive teknikker i veterinærpraksis legger til rette for alternativer for omvendt translasjonell forskning (oversettelse av informasjon fra veterinær klinisk praksis til menneskelig klinisk praksis og omvendt)15. Videreutvikling av organoid teknologi kan sikres ved standardisering av organoid kultur og vedlikeholdsmetoder. Den organoide protokollen som presenteres her er delvis basert på tidligere publisert arbeid av Saxena et al. fra 201536, og metoder ble tilpasset detaljer om hundens tarm- og leverorganoidkultur. Den generelle arbeidsflyten til hundens organoidprotokoller er avbildet i figur 1.
Canine Organoid Isolation Protocol introduserer metoder for å skaffe prøver fra endoskopisk, laparoskopisk og kirurgisk biopsi, samt nekropsier. Den skisserer den første forbehandlingen av vevsprøver og metoder som brukes til transport til laboratoriet. Materialer og reagenser som trengs for organoid isolasjon er oppsummert i avsnittet “Forberedelse for isolasjon”. Prosessen med voksen stamcelleisolasjon fra vevsprøver er nærmere beskrevet. Til slutt diskuteres prosessen med å plating organoider i kuppellignende strukturer ved hjelp av en solubilisert ekstracellulær membranmatrise.
Den andre protokollen, Canine Organoid Maintenance Protocol, beskriver metoder for å dokumentere og dyrke organoider. Medieendringer og deres frekvens diskuteres i denne delen. Videre beskrives laboratorieprosedyrene som passivring og rengjøring av cellekulturene, som er avgjørende for å sikre vellykket vedlikehold av 3D-hundorganoider. Passende passivring er et kritisk skritt i protokollen, og mulige justeringer og feilsøking av dette trinnet diskuteres videre i manuskriptet.
Den siste protokollen er Canine Organoid Harvesting and Biobanking Protocol som inneholder metoder for å forberede fullvoksne organoider for parafin-innebygging og RNA-bevaring. Metoder for organoidprøver av biobanking i lagring av flytende nitrogen er også beskrevet her. Til slutt diskuteres måtene å tine frosne prøver og støtte veksten.
Til slutt tar denne artikkelen sikte på å gi konsistente organoide kulturprosedyrer for hunder gjennom standardisering av interlaboratoriumsprotokoller. Ved å gjøre dette har manuskriptet som mål å lette reproduserbarheten av data avledet fra hundeorganoidmodeller for å øke deres relevans i translasjonell biomedisinsk forskning.
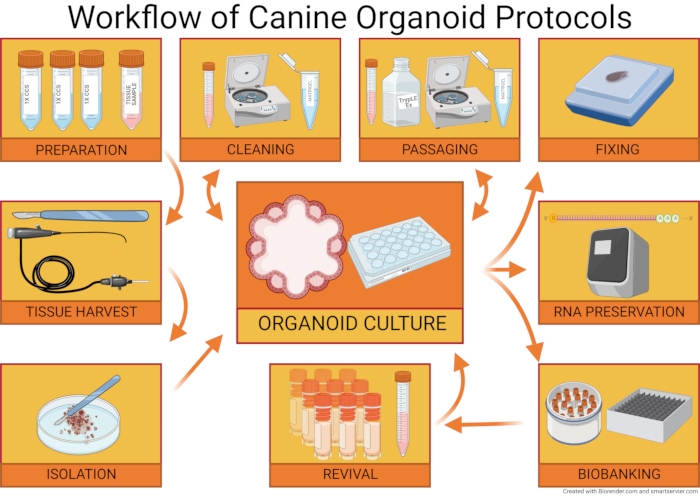
Figur 1: Arbeidsflyt av organoidprotokoller for hunder. Canine Organoid Isolation Protocol beskriver utarbeidelsen av materialene som trengs for organoid isolasjon, høsting av en vevsprøve (ved hjelp av nekropsier, endoskopisk, laparoskopisk og kirurgisk biopsi), og veiledning om celledissosiasjon og plating av den cellulære befolkningen. Canine Organoid Maintenance Protocol diskuterer rengjøring og passivring av organoidkulturen. Organoid Harvesting and Biobanking Protocol diskuterer utarbeidelse av organoidprøver for parafin-innebygging og ytterligere organoid karakterisering. Metoder for å biobank organoid kulturer og gjenopplive dem fra lagring i flytende nitrogen er også diskutert. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Det er for tiden mangel på standardiserte protokoller tilgjengelig for isolering og vedlikehold av hunde lever- og tarmorganoider. Etablering av standard driftsprosedyrer for organoidkulturer er garantert at denne modellen skal gjelde i forskjellige laboratoriemiljøer. Spesielt å gi standardiserte driftsprotokoller for kulturen til disse hundeorganoidmodellene er nøkkelen til å karakterisere organoiders normale vekst under kultur og passivisere for å utlede optimale tidspunkter for ekspansjon og vedlikehold. Canine intestinale organoider dyrket ved hjelp av protokollen har tidligere vært preget av Chandra et al.12.
Et av de mest kritiske trinnene i protokollen er passivring av organoider. Den optimale tiden for den første passasjen av leversfæroider ble fastslått å være på dag 7 etter isolasjon basert på leversfæroidmålingene. Det maksimale volumet av sfæroider ble oppnådd ved dag 7, og samtidig begynte sfæroider å knoppe og danne leverorganoider. Økningen i det totale organoidvolumet fra dag 2-7 etter isolasjon var mer enn 365 ganger, noe som tyder på at den optimale gangtiden er lengre enn hundens tarmorganoidkultur. Etter 7 dager i kulturen ble det ikke observert grove tegn på cellulær apoptose i leversfæroidet, selv uten rengjøring eller passiving (figur 7). Passaging tarm- og leverorganoider kan være utfordrende, da prosedyren kan føre til tap av celler og endret levedyktighet. Resultatene indikerer at langvarig inkubasjon av leverorganoider med trypsinlignende protease (opptil 12 min) ikke påvirker subkulturen negativt. Inkubering av organoider i trypsinlignende protease i mer enn 24 min kan være skadelig for den etterfølgende subkulturen av organoidene.
Ved suboptimal brudd i celleklyngene med den organoide passasjen, kan mekanisk dissosiasjon i stedet for langvarig inkubasjon med trypsinlignende protease være mer fordelaktig. Hvis det oppstår problemer med riktig dissosiasjon av organoidene, kan kort vortexing av prøvene forsøkes å forbedre passasjeutbyttet. På den annen side har vortexing potensial til å ødelegge en kultur og skade celler, så det bør bare brukes når andre prosedyrer har mislyktes gjentatte ganger. Å bryte leverorganoider i enkeltceller senker vekstraten til organoidene, mens det å bryte dem inn i klynger av celler i stor grad kan forbedre deres levedyktighet. Ti minutter ble valgt som inkubasjonstid for organoidprotokollen. Et 12 min inkubasjonstidspunkt ble ansett som ikke cytotoksisk sammenlignet med en 24 min inkubasjon i det trypsinlignende proteaseeksperimentet.
Overlevelseseksperimentet bekreftet at leverorganoider hos hunder kunne overleve i opptil 19,5 dager under ugunstige forhold (strukturell og ernæringsmessig uttømming). Organoider som overlevde disse forholdene lengst ble dyrket med CMGF + media. Denne observasjonen kan ha vært forårsaket av den langsommere veksten av leverorganoider i medier som ikke er supplert med rockhemmer og GSK3β. Organoidkulturer med CMGF+ R/G vokste raskere og kan ha tømt ressursene raskere. Dette eksperimentet åpner muligheter for miniatyrisering av hundens organoidkultur for å oppnå en systemkonvertering med høy gjennomstrømning. En slik teknologi viser potensialet for å legge til rette for narkotikafunn eller toksikologistudier til en betydelig redusert kostnad.
Noen vanlige problemer som oppstår under vedlikehold av hundeorganoid kultur er feil prøvestørkning når du plating, kulturforurensning, og etablere riktig tetthet og størrelse på organoidene. Hvis solubilisert ECM størkner for tidlig under plating, legg den straks på is i 10 minutter. Hvis solubilized ECM ikke danner kuppellignende strukturer, er det sannsynlig at ikke nok medier ble fjernet fra prøven. Hvis dette er tilfelle, fortynn prøven med en mer solubilisert ECM til kupler dannes.
Når sopp- eller bakteriekontaminering finnes i en hel plate (se figur 4), er den beste løsningen å kaste platen. Behandling med antifungale eller antibiotikamedisiner kan forsøkes, men suksessen til et slikt forsøk er ekstremt lav. Hvis en enkelt brønn er forurenset i en plate, kan levedyktige og upåvirkede brønner rengjøres (følg trinn 4.1 til 4.5) til en ny plate og overvåkes nøye. Hvis prøven allerede er nødfrossen, anbefales det å kaste hele prøven, da opptining av prøven utsetter inkubatoren for ytterligere forurensningsrisiko.
Sunn organoid kultur bør være minst i kategorien middels størrelse og middels tetthet eller større. Optimal tetthet er avgjørende for organoid kulturvekst. Lavere tetthet må korrigeres ved å rengjøre organoidene til middels tetthet. Hvis situasjonen med ekstrem tetthet oppstår (overbefolkning), bør organoidene utvides til flere brønner. Grove tegn på cellulær apoptose følger ofte både overbefolkning og lav tetthet av organoidkulturen. Hvis disse problemene ikke korrigeres i tide, vil hele organoidkulturen bli apoptotisk om noen dager. Hvis organoider oppnår ekstra stor størrelse eller svært høy tetthet, bør kulturen brukes til et eksperiment, frysing eller fiksering.
De organoide mediene inneholder for tiden 17 komponenter, og tilsetningen av vekstfaktorer som trengs for organoid vedlikehold og ekspansjon kan derfor være dyrt. Dette problemet kan løses ved å vokse 2D-cellekulturer som syntetiserer vekstfaktorene for å produsere betinget CMGF +. Cellekulturen L-WRN produserer vekstfaktorene Wnt-3a, R-Spondin-3 og Noggin37. Cellekolonien bruker 90% DMEM / F12 og 10% FBS kulturmedier. Når kulturen oppnår 90 prosent samløp, høstes media hver dag i 1 uke. De høstede mediene blandes deretter med 2x CMGF + (uten disse vekstfaktorene). Mens 2D-kulturer kan produsere de nødvendige vekstfaktorene til en brøkdel av kostnaden, må det forventes ekstra tid og forberedelser til å produsere media. Konsentrasjoner av vekstfaktorer mellom betingede mediepartier kan også variere fra 37,38.
Canine voksen stamcelle-avledede organoidkulturer er en unik biomedisinsk modell som kan bidra til å nå målene til One Health Initiative39. Den organoide teknologien kan brukes på mange grunnleggende og biomedisinske forskningsområder, som spenner fra utviklingsbiologi, patofysiologi, legemiddeloppdagelse og testing, toksikologi til studiet av smittsomme sykdommer og regenerativ medisin40. Translasjonell og omvendt translasjonell forskning er begge områder der hundeorganoider gjelder15. Hunder har blitt brukt i århundrer i translasjonelle eksperimentelle omgivelser, og deres følgesvenn dyrestatus har også lagt til rette for sin posisjon som en av de mest utforskede artene i veterinærmedisin.
Til slutt gir dette manuskriptet standardiserte driftsprotokoller for isolasjon, vedlikehold, høsting og biobanking av hundehjerne- og tarmorganoider for å lette anvendelsen av denne modellen i ulike biomedisinske felt. Denne modellen er unikt egnet til å fremme omvendt translasjonell forskning som et verktøy for One Health Initiative for å fremme den inter- og intradisiplinære kunnskapsdelingen.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne ønsker å uttrykke takknemlighet til ansatte ved Veterinary Diagnostic Laboratory of Iowa State University, nemlig Haley M. Lambert, Emily Rahe, Rosalyn M. Branaman, Victoria J. Green og Jennifer M. Groeltz-Thrush, for rettidig behandling av prøvene som tilbys. Forfatterne ønsker å anerkjenne støtte fra fakultetets oppstart, ISU VPR Miller Award, ISU VPR Miller Award og NSF SBIR underpris til ISU # 1912948.
Materials
| Chelating solution | |||
| D-Sorbitol | Fisher Chemical | BP439-500 | |
| DTT | Promega | V3151 | |
| KCl | Fisher Chemical | P217-500 | |
| KH2PO4 | Sigma | P5655-100G | |
| Na2HPO4-2H2O | Sigma | S5136-100G | |
| NaCl | Fisher Chemical | S271-500 | |
| Pen Strep | Gibco | 15140-122 | |
| Sucrose | Fisher Chemical | S5-500 | |
| Organoid media | |||
| [Leu15]-Gastrin I human | Sigma | G9145-.5MG | |
| A-83-01 | PeproTech | 9094360 | |
| Advanced DMEM/F12 | Gibco | 12634-010 | |
| B27 supplement | Gibco | 17504-044 | |
| FBS | Corning | 35-010-CV | |
| Glutamax | Gibco | 35050-061 | |
| HEPES | VWR Life Science | J848-500ML | |
| Human R-Spondin-1 | PeproTech | 120-38-500UG | |
| Murine EGF | PeproTech | 315-09-1MG | |
| Murine Noggin | PeproTech | 250-38-250UG | |
| Murine Wnt-3a | PeproTech | 315-20-10UG | |
| N2 supplement | Gibco | 17502-048 | |
| N-Acetyl-L-cysteine | Sigma | A9165-25G | |
| Nicotinamide | Sigma | N0636-100G | |
| Primocin | InvivoGen | ant-pm-1 | |
| ROCK inhibitor (Y-27632) | EMD Millipore Corp. | SCM 075 | |
| SB202190 (P38 inhibitor) | Sigma | S7067-25MG | |
| Stemolecule CHIR99021 (GSK3β) | Reprocell | 04-0004-base | |
| Trimethoprim | Sigma | T7883-5G | |
| Sulfamethoxazole | Sigma-Aldrich | S7507-10G | |
| Reagents | |||
| Acetic Acid, Glacial | Fisher Chemical | A38-500 | |
| Dimethyl Sulfoxide (DMSO) | Fisher Chemicals | D128-500 | |
| EDTA, pH 8.0, 0.5 M | Invitrogen | 15575-038 | |
| Formaldehyde (37%) | Fisher Chemical | F79P-4 | |
| Glutaraldehyde solution | Sigma | G5882 | |
| Matrigel Matrix For Organoid Culture | Corning | 356255 | Extracellular Membrane Matrix |
| Paraformaldehyde, 97% | Alfa Aesar | A11313 | |
| PBS, 1X (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| PBS, 1X (Phosphate-Buffered Saline) | Corning | 21-040-CM | |
| RNAlater Soln. | Invitrogen | AM7021 | RNA Storage Reagent |
| TrypLE Express | Gibco | 12604-021 | Trypsin-like Protease |
| 기타 | |||
| 6 Well Cell Culture Plate | Corning | 3516 | |
| ACD Hybez II Hybridization System | ACD a biotechne brand | 321710 | |
| Centrifuge Tube, 15 mL | Corning | 430766 | |
| CoolCell LX | Corning | BCS-405MC | |
| Cryogenic Vials | Corning | 430488 | |
| Disposable Centrifuge Tube (50 mL) | Fisherbrand | 05-539-13 | |
| GyroMini Nutating mixer (Rocker) | Labnet | S0500-230V-EU | |
| Heat Bath | Lab-Line Instruments | 3000 | |
| Mr. Frosty Freezing Container | ThermoFisher Scientific | 5100-0001 | |
| NanoDrop 2000 | ThermoFisher Scientific | ND2000CLAPTOP | SpectrophotometerAnalysis |
| Panasonic incubator | Panasonic | MCO-170ML-PA | |
| Parafilm M Wrapping Film | Bemis Company Inc | PM996/EMD | Laboratory Flexible Film Tape |
| Protected Disposable Scalpels | Bard-Parker | 239844 | |
| RNAscope 2.5 HD Assay – RED | ACD a biotechne brand | 322350 | |
| RNAscope H2O2 & Protease Plus Reagents | ACD a biotechne brand | 322330 | |
| RNAscope Target Retrieval Reagents | ACD a biotechne brand | 322000 | |
| RNAscope Wash Buffer Reagents | ACD a biotechne brand | 310091 | |
| Tissue Culture Dish | Dot Scientific | 6676621 | |
| Tissue Culture Plate 24 wells | Fisherbrand | FB012929 |
References
- Hickman, D. L., Johnson, J., Vemulapalli, T. H., Crisler, J. R., Shepherd, R. Commonly used animal models. Principles of Animal Research for Graduate and Undergraduate Students. , 117-175 (2017).
- De Jong, M., Maina, T. Of mice and humans: Are they the same? – Implications in cancer translational research. Journal of Nuclear Medicine. 51 (4), 501-504 (2010).
- Cannarozzi, G., Schneider, A., Gonnet, G. A phylogenomic study of human, dog, and mouse. PLoS Computational Biology. 3 (1), 0009-0014 (2007).
- Jacob, J. A. Researchers turn to canine clinical trials to advance cancer therapies. JAMA – Journal of the American Medical Association. 315 (15), 1550-1552 (2016).
- Ziegler, A., Gonzalez, L., Blikslager, A. Large animal models: The key to translational discovery in digestive disease research. Cellular and Molecular Gastroenterology and Hepatology. 2 (6), 716-724 (2016).
- Swanson, K. S., et al. Phylogenetic and gene-centric metagenomics of the canine intestinal microbiome reveals similarities with humans and mice. ISME Journal. 5 (4), 639-649 (2011).
- Coelho, L. P., et al. Similarity of the dog and human gut microbiomes in gene content and response to diet. Microbiome. 6 (1), 72 (2018).
- Nguyen, T. L. A., Vieira-Silva, S., Liston, A., Raes, J. How informative is the mouse for human gut microbiota research. DMM Disease Models and Mechanisms. 8 (1), 1-16 (2015).
- Bontempo, V. Nutrition and health of dogs and cats: Evolution of petfood. Veterinary Research Communications. 29, 45-50 (2005).
- Allenspach, K., Gaschen, F. Canine chronic enteropathies: A review. Schweizer Archiv fur Tierheilkunde. 145 (5), 209-222 (2003).
- Tribuddharatana, T., Kongpiromchean, Y., Sribhen, K., Sribhen, C. Biochemical alterations and their relationships with the metabolic syndrome components in canine obesity. Kasetsart Journal – Natural Science. 45 (4), 622-628 (2011).
- Chandra, L., et al. Derivation of adult canine intestinal organoids for translational research in gastroenterology. BMC Biology. 17 (1), 33 (2019).
- Schaefer, K., Rensing, S., Hillen, H., Burkhardt, J. E., Germann, P. G. Is Science the only driver in species selection? An internal study to evaluate compound requirements in the minipig compared to the dog in preclinical studies. Toxicologic Pathology. 44 (3), 474-479 (2016).
- MacArthur Clark, J. The 3Rs in research: A contemporary approach to replacement, reduction and refinement. British Journal of Nutrition. 120, 1-7 (2018).
- Schneider, B., et al. Model-based reverse translation between veterinary and human medicine: The one health initiative. CPT: Pharmacometrics and Systems Pharmacology. 7 (2), 65-68 (2018).
- Lehmann, R., et al. Human organoids: A new dimension in cell biology. Molecular Biology of the Cell. 30 (10), 1129-1137 (2019).
- Sato, T., et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 459 (7244), 262-265 (2009).
- Kim, J., Koo, B. K., Knoblich, J. A. Human organoids: model systems for human biology and medicine. Nature Reviews Molecular Cell Biology. 21 (10), 571-584 (2020).
- Jensen, C., Teng, Y. Is it time to start transitioning from 2D to 3D cell culture. Frontiers in Molecular Biosciences. 7, 33 (2020).
- Ho, B. X., Pek, N. M. Q., Soh, B. S. Disease modeling using 3D organoids derived from human induced pluripotent stem cells. International Journal of Molecular Sciences. 19 (4), 936 (2018).
- Truskey, G. A. Human microphysiological systems and organoids as in vitro models for toxicological studies. Frontiers in Public Health. 6, 185 (2018).
- Caipa Garcia, A. L., Arlt, V. M., Phillips, D. H. Organoids for toxicology and genetic toxicology: applications with drugs and prospects for environmental carcinogenesis. Mutagenesis. , (2021).
- Augustyniak, J., et al. Organoids are promising tools for species-specific in vitro toxicological studies. Journal of Applied Toxicology. 39 (12), 1610-1622 (2019).
- Zietek, T., et al. Organoids to study intestinal nutrient transport, drug uptake and metabolism – Update to the human model and expansion of applications. Frontiers in Bioengineering and Biotechnology. 8, 577656 (2020).
- Zietek, T., Rath, E., Haller, D., Daniel, H. Intestinal organoids for assessing nutrient transport, sensing and incretin secretion. Scientific Reports. 5 (1), 1-10 (2015).
- Kar, S. K., et al. Organoids: a promising new in vitro platform in livestock and veterinary research. Veterinary Research. 52 (1), 1-17 (2021).
- Borcherding, D. C., et al. Sa1976 polyphenols reverse the pathologic effects of palmitic acid and high fat diet in canine enteroids. Gastroenterology. 158 (6), 486 (2020).
- Ambrosini, Y. M., et al. Recapitulation of the accessible interface of biopsy-derived canine intestinal organoids to study epithelial-luminal interactions. PLoS ONE. 15 (4), 0231423 (2020).
- Zdyrski, C., et al. Su124 homology directed repair in canine duodenal enteroids to mimic the wild-type P-glycoprotein mutation. Gastroenterology. 160 (6), 625 (2021).
- Li, Y., Tang, P., Cai, S., Peng, J., Hua, G. Organoid based personalized medicine: from bench to bedside. Cell Regeneration. 9 (1), 21 (2020).
- Kurr, L. A., Allenspach, K., Jergens, A., Mochel, J. P. Harnessing the biology of intestinal organoids to accelerate drug discovery in inflammatory bowel disease: A one health approach. The FASEB Journal. 34, 1 (2020).
- Nantasanti, S., et al. Disease modeling and gene therapy of copper storage disease in canine hepatic organoids. Stem Cell Reports. 5 (5), 895-907 (2015).
- Favier, R. P., et al. COMMD1-Deficient dogs accumulate copper in hepatocytes and provide a good model for chronic hepatitis and fibrosis. PLoS ONE. 7 (8), 42158 (2012).
- Kruitwagen, H. S., et al. Long-term survival of transplanted autologous canine liver organoids in a COMMD1-deficient dog model of metabolic liver disease. Cells. 9 (2), 410 (2020).
- Vilgelm, A. E., et al. Fine-needle aspiration-based patient-derived cancer organoids. iScience. 23 (8), 101408 (2020).
- Saxena, K., et al. Human intestinal enteroids: A new model to study human rotavirus infection, host restriction, and pathophysiology. Journal of Virology. 90 (1), 43-56 (2016).
- VanDussen, K. L., Sonnek, N. M., Stappenbeck, T. S. L-WRN conditioned medium for gastrointestinal epithelial stem cell culture shows replicable batch-to-batch activity levels across multiple research teams. Stem Cell Research. 37, 101430 (2019).
- Powell, R. H., Behnke, M. S. WRN conditioned media is sufficient for in vitro propagation of intestinal organoids from large farm and small companion animals. Biology Open. 6 (5), 698-705 (2017).
- Mackenzie, J. S., Jeggo, M. The one health approach-why is it so important. Tropical Medicine and Infectious Disease. 4 (2), 88 (2019).
- Artegiani, B., Clevers, H. Use and application of 3D-organoid technology. Human Molecular Genetics. 27 (2), 99-107 (2018).

