Screeningsassay med højt indhold til identifikation af antistofafhængige cellulære cytotoksikmodificerende forbindelser
Summary
Denne protokol præsenterer en automatiseret, billedbaseret high-throughput teknik til at identificere forbindelser, der modulerer naturligt dræbercellemedieret brystkræftcelledrab i nærvær af et terapeutisk anti-HER-2-antistof.
Abstract
Immunterapi med antigenspecifikke antistoffer eller immuncheckpoint-hæmmere har revolutioneret behandlingen af brystkræft. Brystkræftceller, der udtrykker den epidermale vækstfaktorreceptor HER2, kan målrettes af anti-HER-2-antistoffet trastuzumab. Antistofafhængig cellulær cytotoksicitet (ADCC) er en vigtig mekanisme, der er impliceret i antitumorvirkningen af HER-2. Trastuzumab bundet til kræftceller kan genkendes af Fc-receptorerne i ADCC-effektorceller (f.eks. naturlige dræberceller (NK), makrofager og granulocytter), hvilket udløser disse immuncellers cytotoksiske aktivitet, der fører til kræftcelledød. Vi satte os for at udvikle et billedbaseret assay til kvantificering af ADCC for at identificere nye ADCC-modulatorforbindelser ved screening med højt indhold. I analysen dyrkes HER2-overekspression af JIMT-1 brystkræftceller sammen med NK-92-celler i nærvær af trastuzumab, og målcelledød kvantificeres ved automatiseret mikroskopi og kvantitativ billedanalyse. Målceller skelnes fra effektorceller baseret på deres EGFP-fluorescens. Vi viser, hvordan sammensatte biblioteker kan testes i analysen for at identificere ADCC-modulatorlægemidler. Til dette formål blev en sammensat bibliotekstestplade oprettet ved hjælp af tilfældigt udvalgte fine kemikalier fra laboratoriehylden. Tre mikrotubulusdestabiliserende forbindelser (colchicin, vincristin, podophyllotoxin), der forventes at interferere med NK-cellemigration og degranulering, blev også inkluderet i testbiblioteket. Testskærmen identificerede alle tre positive kontrolforbindelser som hits, der beviser metodens egnethed til at identificere ADCC-modificerende lægemidler i et kemisk bibliotek. Med dette assay kan sammensatte biblioteksskærme udføres for at identificere ADCC-forstærkende forbindelser, der kan anvendes som adjuverende terapeutiske midler til behandling af patienter, der modtager anticancerimmunterapier. Derudover kan metoden også bruges til at identificere eventuelle uønskede ADCC-hæmmende bivirkninger af terapeutiske lægemidler taget af kræftpatienter til forskellige indikationer.
Introduction
Immunterapi med anticancerantistoffer, immuncheckpointhæmmere eller kimære antigenreceptorekspressive T (CAR-T) celler repræsenterer en kraftfuld tilgang til kræftbehandling 1,2,3. Trastuzumab er et humaniseret monoklonalt anti-HER-2 (humant epidermal vækstfaktorreceptor 2) antistof, der anvendes til behandling af HER-2-positiv brystkræft i et tidligt stadium eller metastatisk brystkræft, samt HER-2-positiv metastatisk gastrisk cancer 4,5,6. Det virker primært ved at hæmme den proliferationsstimulerende virkning af den epidermale vækstfaktor4. Det er imidlertid blevet rapporteret, at trastuzumab effektivt udløser kræftcelledød, selvom kræftcellerne har mistet deres lydhørhed over for HER-2-stimulering7. Denne paradoksale virkning af antistoffet skyldes antistofafhængig cellemedieret cytotoksicitet (ADCC)7. ADCC kan medieres af naturlige dræberceller (NK), granulocytter og makrofager, samlet kendt som effektorcellerne i ADCC 8,9. Hvis et antistof, såsom trastuzumab, binder til tumorceller, bruger disse effektorceller deres Fc-receptorer til at binde antistoffets konstante (Fc) region. Antistoffet bygger bro mellem tumorcellerne og de Fc-receptorbærende effektorceller, hvilket udløser frigivelsen af deres cytotoksiske mediatorer10. Naturlige dræberceller frigiver den cytotoksiske last af deres granulater indeholdende perforin for at generere porer i målcellemembranen og granzym (udløsende signalveje for celledød) i immunsynapsen, hvilket fører til apoptose af kræftcellerne (se figur 1).
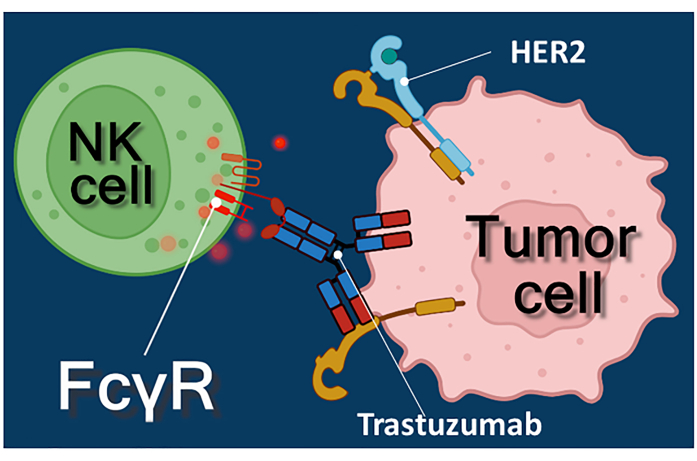
Figur 1: Effektor- og målcelleinteraktioner i ADCC. Celleoverfladen Fcγ-receptoren i effektoren NK-cellen genkender Fc-regionen af anti-HER2-trastuzumab-antistoffet, der er specifikt for HER2-molekylet udtrykt på overfladen af tumorcellen. Således etableres den såkaldte immunologiske synaps mellem de to celler, hvilket inducerer den rettede exocytose af cytotoksiske granuler af effektorcellen. De frigivne perforin- og granzymmolekyler resulterer i sidste ende i apoptose af målcellen. Klik her for at se en større version af denne figur.
Flere assays er tidligere blevet udviklet til kvantificering af cytotoksicitet, herunder ADCC. Guldstandarden er den radioaktive kromfrigivelsesmetode, hvor målcellerne mærkes med radioaktiv 51Cr isotop, og ADCC kvantificeres ved at måle radioaktivitet fra supernatanten af lyserede målceller11. På grund af de åbenlyse problemer på grund af den strengt regulerede håndtering, opbevaring og bortskaffelse af radioaktive farmakoner og affald er denne metode blevet mere og mere upopulær blandt bioforskere. Derudover er det heller ikke acceptabelt for applikationer med høj kapacitet. Måling af aktiviteten af enzymer (f.eks. lactat-dehydrogenase) frigivet fra de dræbte målceller kan tilvejebringe et ikke-radioaktivt alternativ til 51Cr-analysen12. Disse analyser skelner imidlertid ikke mellem mål- og effektorcelledødsfald. ECIS (Electric Cell-Substrate Impedance Sensing) viste sig at være egnet til kvantificering af ADCC13, men ECIS-udstyret er ikke tilgængeligt i de fleste laboratorier, og teknikken er ikke kompatibel med applikationer/screening med høj kapacitet. Fluorescerende mærkede celler repræsenterer et populært alternativ i mange cellebiologiske assays og bruges ofte i flowcytometri eller pladelæserbaserede applikationer14,15,16. Disse analyser indeholder imidlertid ofte vasketrin eller er på anden måde uforenelige med applikationer med høj kapacitet (f.eks. flowcytometribaserede teknikker). Nogle populære cytotoksicitetsanalyser, som i teorien burde være egnede til ADCC-kvantificering, bestemmer ikke pålideligt ADCC-effektivitet13. For nylig, med spredningen af fluorescerende konfokal mikroskopi, bliver billedbaserede assays med højt indhold stadig mere populære inden for forskellige områder af biovidenskab17. På den ene side er cellebilleddannelsesudstyr nu ret allestedsnærværende, mens der på den anden side kan indsamles næsten uendelige morfologiske parametre fra de erhvervede billeder. Derfor satte vi os for at udvikle et ADCC-assay med højt indhold og demonstrere dets egnethed til screening af sammensatte biblioteker.
Her præsenterer vi et billedbaseret ADCC-assay og demonstrerer, hvordan dette assay kan bruges til High-Content Screening (HCS) til at identificere ADCC-modulerende forbindelser. Modellen er baseret på JIMT-1 brystkarcinommålceller, CD16.176V.NK-92 effektorceller og det humaniserede monoklonale anti-HER2-antistof trastuzumab. Med denne metode er det muligt at identificere lægemidler, der kan forbedre NK-cellernes tumordræbende virkning eller at få indsigt i mekanismen bag NK-cellemedieret ADCC ved at identificere små molekyler, der interfererer med ADCC. Vi foreslår, at bioforskere, der sigter mod at kvantificere cellemedieret cytotoksicitet med særligt hensyn til ADCC, kan drage fordel af at bruge dette assay enten til opdagelsesvidenskab eller lægemiddeludvikling. Dette assay kan være et alternativ, hvis et laboratorium har adgang til og en vis erfaring med fluorescerende billeddannelse og kvantitativ billedanalyse.
Protocol
Representative Results
Discussion
ADCC-reaktionen er blevet beskrevet for relativt længe siden. Vigtige molekylære begivenheder i processen er også blevet beskrevet19. Metoder til måling af ADCC spænder fra guldstandarden radioaktiv kromfrigivelsesanalyse, cytoplasmatisk enzymfrigivelsesassays til flere fluorescensbaserede flowcytometri- eller mikropladeassays20. En almindelig begrænsning ved disse analyser er imidlertid, at de ikke er modtagelige for applikationer med høj kapacitet. Tidligere udvikl…
Disclosures
The authors have nothing to disclose.
Acknowledgements
LV modtog støtte fra National Research, Development and Innovation Office bevillinger GINOP-2.3.2-15-2016-00010 TUMORDNS”, GINOP-2.3.2-15-2016-00048-STAYALIVE og OTKA K132193, K147482. CD16.176V.NK-92 celler blev opnået fra Dr. Kerry S. Campbell (Fox Chase Center, Philapedlphia, PA, på vegne af Brink Biologics, lnc. San Diego, CA), er beskyttet af patenter over hele verden og blev licenseret af Nantkwest, lnc. Forfatterne er taknemmelige for György Vereb og Árpád Szöőr for deres hjælp med brugen af NK-92-cellelinjen og for teknisk rådgivning.
Materials
| 5-fluorouracil | Applichem | A7686 | in compound library |
| 96-well Cell Carrier Ultra plate | PerkinElmer | LLC 6055302 | |
| Betulin | Sigma | B9757 | in compound library |
| CD16.176V.NK92 cells | Nankwest Inc. | ||
| Cerulenin | ChemCruz | sc-396822 | in compound library |
| Cisplatin | Santa Cruz Biotechnology | sc-200896 | in compound library |
| Colchicine | Sigma | C9754 | in compound library |
| Concanavalin-A | Calbiochem | 234567 | in compound library |
| Dexamethasone | Sigma | D4902 | in compound library |
| DMEM/F-12 medium | Sigma | D8437 | in JIMT-1 EGFP medium |
| DMSO | Sigma | D2650 | in compound library |
| Etoposide | Sigma | E1383 | E1383 |
| Fetal bovine serum (FBS) | Biosera | FB-1090/500 | JIMT-1 EGFP and NK medium |
| Fisetin | Sigma | F4043 | in compound library |
| Freedom EVO liquid handling robot | TECAN | ||
| Gallotannin | Fluka Chemical Corp. | 16201 | in compound library |
| Glutamine | Gibco | 35,050–061 | in NK medium |
| Harmony software | PerkinElmer | ||
| Humanized anti-HER2 monoclonal antibody (Herzuma) | EGIS Pharmaceuticals, Budapest Hungary | N/A | |
| Humulin R (insulin) | Eli Lilly | HI0219 | JIMT-1 EGFP medium |
| IL-2 | Novartis Hungária Kft. | PHC0026 | in NK medium |
| Isatin | Sigma | 114618 | in compound library |
| MEM Non-essential Amino Acids (MEM-NEAA) | Gibco | 11,140–050 | in NK medium |
| Na-pyruvate | Lonza | BE13-115E | in NK medium |
| Naringenin | Sigma | N5893 | in compound library |
| NQDI-1 | Sigma | SML0185 | in compound library |
| Opera Phenix High-Content Analysis equipment | PerkinElmer | ||
| Penicillin–streptomycin | Biosera | LM-A4118 | JIMT-1 EGFP and NK medium |
| Pentoxyfilline | Sigma | P1784 | in compound library |
| Phosphate buffered saline (PBS) | Lonza | BE17-517Q | to wash the cells |
| Podophyllotoxin | Sigma | P4405 | in compound library |
| Quercetin | Sigma | Q4951 | in compound library |
| Tannic acid | Sigma | T8406 | in compound library |
| Temozolomide | Sigma | T2577 | in compound library |
| Trypan blue 0.4% solution | Sigma | T8154 | for cell counting |
| Vincristine sulfate | Sigma | V0400000 | in compound library |
| α-MEM | Sigma | M8042 | in NK medium |
References
- Gupta, S. L., Basu, S., Soni, V., Jaiswal, R. K. Immunotherapy: an alternative promising therapeutic approach against cancers. Molecular Biology Reports. 49 (10), 9903-9913 (2022).
- Moretti, A., et al. The past, present, and future of non-viral CAR T cells. Frontiers in Immunology. 13, 867013 (2022).
- June, C. H., O’Connor, R. S., Kawalekar, O. U., Ghassemi, S., Milone, M. C. CAR T cell immunotherapy for human cancer. Science. 359 (6382), 1361-1365 (2018).
- Ross, J. S., et al. The HER-2 receptor and breast cancer: ten years of targeted anti-HER-2 therapy and personalized medicine. Oncologist. 14 (4), 320-368 (2009).
- Shitara, K., et al. Discovery and development of trastuzumab deruxtecan and safety management for patients with HER2-positive gastric cancer. Gastric Cancer. 24 (4), 780-789 (2021).
- Gianni, L., et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncology. 13 (1), 25-32 (2012).
- Barok, M., et al. Trastuzumab causes antibody-dependent cellular cytotoxicity-mediated growth inhibition of submacroscopic JIMT-1 breast cancer xenografts despite intrinsic drug resistance. Molecular and Cancer Therapy. 6 (7), 2065-2072 (2007).
- Gauthier, M., Laroye, C., Bensoussan, D., Boura, C., Decot, V. Natural Killer cells and monoclonal antibodies: Two partners for successful antibody dependent cytotoxicity against tumor cells. Crit Rev Oncol Hematol. 160, 103261 (2021).
- Gruijs, M., Sewnath, C. A. N., van Egmond, M. Therapeutic exploitation of neutrophils to fight cancer. Semin Immunol. 57, 101581 (2021).
- Mando, P., Rivero, S. G., Rizzo, M. M., Pinkasz, M., Levy, E. M. Targeting ADCC: A different approach to HER2 breast cancer in the immunotherapy era. Breast. 60, 15-25 (2021).
- van der Haar Avila, I., Marmol, P., Kiessling, R., Pico de Coana, Y. Evaluating antibody-dependent cell-mediated cytotoxicity by chromium release assay. Methods in Molecular Biology. 1913, 167-179 (2019).
- Broussas, M., Broyer, L., Goetsch, L. Evaluation of antibody-dependent cell cytotoxicity using lactate dehydrogenase (LDH) measurement. Methods in Molecular Biology. 988, 305-317 (2013).
- Toth, G., Szollosi, J., Vereb, G. Quantitating ADCC against adherent cells: Impedance-based detection is superior to release, membrane permeability, or caspase activation assays in resolving antibody dose response. Cytometry A. 91 (10), 1021-1029 (2017).
- Chung, S., Nguyen, V., Lin, Y. L., Kamen, L., Song, A. Thaw-and-use target cells pre-labeled with calcein AM for antibody-dependent cell-mediated cytotoxicity assays. Journal of Immunological Methods. 447, 37-46 (2017).
- Lee-MacAry, A. E., et al. Development of a novel flow cytometric cell-mediated cytotoxicity assay using the fluorophores PKH-26 and TO-PRO-3 iodide. Journal of Immunological Methods. 252 (1-2), 83-92 (2001).
- Tanito, K., et al. Comparative evaluation of natural killer cell-mediated cell killing assay based on the leakage of an endogenous enzyme or a pre-loaded fluorophore. Analytical Science. 37 (11), 1571-1575 (2021).
- Lin, S., Schorpp, K., Rothenaigner, I., Hadian, K. Image-based high-content screening in drug discovery. Drug Discovery Today. 25 (8), 1348-1361 (2020).
- Guti, E., et al. The multitargeted receptor tyrosine kinase inhibitor sunitinib induces resistance of HER2 positive breast cancer cells to trastuzumab-mediated ADCC. Cancer Immunology, Immunotherapy. 71 (9), 2151-2168 (2022).
- Li, F., Liu, S. Focusing on NK cells and ADCC: A promising immunotherapy approach in targeted therapy for HER2-positive breast cancer. Frontiers in Immunology. 13, 1083462 (2022).
- Perussia, B., Loza, M. J. Assays for antibody-dependent cell-mediated cytotoxicity (ADCC) and reverse ADCC (redirected cytotoxicity) in human natural killer cells. Methods in Molecular Biology. 121, 179-192 (2000).
- Garcia-Alonso, S., Ocana, A., Pandiella, A. Trastuzumab emtansine: Mechanisms of action and resistance, clinical progress, and beyond. Trends in Cancer. 6 (2), 130-146 (2020).

