Isolering af bronchiale epitelceller fra resekteret lungevæv til biobanking og etablering af veldifferentierede luft-væske-grænsefladekulturer
Summary
Her præsenteres en reproducerbar, overkommelig og robust metode til isolering og udvidelse af primære bronchiale epitelceller til langsigtet biobank og generering af differentierede epitelceller ved dyrkning ved luft-væske-grænsefladen.
Abstract
Luftvejsepitelcellelaget danner den første barriere mellem lungevæv og det ydre miljø og udsættes derved konstant for indåndede stoffer, herunder smitsomme agenser og luftforurenende stoffer. Luftvejsepitellaget spiller en central rolle i en lang række akutte og kroniske lungesygdomme, og forskellige behandlinger rettet mod dette epitel administreres ved indånding. At forstå epithelets rolle i patogenese, og hvordan det kan målrettes mod terapi, kræver robuste og repræsentative modeller. In vitro epitelkulturmodeller anvendes i stigende grad og giver fordelen ved at udføre eksperimenter i et kontrolleret miljø, der udsætter cellerne for forskellige former for stimuli, toksiske stoffer eller infektiøse stoffer. Anvendelsen af primære celler i stedet for udødeliggjorte eller tumorcellelinjer har den fordel, at disse celler differentierer i kultur til et pseudostratificeret polariseret epitelcellelag med en bedre repræsentation af epitelet sammenlignet med cellelinjer.
Præsenteret her er en robust protokol, der er blevet optimeret i løbet af de sidste årtier, til isolering og dyrkning af luftvejsepitelceller fra lungevæv. Denne procedure muliggør vellykket isolering, ekspansion, dyrkning og mucociliær differentiering af primære bronchiale epitelceller (PBEC’er) ved dyrkning ved luft-væske-grænsefladen (ALI) og inkluderer en protokol til biobanking. Desuden beskrives karakteriseringen af disse kulturer ved hjælp af cellespecifikke markørgener. Disse ALI-PBEC-kulturer kan bruges til en række applikationer, herunder udsættelse for hel cigaretrøg eller inflammatoriske mediatorer og co-kultur / infektion med vira eller bakterier.
Protokollen i dette manuskript, der illustrerer proceduren trin for trin, forventes at danne grundlag og/eller reference for dem, der er interesseret i at implementere eller tilpasse sådanne kultursystemer i deres laboratorium.
Introduction
Luftvejsepitelets rolle i en række akutte og kroniske lungesygdomme er blevet beskrevet i forskellige anmeldelser 1,2,3,4,5,6,7. Veldifferentierede kulturer af luftvejsepitelceller er et vigtigt redskab til at opklare luftvejsepitelets rolle. Air-fluid interface (ALI) luftvejsepitelcellekultur anvendes bredt til at fremme differentieringen af luftvejs basale epitelceller og derved studere luftvejsepitelet pålideligt in vitro 8,9. I de seneste år er brugen af sådanne modeller steget yderligere som følge af nye forskningsinitiativer i forbindelse med covid-19-pandemien og en verdensomspændende overgang til dyrefri forskning. Derfor understreger den øgede brug af denne modelcellelinje behovet for at dele procedurer og erfaringer for at opnå robuste resultater. Dette vil også gøre det muligt at sammenligne resultater mellem forskergrupper. Procedurens robusthed er det vigtigste kendetegn og skal derfor underkastes kvalitetskontrol. Flere laboratorier har investeret i at udvikle protokoller til dyrkning af primære luftvejsepitelceller på ALI. Tiden, indsatsen og det nødvendige budget kan reduceres, når disse procedurer deles i detaljer. Disse detaljer omfatter for eksempel valget af cellekulturplast og medier leveret af forskellige producenter, da dette viste sig at påvirke egenskaberne ved de opnåede kulturer10,11,12. Dette understreger vigtigheden af at dele erfaringer og detaljer om kulturprocedurer, da resultaterne kan blive påvirket, og/eller valideringsindsatsen på tværs af forskellige laboratorier kan blive hæmmet i mangel af en sådan indsigt.
Det menneskelige lungeepitel omfatter forskellige celletyper, herunder hovedtyper såsom basalceller, cilierede celler, bægerceller og klubceller. For pålideligt at efterligne epitelcellelaget i luftvejene in vitro skal disse celletyper være repræsenteret i dyrkningsmodellerne, og deres polarisering og funktion opretholdes13,14,15,16. Erkendelsen af, at donorkarakteristika (herunder sygdomstilstand) og cellernes anatomiske oprindelse (dvs. nasal, trakeal, store og små luftveje) kan påvirke cellekulturens cellulære sammensætning og funktionelle reaktioner, er lige så vigtig. Relevant ekspertise og praksis er en forudsætning for succesfuldt at dyrke primære luftvejsepitelceller og vurdere kulturens kvalitet både intuitivt (ved visuel inspektion under kultur) og kvantificerbart. Formålet med dette bidrag er at tilvejebringe en omkostnings- og tidseffektiv metode til isolering og dyrkning af primære humane bronchiale epitelceller (PBEC’er), som også kan anvendes til dyrkning af trakeale og små luftvejsepitelceller. Ud over at beskrive en metode til isolering af sådanne celler fra resekteret lungevæv, præsenteres og diskuteres en metode til ekspansion og biobanking, og endelig til etablering og karakterisering af en veldifferentieret ALI-kultur inden for en rimelig pris og tidsperiode.
Protocol
Representative Results
Discussion
Protokollen præsenteret her beskriver isoleringen af humane bronchiale epitelceller fra resekteret lungevæv, en metode til optimal udvidelse af celler uden tab af differentieringspotentiale, en kryopræserveringsprocedure og en procedure til generering af veldifferentierede ALI-PBEC-kulturer. Desuden gives en beskrivelse af kvalitetskontrol samt instruktioner til overvågning og evaluering af de differentierede ALI-PBEC’er.
Den beskrevne protokol starter med en makroskopisk normal, tumorfri bronchial ring, der resekteres fra en lungelap fra patienter, der gennemgår operation relateret til deres lungekræftdiagnose. Det skal derfor bemærkes, at disse ringe strengt taget ikke kan betragtes som sundt væv, hvilket derfor kan påvirke cellekulturens egenskaber. Alternative kilder til opnåelse af bronchiale epitelceller omfatter anvendelse af bronchiale biopsier, bronchiale børstninger eller væv fra en transplantationsdonor eller modtagerlunger. Uanset kilden bør der ved brug af lungevæv overvejes en risiko for mikrobiel kontaminering, og derfor anvendes antibiotika i de forskellige dyrkningsmedier for at reducere risikoen for mikrobiel kontaminering af cellekulturen. Især mycoplasma er en høj og almindelig risiko i cellekultur på grund af dens mange forskellige virkninger på cellekultur, resistens over for antibiotika, der almindeligvis anvendes i cellekultur, og det faktum, at mycoplasma-kontaminering kun kan bekræftes ved mycoplasma-detektionsassays. Derfor anvendes den bredspektrede antimikrobielle formulering Primocin i den indledende fase af cellekultur efter isolering af celler fra lungevæv, og under dyrkningsprocessen testes tilfældigt udvalgte prøver for tilstedeværelsen af mycoplasma.
Isolationsproceduren, der starter med en bronkial ring, giver tilstrækkeligt udgangsmateriale til at muliggøre den grad af udvidelse af disse primære celler, der er nødvendig for at starte kulturer ved ALI uden at gå på kompromis med differentieringskapaciteten. Imidlertid kan start af udvidelsen af de isolerede epitelceller med et begrænset antal celler udgøre problemer med at opnå et tilstrækkeligt antal indsatser med nok celler, der kan podes til ALI-kultur. Udvidet dyrkning og gentagen passage af primære celler kan resultere i replikativ ældning. Der er foreslået forskellige løsninger for at overvinde denne begrænsning. Horani et al. viste, at Rho-kinasehæmmeren (ROCK) Y-27632 øgede spredningen af basalceller30, Mou et al. brugte dobbelt Smad-hæmning til at udvide basale stamceller, samtidig med at egenskaberne ved det differentierede epitelcellelag 31 opretholdes, og Sachs et al. har udviklet et luftvejsorganoidsystem, der kan bruges til at udvide luftvejsepitelceller og opretholde deres differentieringspotentiale i løbet af flere passager32. Sidstnævnte metode blev også brugt til at udvide celler fra kilder med meget lave celletal, såsom trakeale aspirater (TA’er) fra for tidligt fødte spædbørn (<28 ugers svangerskabsalder) og bronchoalveolær skylning (BAL) væske, før overførsel til ALI-kulturen som beskrevet her33. Det blev konstateret, at celler isoleret fra BAL og TA’er viste en differentieringskapacitet, der lignede celler genereret fra bronchialt væv, selvom forskelle blev observeret, når differentieringen var skæv mod mere cilierede eller mere bægercelleholdige kulturer ved hjælp af Notch-signalhæmning eller Th2-cytokinet IL-1333. Det anbefales derfor, at hvis ALI-PBEC’er dyrkes fra et udgangsmateriale med lavt epitelcelleantal ved hjælp af lignende tilgange, skal kulturerne altid kontrolleres for de grundlæggende kvalitetskriterier, som diskuteret i afsnit 6 i protokollen. Det er vigtigt, at brugen af fødeceller også kan hjælpe med at opnå større celleantal, hvilket er vigtigt i en indstilling til transplanterelig stilladsteknik, hvor tid og cellenummer er afgørende. Dette illustreres af en undersøgelse, hvor autologe epitelceller blev dyrket fra biopsier fra en patient med trakealsygdom, og celler hurtigt blev udvidet i nærværelse af et murin embryonalt fødelag (mitotisk inaktiverede 3T3-J2 fibroblaster) og ovennævnte hæmmer af Rho/ROCK-vejen (Y-27632)34. Den resulterende cellekultur viste sig at være nyttig til genbefolkning af trakealstilladser, og dette kunne derfor ses som en passende protokol til en transplantationsmodel.
Når man bruger den protokol, der er beskrevet i dette bidrag, men også når man bruger andre kulturprotokoller, introduceres uundgåeligt en selektionsbias. Det er vigtigt at indse, at forskelle i protokoldetaljer, såsom oprindelsen af celler, der bruges til at initiere kulturer, mediumsammensætning og andre protokoldetaljer, kan føre til ændringer i kulturernes cellulære sammensætning og derved ændringer i responsen fra ALI-kulturen33,35. Derudover er forskelle i celleegenskaber også blevet observeret, når man sammenligner forskellige medier til differentiering af luftvejscellerne10,11. Ved sammenligning af PneumaCult og cBD-medium blev der observeret forskelle i bægercelle- og klubcelle-mRNA-markører, TEER-værdier og cellelagtykkelse. Baseret på disse observationer, på trods af manglen på statistisk underbygning på grund af det lave antal anvendte donorer, er mediesammensætningen ukendt for kunderne og højere omkostninger ved PneumaCult-mediet, blev beslutningen truffet i vores laboratorium om at bruge cBD-mediet.
Som diskuteret kan celler oprindeligt udvides ved hjælp af organoidkultur og derefter overføres til 2D ALI-indsatssystemet. Dette er vigtigt, da luftvejsepitelorganoider ikke er egnede til eksponering for luftbårne stoffer, mens brugen af ALI 2D-systemet muliggør evaluering af virkningen af luftbårne stoffer såsom cigaretrøg 23,36 på dyrkede luftvejsepitelceller. En anden tilgang til etablering af ALI-luftvejsepitelcellekulturer er at generere luftvejsepitelceller ved differentiering af humane pluripotente stamceller (hiPSC’er)37. I sådanne protokoller kan celler i den sidste fase af differentieringsprotokollen efter differentiering til proksimale luftvejsforfædre differentieres ved dyrkning til ALI ved hjælp af procedurer svarende til dem, der er beskrevet her.
I den nuværende protokol anvendes cBD-medium til kultur på ALI. cBD-medium er et serumfrit medium, der fremstilles ved at tilføje en blanding af forskellige kosttilskud, inspireret af Fulcher et al.38 samt andre undersøgelser. Tilskudsopløsningen indeholder 52 μg / ml bovin hypofyseekstrakt (BPE), 0,5 μg / ml hydrocortison, 0,5 ng / ml human EGF, 0,5 μg / ml adrenalin, 10 μg / ml transferrin, 5 μg / ml insulin, 6,5 ng / ml triiodothyronin og 0,1 ng / ml RA39. Da BPE er et vævsekstrakt og udsættes for batchvis variation, kan substratet ikke betragtes som et fuldt defineret medium, og det er heller ikke dyrefrit. Cellekulturmedium, der er fuldt defineret, foretrækkes for at minimere batch-til-batch-forskelle. I lyset af overgangen til dyrefri forskning er det vigtigt, at der gøres en indsats for at producere definerede medier, der ikke indeholder animalske produkter, og som er økonomisk overkommelige for forskersamfundet.
Forskellige eksperimentelle opsætninger kan bruges baseret på ALI-modellen, afhængigt af forskningsspørgsmålet. For eksempel for at undersøge virkningen af forbindelser, der kan påvirke differentieringsprocessen, kan dette løses ved at tilføje forbindelserne til kulturen under de forskellige stadier af nedsænket kultur, under differentiering eller på det veldifferentierede stadium. Den cellulære sammensætning af ALI-PBEC-kulturen kan påvirkes ved tilsætning af specifikke forbindelser; for eksempel genererer differentiering af ALI-PBEC’er i nærvær af IL-13 en kultur med flere bægerceller og færre cilierede celler, mens behandling med γ-sekretasehæmmeren DAPT (bruges til at blokere Notch-signalering) under differentiering resulterer i en kultur med mere cilierede celler på bekostning af bægerceller 23,40,41,42.
Desuden kan midler til at stimulere celler eller blokere visse processer enten påføres basalrummet eller (i et meget lille volumen) til kulturens apikale rum. Celler kan også udsættes for luftbårne stoffer fra den apikale side. Sådanne eksponeringsdesign er blevet brugt til at undersøge virkningen af dieseludstødning eller hel cigaretrøg på PBEC’er23,43,44. Mediet kan høstes hver gang mediet ændres for at overvåge udskillede proteiner på basalsiden; det samme gælder for den apikale side af cellerne, der vaskes med PBS, mens basalmediet opdateres. Den såkaldte apikale vask høstes, og valgfri dithioerythritol (DTE) tilsættes for at adskille slimet, der produceres af bægercellerne mere effektivt. Cellelysater kan opnås til isolering af total protein, RNA og kromosomalt og mitokondrielt DNA. Cellerne kan undersøges yderligere ved hjælp af antistoffer til specifikke markører ved at skære polyethylenterephthalatmembranen (PET) fra plastindsatsen og yderligere skære denne membran i mindre stykker til flere immunfluorescensfarvninger45. Desuden kan flowcytometri eller FACS også anvendes efter trypsinisering af cellerne i indsatserne. Under ALI-stadiet kan udviklingen af cellebarrieren overvåges ved at måle den elektriske modstand og efterfølgende beregne TEER, hvor den elektriske modstand er omvendt proportional med membranindsatsens overfladeareal. Beregningen er baseret på Ohms lov ved hjælp af følgende formel: 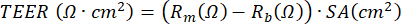 , hvor Rm er den målte elektriske modstand, Rb er den grundlæggende elektriske modstand for en indsats uden belægning og celler, og SA er overfladearealet af skærets membran. Måling af den elektriske modstand ved hjælp af EVOM2- og STX/spisepindeelektroder er ligetil, men meget afhængig af håndteringsprocedurer, når den indføres i brønden. Det er også blevet foreslået, at elektrodens form påvirker målingen af barrierefunktionen af det relativt store overfladeareal17.
, hvor Rm er den målte elektriske modstand, Rb er den grundlæggende elektriske modstand for en indsats uden belægning og celler, og SA er overfladearealet af skærets membran. Måling af den elektriske modstand ved hjælp af EVOM2- og STX/spisepindeelektroder er ligetil, men meget afhængig af håndteringsprocedurer, når den indføres i brønden. Det er også blevet foreslået, at elektrodens form påvirker målingen af barrierefunktionen af det relativt store overfladeareal17.
Yderligere forbedring i ALI-cellekultursystemet, der sigter mod at øge nøjagtig vævsrepræsentation, inkluderer samkultur af yderligere celletype, såsom leukocytter, fibroblaster eller endotelceller46,47,48. Det er blevet observeret, at denne co-kultur af ALI-PBEC med granulocyt-makrofag kolonistimulerende faktor (GM-CSF) eller M-CSF-differentierede makrofager markant påvirker medfødte epitelresponser og reparation48. Det er vigtigt at bemærke, at i sådanne samkulturmodeller kan mediumkompatibilitet være et problem. Da mediet, der anvendes til luftvejsepitelcellekulturen, er udviklet specielt til PBEC’er og muligvis ikke er optimalt egnet til andre celletyper, er optimering nødvendig. En anden form for fremskridt, der ses inden for luftvejsbiologi, som isolerede PBEC’er kan bruges til, er brugen af Organs-on-Chips (OoC) teknologi49,50. Ved hjælp af denne teknologi kan indflydelsen af de mekaniske kræfter ved vejrtrækning og blodgennemstrømning, såsom strækning, luft og medium strømning, studeres 29.
Interdonorvariabilitet kan være signifikant, når der anvendes PBEC’er fra forskellige donorer, og det er derfor vigtigt at overveje at bruge celler fra flere donorer til at tage højde for denne variabilitet i epitelcellekulturundersøgelser. Da kulturen af ALI-PBEC’er er tidskrævende og forbundet med betydelige omkostninger, undersøges muligheden for at etablere ALI-PBEC-kulturer ved at blande celler fra forskellige donorer i en cellekulturindsats. På denne måde kan pilotforsøg let udføres ved hjælp af primære celler, inden man analyserer responserne fra kulturer afledt af forskellige individuelle donorer . Derudover kan donorer med forskellige karakteristika (f.eks. forskellige aldersgrupper eller køn) grupperes til eksplorative undersøgelser. Når der anvendes donorblandinger, er det vigtigt at sikre, at der er lige mange forskellige donorer til stede for at forhindre, at én donor dominerer resultaterne som følge af en højere spredningsrate. Derfor udvides celler fra individuelle donorer separat og podes med en højere densitet i indsatsen sammenlignet med såceller fra en individuel donor for at minimere spredning i indsatsen før overgang til ALI. Respons fra donorblandinger og tilsvarende individuelle donorer blev sammenlignet ved at studere infektionskinetikken for SARS-CoV-2. Ved anvendelse af RT-qPCR og immunofluorescensfarvning blev det observeret, at donorblandingen gav en god repræsentation af de forskellige individuelle donorer ved at vise et lignende antal producerede viruspartikler og et tilsvarende antal inficerede celler28.
For at blive et acceptabelt alternativ til dyremodeller bør genredigering af dyrkede bronchiale epitelceller være mulig51. RNA-interferensteknologi ved hjælp af små interfererende RNA’er (siRNA’er) i ALI-PBEC’er undersøges, men da cellerne skal transfekteres med siRNA under den nedsænkede fase af kulturen, opretholdes knockdown ikke tilstrækkeligt under ALI-kultur på grund af den lange dyrkningsvarighed, medmindre siRNA-transfektion ofte gentages under kultur52. Ikke desto mindre kan siRNA’er med succes anvendes til at modificere genekspression i nedsænkede basalceller. Andre har med succes brugt CRISPR/Cas9-teknologi til at opnå genredigering i primære ALI-luftvejsepitelcellekulturer med ribonukleoprotein (RNP) levering 53. Ved anvendelse af sådanne teknikker er det vigtigt, at cellerne opretholder deres fulde differentieringskapacitet. Fordi primære luftvejscellekulturer ikke kan passeres på ubestemt tid, er klonal udvidelse af de genredigerede celler ikke let, og tilføjelsen af medium til udvælgelse af transfekterede celler er besværlig. Derfor er det svært at opnå den ønskelige knockdown i alle de dyrkede celler. Et alternativ til at generere knockout-kloner er brugen af knock-out-strategier i hiPSC’er54 og brugen af disse celler til at generere luftvejsepitelceller. Et andet, omend suboptimalt, alternativ er at etablere en udødeliggjort PPEC-linje for klonalt at udvide genredigerede celler55.
Den protokol, der præsenteres her, er en måde at generere en veldifferentieret pseudostratificeret ALI-PBEC på, men andre protokoller har også vist sig at etablere en sådan kultur med mindre og større forskelle i forhold til den præsenterede protokol. Efter vores mening er validering af dyrkningsmetoder og streng kvalitetskontrol på tværs af laboratorier afgørende for, at ALI-PBEC-systemet og lignende kultursystemer af luftvejsepitelceller kan blive et gyldigt alternativ til dyreforsøg.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Undersøgelserne ved hjælp af modellen beskrevet i dette bidrag er blevet støttet af en række finansieringsorganisationer, herunder Lung Foundation Netherlands, den hollandske organisation for sundhedsforskning og udvikling (ZonMw, COVID-19 MKMD-tilskud), det hollandske samfund for udskiftning af dyreforsøg (Stichting Proefdiervrij, bevilling # 114025007) samt forskningsbevillinger fra virksomheder som Boehringer Ingelheim og Galapagos. Figur 1 blev oprettet med BioRender.com.
Materials
| 1,000 ohm test resistor | World Precision Instruments | N/A | Used to calibrate the EVOM2 Epithelial Voltohmmeter |
| 4-[2-(5,6,7,8-Tetrahydro-5,5,8,8-tetramethyl-2-naphthalenyl)ethynyl)-benzoic acid (EC 23) | Tocris | 4011 | Used in cBD medium |
| 6-well Clear TC-treated Multiple Well Plates | Corning | 3506 | Used in the first step to grow the cells isolated form the bronchial ring |
| Airway Epithelial Cell Growth Medium Kit | PromoCell | C-21160 | Used to compare to cBD medium |
| Bead Bath 20 Liter | Lab Armor | 74220-720 | Used to pre-warm cell culture solutions |
| BEGM Bronchial Epithelial Cell Growth Medium BulletKit | LONZA | CC-3170 | Used to compare to cBD medium |
| Bovine albumin fraction V (BSA) | Thermo Fisher Scientific | 15260037 | Used in coating solution |
| Bovine pituitary extract (BPE) | Thermo Fisher Scientific | 37000-015 | Used in c-KSFM |
| Bronchial epithelial cell growth supplement (BEpiCGS) | ScienCell Research Laboratories | 3262 | Used in cBD medium |
| Bronchial epithelial cell medium-basal (BEpiCM-b) | ScienCell Research Laboratories | SCC3211-b | Used in cBD medium |
| Cell culture inserts; 12 mm Transwell with 0.4 µm pore polyester membrane insert | Corning | 3460 | Cell culture inserts used in the protocol |
| Cell culture inserts; 12-well inserts, 0.4 µm PET clear | CellQART made by SABEU | 9310412 | Cell culture inserts used to compare with Corning cell culture inserts |
| Cell culture inserts; 12-well ThinCert Tissue culture Inserts | Greiner Bio-One | 82050-032 | Cell culture inserts used to compare with Corning cell culture inserts |
| CELLSTAR flask, TC, PS, 250 ml, 75 cm2 | Greiner Bio-One | 658170 | Used to expand the number cells |
| CFX Maestro 1.0 | Bio-Rad | N/A | Software program for analyzing qPCR data generated with the CFX384 System |
| CFX384 Touch Real-Time PCR Detection System | Bio-Rad | 1855484 | qPCR detection system |
| Chopstick electrode set | World Precision Instruments | STX2 | Used to measure electrical resistance in ALI-PBEC |
| CO2-Incubator | PHCbi | MCO-170AICUV-PE | Cell culture incubator used for mycplasma free cell cultures |
| CO2-Incubator | Hereaus | Heracell 150 | Cell culture incubator used for possibly mycplasma infected cell cultures |
| Coolcell Container | Corning | 432006 | Used to cryopreserve cells at -80 °C before transfer to liquid N2 |
| Countess 3 Automated cell counter | Thermo Fisher Scientific | AMQAX2000 | Used to count cells and determine the cell concentration |
| Cryovials | Nalgene | 479-3224 | Used to cryopreserve cells in |
| D-Glucose | Avantor VWR BDH CHEMICALS | 101174Y | Used in soft trypsin |
| Dimethyl sulfoxide (DMSO) | Avantor VWR | 0231 | Used in cell freeze medium |
| dNTP (10 mM) | Promega | U1515 | Used in the synthesis of cDNA |
| Dulbecco's Modified Eagle's Medium (DMEM) + 4500 mg/l D-Glucose | STEMCELL Technologies | 36250 | Used in cBD medium |
| Dulbecco's Modified Eagle's Medium (DMEM) 4.5 g/l glucose with l-glutamine | LONZA | LOBE12-604F | Used in cBD medium to compare with DMEM from other manufacturers |
| Dulbecco's Modified Eagle's Medium (DMEM), high glucose, pyruvate | Thermo Fisher Scientific | 41966029 | Used in cBD medium to compare with DMEM from other manufacturers |
| Epidermal growth factor (EGF) | Thermo Fisher Scientific | 37000-015 | Used in c-KSFM |
| Ethylenediaminetetraacetic acid (EDTA) | Avantor VWR BDH CHEMICALS | 443885J | Used in soft trypsin |
| EVOM2 Epithelial Voltohmmeter | World Precision Instruments | 91799 | Used with the chopstick electrode set to measure electrical resistance in ALI-PBEC |
| Fibronectin solution, Human | PromoCell | C-43060 | Used in coating solution |
| Glutamax | Thermo Fisher Scientific | 35050038 | Used in cBD medium |
| Hanks balanced salt solution (HBSS) | ScienCell Research Laboratories | SCC0313 | Used to dissolve protease XIV |
| IQ SYBR Green Super mix | Bio-Rad | 170887 | qPCR reagent |
| Isoproterenol hydrochloride, (-)- | Sigma-Aldrich | I-6504 | Used in c-KSFM |
| Keratinocyte-SFM (KSFM) | Thermo Fisher Scientific | 17005-034 | Used in c-KSFM |
| Maxwell RSC Instrument | Promega | AS4500 | Automated RNA isolation system |
| Maxwell RSC simplyRNA Tissue Kit | Promega | AS1340 | Used to isolate total RNA with the Maxwell RSC Instrument |
| M-MLV Reverse transcriptase | Promega | M5301 | Used in the synthesis of cDNA |
| M-MLV Reverse transcriptase 5X reaction buffer | Promega | M531A | Used in the synthesis of cDNA |
| MycoStrip | InvivoGen | rep-mys-10 | Used to detect the presence of mycoplasma in cell culture samples |
| N-2-hydroxyethylpiperazine-N-2-ethane sulfonic acid (HEPES) | Thermo Fisher Scientific | 15630056 | Used in cBD medium |
| Oligo(dT)15 | Qiagen | 79237 | Used in the synthesis of cDNA |
| Penicillin/Streptomycin solution (Pen/Strep) | ScienCell Research Laboratories | SCC0513 | Used as antibiotic in c-KSFM and cBD medium |
| Phosphate buffered saline (PBS) | LUMC pharmacy | N/A | Used in different steps of the protocol |
| Pneumacult-ALI Medium | STEMCELL Technologies | 05002 | Used to grow cells in the differentiation stage to compare to cBD medium |
| Pneumacult-Ex Plus Medium | STEMCELL Technologies | 05040 | Used to grow cells in the submerged stage to compare to cBD medium |
| Primer, ATP5B, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: TCACCCAGGCTGGTTCAGA |
| Primer, ATP5B, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: AGTGGCCAGGGTAGGCTGAT |
| Primer, FOXJ1, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: GGAGGGGACGTAAATCCCTA |
| Primer, FOXJ1, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TTGGTCCCAGTAGTTCCAGC |
| Primer, MUC5AC, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: CCTTCGACGGACAGAGCTAC |
| Primer, MUC5AC, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TCTCGGTGACAACACGAAAG |
| Primer, MUC5B, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: GGGCTTTGACAAGAGAGT |
| Primer, MUC5B, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: AGGATGGTCGTGTTGATGCG |
| Primer, RPL13A, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: AAGGTGGTGGTCGTACGCTGTG |
| Primer, RPL13A, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: CGGGAAGGGTTGGTGTTCATCC |
| Primer, SCGB1A1, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: ACATGAGGGAGGCAGGGGCTC |
| Primer, SCGB1A1, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: ACTCAAAGCATGGCAGCGGCA |
| Primer, TP63, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: CCACCTGGACGTATTCCACTG |
| Primer, TP63, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TCGAATCAAATGACTAGGAGGGG |
| Primocin | InvivoGen | ant-pm-2 | Used as antimicrobial agent against bacteria, mycoplasma, and fungi in c-KSFM medium |
| Protease XIV | Sigma-Aldrich | P5147 | Used for the enzymatic treatment of the bronchial ring |
| RNAsin Recombinant Ribonuclease inhibitor | Promega | N2515 | Used in the synthesis of cDNA |
| Soybean trypsin inhibitor (SBTI) | Sigma-Aldrich | T9128 | Used to inhibit the action of soft trypsin |
| T100 Thermal Cycler | Bio-Rad | 1861096 | Used in the synthesis of cDNA |
| TissueSAFE plus | MILESTONE MEDICAL | N/A | Vacuum transfer system for biological specimens |
| Trypan blue solution | Thermo Fisher Scientific | 15250061 | Used to count live- and dead cells |
| Trypsin 1:250 | Thermo Fisher Scientific | 27250-018 | Used in soft trypsin |
| Type I collagen solution (PureCol) | Advanced BioMatrix | 5005-B | Used in coating solution |
| Universal container, PP, with PE screw cap | Avantor VWR | 216-2053 | Used in the protocol for the Protease XIV treatment of the bronchial ring |
References
- Aghapour, M., et al. Role of air pollutants in airway epithelial barrier dysfunction in asthma and COPD. European Respiratory Review. 31 (163), 210112 (2022).
- de Waal, A. M., Hiemstra, P. S., Ottenhoff, T. H., Joosten, S. A., vander Does, A. M. Lung epithelial cells interact with immune cells and bacteria to shape the microenvironment in tuberculosis. Thorax. 77 (4), 408-416 (2022).
- Duchesne, M., Okoye, I., Lacy, P. Epithelial cell alarmin cytokines: Frontline mediators of the asthma inflammatory response. Frontiers in Immunology. 13, 975914 (2022).
- Hewitt, R. J., Lloyd, C. M. Regulation of immune responses by the airway epithelial cell landscape. Nature Reviews Immunology. 21 (6), 347-362 (2021).
- Ruysseveldt, E., Martens, K., Steelant, B. Airway basal cells, protectors of epithelial walls in health and respiratory diseases. Frontiers in Allergy. 2, 787128 (2021).
- Alysandratos, K. D., Herriges, M. J., Kotton, D. N. Epithelial stem and progenitor cells in lung repair and regeneration. Annual Review of Physiology. 83, 529-550 (2021).
- Hammad, H., Lambrecht, B. N. Barrier epithelial cells and the control of type 2 immunity. Immunity. 43 (1), 29-40 (2015).
- Hynds, R. E., Bonfanti, P., Janes, S. M. Regenerating human epithelia with cultured stem cells: feeder cells, organoids and beyond. EMBO Molecular Medicine. 10 (2), 139-150 (2018).
- Hiemstra, P. S., Tetley, T. D., Janes, S. M. Airway and alveolar epithelial cells in culture. The European Respiratory Journal. 54 (5), 1900742 (2019).
- Saint-Criq, V., et al. Choice of differentiation media significantly impacts cell lineage and response to CFTR modulators in fully differentiated primary cultures of cystic fibrosis human airway epithelial cells. Cells. 9 (9), 2137 (2020).
- Leung, C., Wadsworth, S. J., Yang, S. J., Dorscheid, D. R. Structural and functional variations in human bronchial epithelial cells cultured in air-liquid interface using different growth media. American Journal of Physiology. Lung Cellular and Molecular Physiology. 318 (5), L1063-L1073 (2020).
- Morgan, R., et al. A medium composition containing normal resting glucose that supports differentiation of primary human airway cells. Scientific Reports. 12 (1), 1540 (2022).
- Ghosh, B., et al. Strong correlation between air-liquid interface cultures and in vivo transcriptomics of nasal brush biopsy. American Journal of Physiology. Lung Cellular and Molecular Physiology. 318 (5), L1056-L1062 (2020).
- Pezzulo, A. A., et al. The air-liquid interface and use of primary cell cultures are important to recapitulate the transcriptional profile of in vivo airway epithelia. American Journal of Physiology. Lung Cellular and Molecular Physiology. 300 (1), L25-L31 (2011).
- Dvorak, A., Tilley, A. E., Shaykhiev, R., Wang, R., Crystal, R. G. Do airway epithelium air-liquid cultures represent the in vivo airway epithelium transcriptome. American Journal of Respiratory Cell and Molecular Biology. 44 (4), 465-473 (2011).
- Legebeke, J., et al. Temporal whole-transcriptomic analysis of characterized in vitro and ex vivo primary nasal epithelia. Frontiers in Cell and Developmental Biology. 10, 907511 (2022).
- Srinivasan, B., et al. TEER measurement techniques for in vitro barrier model systems. Journal of Laboratory Automation. 20 (2), 107-126 (2015).
- van Wetering, S., et al. Regulation of secretory leukocyte proteinase inhibitor (SLPI) production by human bronchial epithelial cells: increase of cell-associated SLPI by neutrophil elastase. Journal of Investigative Medicine. 48 (5), 359-366 (2000).
- Balk, S. D. Calcium as a regulator of the proliferation of normal, but not of transformed, chicken fibroblasts in a plasma-containing medium. Proceedings of the National Academy of Sciences. 68 (2), 271-275 (1971).
- Gail, M. H., Boone, C. W., Thompson, C. S. A calcium requirement for fibroblast motility and prolifertion. Experimental Cell Research. 79 (2), 386-390 (1973).
- Dulbecco, R., Elkington, J. Induction of growth in resting fibroblastic cell cultures by Ca. Proceedings of the National Academy of Sciences. 72 (4), 1584-1588 (1975).
- van Wetering, S., et al. Epithelial differentiation is a determinant in the production of eotaxin-2 and -3 by bronchial epithelial cells in response to IL-4 and IL-13. Molecular Immunology. 44 (5), 803-811 (2007).
- Amatngalim, G. D., et al. Aberrant epithelial differentiation by cigarette smoke dysregulates respiratory host defence. The European Respiratory Journal. 51 (4), 1701009 (2018).
- Christie, V. B., et al. Retinoid supplementation of differentiating human neural progenitors and embryonic stem cells leads to enhanced neurogenesis in vitro. Journal of Neuroscience Methods. 193 (2), 239-245 (2010).
- Schrumpf, J. A., Ninaber, D. K., vander Does, A. M., Hiemstra, P. S. TGF-β1 impairs vitamin D-induced and constitutive airway epithelial host defense mechanisms. Journal of Innate Immunity. 12 (1), 74-89 (2020).
- Schrumpf, J. A., et al. Proinflammatory cytokines impair vitamin D-induced host defense in cultured airway epithelial cells. American Journal of Respiratory Cell and Molecular Biology. 56 (6), 749-761 (2017).
- Boei, J. J. W. A., et al. Xenobiotic metabolism in differentiated human bronchial epithelial cells. Archives of Toxicology. 91 (5), 2093-2105 (2017).
- Wang, Y., et al. Impact of human airway epithelial cellular composition on SARS-CoV-2 infection biology. bioRxiv. , (2021).
- Nawroth, J. C., et al. Breathing on Chip: Dynamic flow and stretch tune cellular composition and accelerate mucociliary maturation of airway epithelium in vitro. bioRxiv. , (2022).
- Horani, A., Nath, A., Wasserman, M. G., Huang, T., Brody, S. L. Rho-associated protein kinase inhibition enhances airway epithelial Basal-cell proliferation and lentivirus transduction. American Journal of Respiratory Cell and Molecular Biology. 49 (3), 341-347 (2013).
- Mou, H., et al. Dual SMAD signaling inhibition enables long-term expansion of diverse epithelial basal cells. Cell Stem Cell. 19 (2), 217-231 (2016).
- Sachs, N., et al. Long-term expanding human airway organoids for disease modeling. The EMBO Journal. 38 (4), 100300 (2019).
- Eenjes, E., et al. Disease modeling following organoid-based expansion of airway epithelial cells. American Journal of Physiology. Lung Cellular and Molecular Physiology. 321 (4), L775-L786 (2021).
- Butler, C. R., et al. Rapid expansion of human epithelial stem cells suitable for airway tissue engineering. American Journal of Respiratory and Critical Care Medicine. 194 (2), 156-168 (2016).
- Amatngalim, G. D., et al. Antibacterial defense of human airway epithelial cells from chronic obstructive pulmonary disease patients induced by acute exposure to nontypeable Haemophilus influenzae: modulation by cigarette smoke. Journal of Innate Immunity. 9 (4), 359-374 (2017).
- Plebani, R., et al. 3D lung tissue models for studies on SARS-CoV-2 pathophysiology and therapeutics. International Journal of Molecular Sciences. 23 (17), 10071 (2022).
- Wong, A. P., et al. Directed differentiation of human pluripotent stem cells into mature airway epithelia expressing functional CFTR protein. Nature Biotechnology. 30 (9), 876-882 (2012).
- Fulcher, M. L., Gabriel, S., Burns, K. A., Yankaskas, J. R., Randell, S. H. Well-differentiated human airway epithelial cell cultures. Methods in Molecular Biology. 107, 183-206 (2005).
- Cao, J., Wong, C. K., Yin, Y., Lam, C. W. K. Activation of human bronchial epithelial cells by inflammatory cytokines IL-27 and TNF-alpha: implications for immunopathophysiology of airway inflammation. The Journal of Cellular Physiology. 223 (3), 788-797 (2010).
- Tsao, P. N., et al. Notch signaling controls the balance of ciliated and secretory cell fates in developing airways. Development. 136 (13), 2297-2307 (2009).
- Laoukili, J., et al. IL-13 alters mucociliary differentiation and ciliary beating of human respiratory epithelial cells. The Journal of Clinical Investigation. 108 (12), 1817-1824 (2001).
- Mertens, T. C. J., et al. Cigarette smoke differentially affects IL-13-induced gene expression in human airway epithelial cells. Physiological Reports. 5 (13), e13347 (2017).
- Zarcone, M. C., et al. Effect of diesel exhaust generated by a city bus engine on stress responses and innate immunity in primary bronchial epithelial cell cultures. Toxicology in Vitro. 48, 221-231 (2018).
- vander Does, A. M., et al. Early transcriptional responses of bronchial epithelial cells to whole cigarette smoke mirror those of in-vivo exposed human bronchial mucosa. Respiratory Research. 23 (1), 227 (2022).
- Wang, Y., Ninaber, D. K., van Schadewijk, A., Hiemstra, P. S. Tiotropium and fluticasone inhibit rhinovirus-induced mucin production via multiple mechanisms in differentiated airway epithelial cells. Frontiers in Cellular and Infection Microbiology. 10, 278 (2020).
- Ronaghan, N. J., et al. M1-like, but not M0- or M2-like, macrophages, reduce RSV infection of primary bronchial epithelial cells in a media-dependent fashion. PLoS One. 17 (10), 0276013 (2022).
- Gindele, J. A., et al. Opposing effects of in vitro differentiated macrophages sub-type on epithelial wound healing. PLoS One. 12 (9), e0184386 (2017).
- van Riet, S., et al. Modulation of airway epithelial innate immunity and wound repair by M(GM-CSF) and M(M-CSF) macrophages. Journal of Innate Immunity. 12 (5), 410-421 (2020).
- Huh, D., et al. Reconstituting organ-level lung functions on a chip. Science. 328 (5986), 1662-1668 (2010).
- Stucki, A. O., et al. A lung-on-a-chip array with an integrated bio-inspired respiration mechanism. Lab on a Chip. 15 (5), 1302-1310 (2015).
- Peters-Hall, J. R., et al. Long-term culture and cloning of primary human bronchial basal cells that maintain multipotent differentiation capacity and CFTR channel function. American Journal of Physiology. Lung Cellular and Molecular Physiology. 315 (2), L313-L327 (2018).
- Bartman, C. M., Stelzig, K. E., Linden, D. R., Prakash, Y. S., Chiarella, S. E. Passive siRNA transfection method for gene knockdown in air-liquid interface airway epithelial cell cultures. American Journal of Physiology. Lung Cellular and Molecular Physiology. 321 (1), L280-L286 (2021).
- Koh, K. D., et al. Efficient RNP-directed human gene targeting reveals SPDEF is required for IL-13-induced mucostasis. American Journal of Respiratory Cell and Molecular Biology. 62 (3), 373-381 (2020).
- Bhargava, N., et al. Development of an efficient single-cell cloning and expansion strategy for genome edited induced pluripotent stem cells. Molecular Biology Reports. 49 (8), 7887-7898 (2022).
- Angelopoulou, A., Papaspyropoulos, A., Papantonis, A., Gorgoulis, V. G. CRISPR-Cas9-mediated induction of large chromosomal inversions in human bronchial epithelial cells. STAR Protocols. 3 (2), 101257 (2022).

