Isolera bronkiala epitelceller från resekterad lungvävnad för biobankning och etablera väldifferentierade luft-vätskegränssnittskulturer
Summary
Här presenteras en reproducerbar, prisvärd och robust metod för isolering och expansion av primära bronkialepitelceller för långsiktig biobankning och generering av differentierade epitelceller genom odling vid luft-vätskegränssnittet.
Abstract
Luftvägsepitelcellskiktet utgör den första barriären mellan lungvävnad och den yttre miljön och exponeras därmed ständigt för inandade ämnen, inklusive smittämnen och luftföroreningar. Luftvägsepitelskiktet spelar en central roll i ett stort antal akuta och kroniska lungsjukdomar, och olika behandlingar riktade mot detta epitel administreras genom inandning. Att förstå epitelets roll i patogenes och hur det kan riktas mot terapi kräver robusta och representativa modeller. In vitro-epitelodlingsmodeller används alltmer och erbjuder fördelen att utföra experiment i en kontrollerad miljö, utsätta cellerna för olika typer av stimuli, toxiska ämnen eller smittämnen. Användningen av primära celler istället för odödliga eller tumörcellinjer har fördelen att dessa celler differentieras i kultur till ett pseudostratifierat polariserat epitelcellskikt med en bättre representation av epitelet jämfört med cellinjer.
Här presenteras ett robust protokoll, som har optimerats under de senaste decennierna, för isolering och odling av luftvägsepitelceller från lungvävnad. Denna procedur möjliggör framgångsrik isolering, expansion, odling och mukociliär differentiering av primära bronkialepitelceller (PBECs) genom odling vid luft-vätskegränssnittet (ALI) och inkluderar ett protokoll för biobankning. Vidare beskrivs karakteriseringen av dessa kulturer med hjälp av cellspecifika markörgener. Dessa ALI-PBEC-kulturer kan användas för en rad applikationer, inklusive exponering för hel cigarettrök eller inflammatoriska mediatorer och samkultur/infektion med virus eller bakterier.
Protokollet i detta manuskript, som illustrerar förfarandet steg för steg, förväntas ge en grund och/eller referens för dem som är intresserade av att implementera eller anpassa sådana odlingssystem i sitt laboratorium.
Introduction
Luftvägsepitelets roll i en mängd akuta och kroniska lungsjukdomar har beskrivits i olika recensioner 1,2,3,4,5,6,7. Väl differentierade kulturer av luftvägsepitelceller är ett viktigt verktyg för att avslöja luftvägsepitelets roll. Luft-vätskegränssnitt (ALI) luftvägsepitelcellodling används i stor utsträckning för att främja differentieringen av luftvägsbasala epitelceller och därigenom studera luftvägsepitelet på ett tillförlitligt sätt in vitro 8,9. Under de senaste åren har användningen av sådana modeller ökat ytterligare till följd av nya forskningsinitiativ relaterade till COVID-19-pandemin och en global övergång till djurfri forskning. Därför betonar den ökade användningen av denna modellcellinje behovet av att dela procedurer och erfarenheter för att få robusta resultat. Detta kommer också att göra det möjligt att jämföra resultat mellan forskargrupper. Förfarandets robusthet är den viktigaste egenskapen och måste därför genomgå kvalitetskontroll. Flera laboratorier har investerat i att utveckla protokoll för odling av primära luftvägsepitelceller vid ALI. Tiden, ansträngningen och den budget som krävs kan minskas när dessa procedurer delas i detalj. Dessa detaljer inkluderar till exempel valet av cellodlingsplast och media som tillhandahålls av olika tillverkare, eftersom detta visade sig påverka egenskaperna hos de erhållnakulturerna 10,11,12. Detta betonar vikten av att utbyta erfarenheter och detaljer om kulturförfaranden, eftersom resultaten kan påverkas och/eller valideringsinsatser i olika laboratorier kan hämmas i avsaknad av sådana insikter.
Det mänskliga lungepitelet består av olika celltyper, inklusive huvudtyper såsom basalceller, cilierade celler, bägarceller och klubbceller. För att på ett tillförlitligt sätt efterlikna epitelcellskiktet i luftvägarna in vitro måste dessa celltyper representeras i odlingsmodellerna, och deras polarisering och funktion bibehålls13,14,15,16. Insikten att donatoregenskaper (inklusive sjukdomstillstånd) och cellernas anatomiska ursprung (dvs. nasal, trakeal, stora och små luftvägar) kan påverka cellkulturens cellulära sammansättning och funktionella svar är lika viktigt. Relevant expertis och övning är en förutsättning för att framgångsrikt odla primära luftvägsepitelceller och bedöma kulturens kvalitet både intuitivt (genom visuell inspektion under odling) och kvantifierbart. Syftet med detta bidrag är att tillhandahålla en kostnads- och tidseffektiv metod för isolering och odling av primära humana bronkialepitelceller (PBECs) som också kan tillämpas på odling av trakealceller och små luftvägsepitelceller. Förutom att beskriva en metod för att isolera sådana celler från resekterad lungvävnad presenteras och diskuteras en metod för expansion och biobankning, och slutligen för etablering och karakterisering av en väl differentierad ALI-kultur inom rimlig kostnad och tidsperiod.
Protocol
Representative Results
Discussion
Protokollet som presenteras här beskriver isoleringen av humana bronkialepitelceller från resekterad lungvävnad, en metod för optimal expansion av celler utan förlust av differentieringspotential, ett kryokonserveringsförfarande och ett förfarande för att generera väldifferentierade ALI-PBEC-kulturer. Dessutom ges en beskrivning av kvalitetskontroll samt instruktioner för övervakning och utvärdering av de differentierade ALI-PBECs.
Det beskrivna protokollet börjar med en makroskopiskt normal, tumörfri bronkialring som resekteras från en lunglob från patienter som genomgår operation relaterad till deras lungcancerdiagnos. Det bör därför noteras att dessa ringar strikt inte kan betraktas som frisk vävnad, vilket därför kan påverka cellodlingsegenskaperna. Alternativa källor för att erhålla bronkialepitelceller inkluderar användning av bronkialbiopsier, bronkialborstningar eller vävnad från en transplantationsgivare eller mottagande lungor. Oavsett källa bör en risk för mikrobiell kontaminering beaktas vid användning av lungvävnad, och därför används antibiotika i de olika odlingsmedierna för att minska risken för mikrobiell kontaminering av cellkulturen. I synnerhet är mykoplasma en hög och vanlig risk vid cellodling på grund av dess många olika effekter på cellodling, resistens mot antibiotika som vanligtvis används i cellodling och det faktum att mykoplasmakontaminering endast kan bekräftas genom mykoplasmadetektionsanalyser. Därför används i det inledande skedet av cellodling efter isolering av celler från lungvävnad den bredspektrum antimikrobiella formuleringen Priprimcin, och under odlingsprocessen testas slumpmässigt utvalda prover för närvaro av mykoplasma.
Isoleringsproceduren som börjar med en bronkialring ger tillräckligt utgångsmaterial för att möjliggöra graden av expansion av dessa primära celler som behövs för att starta kulturer vid ALI utan att kompromissa med differentieringskapaciteten. Att starta expansionen av de isolerade epitelcellerna med ett begränsat antal celler kan dock utgöra problem med att erhålla ett tillräckligt antal insatser med tillräckligt många celler som kan sås för ALI-odling. Förlängd odling och upprepad passage av primära celler kan resultera i replikativ åldrande. Olika lösningar har föreslagits för att övervinna denna begränsning. Horani et al. visade att Rho-kinashämmaren (ROCK) Y-27632 ökade spridningen av basalceller30, Mou et al. använde dubbel Smad-hämning för att expandera basala stamceller samtidigt som egenskaperna hos det differentierade epitelcellskiktet 31 bibehölls, och Sachs et al. har utvecklat ett luftvägsorganoidsystem som kan användas för att expandera luftvägsepitelceller och bibehålla deras differentieringspotential under flera passager32. Den senare metoden användes också för att expandera celler från källor med mycket lågt cellantal, såsom trakealaspirat (TA) från prematura spädbarn (<28 veckors graviditetsålder) och bronkoalveolär sköljvätska (BAL), före överföring till ALI-kulturen som beskrivs här33. Det visade sig att celler isolerade från BAL och TA visade en differentieringskapacitet som liknade celler genererade från bronkial vävnad, även om skillnader observerades när differentieringen var skev mot mer cilierade eller mer bägarcellsinnehållande kulturer med användning av Notch-signaleringshämning eller Th2-cytokinet IL-1333. Det rekommenderas därför att om ALI-PBECs odlas från ett utgångsmaterial med lågt epitelialt cellantal med liknande metoder, att alltid kontrollera kulturerna för de grundläggande kvalitetskriterierna, vilket diskuteras i avsnitt 6 i protokollet. Det är viktigt att användningen av matarceller också kan hjälpa till att få större cellnummer, vilket är viktigt i en miljö för transplanterbar ställningsteknik där tid och cellantal är avgörande. Detta illustreras av en studie där autologa epitelceller odlades från biopsier härrörande från en patient med trakealsjukdom och celler snabbt expanderades i närvaro av ett murint embryonalt matarskikt (mitotiskt inaktiverade 3T3-J2-fibroblaster) och den ovan nämnda hämmaren av Rho/ROCK-vägen (Y-27632)34. Den resulterande cellkulturen visade sig vara användbar för återinsättning av trakealställningar, och därmed kan detta ses som ett lämpligt protokoll för en transplantationsmodell.
När man använder protokollet som beskrivs i detta bidrag, men också när man använder andra kulturprotokoll, introduceras oundvikligen en urvalsbias. Det är viktigt att inse att skillnader i protokolldetaljer, såsom ursprunget till celler som används för att initiera kulturer, mediumsammansättning och andra protokolldetaljer, kan leda till förändringar i cellulär sammansättning av kulturerna och därmed förändringar i svaret från ALI-kulturen33,35. Dessutom har skillnader i cellegenskaper också observerats vid jämförelse av olika medier för differentiering av luftvägscellerna10,11. Vid jämförelse av PneumaCult och cBD-medium observerades skillnader i bägarcell- och klubbcells-mRNA-markörer, TEER-värden och cellskikttjocklek. Baserat på dessa observationer, trots bristen på statistisk grund, på grund av det låga antalet donatorer som används, mediets sammansättning är okänd för kunderna och högre kostnader för PneumaCult-mediet, fattades beslutet i vårt laboratorium att använda cBD-medium.
Som diskuterats kan celler initialt expanderas med hjälp av organoidkultur och därefter överföras till 2D ALI-insatssystemet. Detta är viktigt eftersom luftvägsepitelorganoider inte är lämpliga för exponering för luftburna ämnen, medan användningen av ALI 2D-systemet möjliggör utvärdering av effekterna av luftburna ämnen som cigarettrök23,36 på odlade luftvägsepitelceller. Ett annat tillvägagångssätt för att etablera ALI luftvägsepitelcellkulturer är att generera luftvägsepitelceller genom differentiering av humana pluripotenta stamceller (hiPSCs)37. I sådana protokoll, i slutskedet av differentieringsprotokollet efter differentiering till proximala luftvägsprogenitorer, kan celler differentieras genom odling till ALI med hjälp av procedurer som liknar de som beskrivs här.
I det nuvarande protokollet används cBD-medium för odling vid ALI. cBD-medium är ett serumfritt medium som bereds genom att lägga till en blandning av olika kosttillskott, inspirerade av Fulcher et al.38 samt andra studier. Tilläggslösningen innehåller 52 μg/ml bovint hypofysextrakt (BPE), 0,5 μg/ml hydrokortison, 0,5 ng/ml human EGF, 0,5 μg/ml epinefrin, 10 μg/ml transferrin, 5 μg/ml insulin, 6,5 ng/ml trijodtyronin och 0,1 ng/ml RA39. Eftersom BPE är ett vävnadsextrakt och utsätts för satsvis variation kan mediet inte betraktas som ett fullständigt definierat medium och inte heller djurfritt. Cellodlingsmedium som är fullständigt definierat föredras för att minimera skillnader mellan batch och batch. Med tanke på övergången till djurfri forskning är det viktigt att insatser görs för att producera definierade medier som inte innehåller animaliska produkter och som är överkomliga för forskarsamhället.
Olika experimentella uppställningar kan användas baserat på ALI-modellen, beroende på forskningsfrågan. Till exempel, för att undersöka effekterna av föreningar som kan påverka differentieringsprocessen, kan detta åtgärdas genom att tillsätta föreningarna till kulturen under de olika stadierna av nedsänkt kultur, under differentiering eller vid det väldifferentierade stadiet. Den cellulära sammansättningen av ALI-PBEC-kulturen kan påverkas genom tillsats av specifika föreningar; till exempel genererar differentiering av ALI-PBECs i närvaro av IL-13 en kultur med fler bägarceller och färre cilierade celler, medan behandling med γ-sekretashämmaren DAPT (används för att blockera Notch-signalering) under differentiering resulterar i en kultur med mer cilierade celler på bekostnad av bägarceller 23,40,41,42.
Vidare kan medel för att stimulera celler eller blockera vissa processer antingen appliceras på basalfacket eller (i en mycket liten volym) till kulturens apikala fack. Celler kan också utsättas för luftburna ämnen från den apikala sidan. Sådana exponeringsdesigner har använts för att studera effekten av dieselavgaser eller hel cigarettrök på PBECs23,43,44. Mediet kan skördas varje gång mediet ändras för att övervaka utsöndrade proteiner på bassidan; Detsamma gäller för den apikala sidan av cellerna som tvättas med PBS medan basalmediet uppdateras. Den så kallade apikala tvätten skördas och valfri ditioerytritol (DTE) tillsätts för att dissociera slem som produceras av bägarcellerna mer effektivt. Celllysater kan erhållas för isolering av totalt protein, RNA och kromosomalt och mitokondriellt DNA. Cellerna kan studeras ytterligare med hjälp av antikroppar för specifika markörer, genom att skära polyetylentereftalat (PET) -membranet från plastinsatsen och ytterligare skära detta membran i mindre bitar för flera immunofluorescensfärgningar45. Vidare kan flödescytometri eller FACS också användas efter trypsinisering av cellerna i insatserna. Under ALI-steget kan utvecklingen av cellbarriären övervakas genom att mäta det elektriska motståndet och därefter beräkna TEER, där det elektriska motståndet är omvänt proportionellt mot membraninsatsens yta. Beräkningen baseras på Ohms lag med följande formel: 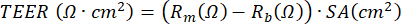 , där Rm är det uppmätta elektriska motståndet, Rb är baslinjens elektriska motstånd för en insats utan beläggning och celler, och SA är ytan på skärets membran. Att mäta det elektriska motståndet med EVOM2- och STX/chopstick-elektroder är enkelt men mycket beroende av hanteringsprocedurer när det införs i brunnen. Elektrodens form har också föreslagits påverka mätningen av barriärfunktionen hos den relativt stora ytan17.
, där Rm är det uppmätta elektriska motståndet, Rb är baslinjens elektriska motstånd för en insats utan beläggning och celler, och SA är ytan på skärets membran. Att mäta det elektriska motståndet med EVOM2- och STX/chopstick-elektroder är enkelt men mycket beroende av hanteringsprocedurer när det införs i brunnen. Elektrodens form har också föreslagits påverka mätningen av barriärfunktionen hos den relativt stora ytan17.
Ytterligare förbättring av ALI-cellodlingssystemet, som syftar till att öka noggrann vävnadsrepresentation, inkluderar samodling av ytterligare celltyper, såsom leukocyter, fibroblaster eller endotelceller46,47,48. Det har observerats att denna samodling av ALI-PBEC med granulocyt-makrofagkolonistimulerande faktor (GM-CSF) eller M-CSF-differentierade makrofager markant påverkar medfödda epitelsvar och reparation48. Det är viktigt att notera att i sådana samkulturmodeller kan medelkompatibilitet vara ett problem. Eftersom mediet som används för luftvägsepitelcellodling är utvecklat specifikt för PBEC och kanske inte är optimalt lämpat för andra celltyper, är optimering nödvändig. En annan typ av framsteg som ses inom luftvägsbiologi för vilken isolerade PBEC kan användas är användningen av Organs-on-Chips (OoC) -teknik49,50. Med hjälp av denna teknik kan påverkan av de mekaniska krafterna för andning och blodflöde, såsom stretch, luft och medelflöde, studeras 29.
Variabilitet mellan donatorer kan vara signifikant vid användning av PBEC från olika donatorer, och därför är det viktigt att överväga att använda celler från flera donatorer för att ta hänsyn till denna variabilitet i epitelcellodlingsstudier. Eftersom odlingen av ALI-PBEC är tidskrävande och förknippad med betydande kostnader, undersöks möjligheten att etablera ALI-PBEC-kulturer genom att blanda celler från olika givare i en cellodlingsinsats. På så sätt kan pilotexperiment lätt utföras med hjälp av primära celler innan man analyserar svaren från kulturer härrörande från olika enskilda givare . Dessutom kan donatorer med olika egenskaper (t.ex. olika åldersgrupp eller kön) grupperas för explorativa studier. Vid användning av donatorblandningar är det viktigt att se till att lika cellantal av olika givare är närvarande, för att förhindra möjligheten att en givare dominerar resultaten till följd av en högre spridningshastighet. Därför expanderas celler från enskilda givare separat och sås med högre densitet i insatsen jämfört med såddceller från en enskild givare, för att minimera proliferation i insatsen före övergång till ALI. Svar från donatorblandningar och motsvarande enskilda givare jämfördes genom att studera infektionskinetiken för SARS-CoV-2. Med hjälp av RT-qPCR och immunofluorescensfärgning observerades att donatorblandningen gav en bra representation av de olika enskilda givarna genom att visa liknande antal producerade viruspartiklar och liknande antal infekterade celler28.
För att bli ett godtagbart alternativ för djurmodeller bör genredigering av odlade bronkialepitelceller vara genomförbar51. RNA-interferensteknik genom att använda små interfererande RNA (siRNA) i ALI-PBECs undersöks, men eftersom cellerna måste transfekteras med siRNA under den nedsänkta fasen av kulturen, upprätthålls inte knockdown tillräckligt under ALI-odling på grund av den långa odlingstiden, såvida inte siRNA-transfektion ofta upprepas under odling52. Ändå kan siRNA framgångsrikt användas för att modifiera genuttryck i nedsänkta basalceller. Andra har framgångsrikt använt CRISPR/Cas9-teknik för att uppnå genredigering i primära ALI luftvägsepitelcellkulturer med ribonukleoprotein (RNP) leverans 53. Vid användning av sådana tekniker är det viktigt att cellerna bibehåller sin fulla differentieringskapacitet. Eftersom primära luftvägscellkulturer inte kan passera på obestämd tid är klonal expansion av de genredigerade cellerna inte lätt och tillsatsen av medium för att välja transfekterade celler är besvärlig. Därför är det svårt att uppnå den önskvärda knockdownen i alla odlade celler. Ett alternativ för att generera knockoutkloner är användningen av knock-out-strategier i hiPSCs54 och användningen av dessa celler för att generera luftvägsepitelceller. Ett annat, om än suboptimalt, alternativ är att etablera en odödlig PBE-linje för att klonalt expandera genredigerade celler55.
Protokollet som presenteras här är ett sätt att generera en väl differentierad pseudostratifierad ALI-PBEC, men andra protokoll har också visat sig etablera en sådan kultur, med mindre och större skillnader jämfört med det presenterade protokollet. Enligt vår mening är validering av odlingsmetoder och sträng kvalitetskontroll över laboratorier avgörande för att ALI-PBEC-systemet och liknande odlingssystem för luftvägsepitelceller ska bli ett giltigt alternativ för djurförsök.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Studierna som använder modellen som beskrivs i detta bidrag har fått stöd av en mängd olika finansieringsorganisationer, inklusive Lung Foundation Netherlands, Netherlands Organization for Health Research and Development (ZonMw, COVID-19 MKMD-bidrag), Dutch Society for the Replacement of Animal Testing (Stichting Proefdiervrij, grant #114025007), samt forskningsbidrag från företag som Boehringer Ingelheim och Galapagos. Figur 1 skapades med BioRender.com.
Materials
| 1,000 ohm test resistor | World Precision Instruments | N/A | Used to calibrate the EVOM2 Epithelial Voltohmmeter |
| 4-[2-(5,6,7,8-Tetrahydro-5,5,8,8-tetramethyl-2-naphthalenyl)ethynyl)-benzoic acid (EC 23) | Tocris | 4011 | Used in cBD medium |
| 6-well Clear TC-treated Multiple Well Plates | Corning | 3506 | Used in the first step to grow the cells isolated form the bronchial ring |
| Airway Epithelial Cell Growth Medium Kit | PromoCell | C-21160 | Used to compare to cBD medium |
| Bead Bath 20 Liter | Lab Armor | 74220-720 | Used to pre-warm cell culture solutions |
| BEGM Bronchial Epithelial Cell Growth Medium BulletKit | LONZA | CC-3170 | Used to compare to cBD medium |
| Bovine albumin fraction V (BSA) | Thermo Fisher Scientific | 15260037 | Used in coating solution |
| Bovine pituitary extract (BPE) | Thermo Fisher Scientific | 37000-015 | Used in c-KSFM |
| Bronchial epithelial cell growth supplement (BEpiCGS) | ScienCell Research Laboratories | 3262 | Used in cBD medium |
| Bronchial epithelial cell medium-basal (BEpiCM-b) | ScienCell Research Laboratories | SCC3211-b | Used in cBD medium |
| Cell culture inserts; 12 mm Transwell with 0.4 µm pore polyester membrane insert | Corning | 3460 | Cell culture inserts used in the protocol |
| Cell culture inserts; 12-well inserts, 0.4 µm PET clear | CellQART made by SABEU | 9310412 | Cell culture inserts used to compare with Corning cell culture inserts |
| Cell culture inserts; 12-well ThinCert Tissue culture Inserts | Greiner Bio-One | 82050-032 | Cell culture inserts used to compare with Corning cell culture inserts |
| CELLSTAR flask, TC, PS, 250 ml, 75 cm2 | Greiner Bio-One | 658170 | Used to expand the number cells |
| CFX Maestro 1.0 | Bio-Rad | N/A | Software program for analyzing qPCR data generated with the CFX384 System |
| CFX384 Touch Real-Time PCR Detection System | Bio-Rad | 1855484 | qPCR detection system |
| Chopstick electrode set | World Precision Instruments | STX2 | Used to measure electrical resistance in ALI-PBEC |
| CO2-Incubator | PHCbi | MCO-170AICUV-PE | Cell culture incubator used for mycplasma free cell cultures |
| CO2-Incubator | Hereaus | Heracell 150 | Cell culture incubator used for possibly mycplasma infected cell cultures |
| Coolcell Container | Corning | 432006 | Used to cryopreserve cells at -80 °C before transfer to liquid N2 |
| Countess 3 Automated cell counter | Thermo Fisher Scientific | AMQAX2000 | Used to count cells and determine the cell concentration |
| Cryovials | Nalgene | 479-3224 | Used to cryopreserve cells in |
| D-Glucose | Avantor VWR BDH CHEMICALS | 101174Y | Used in soft trypsin |
| Dimethyl sulfoxide (DMSO) | Avantor VWR | 0231 | Used in cell freeze medium |
| dNTP (10 mM) | Promega | U1515 | Used in the synthesis of cDNA |
| Dulbecco's Modified Eagle's Medium (DMEM) + 4500 mg/l D-Glucose | STEMCELL Technologies | 36250 | Used in cBD medium |
| Dulbecco's Modified Eagle's Medium (DMEM) 4.5 g/l glucose with l-glutamine | LONZA | LOBE12-604F | Used in cBD medium to compare with DMEM from other manufacturers |
| Dulbecco's Modified Eagle's Medium (DMEM), high glucose, pyruvate | Thermo Fisher Scientific | 41966029 | Used in cBD medium to compare with DMEM from other manufacturers |
| Epidermal growth factor (EGF) | Thermo Fisher Scientific | 37000-015 | Used in c-KSFM |
| Ethylenediaminetetraacetic acid (EDTA) | Avantor VWR BDH CHEMICALS | 443885J | Used in soft trypsin |
| EVOM2 Epithelial Voltohmmeter | World Precision Instruments | 91799 | Used with the chopstick electrode set to measure electrical resistance in ALI-PBEC |
| Fibronectin solution, Human | PromoCell | C-43060 | Used in coating solution |
| Glutamax | Thermo Fisher Scientific | 35050038 | Used in cBD medium |
| Hanks balanced salt solution (HBSS) | ScienCell Research Laboratories | SCC0313 | Used to dissolve protease XIV |
| IQ SYBR Green Super mix | Bio-Rad | 170887 | qPCR reagent |
| Isoproterenol hydrochloride, (-)- | Sigma-Aldrich | I-6504 | Used in c-KSFM |
| Keratinocyte-SFM (KSFM) | Thermo Fisher Scientific | 17005-034 | Used in c-KSFM |
| Maxwell RSC Instrument | Promega | AS4500 | Automated RNA isolation system |
| Maxwell RSC simplyRNA Tissue Kit | Promega | AS1340 | Used to isolate total RNA with the Maxwell RSC Instrument |
| M-MLV Reverse transcriptase | Promega | M5301 | Used in the synthesis of cDNA |
| M-MLV Reverse transcriptase 5X reaction buffer | Promega | M531A | Used in the synthesis of cDNA |
| MycoStrip | InvivoGen | rep-mys-10 | Used to detect the presence of mycoplasma in cell culture samples |
| N-2-hydroxyethylpiperazine-N-2-ethane sulfonic acid (HEPES) | Thermo Fisher Scientific | 15630056 | Used in cBD medium |
| Oligo(dT)15 | Qiagen | 79237 | Used in the synthesis of cDNA |
| Penicillin/Streptomycin solution (Pen/Strep) | ScienCell Research Laboratories | SCC0513 | Used as antibiotic in c-KSFM and cBD medium |
| Phosphate buffered saline (PBS) | LUMC pharmacy | N/A | Used in different steps of the protocol |
| Pneumacult-ALI Medium | STEMCELL Technologies | 05002 | Used to grow cells in the differentiation stage to compare to cBD medium |
| Pneumacult-Ex Plus Medium | STEMCELL Technologies | 05040 | Used to grow cells in the submerged stage to compare to cBD medium |
| Primer, ATP5B, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: TCACCCAGGCTGGTTCAGA |
| Primer, ATP5B, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: AGTGGCCAGGGTAGGCTGAT |
| Primer, FOXJ1, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: GGAGGGGACGTAAATCCCTA |
| Primer, FOXJ1, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TTGGTCCCAGTAGTTCCAGC |
| Primer, MUC5AC, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: CCTTCGACGGACAGAGCTAC |
| Primer, MUC5AC, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TCTCGGTGACAACACGAAAG |
| Primer, MUC5B, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: GGGCTTTGACAAGAGAGT |
| Primer, MUC5B, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: AGGATGGTCGTGTTGATGCG |
| Primer, RPL13A, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: AAGGTGGTGGTCGTACGCTGTG |
| Primer, RPL13A, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: CGGGAAGGGTTGGTGTTCATCC |
| Primer, SCGB1A1, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: ACATGAGGGAGGCAGGGGCTC |
| Primer, SCGB1A1, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: ACTCAAAGCATGGCAGCGGCA |
| Primer, TP63, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: CCACCTGGACGTATTCCACTG |
| Primer, TP63, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TCGAATCAAATGACTAGGAGGGG |
| Primocin | InvivoGen | ant-pm-2 | Used as antimicrobial agent against bacteria, mycoplasma, and fungi in c-KSFM medium |
| Protease XIV | Sigma-Aldrich | P5147 | Used for the enzymatic treatment of the bronchial ring |
| RNAsin Recombinant Ribonuclease inhibitor | Promega | N2515 | Used in the synthesis of cDNA |
| Soybean trypsin inhibitor (SBTI) | Sigma-Aldrich | T9128 | Used to inhibit the action of soft trypsin |
| T100 Thermal Cycler | Bio-Rad | 1861096 | Used in the synthesis of cDNA |
| TissueSAFE plus | MILESTONE MEDICAL | N/A | Vacuum transfer system for biological specimens |
| Trypan blue solution | Thermo Fisher Scientific | 15250061 | Used to count live- and dead cells |
| Trypsin 1:250 | Thermo Fisher Scientific | 27250-018 | Used in soft trypsin |
| Type I collagen solution (PureCol) | Advanced BioMatrix | 5005-B | Used in coating solution |
| Universal container, PP, with PE screw cap | Avantor VWR | 216-2053 | Used in the protocol for the Protease XIV treatment of the bronchial ring |
References
- Aghapour, M., et al. Role of air pollutants in airway epithelial barrier dysfunction in asthma and COPD. European Respiratory Review. 31 (163), 210112 (2022).
- de Waal, A. M., Hiemstra, P. S., Ottenhoff, T. H., Joosten, S. A., vander Does, A. M. Lung epithelial cells interact with immune cells and bacteria to shape the microenvironment in tuberculosis. Thorax. 77 (4), 408-416 (2022).
- Duchesne, M., Okoye, I., Lacy, P. Epithelial cell alarmin cytokines: Frontline mediators of the asthma inflammatory response. Frontiers in Immunology. 13, 975914 (2022).
- Hewitt, R. J., Lloyd, C. M. Regulation of immune responses by the airway epithelial cell landscape. Nature Reviews Immunology. 21 (6), 347-362 (2021).
- Ruysseveldt, E., Martens, K., Steelant, B. Airway basal cells, protectors of epithelial walls in health and respiratory diseases. Frontiers in Allergy. 2, 787128 (2021).
- Alysandratos, K. D., Herriges, M. J., Kotton, D. N. Epithelial stem and progenitor cells in lung repair and regeneration. Annual Review of Physiology. 83, 529-550 (2021).
- Hammad, H., Lambrecht, B. N. Barrier epithelial cells and the control of type 2 immunity. Immunity. 43 (1), 29-40 (2015).
- Hynds, R. E., Bonfanti, P., Janes, S. M. Regenerating human epithelia with cultured stem cells: feeder cells, organoids and beyond. EMBO Molecular Medicine. 10 (2), 139-150 (2018).
- Hiemstra, P. S., Tetley, T. D., Janes, S. M. Airway and alveolar epithelial cells in culture. The European Respiratory Journal. 54 (5), 1900742 (2019).
- Saint-Criq, V., et al. Choice of differentiation media significantly impacts cell lineage and response to CFTR modulators in fully differentiated primary cultures of cystic fibrosis human airway epithelial cells. Cells. 9 (9), 2137 (2020).
- Leung, C., Wadsworth, S. J., Yang, S. J., Dorscheid, D. R. Structural and functional variations in human bronchial epithelial cells cultured in air-liquid interface using different growth media. American Journal of Physiology. Lung Cellular and Molecular Physiology. 318 (5), L1063-L1073 (2020).
- Morgan, R., et al. A medium composition containing normal resting glucose that supports differentiation of primary human airway cells. Scientific Reports. 12 (1), 1540 (2022).
- Ghosh, B., et al. Strong correlation between air-liquid interface cultures and in vivo transcriptomics of nasal brush biopsy. American Journal of Physiology. Lung Cellular and Molecular Physiology. 318 (5), L1056-L1062 (2020).
- Pezzulo, A. A., et al. The air-liquid interface and use of primary cell cultures are important to recapitulate the transcriptional profile of in vivo airway epithelia. American Journal of Physiology. Lung Cellular and Molecular Physiology. 300 (1), L25-L31 (2011).
- Dvorak, A., Tilley, A. E., Shaykhiev, R., Wang, R., Crystal, R. G. Do airway epithelium air-liquid cultures represent the in vivo airway epithelium transcriptome. American Journal of Respiratory Cell and Molecular Biology. 44 (4), 465-473 (2011).
- Legebeke, J., et al. Temporal whole-transcriptomic analysis of characterized in vitro and ex vivo primary nasal epithelia. Frontiers in Cell and Developmental Biology. 10, 907511 (2022).
- Srinivasan, B., et al. TEER measurement techniques for in vitro barrier model systems. Journal of Laboratory Automation. 20 (2), 107-126 (2015).
- van Wetering, S., et al. Regulation of secretory leukocyte proteinase inhibitor (SLPI) production by human bronchial epithelial cells: increase of cell-associated SLPI by neutrophil elastase. Journal of Investigative Medicine. 48 (5), 359-366 (2000).
- Balk, S. D. Calcium as a regulator of the proliferation of normal, but not of transformed, chicken fibroblasts in a plasma-containing medium. Proceedings of the National Academy of Sciences. 68 (2), 271-275 (1971).
- Gail, M. H., Boone, C. W., Thompson, C. S. A calcium requirement for fibroblast motility and prolifertion. Experimental Cell Research. 79 (2), 386-390 (1973).
- Dulbecco, R., Elkington, J. Induction of growth in resting fibroblastic cell cultures by Ca. Proceedings of the National Academy of Sciences. 72 (4), 1584-1588 (1975).
- van Wetering, S., et al. Epithelial differentiation is a determinant in the production of eotaxin-2 and -3 by bronchial epithelial cells in response to IL-4 and IL-13. Molecular Immunology. 44 (5), 803-811 (2007).
- Amatngalim, G. D., et al. Aberrant epithelial differentiation by cigarette smoke dysregulates respiratory host defence. The European Respiratory Journal. 51 (4), 1701009 (2018).
- Christie, V. B., et al. Retinoid supplementation of differentiating human neural progenitors and embryonic stem cells leads to enhanced neurogenesis in vitro. Journal of Neuroscience Methods. 193 (2), 239-245 (2010).
- Schrumpf, J. A., Ninaber, D. K., vander Does, A. M., Hiemstra, P. S. TGF-β1 impairs vitamin D-induced and constitutive airway epithelial host defense mechanisms. Journal of Innate Immunity. 12 (1), 74-89 (2020).
- Schrumpf, J. A., et al. Proinflammatory cytokines impair vitamin D-induced host defense in cultured airway epithelial cells. American Journal of Respiratory Cell and Molecular Biology. 56 (6), 749-761 (2017).
- Boei, J. J. W. A., et al. Xenobiotic metabolism in differentiated human bronchial epithelial cells. Archives of Toxicology. 91 (5), 2093-2105 (2017).
- Wang, Y., et al. Impact of human airway epithelial cellular composition on SARS-CoV-2 infection biology. bioRxiv. , (2021).
- Nawroth, J. C., et al. Breathing on Chip: Dynamic flow and stretch tune cellular composition and accelerate mucociliary maturation of airway epithelium in vitro. bioRxiv. , (2022).
- Horani, A., Nath, A., Wasserman, M. G., Huang, T., Brody, S. L. Rho-associated protein kinase inhibition enhances airway epithelial Basal-cell proliferation and lentivirus transduction. American Journal of Respiratory Cell and Molecular Biology. 49 (3), 341-347 (2013).
- Mou, H., et al. Dual SMAD signaling inhibition enables long-term expansion of diverse epithelial basal cells. Cell Stem Cell. 19 (2), 217-231 (2016).
- Sachs, N., et al. Long-term expanding human airway organoids for disease modeling. The EMBO Journal. 38 (4), 100300 (2019).
- Eenjes, E., et al. Disease modeling following organoid-based expansion of airway epithelial cells. American Journal of Physiology. Lung Cellular and Molecular Physiology. 321 (4), L775-L786 (2021).
- Butler, C. R., et al. Rapid expansion of human epithelial stem cells suitable for airway tissue engineering. American Journal of Respiratory and Critical Care Medicine. 194 (2), 156-168 (2016).
- Amatngalim, G. D., et al. Antibacterial defense of human airway epithelial cells from chronic obstructive pulmonary disease patients induced by acute exposure to nontypeable Haemophilus influenzae: modulation by cigarette smoke. Journal of Innate Immunity. 9 (4), 359-374 (2017).
- Plebani, R., et al. 3D lung tissue models for studies on SARS-CoV-2 pathophysiology and therapeutics. International Journal of Molecular Sciences. 23 (17), 10071 (2022).
- Wong, A. P., et al. Directed differentiation of human pluripotent stem cells into mature airway epithelia expressing functional CFTR protein. Nature Biotechnology. 30 (9), 876-882 (2012).
- Fulcher, M. L., Gabriel, S., Burns, K. A., Yankaskas, J. R., Randell, S. H. Well-differentiated human airway epithelial cell cultures. Methods in Molecular Biology. 107, 183-206 (2005).
- Cao, J., Wong, C. K., Yin, Y., Lam, C. W. K. Activation of human bronchial epithelial cells by inflammatory cytokines IL-27 and TNF-alpha: implications for immunopathophysiology of airway inflammation. The Journal of Cellular Physiology. 223 (3), 788-797 (2010).
- Tsao, P. N., et al. Notch signaling controls the balance of ciliated and secretory cell fates in developing airways. Development. 136 (13), 2297-2307 (2009).
- Laoukili, J., et al. IL-13 alters mucociliary differentiation and ciliary beating of human respiratory epithelial cells. The Journal of Clinical Investigation. 108 (12), 1817-1824 (2001).
- Mertens, T. C. J., et al. Cigarette smoke differentially affects IL-13-induced gene expression in human airway epithelial cells. Physiological Reports. 5 (13), e13347 (2017).
- Zarcone, M. C., et al. Effect of diesel exhaust generated by a city bus engine on stress responses and innate immunity in primary bronchial epithelial cell cultures. Toxicology in Vitro. 48, 221-231 (2018).
- vander Does, A. M., et al. Early transcriptional responses of bronchial epithelial cells to whole cigarette smoke mirror those of in-vivo exposed human bronchial mucosa. Respiratory Research. 23 (1), 227 (2022).
- Wang, Y., Ninaber, D. K., van Schadewijk, A., Hiemstra, P. S. Tiotropium and fluticasone inhibit rhinovirus-induced mucin production via multiple mechanisms in differentiated airway epithelial cells. Frontiers in Cellular and Infection Microbiology. 10, 278 (2020).
- Ronaghan, N. J., et al. M1-like, but not M0- or M2-like, macrophages, reduce RSV infection of primary bronchial epithelial cells in a media-dependent fashion. PLoS One. 17 (10), 0276013 (2022).
- Gindele, J. A., et al. Opposing effects of in vitro differentiated macrophages sub-type on epithelial wound healing. PLoS One. 12 (9), e0184386 (2017).
- van Riet, S., et al. Modulation of airway epithelial innate immunity and wound repair by M(GM-CSF) and M(M-CSF) macrophages. Journal of Innate Immunity. 12 (5), 410-421 (2020).
- Huh, D., et al. Reconstituting organ-level lung functions on a chip. Science. 328 (5986), 1662-1668 (2010).
- Stucki, A. O., et al. A lung-on-a-chip array with an integrated bio-inspired respiration mechanism. Lab on a Chip. 15 (5), 1302-1310 (2015).
- Peters-Hall, J. R., et al. Long-term culture and cloning of primary human bronchial basal cells that maintain multipotent differentiation capacity and CFTR channel function. American Journal of Physiology. Lung Cellular and Molecular Physiology. 315 (2), L313-L327 (2018).
- Bartman, C. M., Stelzig, K. E., Linden, D. R., Prakash, Y. S., Chiarella, S. E. Passive siRNA transfection method for gene knockdown in air-liquid interface airway epithelial cell cultures. American Journal of Physiology. Lung Cellular and Molecular Physiology. 321 (1), L280-L286 (2021).
- Koh, K. D., et al. Efficient RNP-directed human gene targeting reveals SPDEF is required for IL-13-induced mucostasis. American Journal of Respiratory Cell and Molecular Biology. 62 (3), 373-381 (2020).
- Bhargava, N., et al. Development of an efficient single-cell cloning and expansion strategy for genome edited induced pluripotent stem cells. Molecular Biology Reports. 49 (8), 7887-7898 (2022).
- Angelopoulou, A., Papaspyropoulos, A., Papantonis, A., Gorgoulis, V. G. CRISPR-Cas9-mediated induction of large chromosomal inversions in human bronchial epithelial cells. STAR Protocols. 3 (2), 101257 (2022).

