Avbildning av mtHyPer7, en ratiometrisk biosensor för mitokondriell peroxid, i levande jästceller
Summary
Väteperoxid (H2O2) är både en källa till oxidativ skada och en signalmolekyl. Detta protokoll beskriver hur man mäter mitokondriellH2O2med hjälp av mitokondrieriktad HyPer7 (mtHyPer7), en genetiskt kodad ratiometrisk biosensor, i levande jäst. Den beskriver hur man optimerar avbildningsförhållanden och utför kvantitativ cellulär och subcellulär analys med hjälp av fritt tillgänglig programvara.
Abstract
Mitokondriell dysfunktion, eller funktionell förändring, finns i många sjukdomar och tillstånd, inklusive neurodegenerativa och muskuloskeletala störningar, cancer och normalt åldrande. Här beskrivs ett tillvägagångssätt för att bedöma mitokondriell funktion i levande jästceller vid cellulär och subcellulär upplösning med hjälp av en genetiskt kodad, minimalt invasiv, ratiometrisk biosensor. Biosensorn, mitokondrier riktade HyPer7 (mtHyPer7), detekterar väteperoxid (H 2 O2) i mitokondrier. Den består av en mitokondriell signalsekvens sammansmält med ett cirkulärt permuterat fluorescerande protein och den H2O-2-responsiva domänen av ett bakteriellt OxyR-protein. Biosensorn genereras och integreras i jästgenomet med hjälp av ett CRISPR-Cas9-markörfritt system, för mer konsekvent uttryck jämfört med plasmidburna konstruktioner.
mtHyPer7 är kvantitativt inriktad på mitokondrier, har ingen detekterbar effekt på jästtillväxthastighet eller mitokondriell morfologi och ger en kvantitativ avläsning för mitokondriellH2O2under normala tillväxtförhållanden och vid exponering för oxidativ stress. Detta protokoll förklarar hur man optimerar avbildningsförhållandena med hjälp av ett konfokalmikroskopsystem med snurrande skivor och utför kvantitativ analys med hjälp av fritt tillgänglig programvara. Dessa verktyg gör det möjligt att samla in rik spatiotemporal information om mitokondrier både inom celler och mellan celler i en population. Dessutom kan arbetsflödet som beskrivs här användas för att validera andra biosensorer.
Introduction
Mitokondrier är essentiella eukaryota cellulära organeller som är välkända för sin funktion att producera ATP genom oxidativ fosforylering och elektrontransport1. Dessutom är mitokondrier platser för kalciumlagring, syntes av lipider, aminosyror, fettsyra- och järn-svavelkluster och signaltransduktion 2,3. Inom celler bildar mitokondrier ett dynamiskt nätverk med karakteristisk morfologi och distribution, som varierar beroende på celltyp och metaboliskt tillstånd. Dessutom, även om mitokondrier kan smälta samman och dela sig, är inte alla mitokondrier i en cell likvärdiga. Många studier har dokumenterat den funktionella heterogeniteten hos mitokondrier inom enskilda celler i attribut som membranpotential och oxidativt tillstånd 4,5,6. Denna variation i mitokondriell funktion beror delvis på skador på organellen från mtDNA-mutationer (som förekommer i högre takt än i kärn-DNA) och på oxidativ skada av reaktiva syrearter (ROS) som genereras både i och utanför organellen 7,8,9. Skador på organellen mildras av mitokondriella kvalitetskontrollmekanismer som reparerar skadan eller eliminerar mitokondrier som är skadade bortom reparation10.
Väteperoxid (H2O2) är en reaktiv syreart som är en källa till oxidativ skada på cellulära proteiner, nukleinsyror och lipider. MenH2O2fungerar också som en signalmolekyl som reglerar cellulära aktiviteter genom reversibel oxidation av tioler i målproteiner11,12. H2O2 framställs av elektroner som läcker från mitokondrieelektrontransportkedjan och av specifika enzymer, såsom NADPH-oxidas och monoaminoxidaser 13,14,15,16,17,18,19,20. Det inaktiveras också av antioxidantsystem, inklusive de som är baserade på thioredoxin och glutation21,22,23. Således är analys av mitokondriella H2O2-nivåer avgörande för att förstå denna metabolits roll i normal mitokondriell och cellulär funktion och under förhållanden med oxidativ stress.
Det övergripande målet med detta protokoll är att detektera mitokondriellH2O2med hjälp av en genetiskt kodad ratiometrisk H 2 O 2 biosensor, HyPer7, som är riktad mot organellen (mtHyPer7). mtHyPer7 är en chimär som består av den mitokondriella signalsekvensen från ATP9 (Su9-presekvensen), en cirkulärt permuterad form av grönt fluorescerande protein (GFP) och den H2O-2-bindande domänen av OxyR-proteinet från Neisseria meningitidis24 (Figur 1). I cirkulärt permuterad GFP smälter N- och C-terminerna för naturlig GFP samman och nya terminer bildas nära kromoforen, vilket ger större rörlighet till proteinet och större labilitet av dess spektrala egenskaper jämfört med naturlig GFP25. Interaktionen mellan mtHyPer7:s OxyR-domän och H2O2är högaffinitet,H2O2-selektiv,och leder till reversibel oxidation av de konserverade cysteinresterna och disulfidbryggbildning. Konformationsförändringar associerade med oxidationen av OxyR överförs till den cirkulärt permuterade GFP i mtHyPer7, vilket resulterar i en spektral förskjutning i excitationsmaximum för mtHyPer7-kromoforen från 405 nm i reducerat tillstånd till 488 nm i H 2 O2-oxiderattillstånd26. Således återspeglar förhållandet mellan fluorescens från mtHyPer7 som svar på excitation vid 488 nm jämfört med 405 nm oxidationen av sonden med H 2 O2.
Helst bör en biosensor ge en absolut, kvantitativ avläsning i realtid av sin målmolekyl. Tyvärr är detta dock inte alltid möjligt i verkliga mätningar. När det gäller oxidationssensorer, såsom mtHyPer7, påverkas realtidsavläsningen av disulfidbryggans reduktionshastighet. Reduktionssystemen som används av ROS-biosensorer skiljer sig åt, och dessa kan dramatiskt förändra sondresponsdynamiken – vilket visas av jämförelsen mellan HyPer7, reducerad av thioredoxin-systemet, och roGFP2-Tsa2ΔCR, reducerad av glutation-i-jästcytosol27. Således, för att dra en slutsats om den relativa H2O2-koncentrationen från mtHyPer7-förhållandena, måste man anta att reduktionssystemet bibehåller en konstant kapacitet under experimentet. Trots dessa överväganden har HyPer7 och relaterade prober använts i olika sammanhang för att få information om H2O2i levande celler25,28,29.
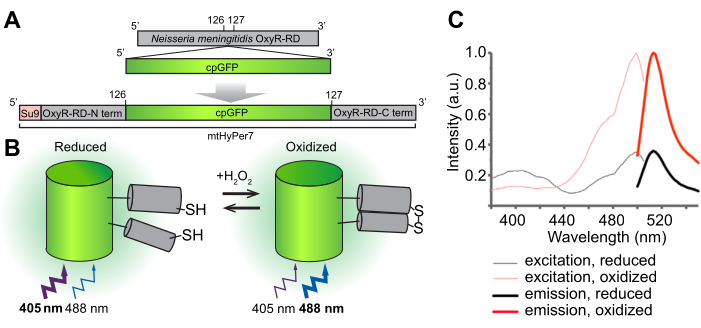
Figur 1: Design, molekylär mekanism och excitations-/emissionsspektra för H2 O2 biosensorn mtHyPer7. (A) MtHyPer7-sonden erhålls genom att föra in cirkulärt permuterad GFP i OxyR-RD-domänen från Neisseria meningitidis. Den innehåller den mitokondriella målsökningssekvensen från subenhet 9 av ATP-syntaset från Neurospora crassa (Su9). (B) Illustration av H 2 O2-avkänningsmekanismenför mtHyPer7. Oxidation av cysteiner i RD-domänen ökar fluorescensemissionen vid excitation vid 488 nm och minskar emissionen som produceras av excitation vid 405 nm. (C) Excitations- och emissionsspektra av HyPer7 i oxiderade och reducerade former. Denna figur återges med tillstånd från Pak et al.24. Förkortningar: GFP = grönt fluorescerande protein; cpGFP = cirkulärt permuterad GFP. Klicka här för att se en större version av denna figur.
Denna ratiometriska avbildning av mtHyPer7 erbjuder viktiga fördelar för mitokondriell H2O2-kvantifiering24,27; Den ger en intern kontroll för sondkoncentrationen. Dessutom är förskjutningen i excitationstoppen som produceras av H2O2-exponering inte fullständig, inte ens vid mättnadskoncentrationer avH2O2. Således kan ratio imaging öka känsligheten genom att införliva två spektralpunkter i analysen.
MtHyPer7-sonden som används här har en mycket hög affinitet förH2O2och relativt låg känslighet för pH24, och har framgångsrikt riktats mot Caenorhabditis elegans mitokondrier30. Detta protein har också använts i jäst27,31. Tidigare studier har dock förlitat sig på plasmidburet uttryck av mtHyPer7, vilket resulterar i cell-till-cell-variabilitet i sonduttryck27. Dessutom integrerades konstruktionen som beskrivs i detta protokoll i en bevarad, genfri region på kromosom X32 med hjälp av en CRISPR-baserad metod för markörfri integration. Uttrycket av den integrerade biosensorgenen styrs också av den starka konstitutiva TEF1-promotorn (Figur 2). Som ett resultat finns det mer stabilt, konsekvent uttryck av biosensorn i jästcellpopulationer jämfört med det som observeras med plasmidburet biosensoruttryck, och celler som bär biosensorn kan förökas utan behov av selektiva medier.
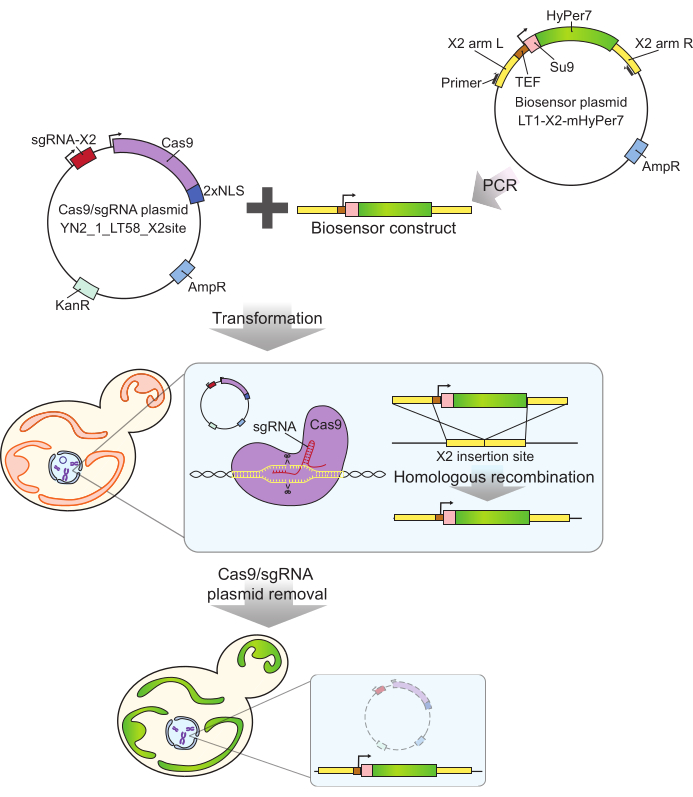
Figur 2: Generering av mtHyPer7-uttryckande celler med CRISPR. Den Cas9- och sgRNA-innehållande plasmiden (YN2_1_LT58_X2site) och PCR-amplifierade mtHyPer7-innehållande biosensorkonstruktionen introduceras i spirande jästceller genom litiumacetattransformation. Det genfria insättningsstället på kromosom X (X2) känns igen och klipps av Cas9-proteinet med sgRNA, och biosensorn integreras i genomet genom homolog rekombination. Efter identifiering av de framgångsrika transformanterna genom mikroskopisk screening, koloni-PCR och sekvensering, avlägsnas Cas9-plasmiden (botas) genom tillväxt i icke-selektiva medier. Förkortningar: sgRNA = single guide RNA; TEF = transkriptionsförstärkare. Klicka här för att se en större version av denna figur.
Slutligen erbjuder mtHyPer7 fördelar jämfört med andra ROS-biosensorer. Till exempel kan organiska färgämnen som används för att detektera ROS (t.ex. dihydroetidium [DHE]2 och MitoSOX3) ge ojämn eller ospecifik färgning och levereras ofta i lösningsmedel som etanol eller dimetylsulfoxid, som kräver ytterligare kontroller för lösningsmedelseffekter. En annan klass av ROS-biosensorer är fluorescensresonansenergiöverföring (FRET)-baserade biosensorer (t.ex. Redoxfluor för cellulärt redoxtillstånd4 och peroxidsensorerna HSP-FRET5, OxyFRET 6 och PerFRET6). Dessa prober är genetiskt kodade och i princip mycket känsliga och kan kvantitativt riktas mot mitokondrier med hjälp av väl karakteriserade mitokondriella signalsekvenser. Det finns dock utmaningar vid användning av FRET-baserade prober, inklusive bakgrund på grund av korsexcitation och genomblödning, och stränga krav på att fluoroforernas närhet och orientering för att FRET ska inträffa33,34. Dessutom består FRET-sonder av två fluorescerande proteiner som kräver större konstruktioner för uttryck i celler av intresse jämfört med spektraskiftande sonder. Protokollet som beskrivs här utvecklades för att dra nytta av styrkorna hos den HyPer7-baserade biosensorn och för att använda denna kompakta, ratiometriska, genetiskt kodade sond med hög affinitet för kvantitativ avbildning av peroxid i mitokondrier i levande jäst.
Protocol
Representative Results
Discussion
I detta protokoll beskrivs en metod för att använda mtHyPer7 som biosensor för att bedöma mitokondriellH2O2i levande spirande jästceller. Biosensorn konstrueras med hjälp av en CRISPR-baserad metod och förs in i en bevarad genfri region i jästgenomet utan användning av selekterbara markörer. Jämfört med plasmidburna biosensorer uttrycks integrerade sådana i alla celler och på konsekventa nivåer, vilket ger mer tillförlitliga kvantifieringsresultat. Inga selekterbara markörer används för att generera mtHyPer7-uttryckande celler, vilket möjliggör användning av ett bredare spektrum av stambakgrunder och underlättar genetisk modifiering av biosensoruttryckande celler. Proteinet mtHyPer7 är korrekt riktat mot mitokondrier utan märkbara effekter på mitokondriell morfologi, funktion, distribution eller cellulär tillväxthastighet. mtHyPer7 visar ett dosberoende svar på externt tillsattH2O2. Dessutom kan mtHyPer7 rapportera om heterogeniteten i mitokondriell kvalitet med subcellulär upplösning. Slutligen, att använda ett konfokalmikroskop med snurrande skiva i motsats till vidvinkelmikroskopi för att avbilda mitokondriellt riktade biosensorer orsakar mindre fotoblekning till fluoroforer och genererar högupplösta bilder för att analysera subcellulära skillnader.
Begränsningar och alternativa tillvägagångssätt
Denna metod är inte lämplig för avbildning av celler i mer än 10 minuter, eftersom cellerna kommer att torka ut under täckglaset. För långtidsavbildning är det bättre att använda agardynmetoden46 eller att immobilisera celler i en odlingsskål med glasbotten fylld med SC-medium.
Valet av biosensor bör styras av målkoncentrationen under experimentella förhållanden. Om känsligheten för HyPer7 är för hög rekommenderas en annan HyPer-version, till exempel HyPer3 eller HyPerRed47,48. Det bör dock noteras att andra HyPer-sonder är mer pH-känsliga. För högre känslighet kan peroxiredoxinbaserad roGFP vara lämpligare (roGFP2Tsa2ΔCR)27.
Oxidationskonstanttillståndet för H 2 O2-sensornär knuten till både oxidations- och reduktionshastigheter. Oxidationshastigheten för biosensorer orsakas huvudsakligen avH2O2, men reduktionshastigheten beror på de antioxidantreduktionssystem som är aktiva i cellen och organellen. Det har visats att HyPer7 huvudsakligen reduceras av thioredoxinsystemet i jästcytosol, och dess reduktion är snabbare än för roGFP2Tsa2ΔCR27. Därför bör probens olika reduktionsmekanismer och responsdynamik beaktas vid tolkning av mätningar av H2O2-biosensorer. I synnerhet, för att härleda H2O2-nivåerfrån biosensoravläsningen, måste det antas att reduktionssystemet bibehåller en konstant kapacitet under experimentet. Som ett alternativ till de skript som beskrivs här har en mängd annan programvara gjorts fritt tillgänglig för analys av redoxsensorer49.
Kritiska steg
Med alla biosensorer är det viktigt att visa att biosensorn i sig inte påverkar processen som mäts. Därför är det viktigt att jämföra tillväxten och mitokondriell morfologi hos stammar under varje experimentellt tillstånd. Här bedöms mitokondriernas morfologi med hjälp av MitoTracker Red, som färgar mitokondrier på ett membranpotentialberoende sätt. Jämförelse av mitokondrierna i otransformerade och biosensortransformerade celler kan dock åstadkommas genom färgning med tetrametylrhodaminmetylester (TMRM), ett alternativt membranpotentialavkännande mitokondriellt vitalfärgämne, eller MitoTracker Green, som färgar mitokondrier oberoende av membranpotential. Om du misstänker skadliga effekter kan det hjälpa att minska uttrycksnivån eller ändra integreringsplatsen.
Validering av probens dos-responsbeteende och signal-brusförhållandet för avbildningstekniken är också viktigt för att samla in robusta resultat. Om variationen inom en grupp överstiger variationen mellan grupperna blir skillnaderna svåra att upptäcka. Variabilitet inom gruppen kan bero på verklig populationsvariation eller på brus i detektionsprocessen. De viktigaste stegen för att öka signal:brus-förhållandet är bildförvärv (pixelvärdesintervall och brus), bakgrundssubtraktion och trösklar.
Bullereffekter kan också reduceras under beräkningsstegen. Det enklaste tillvägagångssättet är att beräkna den viktade medelintensiteten från bildmätningarna (Results.csv), där varje pixel representerar det lokala förhållandet mellan excitationseffektiviteten. Detta ger ett “pixelvist” förhållande. Men om förhållandet mellan bildsignal och brus är lågt kan mer robusta resultat erhållas genom att beräkna den viktade medelintensiteten för en ROI i både täljar- och nämnarkanalerna och sedan beräkna förhållandet mellan dessa två viktade medelvärden (“regionvist” förhållande).
Om du vill välja en tröskelmetod använder du Fiji-kommandot Bild | Justera | Auto Threshold kan användas för att automatiskt prova alla inbyggda Fiji-metoder. För att utvärdera segmentering (trösklar) konverteras en sparad mask till en markering genom att klicka på Redigera | Urval | Skapa markering, läggs till i ROI-hanteraren (genom att trycka på T) och aktiveras sedan på råbildsfilen. Om mitokondrier inte detekteras på ett tillfredsställande sätt bör en annan segmenteringsmetod försökas.
När du jämför bilder är det viktigt att få alla bilder med identiska bildförhållanden, samt att visa alla bilder med identisk kontrastförbättring.
Mitokondriella rörelser måste beaktas vid optimering av avbildningsförhållandena. Om mitokondrierna rör sig signifikant mellan excitation vid 405 och 488 nm kommer förhållandebilden inte att vara korrekt. Det rekommenderas att hålla exponeringstiden <500 ms och att ändra excitationen med den snabbaste tillgängliga metoden (t.ex. en triggerpuls eller akustooptiskt avstämbart filter). När du samlar in en Z-stack bör båda excitationerna utföras för varje Z-steg innan du går vidare till nästa Z-steg.
För visning av resultaten är förändringar i nyans (färg) mer uppenbara för det mänskliga ögat än förändringar i intensitet. Därför konverteras kvotvärdet till en färgskala för enklare visuell tolkning. Färglagda bilder kan vara omodulerade, där alla mitokondriella pixlar visas med samma ljusstyrka, eller intensitetsmodulerade, där pixelintensiteten i originalbilden används för att ställa in intensiteter i den färglagda bilden.
Modifiering och felsökning
Som ett alternativ till att bekräfta mitokondriell funktion genom provokation med parakvat kan celler kopieras eller inokuleras till fermenterbara och icke-fermenterbara kolkällor.
För bakgrundssubtraktion, subtraktion av rullande boll (genom att navigera till Process | Subtrahera bakgrund…) Kan också användas för att ta bort ojämn belysning. Det bör säkerställas att närvaron av celler inte ändrar bakgrunden som subtraheras (genom att markera alternativet Skapa bakgrund och undersöka resultatet).
Sammanfattningsvis ger mtHyPer7-sonden en konsekvent, minimalt invasiv metod för att relatera den morfologiska och funktionella statusen för jästmitokondrier i levande celler, och möjliggör studier av en viktig cellulär stressfaktor och signalmolekyl i ett genetiskt hanterbart, lättillgängligt modellsystem.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna tackar Katherine Filpo Lopez för teknisk experthjälp. Detta arbete stöddes av anslag från National Institutes of Health (NIH) (GM122589 och AG051047) till LP.
Dessa studier använde Confocal and Specialized Microscopy Shared Resource of the Herbert Irving Comprehensive Cancer Center vid Columbia University, delvis finansierat genom NIH/NCI Cancer Center Support Grant P30CA013696.
Materials
| 100x/1.45 Plan Apo Lambda objective lens | Nikon | MRD01905 | |
| Adenine sulfate | Sigma-Aldrich | #A9126 | |
| Bacto Agar | BD Difco | #DF0145170 | |
| Bacto Peptone | BD Difco | #DF0118170 | |
| Bacto Tryptone | BD Difco | #DF211705 | |
| Bacto Yeast Extract | BD Difco | #DF0127179 | |
| BamHI | New England Biolabs | R0136S | |
| BglII | New England Biolabs | R0144S | |
| Carbenicilin | Sigma-Aldrich | C1389 | |
| Carl Zeiss Immersol Immersion Oil | Carl Zeiss | 444960 | |
| Dextrose (D-(+)-Glucose) | Sigma-Aldrich | #G8270 | |
| E. cloni 10G chemical competent cell | Bioserch Technologies | 60108 | |
| FIJI | NIH | Schindelin et al 2012 | |
| G418 (Geneticin) | Sigma-Aldrich | A1720 | |
| GFP emission filter | Chroma | 525/50 | |
| Gibson assembly | New England Biolabs | E2611 | |
| Graphpad Prism 7 | GraphPad | https://www.graphpad.com/scientific-software/prism/ | |
| H2O2 (stable) | Sigma-Aldrich | H1009 | |
| HO-pGPD-mito-roGFP-KanMX6-HO | Pon Lab | JYE057/EP41 | Liao et al 20201 |
| Incubator Shaker | New Brunswick Scientific | E24 | |
| KAPA HiFi PCR kit | Roche Sequencing and Life Science, Kapa Biosystems, Wilmington, MA | KK1006 | |
| L-arginine hydrochloride | Sigma-Aldrich | #A8094 | |
| laser | Agilent | 405 and 488 nm | |
| L-histidine hydrochloride | Sigma-Aldrich | #H5659 | |
| L-leucine | Sigma-Aldrich | #L8912 | |
| L-lysine hydrochloride | Sigma-Aldrich | #L8662 | |
| L-methionine | Sigma-Aldrich | #M9625 | |
| L-phenylalanine | Sigma-Aldrich | #P5482 | |
| L-tryptophan | Sigma-Aldrich | #T8941 | |
| L-tyrosine | Sigma-Aldrich | #T8566 | |
| mHyPer7 plasmid | This study | JYE116 | |
| Microscope coverslips | ThermoScientific | 3406 | #1.5 (170 µm thickness) |
| Microscope slides | ThermoScientific | 3050 | |
| MitoTracker Red CM-H2Xros | ThermoFisherScientific | M7513 | |
| NaCl | Sigma-Aldrich | S9888 | |
| NEBuilder HiFi Assembly Master Mix | New England Biolabs | E2621 | |
| Nikon Elements | Nikon | Microscope acquisition software | |
| Nikon Ti Eclipse inverted microscope | Nikon | ||
| Paraquat (Methyl viologen dichloride hydrate) | Sigma-Aldrich | Cat. #856177 | |
| RStudio | Posit.co | Free desktop version | |
| Spectrophotometer | Beckman | BU530 | |
| Stagetop incubator | Tokai Hit | INU | |
| Uracil | Sigma-Aldrich | #U1128 | |
| Yeast nitrogen base (YNB) containing ammonium sulfate without amino acids | BD Difco | #DF0919073 | |
| YN2_1_LT58_X2site | Addgene | 177705 | Pianale et al 2021 |
| Zyla 4.2 sCMOS camera | Andor |
References
- vander Bliek, A. M., Sedensky, M. M., Morgan, P. G. Cell biology of the mitochondrion. 유전학. 207 (3), 843-871 (2017).
- McBride, H. M., Neuspiel, M., Wasiak, S. Mitochondria: more than just a powerhouse. Current Biology. 16 (14), 551-560 (2006).
- Shi, R., Hou, W., Wang, Z. -. Q., Xu, X. Biogenesis of iron-sulfur clusters and their role in DNA metabolism. Frontiers in Cell and Developmental Biology. 9, 735678 (2021).
- McFaline-Figueroa, J. R., et al. Mitochondrial quality control during inheritance is associated with lifespan and mother-daughter age asymmetry in budding yeast. Aging Cell. 10 (5), 885-895 (2011).
- Higuchi-Sanabria, R., et al. Mitochondrial anchorage and fusion contribute to mitochondrial inheritance and quality control in the budding yeast Saccharomyces cerevisiae. Molecular Biology of the Cell. 27 (5), 776-787 (2016).
- Higuchi-Sanabria, R., et al. Role of asymmetric cell division in lifespan control in Saccharomyces cerevisiae. FEMS Yeast Research. 14 (8), 1133-1146 (2014).
- Lam, Y. T., Aung-Htut, M. T., Lim, Y. L., Yang, H., Dawes, I. W. Changes in reactive oxygen species begin early during replicative aging of Saccharomyces cerevisiae cells. Free Radical Biology & Medicine. 50 (8), 963-970 (2011).
- Laun, P., et al. Aged mother cells of Saccharomyces cerevisiae show markers of oxidative stress and apoptosis. Molecular Microbiology. 39 (5), 1166-1173 (2001).
- Doudican, N. A., Song, B., Shadel, G. S., Doetsch, P. W. Oxidative DNA damage causes mitochondrial genomic instability in Saccharomyces cerevisiae. Molecular and Cellular Biology. 25 (12), 5196-5204 (2005).
- Roca-Portoles, A., Tait, S. W. G. Mitochondrial quality control: from molecule to organelle. Cellular and Molecular Life Sciences. 78 (8), 3853-3866 (2021).
- Sies, H., Berndt, C., Jones, D. P. Oxidative stress. Annual Review of Biochemistry. 86, 715-748 (2017).
- Sies, H., Jones, D. P. Reactive oxygen species (ROS) as pleiotropic physiological signalling agents. Nature Reviews Molecular Cell Biology. 21 (7), 363-383 (2020).
- Imlay, J. A., Fridovich, I. Assay of metabolic superoxide production in Escherichia coli. The Journal of Biological Chemistry. 266 (11), 6957-6965 (1991).
- Fridovich, I. Mitochondria: are they the seat of senescence. Aging Cell. 3 (1), 13-16 (2004).
- Quinlan, C. L., Perevoshchikova, I. V., Hey-Mogensen, M., Orr, A. L., Brand, M. D. Sites of reactive oxygen species generation by mitochondria oxidizing different substrates. Redox Biology. 1 (1), 304-312 (2013).
- Griendling, K. K., Minieri, C. A., Ollerenshaw, J. D., Alexander, R. W. Angiotensin II stimulates NADH and NADPH oxidase activity in cultured vascular smooth muscle cells. Circulation Research. 74 (6), 1141-1148 (1994).
- Griendling, K. K., Sorescu, D., Ushio-Fukai, M. NAD(P)H oxidase: role in cardiovascular biology and disease. Circulation Research. 86 (5), 494-501 (2000).
- Edmondson, D. E., Binda, C., Wang, J., Upadhyay, A. K., Mattevi, A. Molecular and mechanistic properties of the membrane-bound mitochondrial monoamine oxidases. 생화학. 48 (20), 4220-4230 (2009).
- Ramsay, R. R., Singer, T. P. The kinetic mechanisms of monoamine oxidases A and B. Biochemical Society Transactions. 19 (1), 219-223 (1991).
- Ramsay, R. R. Kinetic mechanism of monoamine oxidase A. 생화학. 30 (18), 4624-4629 (1991).
- Handy, D. E., Loscalzo, J. Redox regulation of mitochondrial function. Antioxidants & Redox Signaling. 16 (11), 1323-1367 (2012).
- Wood, Z. A., Schröder, E., Robin Harris, J., Poole, L. B. Structure, mechanism and regulation of peroxiredoxins. Trends in Biochemical Sciences. 28 (1), 32-40 (2003).
- Slade, L., et al. Examination of the superoxide/hydrogen peroxide forming and quenching potential of mouse liver mitochondria. Biochimica et Biophysica Acta. General Subjects. 1861 (8), 1960-1969 (2017).
- Pak, V. V., et al. Ultrasensitive genetically encoded indicator for hydrogen peroxide identifies roles for the oxidant in cell migration and mitochondrial function. Cell Metabolism. 31 (3), 642-653 (2020).
- Topell, S., Hennecke, J., Glockshuber, R. Circularly permuted variants of the green fluorescent protein. FEBS Letters. 457 (2), 283-289 (1999).
- Belousov, V. V., et al. Genetically encoded fluorescent indicator for intracellular hydrogen peroxide. Nature Methods. 3 (4), 281-286 (2006).
- Kritsiligkou, P., Shen, T. K., Dick, T. P. A comparison of Prx- and OxyR-based H2O2 probes expressed in S. cerevisiae. The Journal of Biological Chemistry. 297 (1), 100866 (2021).
- Baird, G. S., Zacharias, D. A., Tsien, R. Y. Circular permutation and receptor insertion within green fluorescent proteins. Proceedings of the National Academy of Sciences. 96 (20), 11241-11246 (1999).
- Abedi, M. R., Caponigro, G., Kamb, A. Green fluorescent protein as a scaffold for intracellular presentation of peptides. Nucleic Acids Research. 26 (2), 623-630 (1998).
- Onukwufor, J. O., et al. A reversible mitochondrial complex I thiol switch mediates hypoxic avoidance behavior in C. elegans. Nature Communications. 13 (1), 2403 (2022).
- Vega, M., et al. Antagonistic effects of mitochondrial matrix and intermembrane space proteases on yeast aging. BMC Biology. 20 (1), 160 (2022).
- Torello Pianale, L., Rugbjerg, P., Olsson, L. Real-time monitoring of the yeast intracellular state during bioprocesses with a toolbox of biosensors. Frontiers in Microbiology. 12, 802169 (2022).
- Imani, M., Mohajeri, N., Rastegar, M., Zarghami, N. Recent advances in FRET-based biosensors for biomedical applications. Analytical Biochemistry. 630, 114323 (2021).
- Zadran, S., et al. Fluorescence resonance energy transfer (FRET)-based biosensors: visualizing cellular dynamics and bioenergetics. Applied Microbiology and Biotechnology. 96 (4), 895-902 (2012).
- Gietz, R. D., Woods, R. A. Transformation of yeast by lithium acetate/single-stranded carrier DNA/polyethylene glycol method. Methods in Enzymology. 350, 87-96 (2002).
- Liao, P. -. C., Wolken, D. M. A., Serrano, E., Srivastava, P., Pon, L. A. Mitochondria-associated degradation pathway (MAD) function beyond the outer membrane. Cell Reports. 32 (2), 107902 (2020).
- Higuchi-Sanabria, R., Swayne, T. C., Boldogh, I. R., Pon, L. A. Live-cell imaging of mitochondria and the actin cytoskeleton in budding yeast. Methods in Molecular Biology. 1365, 25-62 (2016).
- Liao, P. -. C., Yang, E. J., Pon, L. A. Live-cell imaging of mitochondrial redox state in yeast cells. STAR Protocols. 1 (3), 100160 (2020).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Collins, T. J. ImageJ for microscopy. BioTechniques. 43, 25-30 (2007).
- Chazotte, B. Labeling mitochondria with MitoTracker dyes. Cold Spring Harbor Protocols. 2011 (8), 990-992 (2011).
- Aguilaniu, H., Gustafsson, L., Rigoulet, M., Nyström, T. Asymmetric inheritance of oxidatively damaged proteins during cytokinesis. Science. 299 (5613), 1751-1753 (2003).
- Erjavec, N., Larsson, L., Grantham, J., Nyström, T. Accelerated aging and failure to segregate damaged proteins in Sir2 mutants can be suppressed by overproducing the protein aggregation-remodeling factor Hsp104p. Genes & Development. 21 (19), 2410-2421 (2007).
- Erjavec, N., Cvijovic, M., Klipp, E., Nyström, T. Selective benefits of damage partitioning in unicellular systems and its effects on aging. Proceedings of the National Academy of Sciences. 105 (48), 18764-18769 (2008).
- Erjavec, N., Nyström, T. Sir2p-dependent protein segregation gives rise to a superior reactive oxygen species management in the progeny of Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences. 104 (26), 10877-10881 (2007).
- Davidson, R., Liu, Y., Gerien, K. S., Wu, J. Q. Real-time visualization and quantification of contractile ring proteins in single living cells. Methods in Molecular Biology. 1369, 9-23 (2016).
- Bilan, D. S., et al. HyPer-3: a genetically encoded H2O2 probe with improved performance for ratiometric and fluorescence lifetime imaging. ACS Chemical Biology. 8 (3), 535-542 (2013).
- Ermakova, Y. G., et al. Red fluorescent genetically encoded indicator for intracellular hydrogen peroxide. Nature Communications. 5 (1), 5222 (2014).
- Fricker, M. D. Quantitative redox imaging software. Antioxidants & Redox Signaling. 24 (13), 752-762 (2016).
- Yang, E. J., Pernice, W. M., Pon, L. A. A role for cell polarity in lifespan and mitochondrial quality control in the budding yeast Saccharomyces cerevisiae. iSCIENCE. 25 (3), 103957 (2022).

