LipidUNet-maskinlæringsbasert metode for karakterisering og kvantifisering av lipidavleiringer ved bruk av iPSC-avledet retinalpigmentepitel
Summary
Degenerative øyesykdommer som påvirker retinalpigmentepitellaget i øyet har monogen og polygen opprinnelse. Flere sykdomsmodeller og en programvare, LipidUNet, er utviklet for å studere sykdomsmekanismer, samt potensielle terapeutiske inngrep.
Abstract
Retinalpigmentepitelet (RPE) er et monolag av sekskantede celler plassert på baksiden av øyet. Det gir næring og støtte til fotoreceptorer og koroidale kapillærer, utfører fagocytose av fotoreceptor ytre segmenter (POS), og utskiller cytokiner på en polarisert måte for å opprettholde homeostasen til ytre netthinnen. Dysfunksjonell RPE, forårsaket av mutasjoner, aldring og miljøfaktorer, resulterer i degenerasjon av andre retinale lag og forårsaker synstap. Et kjennetegn fenotypisk trekk ved degenererende RPE er intra- og subcellulære lipidrike avsetninger. Disse forekomstene er en vanlig fenotype på tvers av forskjellige retinale degenerative sykdommer. For å reprodusere lipidavsetningsfenotypen av monogene retinale degenerasjoner in vitro, ble indusert pluripotent stamcelleavledet RPE (iRPE) generert fra pasientens fibroblaster. Cellelinjer generert fra pasienter med Stargardt og Late-onset retinal degenerasjon (L-ORD) sykdom ble matet med POS i 7 dager for å replikere RPE fysiologisk funksjon, noe som forårsaket POS fagocytose-indusert patologi i disse sykdommene. For å generere en modell for aldersrelatert makuladegenerasjon (AMD), en polygen sykdom assosiert med alternativ komplementaktivering, ble iRPE utfordret med alternative komplementanafylatoksiner. De intra- og subcellulære lipidavsetningene ble karakterisert ved bruk av Nilrød, bor-dipyrrometen (BODIPY) og apolipoprotein E (APOE). For å kvantifisere tettheten av lipidavsetninger ble det utviklet en maskinlæringsbasert programvare, LipidUNet. Programvaren ble trent på projeksjonsbilder av iRPE med maksimal intensitet på kulturoverflater. I fremtiden vil det bli trent til å analysere tredimensjonale (3D) bilder og kvantifisere volumet av lipiddråper. LipidUNet-programvaren vil være en verdifull ressurs for å oppdage stoffer som reduserer lipidakkumulering i sykdomsmodeller.
Introduction
Retinalpigmentepitelet (RPE) er et monolag av celler som ligger på baksiden av øyet ved siden av retinale fotoreceptorer. RPE spiller en viktig rolle i å opprettholde riktig visjon ved å gi metabolsk og strukturell støtte til fotoreceptorene. Sunne RPE-celler er preget av en distinkt sekskantet morfologi. De er forbundet med tette veikryss, som gjør at RPE kan fungere som en barriere mellom choriocapillaris plassert på basalsiden og fotoreceptorer plassert apikal. For å opprettholde retinaløkosystemet transporterer RPE nøkkelmetabolitter, for eksempel glukose, til fotoreceptorer på en måte som minimerer glukoseforbruket i RPE1. På grunn av denne begrensningen er RPE avhengig av andre metabolitter for å opprettholde sine metabolske behov, inkludert fettsyrer, som RPE konverterer til ketoner gjennom β-oksidasjon2. Gitt tilbøyelighet til RPE til å utnytte fettsyrer, som sannsynligvis resirkuleres fra fotoreceptor ytre segment (POS) fordøyelse, som energikilde, fører skadelige endringer i lipidbehandlingsveiene i RPE ofte til eller er involvert i både monogene og polygene degenerative retinale sykdommer3.
Aldersrelatert makuladegenerasjon (AMD), en polygen degenerativ øyesykdom som forårsaker RPE-degenerasjon, har også vært knyttet til avvikende autofagi og lipidmetabolisme i RPE-monolaget. Svikt i et dysfunksjonelt RPE-monolag for å behandle POS og utføre andre kritiske funksjoner fører til ekstracellulære (sub-RPE) avsetninger kalt basale lineære avsetninger (BLinD) plassert mellom RPE og Bruchs membran – et kjennetegn ved AMD-patologier. Hovedkomponenter i BLinD inkluderer lipoproteiner, hvorav den mest tallrike er apolipoprotein E (APOE)4. Akkumulering av tynne lag av BLinD kan føre til myk drusen, som er anerkjent som et klinisk symptom på AMD 5,6.
Flere grupper har vist at stamcelleavledede in vitro sykdomsmodeller som forårsaker RPE-dysfunksjon har sub-RPE lipidakkumulering 7,8,9. Hallam et al. (2017) genererte indusert pluripotent stamcelleavledet RPE (iRPE) fra pasienter med høy risiko for AMD på grunn av en polymorfisme av CFH-genet. iRPE viste drusenakkumulering, som markert ved APOE, og høyrisiko-RPE akkumulerte større forekomster enn iRPE generert fra lavrisikopasienter10.
For å lage en in vitro-modell som rekapitulerer cellulære kjennetegn ved AMD, som lipiddråper og drusenavsetning, ble iRPE-linjer generert fra pasientblodprøver etablert ved hjelp av en tidligere publisert utviklingsstyrt protokoll11. iRPE ble utsatt for komplementkompetent humant serum (CC-HS), en løsning som inneholder anafylatoksiner som etterligner en mulig årsak til AMD: økt alternativ komplementsignalering8. Den resulterende cellulære og subcellulære avsetningen av lipidavsetninger ble målt ved bruk av vanlige lipid- og lipoproteinmarkører, APOE, Nile Red og BODIPY. Gjennom disse markørene ble det vist at aktivert komplementsignalering via CC-HS forverret lipidakkumulering i iRPE-celler8.
For å utvikle en sykdomsmodell for en monogen retinal degenerativ sykdom, ble iRPE-linjer utviklet fra pasienter med Stargardt sykdom, en sykdom forårsaket av mutasjoner til ABCA4-genet i RPE. Det har tidligere blitt vist at når ABCA4 slås ut, akkumuleres A2E lipofuscin, et intracellulært innskudd kjent for å inneholde høye nivåer av fosfolipider og lysavhengige lipidperoksidasjonsprodukter, inne i RPE12. ABCA4 knockoutlinjer ble utviklet langs pasientlinjene, og begge ble utsatt for POS-fôring. Stargardt iRPE demonstrerte POS-fagocytose-indusert patologi, og viste økt lipidakkumulering kvantifisert ved BODIPY-farging. RPE avledet fra ABCA4 KO iPSCs ble utsatt for CC-HS-behandling; kvantifisering av BODIPY-signalet viste en defekt i lipidhåndtering i Stargardts sykdomsmodell også9.
Gitt utbredelsen av disse sykdommene og behovet for effektive terapier, sammen med de relevante sykdomsmodellene beskrevet ovenfor, er det behov for å etablere robuste metoder for å kvantifisere effekten av potensielle behandlinger. For å kvantifisere lipidavsetninger på en måte som er objektiv, automatisert og standardisert, ble en maskinlæringsbasert programvare, LipidUNet, opprettet slik at lipidavsetning, når den ble parret med maskeanalyseverktøy, raskt og effektivt kan identifiseres ved hjelp av de vanlige markørene Nile Red, BODYPY og APOE. Sammendragsstatistikken som er oppnådd ved hjelp av denne analyserørledningen, kan deretter analyseres og vises grafisk, noe som gjør det enkelt å sammenligne behandlingsbetingelser. Skjemaet til protokollen er vist i figur 1.
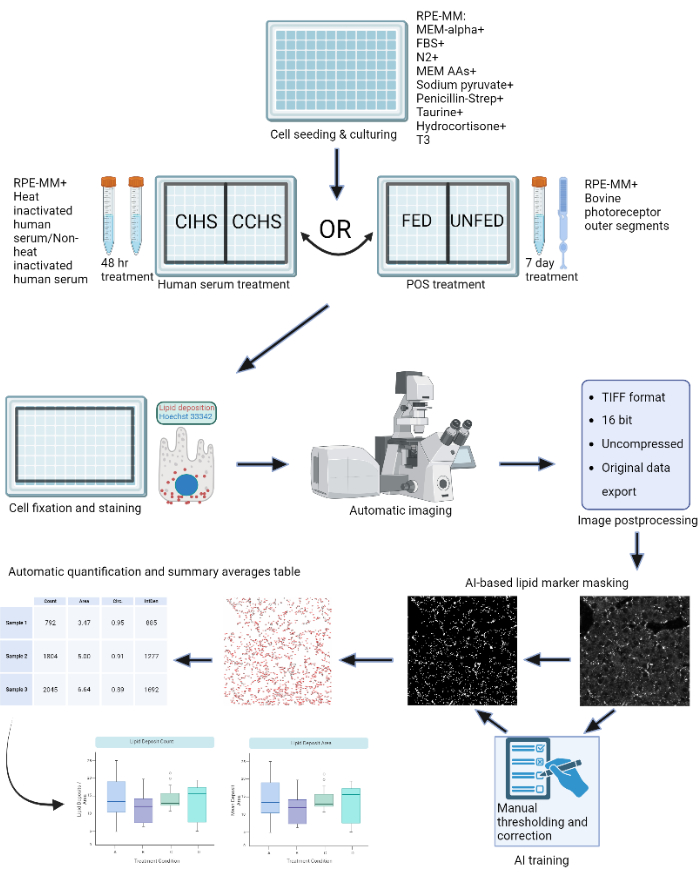
Figur 1: Skjematisk av protokollen: RPE-celler dyrkes på en 96-brønnsplate og utfordres med aktivt humant serum eller renset ytre segmenter av storfe for å modellere forskjellige typer retinal degenerasjoner in vitro. RPE-celler er faste og farget for lipoproteinavsetninger med Nile Red, BODYPY og APOE. Et konfokalmikroskop brukes til å skaffe Z-stabler av fluorescerende merkede lipidpartikler, som deretter behandles til 2D maksimal intensitetsprojeksjoner. En maskinlæringsalgoritme ble trent til å gjenkjenne og korrekt segmentere lipoproteinpartikler. Sammendragstabeller som inneholder partikkelantall og ulike formberegninger genereres og kan brukes til senere plotting og statistisk analyse. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Denne protokollen gir en metode for effektivt å merke, avbilde og kvantifisere lipidavsetninger i monogene og polygene in vitro sykdomsmodeller for degenerative øyesykdommer. Den AI-baserte programvaren, LipidUNet, kan brukes på tre vanlige lipidmarkører, APOE, Nile Red og BODIPY, og gir en rask, automatisk metode for analyse som gjør at kvantifisering kan være standard og objektiv.
Hovedbegrensningen til LipidUNet er det faktum at treningsdatasettet for AI var begrenset til 40x forstørrelsesbilder av celler dyrket i en 96-brønnsplate. Som et resultat av treningsbildesettet er LipidUNet, i sin nåværende form, begrenset til å analysere 40x forstørrelsesbilder. Programvaren kan brukes til å analysere 40x bilder av celler dyrket på andre kulturflater i tillegg til en 96 brønnplate, men det bør utvises forsiktighet for å undersøke de genererte utgangsmaskene for å verifisere nøyaktig terskel av programvaren. Flere bildesett (ved forskjellige forstørrelser) vil være nødvendig for å utvide omfanget av hvilke prøver / bilder den kan analysere.
Protokollen har flere kritiske trinn. I lipidmarkørtrinnet bør brukeren bekrefte at deres valgte merkeforbindelse (BODIPY, APOE, Nile Red) har merket prøven effektivt. Eldre RPE-celler er ofte sterkt pigmenterte, noe som kan svekke det fluorescerende signalet om antistoffimmunfarging. Når fluorescenssignalet er svakt eller når det er for mye bakgrunnsfarging, kan LipidUNet ikke skille lipiddråper nøyaktig. Av en lignende grunn må riktig valgte innsamlingsinnstillinger for det automatiske bildebehandlingstrinnet i protokollen brukes. Hvis bildene som er anskaffet er av dårlig kvalitet, vil LipidUNet slite med å maskere bilder riktig, og derfor vil kvantifiseringen være unøyaktig (figur 6A-L). Til slutt er etterbehandling av bildene et viktig skritt, da LipidUNet har spesifikke krav til at programvaren skal fungere.
Sammenlignet med arbeidsflyter for lipidanalyse som bruker manuell terskelverdi, eller teknikker som involverer automatisk terskel i programvare som Fiji, tilbyr LipidUNet en objektiv og pålitelig segmentering på tvers av bilder med variabel lipidavsetning, noe som gjenspeiles av en liten feilrate i identifiseringen av lipidpartikler (figur 7). Programvaren tillater brukeroppføring av ekstra treningsbilder, noe som muliggjør analyse av bildesett utover de som bruker et 40x forstørrelsesmål eller til og med de som bruker en annen lipidmarkør, som beskrevet i protokollen. I fremtiden vil programvaren bli trent til å analysere 3D-bilder slik at kvantifisering av lipidavsetningsvolum er mulig. Degenerative øyesykdommer som impliserer lipidavsetning som en stor bidragsyter til patologi er utbredt, og tilfeller forventes å øke etter hvert som den eldre befolkningen vokser13. Nøyaktige sykdomsmodeller og effektive analyseverktøy, som vi har skissert i denne protokollen, vil muliggjøre utvikling av nye terapeutiske intervensjoner.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker National Eye Institute (NEI) histologikjerne for bruken av Zeiss konfokale system. Dette arbeidet ble støttet av NEI IRP-midler (tilskuddsnummer ZIA EY000533-04).
Materials
| 0.22 µm Steriflip filter system | EMD Millipore | SCGP00525 | |
| 1x Dulbecco's Phosphate Buffered Saline | Gibco | 14190-144 | |
| 3,3',5-Triiodo-L-thyronine | Sigma | T5516 | |
| Albumin Bovine, Fraction V | MP Biomedical | 160069 | |
| Alexa Fluor 555 rabbit anti-goat IgG (H+L) | Invitrogen | A21431 | APOE secondary antibody |
| APOE primary antibody | Millipore Sigma | AB947 | |
| BODIPY 493/503 | Invitrogen | D3922 | Protect from light |
| Complement competent human serum | Millipore Sigma | S1-LITER | |
| CTS N2 Supplement | Life Technologies | A13707-01 | |
| Fetal Bovine Serum | Hyclone | SH30071.03 | |
| Fluoromount-G | SouthernBiotech | 0100-01 | Slide mounting media |
| Glass Cover Slips #1 1/2 22 mm x 22 mm | Electron Microscopy Sciences | 72204-01 | |
| Glass Microscope Slide 25 mm x 75 mm- 1.2 mm Thick | Electron Microscopy Sciences | 71870-01 | |
| Hydrocortisone | Sigma | H0396 | |
| MEM Alpha | Life Technologies | 12571-063 | |
| MEM non-essential Amino Acids | Life Technologies | 11140 | |
| Nile Red | Sigma | 72485-100MG | Protect from light |
| Paraformaldehyde 16% Solution, EM Grade | Electron Microscopy Sciences | 15710 | |
| Penicillin-Strep | Life Technologies | 15140-148 | |
| Phosphate Buffered Saline 10x | Gibco | 70011-044 | |
| Rod Outer Segments (OS) | InVision Bioresources | 98740 | |
| Sodium bicarbonate | Sigma Aldrich | S5761 | |
| Sodium Pyruvate | Life Technologies | 11360-070 | |
| Sucrose | Sigma Aldrich | S1888 | |
| SYBR Green Master Mix | Bio-Rad | 1725274 | |
| Taurine | Sigma | T0625 | |
| Triton X-100 | Sigma | 9002-93-1 | |
| Tween 20 Ultrapure | Affymetrix | 9005-64-5 | |
| Vitronectin | Life Technologies | A14701SA | |
| Y-27632 dihydrochloride | R&D Systems | 1254 |
References
- Kanow, M. A., et al. Biochemical adaptations of the retina and retinal pigment epithelium support a metabolic ecosystem in the vertebrate eye. eLife. 6, e28899 (2017).
- Adijanto, J., et al. The retinal pigment epithelium utilizes fatty acids for ketogenesis. The Journal of Biological Chemistry. 289 (30), 20570-20582 (2014).
- Farnoodian, M., et al. Cell-autonomous lipid-handling defects in Stargardt iPSC-derived retinal pigment epithelium cells. Stem Cell Reports. 17 (11), 2438-2450 (2022).
- Curcio, C. A. Soft drusen in age-related macular degeneration: Biology and targeting via the oil spill strategies. Investigative Ophthalmology & Visual Science. 59 (4), AMD160-AMD181 (2018).
- Cankova, Z., Huang, J. D., Kruth, H. S., Johnson, M. Passage of low-density lipoproteins through Bruch’s membrane and choroid. Experimental Eye Research. 93 (6), 947-955 (2011).
- Curcio, C. A., et al. Esterified and unesterified cholesterol in drusen and basal deposits of eyes with age-related maculopathy. Experimental Eye Research. 81 (6), 731-741 (2005).
- Miyagishima, K. J., et al. AMPK modulation ameliorates dominant disease phenotypes of CTRP5 variant in retinal degeneration. Communications Biology. 4 (1), 1360 (2021).
- Sharma, R., et al. Epithelial phenotype restoring drugs suppress macular degeneration phenotypes in an iPSC model. Nature Communications. 12 (1), 7293 (2021).
- Farnoodian, M., et al. Cell-autonomous lipid-handling defects in Stargardt iPSC-derived retinal pigment epithelium cells. Stem Cell Reports. 17 (11), 2438-2450 (2022).
- Hallam, D., et al. An induced pluripotent stem cell patient specific model of complement factor H (Y402H) polymorphism displays characteristic features of age-related macular degeneration and indicates a beneficial role for UV light exposure. Stem Cells (Dayton, Ohio). 35 (11), 2305-2320 (2017).
- Sharma, R., Bose, D., Montford, J., Ortolan, D., Bharti, K. Triphasic developmentally guided protocol to generate retinal pigment epithelium from induced pluripotent stem cells. STAR Protocols. 3 (3), 101582 (2022).
- Issa, P. C., Barnard, A. R., Herrmann, P., Washington, I., MacLaren, R. E. Rescue of the Stargardt phenotype in Abca4 knockout mice through inhibition of vitamin A dimerization. Proceedings of the National Academy of Sciences of the United States of America. 112 (27), 8415-8420 (2015).
- GBD 2019 Blindness and Vision Impairment Collaborators. Blindness and Vision Impairment Collaborators. Causes of blindness and vision impairment in 2020 and trends over 30 years, and prevalence of avoidable blindness in relation to VISION 2020: the Right to Sight: an analysis for the Global Burden of Disease Study. Lancet Global Health. 9 (2), e144-e160 (2021).

