जीवित कोशिकाओं और मॉडल झिल्ली में प्लाज्मा झिल्ली की मरम्मत की जांच के लिए एक थर्मोप्लास्मोनिक दृष्टिकोण
Summary
थर्मोप्लास्मोनिक पंचर विधि कोशिकाओं और विशाल यूनिलामेलर पुटिकाओं में प्लाज्मा झिल्ली की मरम्मत के दौरान प्रोटीन प्रतिक्रियाओं का अध्ययन करने के लिए कॉन्फोकल माइक्रोस्कोपी, ऑप्टिकल चिमटी और सोने के नैनोकणों को एकीकृत करती है। तकनीक तेजी से और स्थानीयकृत झिल्ली पंचर को सक्षम बनाती है, जिससे जटिल प्लाज्मा झिल्ली मरम्मत मशीनरी में प्रमुख प्रोटीन और उनकी कार्यात्मक भूमिकाओं की पहचान की अनुमति मिलती है।
Abstract
कोशिका झिल्ली कोशिका के अस्तित्व के लिए महत्वपूर्ण है, और इसकी अखंडता सुनिश्चित करना आवश्यक है क्योंकि कोशिका अपने पूरे जीवन चक्र में चोटों का अनुभव करती है। झिल्ली को नुकसान को रोकने के लिए, कोशिकाओं ने कुशल प्लाज्मा झिल्ली मरम्मत तंत्र विकसित किया है। इन मरम्मत तंत्रों का अध्ययन कॉन्फोकल माइक्रोस्कोपी और नैनोस्केल थर्मोप्लास्मोनिक्स के संयोजन से किया जा सकता है ताकि जीवित कोशिकाओं और झिल्ली मॉडल प्रणालियों में सतह की मरम्मत में शामिल एनेक्सिन जैसे प्रमुख प्रोटीन की भूमिका की पहचान और जांच की जा सके।
पंचर विधि नैनोपार्टिकल विकिरण पर अत्यधिक स्थानीयकृत हीटिंग को प्रेरित करने के लिए एक लेजर को नियोजित करती है। निकट-अवरक्त प्रकाश का उपयोग जैविक नमूने में फोटोटॉक्सिसिटी को कम करता है, जबकि अधिकांश अवशोषण निकट-अवरक्त गुंजयमान प्लास्मोनिक नैनोपार्टिकल में होता है। पुटिका और सेल संलयन अध्ययन के माध्यम से इंट्रासेल्युलर तंत्र और सेलुलर प्रतिक्रियाओं की समझ को बढ़ाने के लिए संभावित फोटोथर्मल और बायोफिजिकल अनुसंधान के लिए इस थर्मोप्लास्मोनिक विधि का शोषण किया गया है। दृष्टिकोण झिल्ली व्यवधान के लिए मौजूदा तरीकों के पूरक होने के लिए दिखाया गया है, जैसे यंत्रवत्, रासायनिक या वैकल्पिक रूप से प्रेरित चोटें, और बेहद स्थानीय चोटों को भड़काकर उच्च स्तर का नियंत्रण प्रदान करती है। चोट की सीमा गोलाकार नैनोपार्टिकल के आसपास के क्षेत्र तक सीमित है, और विभिन्न तरंग दैर्ध्य का उपयोग करके स्पंदित लेज़रों के विपरीत बीम पथ के साथ कोई हानिकारक क्षति नहीं होती है। कुछ सीमाओं के बावजूद, जैसे कि नैनोबबल्स का गठन, थर्मोप्लास्मोनिक विधि सेल व्यवहार्यता से समझौता किए बिना लगभग देशी वातावरण में प्लाज्मा झिल्ली की मरम्मत में सेलुलर प्रतिक्रियाओं की जांच के लिए एक अनूठा उपकरण प्रदान करती है।
जब कॉन्फोकल माइक्रोस्कोपी के साथ एकीकृत किया जाता है, तो पंचर विधि मॉडल झिल्ली प्रणालियों में झिल्ली गतिशीलता की यंत्रवत समझ प्रदान कर सकती है और साथ ही प्रोटीन भर्ती और उनके बायोफिजिकल फ़ंक्शन सहित झिल्ली क्षति के लिए प्रोटीन प्रतिक्रियाओं पर मात्रात्मक जानकारी प्रदान कर सकती है। कुल मिलाकर, कम मॉडल सिस्टम के लिए इस पद्धति का अनुप्रयोग जीवित कोशिकाओं में जटिल प्लाज्मा झिल्ली मरम्मत मशीनरी की हमारी समझ को बढ़ा सकता है।
Introduction
कोशिका झिल्ली, दोनों एक भौतिक बाधा और एक संकेत मंच के रूप में सेवारत, सेल अस्तित्व1 के लिए महत्वपूर्ण है. अपने पूरे सेल चक्र के दौरान, प्लाज्मा झिल्ली (पीएम) क्षति के अधीन है, जैसे यांत्रिक 2,3,4,5 और रासायनिक6 तनाव-प्रेरित चोटें। झिल्ली अखंडता को बनाए रखने और सेल अस्तित्व सुनिश्चित करने के लिए, सेल ने मजबूत प्लाज्मा झिल्ली मरम्मत (पीएमआर) तंत्र विकसित किया है। ये तंत्र विभिन्न रणनीतियों पर निर्भर करते हैं, जैसे कि साइटोस्केलेटन पुनर्गठन, झिल्ली संलयन, और झिल्ली प्रतिस्थापन रणनीतियों 7,8,9,10,11, जिनमें से सभी विशिष्ट प्रोटीन की भर्ती पर निर्भर करते हैं। विशेष रूप से, एनेक्सिन प्रोटीन परिवार के सदस्यों को पीएमआर 1,9,12,13,14,15,16 की प्रक्रियाओं से जुड़े प्रमुख प्रोटीन के रूप में पहचाना गया है। पीएम चोट के बाद, सेल कैल्शियम आयनों (सीए2+), जो सेल के अस्तित्व17 के लिए एक तत्काल खतरा बन गया है की आमद का अनुभव करता है. सीए2 + प्रवाह के जवाब में, एनेक्सिन प्रोटीन, जो मुख्य रूप से साइटोसोल में स्थित हैं, पीएमआर रणनीतियों18 के एक भाग के रूप में क्षतिग्रस्त प्लाज्मा झिल्ली के भीतरी पत्रक से बंधे. एनेक्सिन ए 2 (एएनएक्सए 2) एनेक्सिन परिवार के पहले सदस्यों में से एक था जो डिस्फेरलिन-कमी वाली मांसपेशियों की डिस्ट्रोफी में पीएमआर से जुड़ा था और चोट स्थल 5,19,20,21 के पास पीएम को इंट्रासेल्युलर पुटिकाओं को फ्यूज करके मरम्मत में मध्यस्थता करने का सुझाव दिया गया था। इसके बाद, कई कार्यों को अनुलग्नक22 के लिए जिम्मेदार ठहराया गया है, और पीएमआर में उनकी भूमिका ने पिछले 20 वर्षों में ध्यान आकर्षित किया है। हालांकि, पीएमआर में अनुलग्नकों की सटीक भूमिका पूरी तरह से 15,18,21,22 को समझा नहीं गया है।
यह लेख प्रोटीन-झिल्ली इंटरैक्शन और झिल्ली गतिशीलता को नियंत्रित और अत्यधिक स्थानीयकृत तरीके से जांचने के लिए एक विधि का प्रस्ताव करता है, जिसमें कॉन्फोकल माइक्रोस्कोपी, ऑप्टिकल चिमटी और सोने के नैनोकणों (एयूएनपी) के संयोजन का उपयोग किया जाता है। यह विधि झिल्ली क्षति और सीए2+ प्रवाह के जवाब में प्रोटीन, लिपिड और छोटे अणु इंटरैक्शन के मात्रात्मक अध्ययन को सक्षम बनाती है। जटिलता और झिल्ली की मरम्मत की प्रक्रिया में शामिल घटकों की बहुलता के बावजूद, सरलीकृत झिल्ली प्रणालियों है कि प्लाज्मा झिल्ली की नकल झिल्ली गतिशीलता की एक गहरी यंत्रवत समझ और झिल्ली व्यवधान16 के लिए एनेक्सिन प्रोटीन की प्रतिक्रिया हासिल करने के लिए नियोजित किया गया है. विशाल यूनिलामेलर लिपिड पुटिकाओं (जीयूवी) को एक निर्दिष्ट लिपिड संरचना के साथ मॉडल झिल्ली प्रणाली के रूप में चुना गया था। GUVs को जेल-असिस्टेड हाइड्रेशन विधि का उपयोग करके उत्पन्न किया गया था, विशेष रूप से पॉलीविनाइल अल्कोहल जेल हाइड्रेशन, जैसा कि वेनबर्गर एट अल.23 द्वारा वर्णित है, जिसने GUVs में एनेक्सिन के कुशल एनकैप्सुलेशन की अनुमति दी थी।
धातु नैनोकणों (एनपी) पर निकट-अवरक्त (एनआईआर) लेजर विकिरण का उपयोग एनपी के महत्वपूर्ण हीटिंग को प्रेरित करता है, जिससे जैव चिकित्सा अनुप्रयोगों में शोषित स्थानीय गर्मी स्रोत स्थापित करने के लिए एक प्रभावी तरीका बन जाता है24. विधि शुरू में 2 डी और 3 डी बायोमिमेटिक परख दोनों में एक एकल एयूएनपी के आसपास के तापमान को सीधे मापने के लिए इस्तेमाल किया गया था। इन परखोंमें 25,26, प्लास्मोनिक नैनोकणों को एक समर्थित लिपिड बाइलेयर पर विकिरणित किया गया था या स्थानीय हीटिंग पर स्थानीय थर्मल चरण संक्रमण से गुजरने वाले जीयूवी के पास वैकल्पिक रूप से फंस गया था, जिससे कण के चारों ओर सटीक तापमान प्रोफ़ाइल का परिमाणीकरण और नियंत्रण सक्षम हो गया। जैविक नमूनों की जांच या हेरफेर करते समय इस संदर्भ तापमान प्रोफ़ाइल का उपयोग किया गया है। विधि में आगे की प्रगति पुटिका और सेल संलयन28,29 के लिए अनुमति देता है, झिल्ली27 में नैनोस्कोपिक छिद्रों के प्रेरण की सुविधा प्रदान की है. अन्य अध्ययनों ने उपन्यास संकर पुटिकाओं का निर्माण करके जीयूवी29 और ट्रांसमेम्ब्रेन प्रोटीन30 में परिधीय झिल्ली प्रोटीन के व्यवहार की जांच की है, जबकि सेलुलर प्रतिक्रियाओं या जीन अभिव्यक्ति 28,29,31,32,33को नियंत्रित करने और अध्ययन करने के लिए सेल-विशिष्ट दवा वितरण का भी पता लगाया गया है। हाल ही में, विधि झिल्ली क्षति32,34,35 करने के लिए प्रोटीन प्रतिक्रियाओं की जांच करने के लिए इस्तेमाल किया गया है.
सेलुलर प्रतिक्रियाओं और झिल्ली की मरम्मत का पता लगाने के लिए प्लाज्मा झिल्ली को बाधित करने के लिए कई तरीके मौजूद हैं। इनमें माइक्रोनेडल पंचर, माइक्रोबीड झटकों और सेल स्क्रैपिंग शामिल हैं, जो सभी कोशिका झिल्ली को यंत्रवत् 14,36,37 बाधित कर सकते हैं। रासायनिक प्रेरित क्षति डिटर्जेंट 5,38 या जीवाणु विषाक्त पदार्थों39,40 कि लिपिड bilayer अस्थिर और प्लाज्मा झिल्ली भर में झिल्ली छिद्रों उत्पन्न जोड़कर प्राप्त किया जा सकता है. इसके अलावा, निरंतर तरंग और स्पंदित लेज़रों द्वारा वैकल्पिक रूप से प्रेरित चोटों का उपयोग पीएमआर घटकों का अध्ययन करने के लिए किया गया है, जैसे कि एनेक्सिन प्रोटीन 5,14,21,41, प्लास्मोनिक नैनोपार्टिकल्स 42,43,44,45 के संयोजन में. उच्च शक्ति स्पंदित लेज़रों की दक्षता के बावजूद, वे बीम पथ के साथ सेल के इंटीरियर को महत्वपूर्ण चोट और नुकसान पहुंचा सकते हैं। इसके अलावा, स्पंदित लेजर विकिरण पर जैविक पदार्थ में होने वाले विस्तृत परिवर्तन और क्या यह एक अच्छी तरह से परिभाषित छिद्र बनाता है, आगे की जांच की जानी बाकी है। इस लेख में एक वैकल्पिक विधि प्रस्तुत की गई है, आंतरिक संरचनाओं को महत्वपूर्ण नुकसान पहुंचाए बिना नियंत्रित तरीके सेपीएम में नैनोस्कोपिक छेद को प्रेरित करने के लिए थर्मोप्लास्मोनिक्स को नियोजित करना। यह प्लास्मोनिक एनपी को अत्यधिक केंद्रित एनआईआर लेजर में उजागर करके पूरा किया जाता है, जिसके परिणामस्वरूप एक अत्यंत स्थानीय तापमान वृद्धि होती है जो आसानी से 200 डिग्री सेल्सियस से अधिक तापमान तक पहुंच सकती है, जिससे छोटे नैनोस्कोपिक विस्फोट 25,46,47 हो सकते हैं। इस प्रक्रिया को लेजर तीव्रता के साथ-साथ एनपीएस48 के आकार, आकार और संरचना को समायोजित करके नियंत्रित किया जा सकता है। इस तकनीक को नियोजित करके, शोधकर्ता जीवित कोशिकाओं में पीएम की मरम्मत में प्रोटीन की भूमिका का पता लगा सकते हैं, जो सेल व्यवहार्यता से समझौता किए बिना झिल्ली की मरम्मत में एनेक्सिन प्रोटीन की भागीदारी के बारे में कुछ अनुत्तरित प्रश्नों को संबोधित करने में मदद कर सकता है।
प्लास्मोनिक नैनोकणों के ऑप्टिकल फँसाने को पिछले अध्ययनों 25,49,50,51,52 द्वारा अच्छी तरह से स्थापित किया गया है; हालांकि, नैनोकणों 53,54,55 के थर्मोप्लाज्मोनिक गुणों के बारे में अतिरिक्त अंतर्दृष्टि पूरक सामग्री (पूरक फ़ाइल 1) में प्राप्त की जा सकती है। थर्मोप्लाज्मोनिक विधि का उपयोग सेलुलर प्रतिक्रिया और मरम्मत तंत्र का अध्ययन करने के उद्देश्य से पीएम में नैनोस्कोपिक छेद बनाने के लिए किया जा सकता है। अधिक सटीक रूप से, पंचर को झिल्ली के करीब निकटता में एयूएनपी के ऑप्टिकल हीटिंग के माध्यम से प्राप्त किया जा सकता है, जैसा कि आंकड़े 1 ए और बी में दिखाया गया है। यह स्थानीयकृत पंचर सीए2+ प्रवाह के लिए अनुमति देता है, जिसे कैल्शियम सेंसर द्वारा सत्यापित किया गया था, इस प्रकार पीएमआर मशीनरी को सक्रिय करता है। लाइव सेल प्रयोगों के लिए, 200 एनएम के व्यास वाले एयूएनपी को कॉन्फोकल माइक्रोस्कोपी के माध्यम से पीएमआर में एएनएक्सए 2 की भूमिका की निगरानी के लिए सेल के नीचे की सतह पर स्थिर किया गया था। एनआईआर लेजर(चित्रा 1ए,बी), 1064 एनएम की तरंग दैर्ध्य के साथ, एयूएनपी को विकिरणित करता है, इसके प्लास्मोनिक गुणों(चित्रा 1सी)का शोषण करता है, जिसके परिणामस्वरूप जैविक पारदर्शिता खिड़की49 में पर्याप्त स्थानीय हीटिंग(चित्रा 1डी)होता है, जबकि सेल को कम से कम नुकसान होता है। एयूएनपी के आसपास का उच्च तापमान क्षेत्र एनपी की त्रिज्या के अनुरूप दूरी पर तेजी से 30-40% कम हो जाता है, जैसा कि चित्र 1ई में दर्शाया गया है, जिससे तीनों आयामों में अत्यंत सीमित चोट की अनुमति मिलती है।
अनुपूरक फ़ाइल 1. कृपया इस फ़ाइल को डाउनलोड करने के लिए यहाँ क्लिक करें.
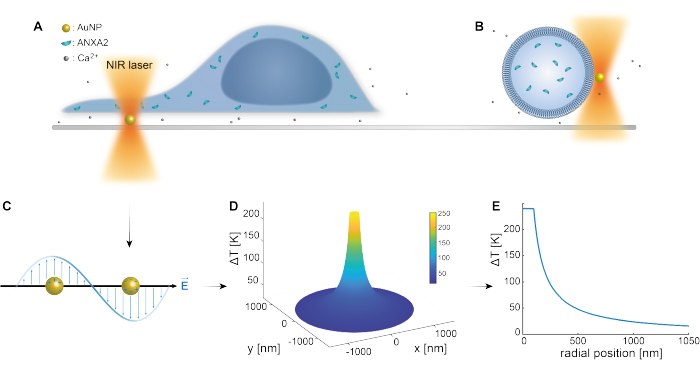
चित्रा 1: प्रयोगात्मक विधि की योजनाबद्ध रूपरेखा। (ए) एएनएक्सए-ट्रांसफ़ेक्ट कोशिकाएं सतह पर स्थिर सोने के नैनोकणों (एयूएनपी) के शीर्ष पर स्थित होती हैं, या (बी) विशाल यूनिलामेलर पुटिकाओं (जीयूवी) को समझाया गया एएनएक्सए युक्त माध्यम में निलंबित कर दिया जाता है एयूएनपी। (सी) एक एकल एयूएनपी एनआईआर ऑप्टिकल ट्रैप द्वारा विकिरणित होता है, जहां आने वाले विद्युत चुम्बकीय क्षेत्र और चालन इलेक्ट्रॉनों के बीच बातचीत एनपी के भीतर इलेक्ट्रॉनों के सामूहिक दोलन की ओर ले जाती है। (D) इस प्रक्रिया के परिणामस्वरूप तापमान में अत्यधिक सीमित लेकिन महत्वपूर्ण वृद्धि होती है। एनपी सतह पर तापमान का अनुमान लगाने के लिए, एमआईई सिद्धांत कार्यरत है, और एक (ई) तापमान प्रोफ़ाइल की गणना एयूएनपी के लिए 200 एनएम के व्यास और लेजर तीव्रता I = 6.36 x 108 W/cm2 के साथ की जाती है। कृपया इस चित्र का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
कोशिका झिल्ली पर थर्मल प्रभाव को कम करने के लिए, एयूएनपी केवल ~ 1 सेकंड के लिए विकिरणित होते हैं। यह हीटिंग के क्षणिक और स्थानीय विस्फोट का कारण बनता है, जो प्रोटीन को नुकसान को कम करता है जिसे आमतौर पर प्रकट होने के लिए अधिक समय की आवश्यकता होती है। झिल्ली पंचर पर, एनेक्सिन प्रोटीन को एक सेकंड के एक अंश में भर्ती किया जाता है, और कुछ सेकंड के भीतर, चोट की साइट (चित्रा 2) के आसपास एक एनेक्सिन रिंग जैसी मचान बनती है। इस दृष्टिकोण को मरम्मत प्रक्रियाओं की पूरी योजना पर प्रकाश डालने के प्रयास में जीवित कोशिकाओं और मॉडल झिल्ली16 दोनों में ANXA5 की भागीदारी का पता लगाने के लिए भी लागू किया गया है। जबकि प्राथमिक ध्यान विभिन्न एनेक्सिन प्रोटीन की सहसंबंधित भर्ती पर रहा है, मरम्मत तंत्र के बायोफिजिकल पहलुओं को अभी तक स्पष्ट नहीं किया गया है।
प्रस्तावित विधि को पूरी तरह से लागू करने के लिए, तीन प्रमुख घटकों की आवश्यकता होती है: कॉन्फोकल माइक्रोस्कोपी, ऑप्टिकल चिमटी और धातु नैनोकण। ऑप्टिकल चिमटी का उपयोग AuNPs को फंसाने के लिए किया जाता है, और उनका निर्माण न्यूमैन एट अल.49 द्वारा उल्लिखित प्रक्रिया का पालन करके प्राप्त किया जा सकता है। हालांकि, अगर एक ऑप्टिकल चिमटी का निर्माण बहुत चुनौतीपूर्ण साबित होता है, तो कोशिकाओं के नीचे स्थिर एयूएनपी को विकिरणित करने के लिए एक कसकर केंद्रित एनआईआर लेजर का उपयोग किया जा सकता है। गोलाकार AuNPs इस प्रोटोकॉल के लिए चुना गया, ट्यून करने योग्य अवशोषण स्पेक्ट्रा के साथ प्लास्मोनिक कणों की एक किस्म भी एनआईआर क्षेत्र48 के भीतर एक अत्यधिक स्थानीयकृत तापमान ढाल प्राप्त करने के लिए इस्तेमाल किया जा सकता है.
फ्लोरोसेंटली लेबल प्रोटीन की भूमिका को देखने के लिए प्रतिदीप्ति इमेजिंग आवश्यक है, और इसलिए, कुल आंतरिक प्रतिबिंब माइक्रोस्कोपी (टीआईआरएफ)56 को कॉन्फोकल इमेजिंग के विकल्प के रूप में माना जा सकता है। हालांकि, इस तकनीक केवल सतह इमेजिंग के लिए अनुमति देता है और मॉडल झिल्ली पुटिका प्रयोगों के साथ संगत नहीं होगा. नतीजतन, ऑप्टिकल चिमटी और confocal खुर्दबीन दोनों नैनोपार्टिकल के सटीक स्थानीयकरण और सेल चोट के आसपास के स्थानीय क्षेत्र की विस्तृत जांच के लिए आवश्यक हैं. एक विवर्तन-सीमित लेजर फोकस के साथ नैनोपार्टिकल को प्रभावी ढंग से विकिरणित करने के लिए, नैनोपार्टिकल की कल्पना करना आवश्यक है। यह प्रतिबिंब माइक्रोस्कोपी द्वारा बेहतर रूप से प्राप्त किया जा सकता है, जो लीका कॉन्फोकल माइक्रोस्कोप की एक मानक इमेजिंग विशेषता है। हालांकि, यदि प्रतिबिंब या प्रकीर्णन इमेजिंग उपलब्ध नहीं है, तो वैकल्पिक तरीकों, जैसे कम कुशल फ्लोरोसेंट एयूएनपी लेबलिंग, पर विचार किया जा सकता है।
सारांश में, इस अध्ययन में प्रस्तुत अत्यधिक नियंत्रणीय और स्थानीयकृत थर्मोप्लास्मोनिक विधि में जीवित कोशिकाओं में सेलुलर प्रतिक्रियाओं और पीएम मरम्मत तंत्र में शामिल आणविक घटकों की जांच के लिए एक उत्कृष्ट मंच के रूप में सेवा करने की क्षमता है। पीएम क्षति पर प्रोटीन प्रतिक्रिया का अध्ययन करने के अलावा, इस दृष्टिकोण का उपयोग स्थानीय रूप से पुटिकाओं को पंचर करने के लिए भी किया जा सकता है, जिससे प्रोटीन-प्रोटीन और प्रोटीन-झिल्ली गतिशीलता दोनों में प्रोटीन प्रतिक्रिया की जांच को सक्षम किया जा सकता है। इसके अलावा, यह विधि प्रोटीन, लिपिड और छोटे अणुओं के बीच बातचीत के मात्रात्मक विश्लेषण की अनुमति देती है जब झिल्ली बाधित होती है। सामूहिक रूप से, इन अग्रिमों में जटिल और जटिल प्लाज्मा झिल्ली मरम्मत मशीनरी के बारे में कुछ अनसुलझे प्रश्नों पर प्रकाश डालने की क्षमता है।
Protocol
Representative Results
Discussion
अध्ययन में झिल्ली व्यवधान के बाद जीवित कोशिकाओं और मॉडल झिल्ली में प्रोटीन प्रतिक्रियाओं की खोज के लिए एक आशाजनक तकनीक के रूप में थर्मोप्लास्मोनिक दृष्टिकोण पर प्रकाश डाला गया है। यह विधि न केवल प्रोटीन भर्ती पर व्यापक जानकारी प्रदान करती है, बल्कि प्रोटीन-झिल्ली गतिशीलता में शामिल प्रोटीन के बायोफिजिकल फ़ंक्शन पर भी प्रदान करती है। नतीजतन, यह सतह की मरम्मत के लिए जिम्मेदार आणविक घटकों की पहचान की सुविधा प्रदान करता है और प्लाज्मा झिल्ली की मरम्मत की जटिल अभी तक महत्वपूर्ण मशीनरी की समझ को आगे बढ़ाता है। यद्यपि यांत्रिक, रासायनिक और ऑप्टिकल तकनीकों जैसे झिल्ली व्यवधान को प्रेरित करने के लिए विभिन्न विधियां मौजूद हैं, ये विधियां सीमाओं से ग्रस्त हैं, जैसे कि कोशिकाओं के लिए गैर-विशिष्ट होना, कोशिका झिल्ली को कई चोटें पैदा करना, या झिल्ली को महत्वपूर्ण नुकसान पहुंचाना और उच्च शक्ति स्पंदित लेजर का उपयोग करते समय लेजर पथ के साथ आंतरिक सेलुलर सामग्री को समाप्त करना। जबकि कॉन्फोकल माइक्रोस्कोपी और ऑप्टिकल चिमटी का एकीकरण सबसे व्यापक जानकारी प्रदान करता है, वैकल्पिक इमेजिंग तौर-तरीकों का भी उपयोग किया जा सकता है। उदाहरण के लिए, प्लास्मोनिक नैनोपार्टिकल की इमेजिंग प्रतिबिंब माइक्रोस्कोपी का उपयोग करके प्राप्त की जाती है, लीका कॉन्फोकल माइक्रोस्कोप में एक अंतर्निहित इमेजिंग मोड, अतिरिक्त इमेजिंग तकनीक, जैसे डार्कफील्ड माइक्रोस्कोपी65,66, अन्य बिखरने के तरीके जैसे आईएससीएटी 67,68, या नैनोकण के फ्लोरोसेंट लेबलिंग, एयूएनपी विज़ुअलाइज़ेशन के लिए नियोजित किया जा सकता है, हालांकि यह विधि की प्रयोज्यता को सीमित कर सकता है।
प्रस्तुत विधि मॉडल झिल्ली में नैनोस्कोपिक छेद को प्रेरित करने में भी सक्षम है, जिससे विभिन्न अनुलग्नकों के बीच तालमेल प्रभाव की जांच सक्षम हो जाती है। यह अलग-अलग लेबल वाले पुनः संयोजक एनेक्सिन, जैसे, आरएफपी और जीएफपी को क्रमशः एनकैप्सुलेट करके प्राप्त किया जाता है, इसके बाद थर्मोप्लास्मोनिक पंचर होता है। यह मॉडल प्रणाली अंतर्दृष्टि प्रदान करती है कि कैसे एनेक्सिन मुक्त किनारों के आसपास के क्षेत्र में झिल्ली के साथ बातचीत करते हैं, जैसा कि चित्र 2 डी में दिखाया गया है। हालांकि, कोशिकाओं के विपरीत, जीयूवी पर लगाए गए छिद्रों का विस्तार जारी रहता है, इसके बाद पुटिका का अस्थिर हो जाता है। छेद व्यास के तेजी से विस्तार के कारण कन्फोकल माइक्रोस्कोपी का उपयोग करके छेद के विकास को इमेजिंग करना चुनौतीपूर्ण हो सकता है, लेकिन समय के साथ कई जेड-स्टैक पर कब्जा करके पूरा किया जा सकता है। एक वैकल्पिक तरीका तेजी से इमेजिंग के लिए कताई डिस्क कॉन्फोकल का उपयोग करना होगा। इसके अलावा, थर्मोप्लाज्मोनिक दृष्टिकोण आमतौर पर प्रति घंटे इष्टतम परिणामों की एक सीमित संख्या पैदा करता है जब एकल कोशिकाओं या जीयूवी प्रयोगों पर लागू होता है, आमतौर पर दो से तीन, 20 डिग्री सेल्सियस और 30 डिग्री सेल्सियस के बीच नमूना तापमान पर। प्रोटीन-झिल्ली गतिशीलता का सबसे सटीक अवलोकन प्राप्त करने के लिए, कोशिकाओं को HEPES युक्त बफर में रखने और हर घंटे नमूना बदलने की सिफारिश की जाती है। वैकल्पिक रूप से, प्रयोगात्मक खिड़की 5% सीओ2 के साथ 37 डिग्री सेल्सियस के एक निरंतर तापमान पर, यानी, एक सेल इनक्यूबेटिंग चैम्बर में प्रयोगों प्रदर्शन द्वारा बढ़ाया जा सकता है. इसके अलावा, इस दृष्टिकोण को अन्य इमेजिंग तकनीकों के साथ जोड़ना, जैसे स्टोकेस्टिक ऑप्टिकल पुनर्निर्माण माइक्रोस्कोपी (स्टॉर्म), बायोफिजिकल फ़ंक्शन और एकल-अणु स्तर पर झिल्ली की मरम्मत में शामिल प्रमुख प्रोटीनों की बातचीत की गहरी समझ प्रदान कर सकता है। यह चोट की साइट पर विस्तृत जानकारी प्रदान कर सकता है, जिसमें घाव की ज्यामिति और एनेक्सिन प्रोटीन का स्थान शामिल है, साथ ही झिल्ली की सतह की मरम्मत में शामिल अन्य प्रमुख खिलाड़ियों की पहचान भी कर सकता है।
झिल्ली की चोट को प्रेरित करने में अधिकतम प्रभावशीलता और सटीकता प्राप्त करने के लिए, प्रत्येक प्रयोग से पहले लेजर फोकस के स्थान को सत्यापित करना और यह सुनिश्चित करना अनिवार्य है कि लेजर फोकस की अक्षीय स्थिति कॉन्फोकल फोकस के साथ मेल खाती है। यह संरेखण एयूएनपी इमेजिंग के दौरान तीव्रता का अनुकूलन करता है, जिससे अधिकतम स्थानीय तापमान में वृद्धि होती है और परिणामस्वरूप कम लेजर शक्ति पर झिल्ली की चोट होती है। इस प्रक्रिया को मैन्युअल रूप से निष्पादित किया जाता है और इसलिए झिल्ली टूटना दक्षता में परिवर्तनशीलता के लिए अतिसंवेदनशील होता है क्योंकि फोकस मैन्युअल रूप से एक ऐसी स्थिति में अनुवादित होता है जो कण के स्थान के साथ मेल खाता है। सूक्ष्मदर्शी में जिसमें प्रतिबिंब मोड की कमी होती है, जैसा कि कुछ वाणिज्यिक प्रणालियों में होता है, लेजर फोकस और कण का सह-स्थानीयकरण चुनौतीपूर्ण हो सकता है। ऐसे मामलों में, वैकल्पिक इमेजिंग मोड (जैसे, उज्ज्वल क्षेत्र) नियोजित किया जा सकता है, और एक धीमी गति से रेखापुंज स्कैन अपेक्षित कण स्थिति के आसपास किया जा सकता है. यह ध्यान दिया जाना चाहिए कि कम लेजर शक्ति केवल झिल्ली पारगम्यता को प्रेरित करने की संभावना है, जबकि उच्च लेजर शक्ति एनपी के आसपास तापमान उत्पन्न कर सकती है जो पानी के क्वथनांक से अधिक है, भले ही कांच की सतह का शीतलन प्रभाव हो। यह अनुमान है कि एनपी के आसपास नैनोबबल्स का गठन 200 डिग्री सेल्सियस और 300 डिग्री सेल्सियस25,48 के बीच होता है, जहां विस्फोटक गर्मी के परिणामस्वरूप लेजर फोकस या कण विखंडन से कण विस्थापन हो सकता है। इसके अतिरिक्त, हीटिंग के दौरान नैनो या सूक्ष्म बुलबुले का गठन इस पद्धति के लिए एक चुनौती है। चूंकि हवा के इंटरफेस झिल्ली को गीला करते हैं और प्रोटीन अस्थिरता का कारण बन सकते हैं, जो अवांछनीय है, झिल्ली की मरम्मत की जांच करते समय हीटिंग को सीमित करना अनिवार्य है। विशेष रूप से, सोने के नैनोशेल उच्च तापमान को सहन नहीं करते हैं और इन परिस्थितियों में नीचा दिखाएंगे, जैसा कि उच्च-रिज़ॉल्यूशन माइक्रोस्कोपी58 द्वारा प्रदर्शित किया गया है।
यह लेख झिल्ली में अत्यधिक स्थानीयकृत पंचर करने के लिए थर्मोप्लास्मोनिक्स का उपयोग करने के लिए एक विस्तृत प्रोटोकॉल प्रदान करता है, जो कोशिकाओं और मॉडल झिल्ली दोनों पर लागू होता है। हीटिंग की सीमा को और कम करने के लिए, एनआईआर प्रकाश के साथ गुंजयमान छोटे नैनोकणों का उपयोग किया जा सकता है, जिससे एंडोसोम, एंडोप्लाज्मिक रेटिकुलम और परमाणु लिफाफे में इंट्रासेल्युलर पंचर सक्षम हो सकते हैं। छड़ और nanomatryoshkas48 सहित इस तरह के nanoparticles, endocytosed सोने नैनोकणों है कि आसानी से सेल की सतह पर ले जाया जाता है और नाभिक69 की ओर तस्करी को लक्षित करके परमाणु लिफाफा की मरम्मत की जांच करने के लिए इस्तेमाल किया जा सकता है. कुल मिलाकर, यह तकनीक पीएमआर में शामिल प्रमुख आणविक घटकों की पहचान और परीक्षा को सक्षम बनाती है, कोशिकाओं की व्यवहार्यता को संरक्षित करते हुए उनके बायोफिजिकल फ़ंक्शन और भूमिका को स्पष्ट करती है।
Disclosures
The authors have nothing to disclose.
Acknowledgements
हम हमें पुनः संयोजक एनेक्सिन प्रोटीन और एनेक्सिन के लिए प्लास्मिड एन्कोडिंग प्रदान करने के लिए जेस्पर नाइलैंडस्टेड का शुक्रिया अदा करना चाहते हैं। इस काम को डेनिश काउंसिल फॉर इंडिपेंडेंट रिसर्च, नेचुरल साइंसेज (DFF-4181-00196) द्वारा नोवो नॉर्डिस्क फाउंडेशन इंटरडिसिप्लिनरी सिनर्जी प्रोग्राम 2018 (NNF18OC0034936), वैज्ञानिक समिति डेनिश कैंसर सोसाइटी (R90-A5847-14-S2), लुंडबेक फाउंडेशन (R218-2016-534), और लुंडबेक फाउंडेशन सेंटर ऑफ एक्सीलेंस (नैनोमेडिसिन में बायोमेम्ब्रेन) द्वारा आर्थिक रूप से समर्थित किया गया था।
Materials
| 1064 nm trapping laser | Spectra Physics | N/A | Spectra Physics J201-BL-106C, Nd: YVO4 NIR laser |
| 160 nm Gold Nanoshells | NanoComposix | NCXGSIR150 | |
| 200 nm Gold Nanoparticles | BBI Solutions | EM.GC200/7 | |
| 35 mm glass surface MatTex microwell | MATTEK | P35G-1.5-14-C | |
| Amber-glass vials | Supelco Sigma Aldrich | 243438 | |
| Annexin A2 plasmids | N/A | N/A | Received from our collaborator at the Danish Cancer Research Center |
| Annexin A4 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA4 received from our collaborator at the Danish Cancer Research Center |
| Annexin A5 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA5 received from our collaborator at the Danish Cancer Research Center |
| beta-casein | Sigma Life Science | C6905-1G | |
| CaCl2 | Suprlco (sigma Aldrich) | 10035-04-8 | |
| Centrifuge 5702 | Eppendorf | 5702 | |
| Chloroform | VWR Chemicals | 67-66-3 | |
| Culture dish (Nunclon Delta Surface) | Thermo scientific | 150460 | |
| DID cell-labelling Solution | Invitrogen | 7757 | |
| Distilled water | Gibco | 15230-089 | |
| DOPC | Avanti Polar Lipids | 850375C | Dissolved in chloroform |
| DOPS | Avanti Polar Lipids | 840035C | Dissolved in chloroform |
| Dulbecco's Modified Eage's Medium | Thermo Fisher Scientific | 11995065 | |
| FIJI ImageJ distribution | ImageJ2 | N/A | |
| GCaMP6s-CAAX | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Gibco Fetal Bovine Serum | Fisher Scientific | 11573397 | 10% of the culture medium |
| Glucose | PROLABO | 24 374.297 | |
| Hamilton syringes | Hamilton Company | N/A | 50 and 500 microliters |
| Harrick Plasma Cleaner PDG-002 | Harrick Plasma | N/A | |
| HEK293T cells | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Leica Acousto-Optical Beam Splitter (AOBS) | Leica | N/A | |
| Leica PL APO 63x water immersion objective, NA = 1.2 | Leica | N/A | |
| Leica SP5 confocal scanning microscope | Leica | N/A | |
| Lipofectamine | Fisher Scientific | 15338030 | |
| MatLab | The Mathworks, Inc., Natick, Massachusetts, United States | N/A | |
| NaCl | VWR Chemicals | 7647-14-5 | |
| Opti-MEM Reduced-Serum Medium | Thermo Fisher Scientific | 11058021 | |
| Parafilm | Bemis | PM-992 | |
| Penicillin-Streptomycin | Thermo Fisher Scientific | 15140122 | 1% of the culture medium |
| Phosphate Buffered Saline (PBS) | Thermo Fisher Scientific | 10010023 | |
| Piezoelectric stage (PI 731.20) | Physik Instrumente (Germany) | N/A | |
| Poly-L-Lysine | Sigma-Aldrich | P8920-100ML | 0.01-0.1% for coating |
| Polyvinyl alcohol | Sigma-Aldrich | 363065-25G | |
| round glass slide 25 mm Ø | VWR | 631-1584 | |
| Sonicator Brandson 2800 | Brandson | N/A | |
| sucrose | Sigma Life Science | 57-50-1 | |
| T25 tissue culture flask | Falcon | 353108 | Blue Vented cap |
| Tris-HCl | Invitrogen | 15567-027 | |
| TrypLE | Thermo Fisher Scientific | A1285901 | |
| Trypsin-EDTA | Fisher Scientific | 11590626 | |
| VWR Mixer mini vortex 230V EU | VWR | 12620-84 | ECN: 444-2790, SN: 150713022 |
References
- Bendix, P. M., et al. Interdisciplinary synergy to reveal mechanisms of annexin-mediated plasma membrane shaping and repair. Cells. 9 (4), 1029 (2020).
- Gajic, O., Lee, J., Doerr, C. H., Berrios, J. C., Myers, J. L., Hubmayr, R. D. Ventilator-induced Cell Wounding and Repair in the Intact Lung. American Journal of Respiratory and Critical Care Medicine. 167, 1057-1063 (2003).
- McNeil, P. L., Khakee, R. Disruptions of muscle fiber plasma membranes. Role in exercise-induced damage. The American Journal of Pathology. 140 (5), 1097-1109 (1992).
- Yu, Q. C., McNeil, P. L. Transient disruptions of aortic endothelial cell plasma membranes. The American Journal of Pathology. 141 (6), 1349-1360 (1992).
- Boye, T. L., et al. Annexin A4 and A6 induce membrane curvature and constriction during cell membrane repair. Nature Communications. 8, 1623 (2017).
- Bischofberger, M., Gonzalez, M. R., van der Goot, F. G. Membrane injury by pore-forming proteins. Current Opinion in Cell Biology. 21, 589-595 (2009).
- Tang, S. K. Y., Marshall, W. F. Self-repairing cells. Science (New York, N.Y.). 356, 1022-1025 (2017).
- Abreu-Blanco, M. T., Verboon, J. M., Parkhurst, S. M. Single cell wound repair: Dealing with life’s little traumas. Bioarchitecture. 1, 114-121 (2011).
- Sønder, S. L., et al. Annexin A7 is required for ESCRT III-mediated plasma membrane repair. Scientific Reports. 9, 6726 (2019).
- Andrews, N. W., Almeida, P. E., Corrotte, M. Damage control: cellular mechanisms of plasma membrane repair. Trends in Cell Biology. 24 (12), 734-742 (2014).
- Idone, V., Tam, C., Goss, J. W., Toomre, D., Pypaert, M., Andrews, N. W. Repair of injured plasma membrane by rapid Ca2+-dependent endocytosis. The Journal of Cell Biology. 180 (5), 905-914 (2008).
- Lauritzen, S. P., Boye, T. L., Nylandsted, J. Annexins are instrumental for efficient plasma membrane repair in cancer cells. Seminars in Cell & Developmental Biology. 45, 32-38 (2015).
- Häger, S. C., Nylandsted, J. Annexins: players of single cell wound healing and regeneration. Communicative & Integrative Biology. 12 (1), 162-165 (2019).
- Jaiswal, J. K., et al. S100A11 is required for efficient plasma membrane repair and survival of invasive cancer cells. Nature Communications. 5, 3795 (2014).
- Draeger, A., Monastyrskaya, K., Babiychuk, E. B. Plasma membrane repair and cellular damage control: The annexin survival kit. Biochemical Pharmacology. 81 (6), 703-712 (2011).
- Moreno-Pescador, G. S., et al. Thermoplasmonic nano-rupture of cells reveals annexin V function in plasma membrane repair. Nanoscale. 14 (21), 7778-7787 (2022).
- Zhivotovsky, B., Orrenius, S. Calcium and cell death mechanisms: A perspective from the cell death community. Cell Calcium. 50 (3), 211-221 (2011).
- Gerke, V., Moss, S. E. Annexins: From structure to function. Physiological Reviews. 82 (2), 331-371 (2002).
- Idone, V., Tam, C., Andrews, N. W. Two-way traffic on the road to plasma membrane repair. Trends in Cell Biology. 18 (11), 552-559 (2008).
- Boye, T. L., et al. Annexins induce curvature on free-edge membranes displaying distinct morphologies. Scientific Reports. 8, 10309 (2018).
- Bouter, A., et al. Annexin-A5 assembled into two-dimensional arrays promotes cell membrane repair. Nature Communications. 2, 270 (2011).
- Boye, T. L., Nylandsted, J. Annexins in plasma membrane repair. Biological Chemistry. 397 (10), 961-969 (2016).
- Weinberger, A., et al. Gel-assisted formation of giant unilamellar vesicles. Biophysical Journal. 105 (1), 154-164 (2013).
- Numata, T., Tatsuta, H., Morita, Y., Otani, Y., Umeda, N. Localized thermal processing with a laser-trapped and heated metal nanoparticle. IEEJ Transactions on Electrical and Electronic Engineering. 2, 398-401 (2007).
- Bendix, P. M., Reihani, S. N. S., Oddershede, L. B. Direct measurements of heating by electromagnetically trapped gold nanoparticles on supported lipid bilayers. ACS Nano. 4 (4), 2256-2262 (2010).
- Kyrsting, A., Bendix, P. M., Stamou, D. G., Oddershede, L. B. Heat profiling of three-dimensionally optically trapped gold nanoparticles using vesicle cargo release. Nano Letters. 11 (2), 888-892 (2011).
- Andersen, T., Kyrsting, A., Bendix, P. M. Local and transient permeation events are associated with local melting of giant liposomes. Soft Matter. 10 (24), 4268-4274 (2014).
- Bahadori, A., Oddershede, L. B., Bendix, P. M. Hot-nanoparticle-mediated fusion of selected cells. Nano Research. 10, 2034-2045 (2017).
- Rørvig-Lund, A., Bahadori, A., Semsey, S., Bendix, P. M., Oddershede, L. B. Vesicle fusion triggered by optically heated gold nanoparticles. Nano Letters. 15 (6), 4183-4188 (2015).
- Moreno-Pescador, G., Arastoo, M. R., Ruhoff, V. T., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic vesicle fusion reveals membrane phase segregation of influenza spike proteins. Nano Letters. 23 (8), 3377-3384 (2023).
- Bahadori, A., Lund, A. R., Semsey, S., Oddershede, L. B., Bendix, P. M. Controlled cellular fusion using optically trapped plasmonic nano-heaters. SPIE Proceedings. SPIE 9922, Optical Trapping and Optical Micromanipulation XIII. 992211, (2016).
- Bahadori, A., Moreno-Pescador, G., Oddershede, L. B., Bendix, P. M. Remotely controlled fusion of selected vesicles and living cells: a key issue review. Reports on Progress in Physics. 81 (3), 32602 (2018).
- Moreno-Pescador, G., Arastoo, M. R., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic induced vesicle fusion for investigating membrane protein phase affinity. bioRxiv. , (2022).
- Pescador, G. S. M., et al. Investigating plasma-membrane repair employing thermoplasmonics. Biophysical Journal. 120 (3), 45A (2021).
- Moreno-Pescador, G. S., Qoqaj, I., Thusgaard Ruhoff, V., Iversen, J., Nylandsted, J., Bendix, P. M. Effect of local thermoplasmonic heating on biological membranes. SPIE 11083, Optical Trapping and Optical Micromanipulation XVI. 110830M, (2019).
- Bement, W. M., Mandato, C. A., Kirsch, M. N. Wound-induced assembly and closure of an actomyosin purse string in Xenopus oocytes. Current Biology. 9 (11), 579-587 (1999).
- Weisleder, N., et al. Recombinant MG53 protein modulates therapeutic cell membrane repair in treatment of muscular dystrophy. Science Translational Medicine. 4 (139), 139ra85 (2012).
- Sudji, I. R., Subburaj, Y., Frenkel, N., García-Sáez, A. J., Wink, M. Membrane disintegration caused by the steroid saponin digitonin is related to the presence of cholesterol. Molecules. 20 (11), 20146-20160 (2015).
- Babiychuk, E. B., Monastyrskaya, K., Potez, S., Draeger, A. Intracellular Ca2+ operates a switch between repair and lysis of streptolysin O-perforated cells. Cell Death & Differentiation. 16, 1126-1134 (2009).
- Nygård Skalman, L., Holst, M. R., Larsson, E., Lundmark, R. Plasma membrane damage caused by listeriolysin O is not repaired through endocytosis of the membrane pore. Biology Open. 7 (10), bio035287 (2018).
- Swaggart, K. A., et al. Annexin A6 modifies muscular dystrophy by mediating sarcolemmal repair. Proceedings of the National Academy of Sciences of the United States of America. 111, 6004-6009 (2014).
- Yeheskely-Hayon, D., Minai, L., Golan, L., Dann, E. J., Yelin, D. Optically induced cell fusion using bispecific nanoparticles. Small. 9 (22), 3771-3777 (2013).
- Minai, L., Yeheskely-Hayon, D., Golan, L., Bisker, G., Dann, E. J., Yelin, D. Optical nanomanipulations of malignant cells: Controlled cell damage and fusion. Small. 8 (11), 1732-1739 (2012).
- Lukianova-Hleb, E., et al. Plasmonic nanobubbles as transient vapor nanobubbles generated around plasmonic nanoparticles. ACS Nano. 4 (4), 2109-2123 (2010).
- Vogel, A., Noack, J., Hüttman, G., Paltauf, G. Mechanisms of femtosecond laser nanosurgery of cells and tissues. Applied Physics B. 81, 1015-1047 (2005).
- Baffou, G., Polleux, J., Rigneault, H., Monneret, S. Super-heating and micro-bubble generation around plasmonic nanoparticles under cw illumination. Journal of Physical Chemistry C. 118 (9), 4890-4898 (2014).
- Sasikumar, K., Liang, Z., Cahill, D. G., Keblinski, P. Curvature induced phase stability of an intensely heated liquid. Journal of Chemical Physics. 140 (23), 234506 (2014).
- Jauffred, L., Samadi, A., Klingberg, H., Bendix, P. M., Oddershede, L. B. Plasmonic heating of nanostructures. Chemical Reviews. 119 (13), 8087-8130 (2019).
- Neuman, K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nature Methods. 5 (6), 491-505 (2008).
- Bendix, P. M., Jauffred, L., Norregaard, K., Oddershede, L. B. Optical trapping of nanoparticles and quantum dots. IEEE Journal of Selected Topics in Quantum Electronics. 20, 15-26 (2014).
- Samadi, A., Bendix, P. M., Oddershede, L. B. Optical manipulation of individual strongly absorbing platinum nanoparticles. Nanoscale. 46, 18449-18455 (2017).
- Jørgensen, J. T., Norregaard, K., Tian, P., Bendix, P. M., Kjaer, A., Oddershede, L. B. Single particle and PET-based platform for identifying optimal plasmonic nano-heaters for photothermal cancer therapy. Scientific Reports. 6, 30076 (2016).
- Goldenberg, H., Tranter, C. J. Heat flow in an infinite medium heated by a sphere. British Journal of Applied Physics. 3 (9), 296-298 (1952).
- Eustis, S., El-Sayed, M. A. Why gold nanoparticles are more precious than pretty gold: Noble metal surface plasmon resonance and its enhancement of the radiative and nonradiative properties of nanocrystals of different shapes. Chemical Society Reviews. 35, 209-217 (2006).
- Landau, L. D., Lifshitz, E. M. . Fluid Mechanics: Landau and Lifshitz: Course of Theoretical Physics. 6, (2013).
- Niederauer, C., Seynen, M., Zomerdijk, J., Kamp, M., Ganzinger, K. A. The K2: Open-source simultaneous triple-color TIRF microscope for live-cell and single-molecule imaging. HardwareX. 13, e00404 (2023).
- Richardson, A. C., Reihani, N., Oddershede, L. B. Combining confocal microscopy with precise force-scope optical tweezers. SPIE Proceedings:SPIE 6326, Optical Trapping and Optical Micromanipulation III. 632628, (2006).
- Samadi, A., Klingberg, H., Jauffred, L., Kjær, A., Bendix, P. M., Oddershede, L. B. Platinum nanoparticles: a non-toxic, effective and thermally stable alternative plasmonic material for cancer therapy and bioengineering. Nanoscale. 10 (19), 9097-9107 (2018).
- . Available from: https://www.thermofisher.com/order/catalog/product/A7816 (2023)
- Kreibig, U., Vollmer, M. Theoretical considerations. In: Optical Properties of Metal Clusters. 25, (1995).
- Mie, G. Beiträge zur Optik trüber Medien, speziell kolloidaler Metallösungen. Annalen der Physik. 330 (3), 377-445 (1908).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529 (2017).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9, 676-682 (2012).
- Klenow, M. B., Heitmann, A. S. B., Nylandsted, J., Simonsen, A. C. Timescale of hole closure during plasma membrane repair estimated by calcium imaging and numerical modeling. Scientific Reports. 11, 4226 (2021).
- Li, T., Wu, X., Liu, F., Li, N. Analytical methods based on the light-scattering of plasmonic nanoparticles at the single particle level with dark-field microscopy imaging. Analyst. 142 (2), 248-256 (2017).
- Gibbs-Flournoy, E. A., Bromberg, P. A., Hofer, T. P. J., Samet, J. M., Zucker, R. M. Darkfield-Confocal Microscopy detection of nanoscale particle internalization by human lung cells. Particle and Fibre Toxicology. 8 (1), 2 (2011).
- Taylor, R. W., Sandoghdar, V. Interferometric scattering microscopy: Seeing single nanoparticles and molecules via Rayleigh scattering. Nano Letters. 19 (8), 4827-4835 (2019).
- Wu, Y., Ali, M. R. K., Chen, K., Fang, N., El-Sayed, M. A. Gold nanoparticles in biological optical imaging. Nano Today. 24, 120-140 (2019).
- Klingberg, H., Oddershede, L. B., Loeschner, K., Larsen, E. H., Loft, S., Møller, P. Uptake of gold nanoparticles in primary human endothelial cells. Toxicology Research. 4 (3), 566-666 (2015).

