En termoplasmonisk tilnærming for å undersøke plasmamembranreparasjon i levende celler og modellmembraner
Summary
Den termoplasmoniske punkteringsmetoden integrerer konfokalmikroskopi, optisk pinsett og gullnanopartikler for å studere proteinresponser under reparasjon av plasmamembraner i celler og gigantiske unilamellære vesikler. Teknikken muliggjør rask og lokalisert membranpunktering, noe som gjør det mulig å identifisere nøkkelproteiner og deres funksjonelle roller i det intrikate plasmamembranreparasjonsmaskineriet.
Abstract
Cellemembranen er avgjørende for celleoverlevelse, og det er viktig å sikre integriteten ettersom cellen opplever skader gjennom hele livssyklusen. For å forhindre skade på membranen har cellene utviklet effektive plasmamembranreparasjonsmekanismer. Disse reparasjonsmekanismene kan studeres ved å kombinere konfokalmikroskopi og nanoskala termoplasmonikk for å identifisere og undersøke rollen til nøkkelproteiner, som anneksiner, involvert i overflatereparasjon i levende celler og membranmodellsystemer.
Punkteringsmetoden benytter en laser for å indusere svært lokalisert oppvarming ved nanopartikkelbestråling. Bruken av nær-infrarødt lys minimerer fototoksisitet i den biologiske prøven, mens størstedelen av absorpsjonen foregår i den nær-infrarøde resonansplasmoniske nanopartikkelen. Denne termoplasmoniske metoden har blitt utnyttet for potensiell fototermisk og biofysisk forskning for å forbedre forståelsen av intracellulære mekanismer og cellulære responser gjennom vesikkel- og cellefusjonsstudier. Tilnærmingen har vist seg å være komplementær til eksisterende metoder for membranforstyrrelser, for eksempel mekaniske, kjemiske eller optisk induserte skader, og gir et høyt nivå av kontroll ved å forårsake ekstremt lokaliserte skader. Omfanget av skaden er begrenset til nærheten av den sfæriske nanopartikkelen, og det oppstår ingen skadelig skade langs strålebanen i motsetning til pulserende lasere som bruker forskjellige bølgelengder. Til tross for visse begrensninger, for eksempel dannelsen av nanobobler, tilbyr den termoplasmoniske metoden et unikt verktøy for å undersøke cellulære responser i plasmamembranreparasjon i et nesten innfødt miljø uten å kompromittere cellens levedyktighet.
Når den integreres med konfokalmikroskopi, kan punkteringsmetoden gi en mekanistisk forståelse av membrandynamikk i modellmembransystemer, samt kvantitativ informasjon om proteinresponser på membranskader, inkludert proteinrekruttering og deres biofysiske funksjon. Samlet sett kan anvendelsen av denne metoden på reduserte modellsystemer øke vår forståelse av det intrikate plasmamembranreparasjonsmaskineriet i levende celler.
Introduction
Cellemembranen, som fungerer både som en fysisk barriere og en signalplattform, er avgjørende for celleoverlevelse1. Gjennom hele cellesyklusen blir plasmamembranen (PM) utsatt for skader, for eksempel mekaniske 2,3,4,5 og kjemiske6 stressinduserte skader. For å opprettholde membranintegritet og sikre celleoverlevelse har cellen utviklet robuste mekanismer for reparasjon av plasmamembraner (PMR). Disse mekanismene avhenger av ulike strategier, for eksempel cytoskjelettomorganisering, membranfusjon og membranutskiftingsstrategier 7,8,9,10,11, som alle er avhengige av rekruttering av spesifikke proteiner. Spesielt har medlemmer av anneksinproteinfamilien blitt identifisert som nøkkelproteiner assosiert med prosessene til PMR 1,9,12,13,14,15,16. Etter PM-skade opplever cellen en tilstrømning av kalsiumioner (Ca2+), noe som utgjør en umiddelbar trussel mot cellens overlevelse17. Som svar på Ca2+ tilstrømning binder anneksinproteiner, som hovedsakelig er lokalisert i cytosolen, seg til den indre brosjyren til den skadede plasmamembranen som en del av PMR-strategiene18. Vedlegg A2 (ANXA2) var et av de første medlemmene av anneksinfamilien som ble assosiert med PMR ved dysferlinmangelfull muskeldystrofi og ble foreslått å formidle reparasjon ved å smelte intracellulære vesikler til PM nær skadestedet 5,19,20,21. I ettertid har flere funksjoner blitt tilskrevet vedlegg22, og deres rolle i PMR har fått økt oppmerksomhet de siste 20 årene. Den eksakte rollen til anneksiner i PMR er imidlertid ikke fullt ut forstått 15,18,21,22.
Denne artikkelen foreslår en metode for å undersøke proteinmembraninteraksjon og membrandynamikk på en kontrollert og svært lokalisert måte, ved hjelp av en kombinasjon av konfokalmikroskopi, optisk pinsett og gullnanopartikler (AuNPs). Denne metoden muliggjør kvantitativ studie av protein-, lipid- og småmolekylære interaksjoner som respons på membranskader og Ca2+ tilstrømning. Til tross for kompleksiteten og mangfoldet av komponenter som er involvert i prosessen med membranreparasjon, har forenklede membransystemer som etterligner plasmamembranen blitt brukt for å få en dypere mekanistisk forståelse av membrandynamikk og anneksinproteiners respons på membranforstyrrelser16. Giant unilamellar lipidvesikler (GUVer) ble valgt som modellmembransystem med en spesifisert lipidsammensetning. GUVene ble generert ved hjelp av gelassistert hydreringsmetode, spesielt polyvinylalkoholgelhydrering, som beskrevet av Weinberger et al.23, som tillot effektiv innkapsling av vedlegg i GUVer.
Utnyttelsen av nær-infrarød (NIR) laserbestråling på metalliske nanopartikler (NP) induserer betydelig oppvarming av NP, noe som gjør det til en effektiv metode for å etablere en lokal varmekilde utnyttet i biomedisinske applikasjoner24. Metoden ble opprinnelig brukt til å direkte måle temperaturen rundt en enkelt AuNP i både 2D og 3D biomimetiske analyser. I disse analysene 25,26 ble de plasmoniske nanopartiklene bestrålt på et støttet lipid-dobbeltlag eller optisk fanget nær GUVer som gjennomgikk en lokal termisk faseovergang ved lokal oppvarming, noe som muliggjorde kvantifisering og kontroll av den nøyaktige temperaturprofilen rundt partikkelen. Denne referansetemperaturprofilen har blitt brukt ved undersøkelse eller manipulering av biologiske prøver. Ytterligere fremskritt i metoden har gjort det lettere å induksjonere nanoskopiske porer i membraner27, noe som muliggjør vesikkel og cellefusjon 28,29. Andre studier har undersøkt oppførselen til perifere membranproteiner i GUVer29 og transmembranproteiner30 ved å skape nye hybridvesikler, mens cellespesifikk legemiddellevering også har blitt utforsket for å kontrollere og studere cellulære responser eller genuttrykk 28,29,31,32,33. Nylig har metoden blitt brukt til å undersøke proteinresponser på membranskader 32,34,35.
Det finnes flere metoder for å forstyrre plasmamembranen for å utforske cellulære responser og membranreparasjon. Disse inkluderer mikronålpunkteringer, mikroperleristing og celleskraping, som alle kan forstyrre cellemembranen mekanisk 14,36,37. Kjemisk indusert skade kan oppnås ved å tilsette vaskemidler 5,38 eller bakterielle toksiner39,40 som destabiliserer lipid-dobbeltlaget og genererer membranporer over plasmamembranen. Videre har optisk induserte skader ved kontinuerlige bølge- og pulserende lasere blitt brukt til å studere PMR-komponenter, slik som anneksinproteiner 5,14,21,41, i kombinasjon med plasmoniske nanopartikler 42,43,44,45 . Til tross for effektiviteten til pulserende lasere med høy effekt, kan de forårsake betydelige skader og skade på cellens indre langs strålebanen. Videre gjenstår de detaljerte endringene som skjer i det biologiske materialet ved pulserende laserbestråling og om det skaper en veldefinert pore, å bli undersøkt nærmere. En alternativ metode presenteres i denne artikkelen, ved bruk av termoplasmonikk for å indusere nanoskopiske hull i PM på en kontrollert måte34,35 uten å forårsake betydelig skade på de indre strukturer. Dette oppnås ved å utsette plasmoniske NP for en svært fokusert NIR-laser, noe som resulterer i en ekstremt lokalisert temperaturøkning som lett kan nå temperaturer over 200 ° C, noe som kan føre til små nanoskopiske eksplosjoner 25,46,47. Denne prosessen kan styres ved å justere laserintensiteten samt størrelsen, formen og sammensetningen av NPs48. Ved å bruke denne teknikken kan forskere utforske rollen som proteiner i PM-reparasjon i levende celler, noe som kan bidra til å løse noen av de ubesvarte spørsmålene om involvering av anneksinproteiner i membranreparasjon uten å kompromittere cellens levedyktighet.
Den optiske fangsten av plasmoniske nanopartikler har blitt godt etablert av tidligere studier 25,49,50,51,52; Imidlertid kan ytterligere innsikt om de termoplasmoniske egenskapene til nanopartiklene 53,54,55 fås i tilleggsmaterialene (tilleggsfil 1). Den termoplasmoniske metoden kan brukes til å lage nanoskopiske hull i PM med det formål å studere cellulær respons og reparasjonsmekanismer. Nærmere bestemt kan punkteringen oppnås ved optisk oppvarming av AuNP i nærheten av membranen, som vist i figur 1A og B. Denne lokaliserte punkteringen tillater Ca2+ tilstrømning, som ble verifisert av en kalsiumsensor, og dermed aktiverte PMR-maskineriet. For levende celleforsøk ble AuNP med en diameter på 200 nm immobilisert på overflaten under cellen for å overvåke ANXA2s rolle i PMR via konfokal mikroskopi. NIR-laseren (figur 1A,B), med en bølgelengde på 1064 nm, bestråler AuNP, utnytter dens plasmoniske egenskaper (figur 1C), noe som resulterer i betydelig lokal oppvarming (figur 1D) i det biologiske gjennomsiktighetsvinduet49 samtidig som den forårsaker minimal skade på selve cellen. Høytemperaturområdet rundt AuNP reduseres raskt med 30-40% i en avstand som tilsvarer NPs radius, som vist i figur 1E, noe som muliggjør en ekstremt begrenset skade i alle tre dimensjoner.
Tilleggsfil 1. Klikk her for å laste ned denne filen.
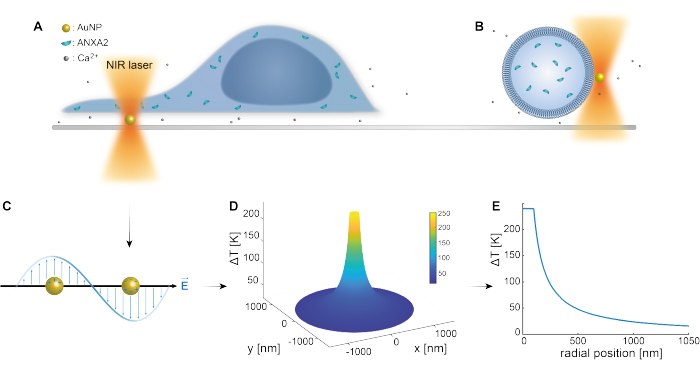
Figur 1: Skjematisk oversikt over eksperimentell metode. (A) ANXA-transfekterte celler ligger på toppen av immobiliserte gullnanopartikler (AuNPs) på overflaten, eller (B) gigantiske unilamellære vesikler (GUVer) med innkapslet ANXA er suspendert i et medium som inneholder AuNPs. (C) En enkelt AuNP bestråles av NIRs optiske felle, hvor vekselvirkningen mellom det innkommende elektromagnetiske feltet og ledningselektronene fører til den kollektive svingningen av elektroner i NP. (D) Denne prosessen resulterer i en svært begrenset, men likevel betydelig temperaturøkning. For å estimere temperaturen på NP-overflaten brukes Mie-teorien, og en (E) temperaturprofil beregnes for en AuNP med en diameter på 200 nm og laserintensitet I = 6,36 x 108 W/cm2. Klikk her for å se en større versjon av denne figuren.
For å minimere den termiske effekten på cellemembranen, blir AuNPene bare bestrålt i ~ 1 sekund. Dette fører til en forbigående og lokal utbrudd av oppvarming, noe som reduserer skaden på proteiner som vanligvis krever mer tid til å utfolde seg. Ved membranpunktering rekrutteres anneksinproteiner på brøkdelen av et sekund, og i løpet av få sekunder dannes et anneksinringlignende stillas rundt skadestedet (figur 2). Denne tilnærmingen har også blitt brukt til å utforske involvering av ANXA5 i både levende celler og modellmembraner16 i et forsøk på å kaste lys over hele skjemaet for reparasjonsprosessene. Mens hovedfokuset har vært på korrelerende rekruttering av ulike anneksinproteiner, har de biofysiske aspektene av reparasjonsmekanismen ennå ikke blitt belyst.
For å fullt ut implementere den foreslåtte metoden kreves tre nøkkelkomponenter: konfokalmikroskopi, optisk pinsett og metall nanopartikler. Optisk pinsett brukes til å fange AuNPs, og deres konstruksjon kan oppnås ved å følge prosedyren skissert av Neuman et al.49. Men hvis det viser seg å være for utfordrende å bygge en optisk pinsett, kan en tett fokusert NIR-laser brukes til å bestråle AuNPs immobilisert under cellene. Mens sfæriske AuNPer ble valgt for denne protokollen, kunne en rekke plasmoniske partikler med justerbare absorpsjonsspektra også benyttes for å oppnå en svært lokalisert temperaturgradient innenfor NIR-regionen48.
Fluorescensavbildning er nødvendig for å observere rollen til de fluorescerende merkede proteinene, og derfor kan total intern refleksjonsmikroskopi (TIRF)56 betraktes som et alternativ til konfokal avbildning. Denne teknikken tillater imidlertid bare overflateavbildning og vil ikke være kompatibel med modellmembranvesikelforsøkene. Følgelig er både den optiske pinsetten og konfokalmikroskopet avgjørende for den nøyaktige lokaliseringen av nanopartikkelen og detaljert undersøkelse av lokalområdet rundt celleskaden. For effektivt å bestråle nanopartikkelen med et diffraksjonsbegrenset laserfokus, er det nødvendig å visualisere nanopartikkelen. Dette kan oppnås optimalt ved refleksjonsmikroskopi, som er en standard avbildningsfunksjon i Leicas konfokale mikroskoper. Imidlertid, hvis refleksjon eller spredningsavbildning ikke er tilgjengelig, kan alternative metoder, for eksempel den mindre effektive fluorescerende AuNP-merkingen, vurderes.
Oppsummert har den svært kontrollerbare og lokaliserte termoplasmoniske metoden som presenteres i denne studien, potensial til å tjene som en utmerket plattform for å undersøke molekylære komponenter involvert i cellulære responser og PM-reparasjonsmekanismer i levende celler. I tillegg til å studere proteinresponsen ved PM-skade, kan denne tilnærmingen også brukes til lokalt punktering av vesikler, og dermed muliggjøre en undersøkelse av proteinresponsen i både protein-protein og proteinmembrandynamikk. Videre tillater denne metoden en kvantitativ analyse av samspillet mellom proteiner, lipider og små molekyler når membraner forstyrres. Samlet har disse fremskrittene potensial til å kaste lys over noen av de uløste spørsmålene angående det intrikate og komplekse plasmamembranreparasjonsmaskineriet.
Protocol
Representative Results
Discussion
Studien fremhever den termoplasmoniske tilnærmingen som en lovende teknikk for å utforske proteinresponser i levende celler og modellmembraner etter membranforstyrrelser. Denne metoden gir ikke bare omfattende informasjon om proteinrekruttering, men også om den biofysiske funksjonen til proteiner involvert i proteinmembrandynamikk. Følgelig letter det identifiseringen av molekylære komponenter som er ansvarlige for overflatereparasjon og fremmer forståelsen av det komplekse, men vitale maskineriet for reparasjon av plasmamembran. Selv om det finnes ulike metoder for å indusere membranforstyrrelser, for eksempel mekaniske, kjemiske og optiske teknikker, lider disse metodene av begrensninger, for eksempel å være ikke-spesifikke for celler, generere flere skader på cellemembranen, eller forårsake betydelig skade på membranen og ablatere internt cellulært materiale langs laserbanen ved bruk av høyeffekts pulserende lasere. Mens integrasjonen av konfokalmikroskopi og optisk pinsett gir den mest omfattende informasjonen, kan alternative bildebehandlingsmodaliteter også brukes. For eksempel, da avbildning av den plasmoniske nanopartikkelen oppnås ved hjelp av refleksjonsmikroskopi, en innebygd bildebehandlingsmodus i Leica konfokale mikroskoper, kan ytterligere bildebehandlingsteknikker, som mørkefeltsmikroskopi65,66, andre spredningsmetoder som iSCAT67,68 eller fluorescerende merking av nanopartikkelen, brukes til AuNP-visualisering, selv om dette kan begrense anvendeligheten av metoden.
Den presenterte metoden er i tillegg i stand til å indusere nanoskopiske hull i modellmembraner, noe som muliggjør undersøkelse av synergieffektene mellom forskjellige anneksiner. Dette oppnås ved å innkapsle forskjellig merkede rekombinante anneksiner, henholdsvis RFP og GFP, etterfulgt av termoplasmonisk punktering. Dette modellsystemet gir innsikt i hvordan anneksiner vekselvirker med membraner i nærheten av frie kanter, som vist i figur 2D. Imidlertid, i motsetning til i celler, fortsetter hullene påført GUVer å ekspandere, etterfulgt av destabilisering av vesiklet. Avbildning av hullutviklingen ved hjelp av konfokalmikroskopi kan være utfordrende på grunn av den raske utvidelsen av hulldiameteren, men kan oppnås ved å fange flere z-stabler over tid. En alternativ metode ville være å bruke en spinnende disk confocal for raskere avbildning. Videre gir den termoplasmoniske tilnærmingen vanligvis et begrenset antall optimale resultater per time når den brukes på enkeltceller eller GUV-eksperimenter, vanligvis to til tre, ved prøvetemperaturer mellom 20 ° C og 30 ° C. For å oppnå den mest nøyaktige observasjonen av proteinmembrandynamikk, anbefales det å holde cellene i en HEPES-holdig buffer og erstatte prøven hver time. Alternativt kan eksperimentvinduet utvides ved å utføre eksperimentene i et celleinkubasjonskammer, dvs. ved en konstant temperatur på 37 °C med 5% CO2. Videre kan kombinere denne tilnærmingen med andre bildebehandlingsteknikker, for eksempel stokastisk optisk rekonstruksjonsmikroskopi (STORM), gi en dypere forståelse av den biofysiske funksjonen og samspillet mellom nøkkelproteiner involvert i membranreparasjon på enkeltmolekylnivå. Dette kan gi detaljert informasjon om skadestedet, inkludert sårgeometri og plassering av annexinproteiner, samt identifisere andre viktige aktører involvert i reparasjon av membranoverflaten.
For å oppnå maksimal effektivitet og presisjon ved indusering av membranskade, er det viktig å verifisere plasseringen av laserfokuset før hvert eksperiment og sikre at den aksiale posisjonen til laserfokuset sammenfaller med konfokalfokuset. Denne justeringen optimaliserer intensiteten under AuNP-avbildning, noe som fører til maksimal lokal temperaturøkning og påfølgende membranskade ved lavere lasereffekt. Denne prosessen utføres manuelt og er derfor utsatt for variabilitet i membranbruddeffektivitet ettersom fokuset manuelt oversettes til en posisjon som sammenfaller med partikkelens plassering. I mikroskoper som mangler refleksjonsmodus, som i noen kommersielle systemer, kan samlokalisering av laserfokus og partikkel være utfordrende. I slike tilfeller kan alternative avbildningsmodi (f.eks. lysfelt) benyttes, og en langsom rasterskanning kan utføres rundt den forventede partikkelposisjonen. Det skal bemerkes at lav lasereffekt sannsynligvis bare vil indusere membranpermeabilisering, mens høy lasereffekt kan generere temperaturer rundt NP som overskrider kokepunktet for vann, selv om glassoverflaten har en avkjølende effekt. Det er anslått at dannelsen av nanobobler som omgir NPene skjer mellom 200 ° C og 300 ° C 25,48, hvor eksplosiv varme kan resultere i enten partikkelforskyvning fra laserfokus eller partikkelfragmentering. I tillegg utgjør dannelsen av nano eller mikrobobler under oppvarming en utfordring for denne metoden. Siden luftgrensesnitt dewet membraner og kan forårsake protein destabilisering, noe som er uønsket, er det viktig å begrense oppvarmingen når man undersøker membranreparasjon. Spesielt toler gull nanoshells ikke høye temperaturer og vil nedbrytes under disse forholdene, som demonstrert ved høyoppløselig mikroskopi58.
Denne artikkelen gir en detaljert protokoll for bruk av termoplasmonikk for å utføre svært lokaliserte punkteringer i membraner, som gjelder for både celler og modellmembraner. For ytterligere å redusere omfanget av oppvarming, kan mindre nanopartikler resonans med NIR-lys utnyttes, noe som muliggjør intracellulære punkteringer i endosomer, endoplasmatisk retikulum og nukleær konvolutt. Slike nanopartikler, inkludert stenger og nanomatryoshkas48, kan brukes til å undersøke kjernefysisk konvoluttreparasjon ved å målrette endocytoserte gullnanopartikler som lett tas opp på celleoverflaten og trafikkeres mot kjernen69. Samlet sett muliggjør denne teknikken identifisering og undersøkelse av viktige molekylære komponenter involvert i PMR, som belyser deres biofysiske funksjon og rolle samtidig som cellens levedyktighet opprettholdes.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker Jesper Nylandsted for å gi oss rekombinante anneksinproteiner og plasmider som koder for anneksiner. Dette arbeidet ble støttet økonomisk av Rådet for Selvstendig Forskning, Naturvitenskap (DFF-4181-00196), av Novo Nordisk Foundation Interdisciplinary Synergy Program 2018 (NNF18OC0034936), Vitenskapskomiteen Danish Cancer Society (R90-A5847-14-S2), Lundbeck Foundation (R218-2016-534), og av Lundbeck Foundation Center of Excellence (Biomembranes in Nanomedicine).
Materials
| 1064 nm trapping laser | Spectra Physics | N/A | Spectra Physics J201-BL-106C, Nd: YVO4 NIR laser |
| 160 nm Gold Nanoshells | NanoComposix | NCXGSIR150 | |
| 200 nm Gold Nanoparticles | BBI Solutions | EM.GC200/7 | |
| 35 mm glass surface MatTex microwell | MATTEK | P35G-1.5-14-C | |
| Amber-glass vials | Supelco Sigma Aldrich | 243438 | |
| Annexin A2 plasmids | N/A | N/A | Received from our collaborator at the Danish Cancer Research Center |
| Annexin A4 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA4 received from our collaborator at the Danish Cancer Research Center |
| Annexin A5 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA5 received from our collaborator at the Danish Cancer Research Center |
| beta-casein | Sigma Life Science | C6905-1G | |
| CaCl2 | Suprlco (sigma Aldrich) | 10035-04-8 | |
| Centrifuge 5702 | Eppendorf | 5702 | |
| Chloroform | VWR Chemicals | 67-66-3 | |
| Culture dish (Nunclon Delta Surface) | Thermo scientific | 150460 | |
| DID cell-labelling Solution | Invitrogen | 7757 | |
| Distilled water | Gibco | 15230-089 | |
| DOPC | Avanti Polar Lipids | 850375C | Dissolved in chloroform |
| DOPS | Avanti Polar Lipids | 840035C | Dissolved in chloroform |
| Dulbecco's Modified Eage's Medium | Thermo Fisher Scientific | 11995065 | |
| FIJI ImageJ distribution | ImageJ2 | N/A | |
| GCaMP6s-CAAX | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Gibco Fetal Bovine Serum | Fisher Scientific | 11573397 | 10% of the culture medium |
| Glucose | PROLABO | 24 374.297 | |
| Hamilton syringes | Hamilton Company | N/A | 50 and 500 microliters |
| Harrick Plasma Cleaner PDG-002 | Harrick Plasma | N/A | |
| HEK293T cells | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Leica Acousto-Optical Beam Splitter (AOBS) | Leica | N/A | |
| Leica PL APO 63x water immersion objective, NA = 1.2 | Leica | N/A | |
| Leica SP5 confocal scanning microscope | Leica | N/A | |
| Lipofectamine | Fisher Scientific | 15338030 | |
| MatLab | The Mathworks, Inc., Natick, Massachusetts, United States | N/A | |
| NaCl | VWR Chemicals | 7647-14-5 | |
| Opti-MEM Reduced-Serum Medium | Thermo Fisher Scientific | 11058021 | |
| Parafilm | Bemis | PM-992 | |
| Penicillin-Streptomycin | Thermo Fisher Scientific | 15140122 | 1% of the culture medium |
| Phosphate Buffered Saline (PBS) | Thermo Fisher Scientific | 10010023 | |
| Piezoelectric stage (PI 731.20) | Physik Instrumente (Germany) | N/A | |
| Poly-L-Lysine | Sigma-Aldrich | P8920-100ML | 0.01-0.1% for coating |
| Polyvinyl alcohol | Sigma-Aldrich | 363065-25G | |
| round glass slide 25 mm Ø | VWR | 631-1584 | |
| Sonicator Brandson 2800 | Brandson | N/A | |
| sucrose | Sigma Life Science | 57-50-1 | |
| T25 tissue culture flask | Falcon | 353108 | Blue Vented cap |
| Tris-HCl | Invitrogen | 15567-027 | |
| TrypLE | Thermo Fisher Scientific | A1285901 | |
| Trypsin-EDTA | Fisher Scientific | 11590626 | |
| VWR Mixer mini vortex 230V EU | VWR | 12620-84 | ECN: 444-2790, SN: 150713022 |
References
- Bendix, P. M., et al. Interdisciplinary synergy to reveal mechanisms of annexin-mediated plasma membrane shaping and repair. Cells. 9 (4), 1029 (2020).
- Gajic, O., Lee, J., Doerr, C. H., Berrios, J. C., Myers, J. L., Hubmayr, R. D. Ventilator-induced Cell Wounding and Repair in the Intact Lung. American Journal of Respiratory and Critical Care Medicine. 167, 1057-1063 (2003).
- McNeil, P. L., Khakee, R. Disruptions of muscle fiber plasma membranes. Role in exercise-induced damage. The American Journal of Pathology. 140 (5), 1097-1109 (1992).
- Yu, Q. C., McNeil, P. L. Transient disruptions of aortic endothelial cell plasma membranes. The American Journal of Pathology. 141 (6), 1349-1360 (1992).
- Boye, T. L., et al. Annexin A4 and A6 induce membrane curvature and constriction during cell membrane repair. Nature Communications. 8, 1623 (2017).
- Bischofberger, M., Gonzalez, M. R., van der Goot, F. G. Membrane injury by pore-forming proteins. Current Opinion in Cell Biology. 21, 589-595 (2009).
- Tang, S. K. Y., Marshall, W. F. Self-repairing cells. Science (New York, N.Y.). 356, 1022-1025 (2017).
- Abreu-Blanco, M. T., Verboon, J. M., Parkhurst, S. M. Single cell wound repair: Dealing with life’s little traumas. Bioarchitecture. 1, 114-121 (2011).
- Sønder, S. L., et al. Annexin A7 is required for ESCRT III-mediated plasma membrane repair. Scientific Reports. 9, 6726 (2019).
- Andrews, N. W., Almeida, P. E., Corrotte, M. Damage control: cellular mechanisms of plasma membrane repair. Trends in Cell Biology. 24 (12), 734-742 (2014).
- Idone, V., Tam, C., Goss, J. W., Toomre, D., Pypaert, M., Andrews, N. W. Repair of injured plasma membrane by rapid Ca2+-dependent endocytosis. The Journal of Cell Biology. 180 (5), 905-914 (2008).
- Lauritzen, S. P., Boye, T. L., Nylandsted, J. Annexins are instrumental for efficient plasma membrane repair in cancer cells. Seminars in Cell & Developmental Biology. 45, 32-38 (2015).
- Häger, S. C., Nylandsted, J. Annexins: players of single cell wound healing and regeneration. Communicative & Integrative Biology. 12 (1), 162-165 (2019).
- Jaiswal, J. K., et al. S100A11 is required for efficient plasma membrane repair and survival of invasive cancer cells. Nature Communications. 5, 3795 (2014).
- Draeger, A., Monastyrskaya, K., Babiychuk, E. B. Plasma membrane repair and cellular damage control: The annexin survival kit. Biochemical Pharmacology. 81 (6), 703-712 (2011).
- Moreno-Pescador, G. S., et al. Thermoplasmonic nano-rupture of cells reveals annexin V function in plasma membrane repair. Nanoscale. 14 (21), 7778-7787 (2022).
- Zhivotovsky, B., Orrenius, S. Calcium and cell death mechanisms: A perspective from the cell death community. Cell Calcium. 50 (3), 211-221 (2011).
- Gerke, V., Moss, S. E. Annexins: From structure to function. Physiological Reviews. 82 (2), 331-371 (2002).
- Idone, V., Tam, C., Andrews, N. W. Two-way traffic on the road to plasma membrane repair. Trends in Cell Biology. 18 (11), 552-559 (2008).
- Boye, T. L., et al. Annexins induce curvature on free-edge membranes displaying distinct morphologies. Scientific Reports. 8, 10309 (2018).
- Bouter, A., et al. Annexin-A5 assembled into two-dimensional arrays promotes cell membrane repair. Nature Communications. 2, 270 (2011).
- Boye, T. L., Nylandsted, J. Annexins in plasma membrane repair. Biological Chemistry. 397 (10), 961-969 (2016).
- Weinberger, A., et al. Gel-assisted formation of giant unilamellar vesicles. Biophysical Journal. 105 (1), 154-164 (2013).
- Numata, T., Tatsuta, H., Morita, Y., Otani, Y., Umeda, N. Localized thermal processing with a laser-trapped and heated metal nanoparticle. IEEJ Transactions on Electrical and Electronic Engineering. 2, 398-401 (2007).
- Bendix, P. M., Reihani, S. N. S., Oddershede, L. B. Direct measurements of heating by electromagnetically trapped gold nanoparticles on supported lipid bilayers. ACS Nano. 4 (4), 2256-2262 (2010).
- Kyrsting, A., Bendix, P. M., Stamou, D. G., Oddershede, L. B. Heat profiling of three-dimensionally optically trapped gold nanoparticles using vesicle cargo release. Nano Letters. 11 (2), 888-892 (2011).
- Andersen, T., Kyrsting, A., Bendix, P. M. Local and transient permeation events are associated with local melting of giant liposomes. Soft Matter. 10 (24), 4268-4274 (2014).
- Bahadori, A., Oddershede, L. B., Bendix, P. M. Hot-nanoparticle-mediated fusion of selected cells. Nano Research. 10, 2034-2045 (2017).
- Rørvig-Lund, A., Bahadori, A., Semsey, S., Bendix, P. M., Oddershede, L. B. Vesicle fusion triggered by optically heated gold nanoparticles. Nano Letters. 15 (6), 4183-4188 (2015).
- Moreno-Pescador, G., Arastoo, M. R., Ruhoff, V. T., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic vesicle fusion reveals membrane phase segregation of influenza spike proteins. Nano Letters. 23 (8), 3377-3384 (2023).
- Bahadori, A., Lund, A. R., Semsey, S., Oddershede, L. B., Bendix, P. M. Controlled cellular fusion using optically trapped plasmonic nano-heaters. SPIE Proceedings. SPIE 9922, Optical Trapping and Optical Micromanipulation XIII. 992211, (2016).
- Bahadori, A., Moreno-Pescador, G., Oddershede, L. B., Bendix, P. M. Remotely controlled fusion of selected vesicles and living cells: a key issue review. Reports on Progress in Physics. 81 (3), 32602 (2018).
- Moreno-Pescador, G., Arastoo, M. R., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic induced vesicle fusion for investigating membrane protein phase affinity. bioRxiv. , (2022).
- Pescador, G. S. M., et al. Investigating plasma-membrane repair employing thermoplasmonics. Biophysical Journal. 120 (3), 45A (2021).
- Moreno-Pescador, G. S., Qoqaj, I., Thusgaard Ruhoff, V., Iversen, J., Nylandsted, J., Bendix, P. M. Effect of local thermoplasmonic heating on biological membranes. SPIE 11083, Optical Trapping and Optical Micromanipulation XVI. 110830M, (2019).
- Bement, W. M., Mandato, C. A., Kirsch, M. N. Wound-induced assembly and closure of an actomyosin purse string in Xenopus oocytes. Current Biology. 9 (11), 579-587 (1999).
- Weisleder, N., et al. Recombinant MG53 protein modulates therapeutic cell membrane repair in treatment of muscular dystrophy. Science Translational Medicine. 4 (139), 139ra85 (2012).
- Sudji, I. R., Subburaj, Y., Frenkel, N., García-Sáez, A. J., Wink, M. Membrane disintegration caused by the steroid saponin digitonin is related to the presence of cholesterol. Molecules. 20 (11), 20146-20160 (2015).
- Babiychuk, E. B., Monastyrskaya, K., Potez, S., Draeger, A. Intracellular Ca2+ operates a switch between repair and lysis of streptolysin O-perforated cells. Cell Death & Differentiation. 16, 1126-1134 (2009).
- Nygård Skalman, L., Holst, M. R., Larsson, E., Lundmark, R. Plasma membrane damage caused by listeriolysin O is not repaired through endocytosis of the membrane pore. Biology Open. 7 (10), bio035287 (2018).
- Swaggart, K. A., et al. Annexin A6 modifies muscular dystrophy by mediating sarcolemmal repair. Proceedings of the National Academy of Sciences of the United States of America. 111, 6004-6009 (2014).
- Yeheskely-Hayon, D., Minai, L., Golan, L., Dann, E. J., Yelin, D. Optically induced cell fusion using bispecific nanoparticles. Small. 9 (22), 3771-3777 (2013).
- Minai, L., Yeheskely-Hayon, D., Golan, L., Bisker, G., Dann, E. J., Yelin, D. Optical nanomanipulations of malignant cells: Controlled cell damage and fusion. Small. 8 (11), 1732-1739 (2012).
- Lukianova-Hleb, E., et al. Plasmonic nanobubbles as transient vapor nanobubbles generated around plasmonic nanoparticles. ACS Nano. 4 (4), 2109-2123 (2010).
- Vogel, A., Noack, J., Hüttman, G., Paltauf, G. Mechanisms of femtosecond laser nanosurgery of cells and tissues. Applied Physics B. 81, 1015-1047 (2005).
- Baffou, G., Polleux, J., Rigneault, H., Monneret, S. Super-heating and micro-bubble generation around plasmonic nanoparticles under cw illumination. Journal of Physical Chemistry C. 118 (9), 4890-4898 (2014).
- Sasikumar, K., Liang, Z., Cahill, D. G., Keblinski, P. Curvature induced phase stability of an intensely heated liquid. Journal of Chemical Physics. 140 (23), 234506 (2014).
- Jauffred, L., Samadi, A., Klingberg, H., Bendix, P. M., Oddershede, L. B. Plasmonic heating of nanostructures. Chemical Reviews. 119 (13), 8087-8130 (2019).
- Neuman, K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nature Methods. 5 (6), 491-505 (2008).
- Bendix, P. M., Jauffred, L., Norregaard, K., Oddershede, L. B. Optical trapping of nanoparticles and quantum dots. IEEE Journal of Selected Topics in Quantum Electronics. 20, 15-26 (2014).
- Samadi, A., Bendix, P. M., Oddershede, L. B. Optical manipulation of individual strongly absorbing platinum nanoparticles. Nanoscale. 46, 18449-18455 (2017).
- Jørgensen, J. T., Norregaard, K., Tian, P., Bendix, P. M., Kjaer, A., Oddershede, L. B. Single particle and PET-based platform for identifying optimal plasmonic nano-heaters for photothermal cancer therapy. Scientific Reports. 6, 30076 (2016).
- Goldenberg, H., Tranter, C. J. Heat flow in an infinite medium heated by a sphere. British Journal of Applied Physics. 3 (9), 296-298 (1952).
- Eustis, S., El-Sayed, M. A. Why gold nanoparticles are more precious than pretty gold: Noble metal surface plasmon resonance and its enhancement of the radiative and nonradiative properties of nanocrystals of different shapes. Chemical Society Reviews. 35, 209-217 (2006).
- Landau, L. D., Lifshitz, E. M. . Fluid Mechanics: Landau and Lifshitz: Course of Theoretical Physics. 6, (2013).
- Niederauer, C., Seynen, M., Zomerdijk, J., Kamp, M., Ganzinger, K. A. The K2: Open-source simultaneous triple-color TIRF microscope for live-cell and single-molecule imaging. HardwareX. 13, e00404 (2023).
- Richardson, A. C., Reihani, N., Oddershede, L. B. Combining confocal microscopy with precise force-scope optical tweezers. SPIE Proceedings:SPIE 6326, Optical Trapping and Optical Micromanipulation III. 632628, (2006).
- Samadi, A., Klingberg, H., Jauffred, L., Kjær, A., Bendix, P. M., Oddershede, L. B. Platinum nanoparticles: a non-toxic, effective and thermally stable alternative plasmonic material for cancer therapy and bioengineering. Nanoscale. 10 (19), 9097-9107 (2018).
- . Available from: https://www.thermofisher.com/order/catalog/product/A7816 (2023)
- Kreibig, U., Vollmer, M. Theoretical considerations. In: Optical Properties of Metal Clusters. 25, (1995).
- Mie, G. Beiträge zur Optik trüber Medien, speziell kolloidaler Metallösungen. Annalen der Physik. 330 (3), 377-445 (1908).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529 (2017).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9, 676-682 (2012).
- Klenow, M. B., Heitmann, A. S. B., Nylandsted, J., Simonsen, A. C. Timescale of hole closure during plasma membrane repair estimated by calcium imaging and numerical modeling. Scientific Reports. 11, 4226 (2021).
- Li, T., Wu, X., Liu, F., Li, N. Analytical methods based on the light-scattering of plasmonic nanoparticles at the single particle level with dark-field microscopy imaging. Analyst. 142 (2), 248-256 (2017).
- Gibbs-Flournoy, E. A., Bromberg, P. A., Hofer, T. P. J., Samet, J. M., Zucker, R. M. Darkfield-Confocal Microscopy detection of nanoscale particle internalization by human lung cells. Particle and Fibre Toxicology. 8 (1), 2 (2011).
- Taylor, R. W., Sandoghdar, V. Interferometric scattering microscopy: Seeing single nanoparticles and molecules via Rayleigh scattering. Nano Letters. 19 (8), 4827-4835 (2019).
- Wu, Y., Ali, M. R. K., Chen, K., Fang, N., El-Sayed, M. A. Gold nanoparticles in biological optical imaging. Nano Today. 24, 120-140 (2019).
- Klingberg, H., Oddershede, L. B., Loeschner, K., Larsen, E. H., Loft, S., Møller, P. Uptake of gold nanoparticles in primary human endothelial cells. Toxicology Research. 4 (3), 566-666 (2015).

