En termoplasmonisk metod för att undersöka reparation av plasmamembran i levande celler och modellmembran
Summary
Den termoplasmoniska punkteringsmetoden integrerar konfokalmikroskopi, optisk pincett och guldnanopartiklar för att studera proteinsvar under reparation av plasmamembran i celler och gigantiska unilamellära vesiklar. Tekniken möjliggör snabb och lokaliserad membranpunktion, vilket gör det möjligt att identifiera nyckelproteiner och deras funktionella roller i det intrikata plasmamembranreparationsmaskineriet.
Abstract
Cellmembranet är avgörande för cellens överlevnad, och att säkerställa dess integritet är viktigt eftersom cellen upplever skador under hela sin livscykel. För att förhindra skador på membranet har cellerna utvecklat effektiva mekanismer för reparation av plasmamembran. Dessa reparationsmekanismer kan studeras genom att kombinera konfokalmikroskopi och termoplasmonik i nanoskala för att identifiera och undersöka rollen för nyckelproteiner, såsom annexiner, som är involverade i ytreparation i levande celler och membranmodellsystem.
Punkteringsmetoden använder en laser för att inducera mycket lokal uppvärmning vid bestrålning av nanopartiklar. Användningen av nära-infrarött ljus minimerar fototoxiciteten i det biologiska provet, medan majoriteten av absorptionen sker i den nära-infraröda resonansplasmoniska nanopartikeln. Denna termoplasmoniska metod har utnyttjats för potentiell fototermisk och biofysisk forskning för att öka förståelsen för intracellulära mekanismer och cellulära svar genom vesikel- och cellfusionsstudier. Tillvägagångssättet har visat sig vara ett komplement till befintliga metoder för membranstörningar, såsom mekaniskt, kemiskt eller optiskt inducerade skador, och ger en hög grad av kontroll genom att tillfoga extremt lokala skador. Skadans omfattning är begränsad till närheten av den sfäriska nanopartikeln, och ingen skadlig skada uppstår längs strålvägen i motsats till pulsade lasrar med olika våglängder. Trots vissa begränsningar, såsom bildandet av nanobubblor, erbjuder den termoplasmoniska metoden ett unikt verktyg för att undersöka cellulära svar vid reparation av plasmamembran i en nästan naturlig miljö utan att kompromissa med cellviabiliteten.
När punkteringsmetoden integreras med konfokalmikroskopi kan den ge en mekanistisk förståelse av membrandynamik i modellmembransystem samt kvantitativ information om proteiners svar på membranskador, inklusive proteinrekrytering och deras biofysiska funktion. Sammantaget kan tillämpningen av denna metod på reducerade modellsystem öka vår förståelse för det intrikata plasmamembranreparationsmaskineriet i levande celler.
Introduction
Cellmembranet, som fungerar både som en fysisk barriär och en signalplattform, är avgörande för cellens överlevnad1. Under hela sin cellcykel utsätts plasmamembranet (PM) för skador, såsom mekaniska 2,3,4,5 och kemiska6 stressinducerade skador. För att upprätthålla membranintegriteten och säkerställa cellens överlevnad har cellen utvecklat robusta mekanismer för reparation av plasmamembran (PMR). Dessa mekanismer beror på olika strategier, såsom omorganisation av cytoskelett, membranfusion och membranersättningsstrategier 7,8,9,10,11, som alla är beroende av rekrytering av specifika proteiner. Noterbart är att medlemmar av annexinproteinfamiljen har identifierats som nyckelproteiner associerade med processerna för PMR 1,9,12,13,14,15,16. Efter partikelskada upplever cellen ett inflöde av kalciumjoner (Ca2+), vilket utgör ett omedelbart hot mot cellens överlevnad17. Som svar på Ca2+-inflöde binder annexinproteiner, som huvudsakligen finns i cytosolen, till det inre bladet i det skadade plasmamembranet som en del av PMR-strategierna18. Annexin A2 (ANXA2) var en av de första medlemmarna i annexinfamiljen som associerades med PMR vid dysferlin-bristfällig muskeldystrofi och föreslogs förmedla reparation genom att smälta intracellulära vesiklar till PM nära skadestället 5,19,20,21. Därefter har flera funktioner tillskrivits annexiner22, och deras roll i PMR har fått ökad uppmärksamhet under de senaste 20 åren. Den exakta rollen för annexiner i PMR är dock fortfarande inte helt klarlagd 15,18,21,22.
Denna artikel föreslår en metod för att undersöka protein-membraninteraktion och membrandynamik på ett kontrollerat och mycket lokaliserat sätt, med hjälp av en kombination av konfokalmikroskopi, optisk pincett och guldnanopartiklar (AuNP). Denna metod möjliggör kvantitativa studier av protein-, lipid- och småmolekylinteraktioner som svar på membranskador och Ca2+ -inflöde. Trots komplexiteten och mångfalden av komponenter som är involverade i processen för membranreparation, har förenklade membransystem som efterliknar plasmamembranet använts för att få en djupare mekanistisk förståelse av membrandynamik och annexinproteiners respons på membranstörningar16. Gigantiska unilamellära lipidvesiklar (GUV) valdes som modellmembransystem med en specificerad lipidsammansättning. GUV:erna genererades med hjälp av den gelassisterade hydratiseringsmetoden, särskilt polyvinylalkoholgelhydratisering, som beskrivs av Weinberger et al.23, vilket möjliggjorde effektiv inkapsling av annexiner i GUV:er.
Användningen av nära-infraröd (NIR) laserbestrålning på metalliska nanopartiklar (NP) inducerar betydande uppvärmning av NP, vilket gör det till en effektiv metod för att etablera en lokal värmekälla som utnyttjas i biomedicinska tillämpningar24. Metoden användes ursprungligen för att direkt mäta temperaturen kring en enda AuNP i både 2D och 3D biomimetiska analyser. I dessa analyser25,26 bestrålades de plasmoniska nanopartiklarna på ett lipiddubbelskikt eller optiskt fångade nära GUV:er som genomgick en lokal termisk fasövergång vid lokal uppvärmning, vilket möjliggjorde kvantifiering och kontroll av den exakta temperaturprofilen runt partikeln. Denna referenstemperaturprofil har använts vid undersökning eller manipulering av biologiska prover. Ytterligare framsteg i metoden har underlättat induktionen av nanoskopiska porer i membran27, vilket möjliggör vesikel- och cellfusion28,29. Andra studier har undersökt beteendet hos perifera membranproteiner i GUVs29 och transmembranproteiner30 genom att skapa nya hybridvesiklar, medan cellspecifik läkemedelsleverans också har utforskats för att kontrollera och studera cellulära svar eller genuttryck 28,29,31,32,33. På senare tid har metoden använts för att undersöka proteiners respons på membranskador 32,34,35.
Det finns flera metoder för att störa plasmamembranet för att utforska cellulära svar och membranreparation. Dessa inkluderar mikronålspunkteringar, skakning av mikropärlor och cellskrapning, som alla kan störa cellmembranet mekaniskt 14,36,37. Kemiskt inducerad skada kan uppnås genom tillsats av rengöringsmedel 5,38 eller bakterietoxiner39,40 som destabiliserar lipiddubbelskiktet och genererar membranporer över plasmamembranet. Dessutom har optiskt inducerade skador av kontinuerliga vågor och pulsade lasrar använts för att studera PMR-komponenter, såsom annexinproteiner 5,14,21,41, i kombination med plasmoniska nanopartiklar 42,43,44,45. Trots effektiviteten hos pulsade lasrar med hög effekt kan de orsaka betydande skador och skador på cellens inre längs strålvägen. Dessutom återstår det att undersöka de detaljerade förändringar som sker i det biologiska materialet vid pulsad laserbestrålning och om det skapar en väldefinierad por. En alternativ metod presenteras i denna artikel, som använder termoplasmonik för att inducera nanoskopiska hål i PM på ett kontrollerat sätt34,35 utan att orsaka betydande skada på de inre strukturerna. Detta åstadkoms genom att exponera plasmoniska NP för en mycket fokuserad NIR-laser, vilket resulterar i en extremt lokal temperaturökning som lätt kan nå temperaturer över 200 °C, vilket kan leda till små nanoskopiska explosioner 25,46,47. Denna process kan styras genom att justera laserintensiteten samt storleken, formen och sammansättningen av NP48. Genom att använda denna teknik kan forskare utforska proteinernas roll i PM-reparation i levande celler, vilket kan hjälpa till att ta itu med några av de obesvarade frågorna om annexinproteiners inblandning i membranreparation utan att äventyra cellviabiliteten.
Den optiska infångningen av plasmoniska nanopartiklar är väl etablerad i tidigare studier 25,49,50,51,52; Ytterligare insikter om de termoplasmoniska egenskaperna hos nanopartiklarna 53,54,55 kan dock erhållas i de kompletterande materialen (Supplementary File 1). Den termoplasmoniska metoden kan användas för att skapa nanoskopiska hål i PM i syfte att studera cellulära respons- och reparationsmekanismer. Mer exakt kan punkteringen åstadkommas genom optisk uppvärmning av AuNP i närheten av membranet, som visas i figurerna 1A och B. Denna lokaliserade punktering möjliggör Ca2+-inflöde, vilket verifierades av en kalciumsensor, vilket aktiverar PMR-maskineriet. För experiment med levande celler immobiliserades AuNP med en diameter på 200 nm på ytan under cellen för att övervaka ANXA2:s roll i PMR via konfokalmikroskopi. NIR-lasern (figur 1A,B), med en våglängd på 1064 nm, bestrålar AuNP och utnyttjar dess plasmoniska egenskaper (figur 1C), vilket resulterar i betydande lokal uppvärmning (figur 1D) i det biologiska transparensfönstret49 samtidigt som den orsakar minimal skada på själva cellen. Högtemperaturområdet som omger AuNP minskar snabbt med 30-40 % på ett avstånd som motsvarar NP:s radie, som visas i figur 1E, vilket möjliggör en extremt begränsad skada i alla tre dimensionerna.
Kompletterande fil 1. Klicka här för att ladda ner den här filen.
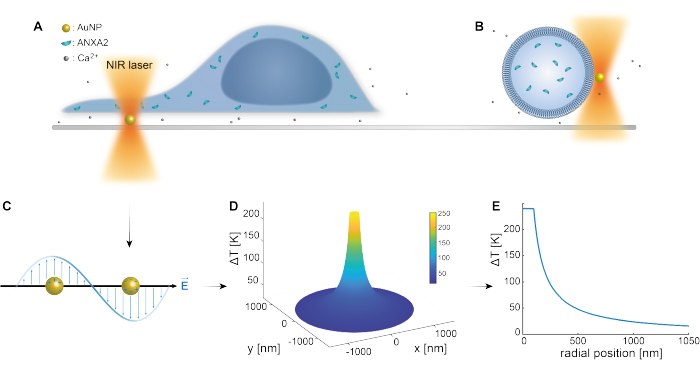
Figur 1: Schematisk översikt över den experimentella metoden. (A) ANXA-transfekterade celler är belägna ovanpå immobiliserade guldnanopartiklar (AuNP) på ytan, eller (B) gigantiska unilamellära vesiklar (GUV) med inkapslad ANXA är suspenderade i ett medium som innehåller AuNPs. (C) En enda AuNP bestrålas av den optiska NIR-fällan, där interaktionen mellan det inkommande elektromagnetiska fältet och ledningselektronerna leder till en kollektiv svängning av elektroner inom NP. (D) Denna process resulterar i en mycket begränsad men ändå betydande temperaturökning. För att uppskatta temperaturen vid NP-ytan används Mie-teorin, och en (E) temperaturprofil beräknas för en AuNP med en diameter på 200 nm och laserintensiteten I = 6,36 x 108 W/cm2. Klicka här för att se en större version av denna figur.
För att minimera den termiska effekten på cellmembranet bestrålas AuNP endast i ~1 sekund. Detta orsakar en övergående och lokal explosion av uppvärmning, vilket minskar skadorna på proteiner som vanligtvis kräver mer tid för att utvecklas. Vid membranpunktion rekryteras annexinproteiner på bråkdelen av en sekund, och inom några sekunder bildas en annexinringliknande ställning runt skadestället (Figur 2). Detta tillvägagångssätt har också tillämpats för att utforska involveringen av ANXA5 i både levande celler och modellmembran16 i ett försök att belysa hela schemat för reparationsprocesserna. Medan det primära fokuset har legat på korrelerande rekrytering av olika annexinproteiner, har de biofysiska aspekterna av reparationsmekanismen ännu inte klarlagts.
För att fullt ut implementera den föreslagna metoden krävs tre nyckelkomponenter: konfokalmikroskopi, optisk pincett och metallnanopartiklar. Optisk pincett används för att fånga AuNPs, och deras konstruktion kan uppnås genom att följa proceduren som beskrivs av Neuman et al.49. Men om det visar sig vara för utmanande att bygga en optisk pincett, kan en tätt fokuserad NIR-laser användas för att bestråla AuNPs immobiliserade under cellerna. Medan sfäriska AuNP valdes för detta protokoll, kunde en mängd plasmoniska partiklar med avstämbara absorptionsspektra också användas för att uppnå en mycket lokal temperaturgradient inom NIR-regionen48.
Fluorescensavbildning är nödvändig för att observera de fluorescerande märkta proteinernas roll, och därför kan total intern reflektionsmikroskopi (TIRF)56 övervägas som ett alternativ till konfokal avbildning. Denna teknik tillåter dock endast ytavbildning och skulle inte vara kompatibel med modellmembranvesikelexperimenten. Följaktligen är både den optiska pincetten och konfokalmikroskopet viktiga för den exakta lokaliseringen av nanopartikeln och detaljerad undersökning av det lokala området kring cellskadan. För att effektivt bestråla nanopartikeln med ett diffraktionsbegränsat laserfokus är det nödvändigt att visualisera nanopartikeln. Detta kan uppnås optimalt genom reflektionsmikroskopi, som är en standardavbildningsfunktion för Leicas konfokalmikroskop. Om reflektions- eller spridningsavbildning inte är tillgänglig kan dock alternativa metoder, såsom den mindre effektiva fluorescerande AuNP-märkningen, övervägas.
Sammanfattningsvis har den mycket kontrollerbara och lokaliserade termoplasmoniska metoden som presenteras i denna studie potential att fungera som en utmärkt plattform för att undersöka de molekylära komponenter som är involverade i cellulära svar och PM-reparationsmekanismer i levande celler. Förutom att studera proteinresponsen vid PM-skada kan detta tillvägagångssätt också användas för att lokalt punktera vesiklar, vilket möjliggör en undersökning av proteinresponsen i både protein-protein och protein-membrandynamik. Dessutom möjliggör denna metod en kvantitativ analys av interaktionerna mellan proteiner, lipider och små molekyler när membran störs. Sammantaget har dessa framsteg potential att kasta ljus över några av de olösta frågorna om det intrikata och komplexa maskineriet för reparation av plasmamembran.
Protocol
Representative Results
Discussion
Studien lyfter fram det termoplasmoniska tillvägagångssättet som en lovande teknik för att utforska proteinsvar i levande celler och modellmembran efter membranstörningar. Denna metod ger inte bara omfattande information om proteinrekrytering utan också om den biofysiska funktionen hos proteiner som är involverade i protein-membrandynamik. Följaktligen underlättar det identifieringen av molekylära komponenter som är ansvariga för ytreparation och ökar förståelsen för det komplexa men ändå viktiga maskineriet för reparation av plasmamembran. Även om det finns olika metoder för att inducera membranstörningar, såsom mekaniska, kemiska och optiska tekniker, lider dessa metoder av begränsningar, såsom att de är ospecifika för celler, genererar flera skador på cellmembranet eller orsakar betydande skador på membranet och ablaterar internt cellulärt material längs laservägen när man använder pulserande lasrar med hög effekt. Integreringen av konfokalmikroskopi och optisk pincett ger den mest omfattande informationen, men alternativa avbildningsmetoder kan också användas. Till exempel, eftersom avbildningen av den plasmoniska nanopartikeln uppnås med hjälp av reflektionsmikroskopi, kan ett inbyggt avbildningsläge i Leicas konfokalmikroskop, ytterligare avbildningstekniker, såsom mörkfältsmikroskopi65,66, andra spridningsmetoder som iSCAT67,68 eller fluorescerande märkning av nanopartikeln, användas för AuNP-visualisering, även om detta kan begränsa metodens tillämplighet.
Den presenterade metoden är dessutom kapabel att inducera nanoskopiska hål i modellmembran, vilket möjliggör undersökning av synergieffekterna mellan olika annexiner. Detta uppnås genom inkapsling av olika märkta rekombinanta annexiner, t.ex. RFP respektive GFP, följt av termoplasmonisk punktion. Detta modellsystem ger insikt i hur annexiner interagerar med membran i närheten av fria kanter, vilket visas i figur 2D. Men till skillnad från i celler fortsätter hålen som tillfogas GUV:er att expandera, följt av destabilisering av vesikeln. Att avbilda hålets utveckling med hjälp av konfokalmikroskopi kan vara utmanande på grund av den snabba expansionen av håldiametern, men kan åstadkommas genom att fånga flera z-stackar över tid. En alternativ metod skulle vara att använda en konfokal med snurrande skiva för snabbare avbildning. Dessutom ger den termoplasmoniska metoden vanligtvis ett begränsat antal optimala resultat per timme när den tillämpas på enskilda celler eller GUV-experiment, vanligtvis två till tre, vid provtemperaturer mellan 20 °C och 30 °C. För att få den mest exakta observationen av protein-membrandynamiken rekommenderas att hålla cellerna i en HEPES-innehållande buffert och byta ut provet varje timme. Alternativt kan försöksfönstret förlängas genom att experimenten utförs i en cellinkubationskammare, dvs. vid en konstant temperatur på 37 °C med 5 % CO2 . Att kombinera detta tillvägagångssätt med andra avbildningstekniker, såsom stokastisk optisk rekonstruktionsmikroskopi (STORM), kan ge en djupare förståelse för den biofysiska funktionen och interaktionen mellan nyckelproteiner som är involverade i membranreparation på en enda molekylnivå. Detta skulle kunna ge detaljerad information om skadestället, inklusive sårgeometrin och placeringen av annexinproteiner, samt identifiera andra nyckelaktörer som är involverade i reparationen av membranytan.
För att uppnå maximal effektivitet och precision när det gäller att inducera membranskada är det absolut nödvändigt att verifiera laserfokusets placering före varje experiment och se till att laserfokusets axiella position sammanfaller med det konfokala fokuset. Denna inriktning optimerar intensiteten under AuNP-avbildning, vilket leder till en maximal lokal temperaturökning och därmed membranskada vid lägre lasereffekt. Denna process utförs manuellt och är därför känslig för variabilitet i membranbrotteffektivitet eftersom fokus manuellt översätts till en position som sammanfaller med partikelns plats. I mikroskop som saknar reflektionsläge, som i vissa kommersiella system, kan samlokalisering av laserfokus och partiklar vara utmanande. I sådana fall kan alternativa avbildningslägen (t.ex. ljusfält) användas, och en långsam rasterskanning kan utföras runt den förväntade partikelpositionen. Det bör noteras att låg lasereffekt sannolikt endast inducerar membranpermeabilisering, medan hög lasereffekt kan generera temperaturer runt NP som överstiger vattnets kokpunkt, även om glasytan har en kylande effekt. Det uppskattas att bildandet av nanobubblor som omger NP sker mellan 200 °C och 300 °C25,48, där den explosiva värmen kan resultera i antingen partikelförskjutning från laserfokus eller partikelfragmentering. Dessutom utgör bildandet av nano- eller mikrobubblor under uppvärmning en utmaning för denna metod. Eftersom luftgränssnitt avvätar membran och kan orsaka proteindestabilisering, vilket är oönskat, är det absolut nödvändigt att begränsa uppvärmningen när man undersöker membranreparation. Noterbart är att guldnanoskal inte tål höga temperaturer och kommer att brytas ned under dessa förhållanden, vilket demonstreras av högupplöst mikroskopi58.
Den här artikeln innehåller ett detaljerat protokoll för att använda termoplasmonik för att utföra mycket lokaliserade punkteringar i membran, vilket är tillämpligt på både celler och modellmembran. För att ytterligare minska uppvärmningen kan mindre nanopartiklar som resonerar med NIR-ljus användas, vilket möjliggör intracellulära punkteringar i endosomer, det endoplasmatiska nätverket och kärnhöljet. Sådana nanopartiklar, inklusive stavar och nanomatrjosjkor48, kan användas för att undersöka reparation av kärnhöljet genom att rikta in sig på endocytoserade guldnanopartiklar som lätt tas upp vid cellytan och transporteras mot kärnan69. Sammantaget möjliggör denna teknik identifiering och undersökning av viktiga molekylära komponenter som är involverade i PMR, vilket belyser deras biofysiska funktion och roll samtidigt som cellernas livskraft bevaras.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi vill tacka Jesper Nylandsted för att han försett oss med rekombinanta annexinproteiner och plasmider som kodar för annexiner. Detta arbete stöddes ekonomiskt av Danish Council for Independent Research, Natural Sciences (DFF-4181-00196), av Novo Nordisk Foundation Interdisciplinary Synergy Program 2018 (NNF18OC0034936), Scientific Committee Danish Cancer Society (R90-A5847-14-S2), Lundbeck Foundation (R218-2016-534) och av Lundbeck Foundation Center of Excellence (Biomembranes in Nanomedicine).
Materials
| 1064 nm trapping laser | Spectra Physics | N/A | Spectra Physics J201-BL-106C, Nd: YVO4 NIR laser |
| 160 nm Gold Nanoshells | NanoComposix | NCXGSIR150 | |
| 200 nm Gold Nanoparticles | BBI Solutions | EM.GC200/7 | |
| 35 mm glass surface MatTex microwell | MATTEK | P35G-1.5-14-C | |
| Amber-glass vials | Supelco Sigma Aldrich | 243438 | |
| Annexin A2 plasmids | N/A | N/A | Received from our collaborator at the Danish Cancer Research Center |
| Annexin A4 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA4 received from our collaborator at the Danish Cancer Research Center |
| Annexin A5 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA5 received from our collaborator at the Danish Cancer Research Center |
| beta-casein | Sigma Life Science | C6905-1G | |
| CaCl2 | Suprlco (sigma Aldrich) | 10035-04-8 | |
| Centrifuge 5702 | Eppendorf | 5702 | |
| Chloroform | VWR Chemicals | 67-66-3 | |
| Culture dish (Nunclon Delta Surface) | Thermo scientific | 150460 | |
| DID cell-labelling Solution | Invitrogen | 7757 | |
| Distilled water | Gibco | 15230-089 | |
| DOPC | Avanti Polar Lipids | 850375C | Dissolved in chloroform |
| DOPS | Avanti Polar Lipids | 840035C | Dissolved in chloroform |
| Dulbecco's Modified Eage's Medium | Thermo Fisher Scientific | 11995065 | |
| FIJI ImageJ distribution | ImageJ2 | N/A | |
| GCaMP6s-CAAX | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Gibco Fetal Bovine Serum | Fisher Scientific | 11573397 | 10% of the culture medium |
| Glucose | PROLABO | 24 374.297 | |
| Hamilton syringes | Hamilton Company | N/A | 50 and 500 microliters |
| Harrick Plasma Cleaner PDG-002 | Harrick Plasma | N/A | |
| HEK293T cells | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Leica Acousto-Optical Beam Splitter (AOBS) | Leica | N/A | |
| Leica PL APO 63x water immersion objective, NA = 1.2 | Leica | N/A | |
| Leica SP5 confocal scanning microscope | Leica | N/A | |
| Lipofectamine | Fisher Scientific | 15338030 | |
| MatLab | The Mathworks, Inc., Natick, Massachusetts, United States | N/A | |
| NaCl | VWR Chemicals | 7647-14-5 | |
| Opti-MEM Reduced-Serum Medium | Thermo Fisher Scientific | 11058021 | |
| Parafilm | Bemis | PM-992 | |
| Penicillin-Streptomycin | Thermo Fisher Scientific | 15140122 | 1% of the culture medium |
| Phosphate Buffered Saline (PBS) | Thermo Fisher Scientific | 10010023 | |
| Piezoelectric stage (PI 731.20) | Physik Instrumente (Germany) | N/A | |
| Poly-L-Lysine | Sigma-Aldrich | P8920-100ML | 0.01-0.1% for coating |
| Polyvinyl alcohol | Sigma-Aldrich | 363065-25G | |
| round glass slide 25 mm Ø | VWR | 631-1584 | |
| Sonicator Brandson 2800 | Brandson | N/A | |
| sucrose | Sigma Life Science | 57-50-1 | |
| T25 tissue culture flask | Falcon | 353108 | Blue Vented cap |
| Tris-HCl | Invitrogen | 15567-027 | |
| TrypLE | Thermo Fisher Scientific | A1285901 | |
| Trypsin-EDTA | Fisher Scientific | 11590626 | |
| VWR Mixer mini vortex 230V EU | VWR | 12620-84 | ECN: 444-2790, SN: 150713022 |
References
- Bendix, P. M., et al. Interdisciplinary synergy to reveal mechanisms of annexin-mediated plasma membrane shaping and repair. Cells. 9 (4), 1029 (2020).
- Gajic, O., Lee, J., Doerr, C. H., Berrios, J. C., Myers, J. L., Hubmayr, R. D. Ventilator-induced Cell Wounding and Repair in the Intact Lung. American Journal of Respiratory and Critical Care Medicine. 167, 1057-1063 (2003).
- McNeil, P. L., Khakee, R. Disruptions of muscle fiber plasma membranes. Role in exercise-induced damage. The American Journal of Pathology. 140 (5), 1097-1109 (1992).
- Yu, Q. C., McNeil, P. L. Transient disruptions of aortic endothelial cell plasma membranes. The American Journal of Pathology. 141 (6), 1349-1360 (1992).
- Boye, T. L., et al. Annexin A4 and A6 induce membrane curvature and constriction during cell membrane repair. Nature Communications. 8, 1623 (2017).
- Bischofberger, M., Gonzalez, M. R., van der Goot, F. G. Membrane injury by pore-forming proteins. Current Opinion in Cell Biology. 21, 589-595 (2009).
- Tang, S. K. Y., Marshall, W. F. Self-repairing cells. Science (New York, N.Y.). 356, 1022-1025 (2017).
- Abreu-Blanco, M. T., Verboon, J. M., Parkhurst, S. M. Single cell wound repair: Dealing with life’s little traumas. Bioarchitecture. 1, 114-121 (2011).
- Sønder, S. L., et al. Annexin A7 is required for ESCRT III-mediated plasma membrane repair. Scientific Reports. 9, 6726 (2019).
- Andrews, N. W., Almeida, P. E., Corrotte, M. Damage control: cellular mechanisms of plasma membrane repair. Trends in Cell Biology. 24 (12), 734-742 (2014).
- Idone, V., Tam, C., Goss, J. W., Toomre, D., Pypaert, M., Andrews, N. W. Repair of injured plasma membrane by rapid Ca2+-dependent endocytosis. The Journal of Cell Biology. 180 (5), 905-914 (2008).
- Lauritzen, S. P., Boye, T. L., Nylandsted, J. Annexins are instrumental for efficient plasma membrane repair in cancer cells. Seminars in Cell & Developmental Biology. 45, 32-38 (2015).
- Häger, S. C., Nylandsted, J. Annexins: players of single cell wound healing and regeneration. Communicative & Integrative Biology. 12 (1), 162-165 (2019).
- Jaiswal, J. K., et al. S100A11 is required for efficient plasma membrane repair and survival of invasive cancer cells. Nature Communications. 5, 3795 (2014).
- Draeger, A., Monastyrskaya, K., Babiychuk, E. B. Plasma membrane repair and cellular damage control: The annexin survival kit. Biochemical Pharmacology. 81 (6), 703-712 (2011).
- Moreno-Pescador, G. S., et al. Thermoplasmonic nano-rupture of cells reveals annexin V function in plasma membrane repair. Nanoscale. 14 (21), 7778-7787 (2022).
- Zhivotovsky, B., Orrenius, S. Calcium and cell death mechanisms: A perspective from the cell death community. Cell Calcium. 50 (3), 211-221 (2011).
- Gerke, V., Moss, S. E. Annexins: From structure to function. Physiological Reviews. 82 (2), 331-371 (2002).
- Idone, V., Tam, C., Andrews, N. W. Two-way traffic on the road to plasma membrane repair. Trends in Cell Biology. 18 (11), 552-559 (2008).
- Boye, T. L., et al. Annexins induce curvature on free-edge membranes displaying distinct morphologies. Scientific Reports. 8, 10309 (2018).
- Bouter, A., et al. Annexin-A5 assembled into two-dimensional arrays promotes cell membrane repair. Nature Communications. 2, 270 (2011).
- Boye, T. L., Nylandsted, J. Annexins in plasma membrane repair. Biological Chemistry. 397 (10), 961-969 (2016).
- Weinberger, A., et al. Gel-assisted formation of giant unilamellar vesicles. Biophysical Journal. 105 (1), 154-164 (2013).
- Numata, T., Tatsuta, H., Morita, Y., Otani, Y., Umeda, N. Localized thermal processing with a laser-trapped and heated metal nanoparticle. IEEJ Transactions on Electrical and Electronic Engineering. 2, 398-401 (2007).
- Bendix, P. M., Reihani, S. N. S., Oddershede, L. B. Direct measurements of heating by electromagnetically trapped gold nanoparticles on supported lipid bilayers. ACS Nano. 4 (4), 2256-2262 (2010).
- Kyrsting, A., Bendix, P. M., Stamou, D. G., Oddershede, L. B. Heat profiling of three-dimensionally optically trapped gold nanoparticles using vesicle cargo release. Nano Letters. 11 (2), 888-892 (2011).
- Andersen, T., Kyrsting, A., Bendix, P. M. Local and transient permeation events are associated with local melting of giant liposomes. Soft Matter. 10 (24), 4268-4274 (2014).
- Bahadori, A., Oddershede, L. B., Bendix, P. M. Hot-nanoparticle-mediated fusion of selected cells. Nano Research. 10, 2034-2045 (2017).
- Rørvig-Lund, A., Bahadori, A., Semsey, S., Bendix, P. M., Oddershede, L. B. Vesicle fusion triggered by optically heated gold nanoparticles. Nano Letters. 15 (6), 4183-4188 (2015).
- Moreno-Pescador, G., Arastoo, M. R., Ruhoff, V. T., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic vesicle fusion reveals membrane phase segregation of influenza spike proteins. Nano Letters. 23 (8), 3377-3384 (2023).
- Bahadori, A., Lund, A. R., Semsey, S., Oddershede, L. B., Bendix, P. M. Controlled cellular fusion using optically trapped plasmonic nano-heaters. SPIE Proceedings. SPIE 9922, Optical Trapping and Optical Micromanipulation XIII. 992211, (2016).
- Bahadori, A., Moreno-Pescador, G., Oddershede, L. B., Bendix, P. M. Remotely controlled fusion of selected vesicles and living cells: a key issue review. Reports on Progress in Physics. 81 (3), 32602 (2018).
- Moreno-Pescador, G., Arastoo, M. R., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic induced vesicle fusion for investigating membrane protein phase affinity. bioRxiv. , (2022).
- Pescador, G. S. M., et al. Investigating plasma-membrane repair employing thermoplasmonics. Biophysical Journal. 120 (3), 45A (2021).
- Moreno-Pescador, G. S., Qoqaj, I., Thusgaard Ruhoff, V., Iversen, J., Nylandsted, J., Bendix, P. M. Effect of local thermoplasmonic heating on biological membranes. SPIE 11083, Optical Trapping and Optical Micromanipulation XVI. 110830M, (2019).
- Bement, W. M., Mandato, C. A., Kirsch, M. N. Wound-induced assembly and closure of an actomyosin purse string in Xenopus oocytes. Current Biology. 9 (11), 579-587 (1999).
- Weisleder, N., et al. Recombinant MG53 protein modulates therapeutic cell membrane repair in treatment of muscular dystrophy. Science Translational Medicine. 4 (139), 139ra85 (2012).
- Sudji, I. R., Subburaj, Y., Frenkel, N., García-Sáez, A. J., Wink, M. Membrane disintegration caused by the steroid saponin digitonin is related to the presence of cholesterol. Molecules. 20 (11), 20146-20160 (2015).
- Babiychuk, E. B., Monastyrskaya, K., Potez, S., Draeger, A. Intracellular Ca2+ operates a switch between repair and lysis of streptolysin O-perforated cells. Cell Death & Differentiation. 16, 1126-1134 (2009).
- Nygård Skalman, L., Holst, M. R., Larsson, E., Lundmark, R. Plasma membrane damage caused by listeriolysin O is not repaired through endocytosis of the membrane pore. Biology Open. 7 (10), bio035287 (2018).
- Swaggart, K. A., et al. Annexin A6 modifies muscular dystrophy by mediating sarcolemmal repair. Proceedings of the National Academy of Sciences of the United States of America. 111, 6004-6009 (2014).
- Yeheskely-Hayon, D., Minai, L., Golan, L., Dann, E. J., Yelin, D. Optically induced cell fusion using bispecific nanoparticles. Small. 9 (22), 3771-3777 (2013).
- Minai, L., Yeheskely-Hayon, D., Golan, L., Bisker, G., Dann, E. J., Yelin, D. Optical nanomanipulations of malignant cells: Controlled cell damage and fusion. Small. 8 (11), 1732-1739 (2012).
- Lukianova-Hleb, E., et al. Plasmonic nanobubbles as transient vapor nanobubbles generated around plasmonic nanoparticles. ACS Nano. 4 (4), 2109-2123 (2010).
- Vogel, A., Noack, J., Hüttman, G., Paltauf, G. Mechanisms of femtosecond laser nanosurgery of cells and tissues. Applied Physics B. 81, 1015-1047 (2005).
- Baffou, G., Polleux, J., Rigneault, H., Monneret, S. Super-heating and micro-bubble generation around plasmonic nanoparticles under cw illumination. Journal of Physical Chemistry C. 118 (9), 4890-4898 (2014).
- Sasikumar, K., Liang, Z., Cahill, D. G., Keblinski, P. Curvature induced phase stability of an intensely heated liquid. Journal of Chemical Physics. 140 (23), 234506 (2014).
- Jauffred, L., Samadi, A., Klingberg, H., Bendix, P. M., Oddershede, L. B. Plasmonic heating of nanostructures. Chemical Reviews. 119 (13), 8087-8130 (2019).
- Neuman, K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nature Methods. 5 (6), 491-505 (2008).
- Bendix, P. M., Jauffred, L., Norregaard, K., Oddershede, L. B. Optical trapping of nanoparticles and quantum dots. IEEE Journal of Selected Topics in Quantum Electronics. 20, 15-26 (2014).
- Samadi, A., Bendix, P. M., Oddershede, L. B. Optical manipulation of individual strongly absorbing platinum nanoparticles. Nanoscale. 46, 18449-18455 (2017).
- Jørgensen, J. T., Norregaard, K., Tian, P., Bendix, P. M., Kjaer, A., Oddershede, L. B. Single particle and PET-based platform for identifying optimal plasmonic nano-heaters for photothermal cancer therapy. Scientific Reports. 6, 30076 (2016).
- Goldenberg, H., Tranter, C. J. Heat flow in an infinite medium heated by a sphere. British Journal of Applied Physics. 3 (9), 296-298 (1952).
- Eustis, S., El-Sayed, M. A. Why gold nanoparticles are more precious than pretty gold: Noble metal surface plasmon resonance and its enhancement of the radiative and nonradiative properties of nanocrystals of different shapes. Chemical Society Reviews. 35, 209-217 (2006).
- Landau, L. D., Lifshitz, E. M. . Fluid Mechanics: Landau and Lifshitz: Course of Theoretical Physics. 6, (2013).
- Niederauer, C., Seynen, M., Zomerdijk, J., Kamp, M., Ganzinger, K. A. The K2: Open-source simultaneous triple-color TIRF microscope for live-cell and single-molecule imaging. HardwareX. 13, e00404 (2023).
- Richardson, A. C., Reihani, N., Oddershede, L. B. Combining confocal microscopy with precise force-scope optical tweezers. SPIE Proceedings:SPIE 6326, Optical Trapping and Optical Micromanipulation III. 632628, (2006).
- Samadi, A., Klingberg, H., Jauffred, L., Kjær, A., Bendix, P. M., Oddershede, L. B. Platinum nanoparticles: a non-toxic, effective and thermally stable alternative plasmonic material for cancer therapy and bioengineering. Nanoscale. 10 (19), 9097-9107 (2018).
- . Available from: https://www.thermofisher.com/order/catalog/product/A7816 (2023)
- Kreibig, U., Vollmer, M. Theoretical considerations. In: Optical Properties of Metal Clusters. 25, (1995).
- Mie, G. Beiträge zur Optik trüber Medien, speziell kolloidaler Metallösungen. Annalen der Physik. 330 (3), 377-445 (1908).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529 (2017).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9, 676-682 (2012).
- Klenow, M. B., Heitmann, A. S. B., Nylandsted, J., Simonsen, A. C. Timescale of hole closure during plasma membrane repair estimated by calcium imaging and numerical modeling. Scientific Reports. 11, 4226 (2021).
- Li, T., Wu, X., Liu, F., Li, N. Analytical methods based on the light-scattering of plasmonic nanoparticles at the single particle level with dark-field microscopy imaging. Analyst. 142 (2), 248-256 (2017).
- Gibbs-Flournoy, E. A., Bromberg, P. A., Hofer, T. P. J., Samet, J. M., Zucker, R. M. Darkfield-Confocal Microscopy detection of nanoscale particle internalization by human lung cells. Particle and Fibre Toxicology. 8 (1), 2 (2011).
- Taylor, R. W., Sandoghdar, V. Interferometric scattering microscopy: Seeing single nanoparticles and molecules via Rayleigh scattering. Nano Letters. 19 (8), 4827-4835 (2019).
- Wu, Y., Ali, M. R. K., Chen, K., Fang, N., El-Sayed, M. A. Gold nanoparticles in biological optical imaging. Nano Today. 24, 120-140 (2019).
- Klingberg, H., Oddershede, L. B., Loeschner, K., Larsen, E. H., Loft, S., Møller, P. Uptake of gold nanoparticles in primary human endothelial cells. Toxicology Research. 4 (3), 566-666 (2015).

