Tredimensjonal bioprinting av humane iPSC-avledede nevron-astrocytt-kokulturer for screeningapplikasjoner
Summary
Her presenterer vi en protokoll for å produsere 3D-bioprintede kokulturer av iPSC-avledede nevroner og astrocytter. Denne kokulturmodellen, generert i et hydrogelstillas i 96- eller 384-brønnformater, demonstrerer høy levedyktighet etter utskrift og nevrittutvekst innen 7 dager og viser uttrykket av modenhetsmarkører for begge celletyper.
Abstract
For at en cellemodell skal være levedyktig for legemiddelscreening, må systemet oppfylle krav til gjennomstrømning og homogenitet sammen med å ha en effektiv utviklingstid. Mange publiserte 3D-modeller tilfredsstiller imidlertid ikke disse kriteriene. Dette begrenser derfor deres nytte i tidlige legemiddeloppdagelsesapplikasjoner. Tredimensjonal (3D) bioprinting er en ny teknologi som kan brukes til utvikling av 3D-modeller for å fremskynde utviklingstiden, øke standardiseringen og øke gjennomstrømningen. Her presenterer vi en protokoll for å utvikle 3D bioprintede kokulturmodeller av humane induserte pluripotente stamceller (iPSC)-avledede glutamaterge nevroner og astrocytter. Disse kokulturene er innebygd i en hydrogelmatrise av bioaktive peptider, fulllengde ekstracellulære matriksproteiner (ECM), og med en fysiologisk stivhet på 1, 1 kPa. Modellen kan raskt etableres i 96-brønns og 384-brønns formater og gir en gjennomsnittlig levedyktighet etter utskrift på 72%. Astrocytt-til-nevronforholdet i denne modellen er vist å være 1: 1, 5, som er innenfor det fysiologiske området for den menneskelige hjerne. Disse 3D-bioprintede cellepopulasjonene viser også uttrykk for modne nevrale celletypemarkører og vekst av neuritt- og astrocytprojeksjoner innen 7 dager etter kultur. Som et resultat er denne modellen egnet for analyse ved hjelp av cellefarger og immunfargingsteknikker sammen med nevrittutvekstanalyser. Evnen til å produsere disse fysiologisk representative modellene i stor skala gjør dem ideelle for bruk i screeninganalyser med middels til høy gjennomstrømning for nevrovitenskapsmål.
Introduction
Forskning på sykdommer i sentralnervesystemet (CNS) i legemiddelforskningsindustrien utvides1. Imidlertid har mange utbredte CNS-sykdommer som epilepsi, schizofreni og Alzheimers sykdom fortsatt ingen kurative behandlinger 2,3,4. Mangelen på effektive terapeutiske midler på tvers av CNS-sykdommer kan, i det minste delvis, tilskrives mangel på nøyaktige in vitro-modeller av hjernen5. Dette har resultert i et translasjonsgap mellom nåværende in vitro-modeller og in vivo-data og en påfølgende flaskehals i forskningsinnsatsen.
Drevet av dette translasjonsgapet har det vært en betydelig økning i utviklingen av nye 3D-cellemodeller de siste årene, inkludert nevrale organoider, nevrosfæroider og stillasbaserte modeller6. 3D-strukturen til disse modellene hjelper til med å rekapitulere det nevrale mikromiljøet, inkludert biomekaniske påkjenninger, cellekontakter og hjernens ekstracellulære matrise (ECM)7. Hjernens ECM er et dynamisk element i nevrofysiologi som opptar mellomrommet mellom nevrale celletyper, inkludert nevroner, astrocytter, oligodendrocytter og den nevrovaskulære enheten7. Rekapitulering av hjernens ECM har vist seg å påvirke nevronal morfologi og nevronavfyring, og mange komplekse 3D-modeller av hjernen har vist avsetning av ECM-proteiner av nevrale celletyper 8,9,10,11. Stillasbaserte modeller består av modne nevrale kokulturer suspendert i en porøs syntetisk eller biologisk hydrogelmatrise som representerer hjernen ECM12. I motsetning til organoide og sfæroide systemer, tillater stillasbaserte 3D-modeller tilpasning av ECM-proteiner som er tilstede og har den ekstra fordelen av tunabilitet av hydrogelstivhet for å etterligne biomekaniske påkjenninger13,14.
Selv om et overveldende flertall av 3D-nevrale modeller viser en økt rekapitulering av hjernens mikromiljø, er ikke alle modeller godt egnet til å implementere legemiddeloppdagelsesapplikasjoner15. For at en 3D-modell skal kunne implementeres i industrielle prosesser, må systemet oppfylle gjennomstrømningskrav for screeningapplikasjoner og ha relativt kort utviklingstid16. 3D Bioprinting er en ny teknologi som gir potensial til å lage 3D-stillasbaserte nevrale modeller med rask utviklingstid, økt gjennomstrømning og høyere nivåer av presisjonskontroll, sammen med fjerning av variabilitet forårsaket av menneskelig feil17. Denne protokollen presenterer en 3D-kokulturmodell av humane iPSC-avledede glutamaterge nevroner og astrocytter i et hydrogelstillas. Dette hydrogelstillaset inneholder fysiologisk representative bioaktive peptider (RGD, IKVAV, YIGSR) og ECM-proteiner innenfor en mimetisk biomekanisk stivhet. Disse ECM-proteinene i full lengde inkluderer laminin-211 i full lengde og hyaluronsyre, rikelig i den humane cortex, med en stivhet på 1,1 kPa i tråd med in vivo-målinger 18. Denne modellen er designet med praktisk for narkotikaforskning, og er opprettet ved hjelp av en 3D-bioprinter i et 96-brønns eller 384-brønns plateformat egnet for screeninganalyse ved hjelp av bildebehandlingsteknikker med cellefarger og antistoffer, sammen med nevrittutvekstanalyser. Celler viser uttrykk for nevrale celletypemarkører og vekst av nevritt- og astrocytiske projeksjoner innen 7 dager etter kultur. Dermed vil denne protokollen presentere metodikken for å utvikle en 3D-nevral kokulturmodell med høy gjennomstrømning for bruk i legemiddeloppdagelsesapplikasjoner.
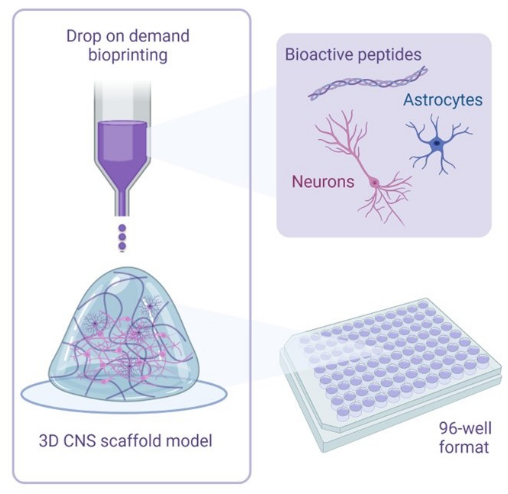
Figur 1: Illustrerende oversikt over metodikk brukt til 3D-bioprint-kokulturer. Humane iPSC-avledede nevroner og astrocytter kombineres med aktivator- og bioblekkløsninger som inneholder bioaktive peptider og bioprintes til hydrogelstillas i 96-brønns eller 384-brønnformater ved hjelp av drop-on-demand bioprintingsteknologi. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Behovet for nøyaktige modeller av CNS har aldri vært høyere, og begrensninger i todimensjonale (2D) tradisjonelle cellekulturmodeller har drevet en generasjon komplekse CNS-modeller de siste årene19. Imidlertid har mange komplekse 3D-modeller som representerer interaksjoner mellom nevrale celletyper og ECM begrensninger som vil forhindre anvendelse av disse modellene i industrielle prosesser 6,20,21. I denne protokollen utvikler vi en 3D-kokulturmodell av humane iPSC-avledede nevroner og astrocytter, som tar sikte på å løse noen av disse begrensningene ved hjelp av 3D bioprinting-teknologi for å skape et bioaktivt hydrogelstillas i 96-brønns og 384-brønnformater.
Metodikken for å utvikle disse modellene har blitt forenklet gjennom programvaren for platekartdesign, automatisk genererte utskriftsprotokoller og veiledet utskriftsprosess fra bioprinteren. På grunn av den følsomme naturen til de følsomme iPSC-avledede celletypene som brukes i denne protokollen, bør det imidlertid utvises forsiktighet med følgende kritiske trinn i tining og kultur. For det første har inkluderingen av ROCK-inhibitor (ROCKi) flere fordeler gjennom bioprintingsprosessen og i tidlig kultur. Celletining er et kritisk punkt der nevronene kan oppleve en stressrespons, og feil tineprotokoller kan redusere sjansene for overlevelse22. Det anbefales vanligvis å tine celler, legge til media og heve celler til inkubatortemperatur så effektivt som mulig23. Under bioprintingsprosessen beskrevet i denne protokollen er det imidlertid nødvendig at nevroner og astrocytter resuspenderes i en aktivatorløsning i stedet for media, og celler vil ikke bli hevet over romtemperatur før slutten av utskriftskjøringen (opptil 30 minutter etter tining). Dermed er tilsetningen av ROCKi til mediet umiddelbart etter tining og inkludert dette under de to sentrifugeringstrinnene (trinn 2.1–2.7 og 1.3.15-1.3.20) avgjørende for å hemme cellespenningsveier, noe som vil resultere i lavere levedyktighetsnivåer24. Videre har ROCKi vist seg å fremme nevrittutvekst og forbedre nevronmodning25. Dermed fortsetter ROCKi-tilskudd i 48 timer etter bioprinting. Det er imidlertid viktig å fjerne ROCKi-tilskudd etter 48 timer for å sikre fullstendig vask under de påfølgende medieendringene før celler brukes til analyse.
Et ytterligere skritt som krever kritisk oppmerksomhet er under post-print media tillegg og medieendringer (trinn 2.8-2.13). Det biotrykte hydrogelstillaset har en ekvivalent biomekanisk stivhet på bare 1,1 kPa, tilsvarende grå substans. Som beskrevet i trinn 2.10 er det avgjørende å pipette forsiktig inn i siden av brønnen under medietilsetning og aspirasjon for å forhindre forstyrrelser. Dette er spesielt relevant for 384-brønnsplater, hvor gelnivået tar opp en høyere andel av totalt brønnvolum. Denne metoden bør også brukes i 2D-kontrollbrønner for å forhindre kantløfting av celler og skjæring av nevrittutvekster. Forfatterne ønsker også å fremheve viktigheten av steril teknikk i bioprinteren, som bør behandles med tilsvarende forsiktighet som et biosikkerhetsskap som brukes til iPSC-avledede cellekulturer. Dette inkluderer steril filtrering av 70 % EtOH og dH2O som brukes i prosedyrene for grønt lys og utskrift, å holde lokk på blekkpatronene og platene mens du beveger hendene inn og ut av bioprinteren, og dekontaminering av overflater inne i bioprinteren med 70 % etanolservietter før og etter utskrift.
Det biotrykte hydrogelstillaset, dannet av bioblekk- og aktivatorløsninger, valgt for å utvikle denne modellen, er valgt fra en rekke bioblekk- og aktivatorløsninger utviklet av Inventia Life Science for bruk i RASTRUM-bioprinteren. Laminin og hyaluronsyre ble identifisert som molekyler av relevans for iPSC-avledet nevronmodning på grunn av deres rolle i aksonal veiledning, synapsedannelse og dannelse av det perinevrale nettet26,27. Videre ble en biomekanisk stivhet på 1,1 kPa valgt, da hydrogeler med lavere tetthet har vist seg å muliggjøre bedre nevrittutvekst fra nevroner12. Hvis det gjøres endringer i protokollen ved å bruke nevroner og astrocytter som har blitt differensiert internt eller fra en annen kommersiell leverandør, vil det bli anbefalt å gjøre en matrisevalgstest for å bestemme det mest støttende hydrogelstillaset15. Videre kan celletetthet også måtte optimaliseres dersom endringer i cellekilder gjøres for å sikre optimal levedyktighet og forhindre hydrogeloverbefolkning. For alle modifikasjoner og feilsøking relatert til bioprinterfunksjonen, anbefaler forfatterne å kontakte produsenter og referere til produsentprotokoller.
CNS inneholder et bredt spekter av nevrale subtyper og gliaceller, som alle eksisterer i forskjellige hjernenisjer og har spesifikke roller som bidrar til nevral funksjon28. Innenfor rammen av dette brede omfanget representerer denne modellen bare de to mest tallrike celletypene (astrocytter og eksitatoriske glutamaterge nevroner). Viktige celletyper som mikroglia, oligodendrocytter og blod-hjernebarrieredannende endotelceller er utelatt fra dette systemet. Inklusjon av mikroglia kan være relevant for fokus på nevroimmune interaksjoner, og oligodendrocytter kan være av interesse ved sykdommer som påvirker sentral myelinisering. I tillegg til deres rolle i patologi, skiller celler som blod-hjernebarrieredannende endotelceller ut legemiddelmetaboliserende enzymer, noe som kan påvirke bruken av denne modellen for farmakokinetiske analyser29. En ytterligere begrensning av modellen kan være forholdet mellom astrocytter og nevroner; Forholdet mellom astrocytter og nevroner varierer sterkt mellom hjernegrupper, med foreslåtte verdier på mellom 1: 1 og 1: 330,31. Denne modellen har et omtrentlig forhold på 1: 1, 5 astrocytter til nevroner; Dermed kan denne modellen ikke være relevant for å modellere hjerneområder der astrocytter er mer rikelig, for eksempel i hvite substansområder30.
Andre protokoller for å utvikle 3D bioprintede kokulturmodeller har blitt publisert de siste årene. En publikasjon av Sullivan et al., 2021, presenterte en 3D bioprintet nevral modell ved bruk av iPSC-avledede nevrale stamceller, som demonstrerer høy levedyktighet etter utskrift og forbedring av nevronfunksjon sammenlignet med 2D-kulturer32. I denne protokollen ble imidlertid nevrale stamceller brukt som cellekilde og ble opprettholdt i kultur i 4 uker. I denne protokollen ble kommersielt tilgjengelige iPSC-avledede glutamaterge nevroner og astrocytter brukt. Dette gjør at et 3D-nettverk av samdyrkede celler kan etableres på så lite som 7 dager; Som demonstrert ved nevrittvekstanalyse, begynner nevrittutvekst innen 24 timer og fortsetter på en lineær måte gjennom hele 156 timers perioden for hvilken cellevekst ble overvåket. Den raske etableringen av disse nettverkene kan delvis tilskrives bruken av glutamatergiske nevroner som bruker optimalisert doksycyklininduserbart genuttrykk av NGN2, som viser uttrykk for modne neuronale subtypemarkører innen 7 dager, selv i 2D-kultur33. Forkortelsen av denne vekstperioden ved hjelp av denne teknikken er viktig for å implementere modeller innen biofarmasøytisk industri, da analyseutvikling krever rask behandlingstid og utvikling av cellemodeller15.
Avslutningsvis viser denne modellen potensial for en 3D-modell av nevroner og astrocytter, som etableres raskt og praktisk for screeningformål. Fremtidige applikasjoner for denne modelltypen kan være for legemiddeloppdagelsesarbeid på tvers av forskjellige CNS-sykdommer, med mulighet til å utvide til forskjellige sykdommer ved hjelp av pasient- eller genredigerte sykdoms-iPSC-linjer. Videre tillater bruken av doksycyklininduserbare NGN2-uttrykk iPSC-avledede glutamatergiske nevroner celler å nå modenhet på kortere tid, noe som kan brukes til å utvikle modeller av den aldrende hjernen for nevrodegenerasjonsforskning. Dette systemet kan også utvides ved bruk av flere celletyper i kokultur, inkludert mikroglia og oligodendrocytter.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne takker Alex Volkerling, Martin Engel og Rachel Bleach for deres hjelp med å utvikle protokollen og tilbakemeldinger på manuskriptet.
Materials
| 2-mercaptoethanol | Thermofisher | 31350010 | |
| 384-well plate | PerkinElmer | 6057300 | |
| 96-well plate | PerkinElmer | 6055300 | |
| Activator fluid F299 | Inventia Life Science | N/A | |
| Activator fluid F3 | Inventia Life Science | N/A | |
| B27 (50x) minus Vit A | Thermofisher | 12587010 | |
| Bioink fluid F261 | Inventia Life Science | N/A | |
| Bioink fluid F32 | Inventia Life Science | N/A | |
| Doxycycline hyclate | Sigma Aldrich | D5207 | |
| GlutaMAX (100x) | Thermofisher | 35050061 | |
| Goat anti-mouse IgG H&L Alexa Fluor 647 | Abcam | ab150115 | |
| Goat anti-rabbit IgG H&L Alexa Fluor 488 | Abcam | ab150077 | |
| Hoechst | Abcam | ab228551 | |
| Human BDNF Recombinant Protein | Thermofisher | PHC7074 | |
| Human NT3 Recombinant Protein | Thermofisher | PHC7036 | |
| iCell Astrocytes | Fujifilm CDI | 1434 | |
| INCell Analyser 6500HS | Molecular Devices | N/A | high content imaging system |
| Incucyte S3 | Sartorius | N/A | |
| ioGlutamatergic Neurons (Large vial) | Bit.bio | e001 | |
| Laminin (1 mg/mL) | Sigma Aldrich | L2020 | |
| Live/dead kit (Calcein-AM, Ethidium homo-dimer-1) | Invitrogen | L3224 | |
| Mouse anti-BIII tubulin NL637 conjugated | R&D systems | SC024 | |
| Neurobasal media | Thermofisher | 21103049 | |
| Normal Donkey Serum | Abcam | ab7475 | |
| NucBlue Live (Hoechst 33342) | Thermofisher | R37605 | |
| Opti-MEM | Thermofisher | 11058021 | |
| Paraformaldehyde | Sigma Aldrich | P6148 | |
| PEI 50% in H2O | Sigma Aldrich | 181978 | |
| Pierce Borate Buffer 20x | Thermofisher | 28341 | |
| Prism | GraphPad | Data analysis software | |
| Rabbit anti-ionotropic glutamatre receptor 2 (GluR2) | Abcam | ab206293 | |
| RASTRUM(TM) Bioprinter | Inventia Life Science | N/A | Bioprinter |
| RASTRUM(TM) Bioprinter Cartridges | Inventia Life Science | N/A | Bioprinter Cartridges |
| RASTRUM(TM) Targeting plate | Inventia Life Science | N/A | Targeting plate |
| Rho kinase (ROCK) inhibitor | Abcam | ab120129 | |
| Sheep anti-GFAP NL493 conjugated | R&D systems | SC024 | |
| Signals Image Artist | PerkinElmer | N/A | Image analysis platform |
| Triton X-100 | Thermofisher | HFH10 | |
| Zeiss Axio Observer | Zeiss | N/A | Inverted microscope platform |
References
- Jung, Y. L., Hwang, J., Yoo, H. S. Disease burden metrics the innovations of leading pharmaceutical companies: a global and regional comparative study. Globalization and Health. 16 (1), 80-80 (2020).
- Potkin, S. G., et al. The neurobiology of treatment-resistant schizophrenia: paths to antipsychotic resistance and a roadmap for future research. npj Schizophrenia. 6, 1 (2020).
- Zahra, W., et al., Keswani, C., et al. The Global Economic Impact of Neurodegenerative Diseases: Opportunities and Challenges. Bioeconomy for Sustainable Development. , (2019).
- Perucca, E. The pharmacological treatment of epilepsy: recent advances and future perspectives. Acta Epileptologica. 3 (1), 22 (2021).
- Nikolakopoulou, P., et al. Recent progress in translational engineered in vitro models of the central nervous system. Brain. 143 (11), 3181-3213 (2020).
- Whitehouse, C., Corbett, N., Brownlees, J. 3D models of neurodegeneration: implementation in drug discovery. Trends in Pharmacological Sciences. 44 (4), 208-221 (2023).
- Rauti, R., Renous, N., Maoz, B. M. Mimicking the brain extracellular matrix in vitro: A review of current methodologies and challenges. Israel Journal of Chemistry. 60 (12), 1141-1151 (2020).
- Fawcett, J. W., Oohashi, T., Pizzorusso, T. The roles of perineuronal nets and the perinodal extracellular matrix in neuronal function. Nature Reviews Neuroscience. 20 (8), 451-465 (2019).
- Lam, D., et al. Tissue-specific extracellular matrix accelerates the formation of neural networks and communities in a neuron-glia co-culture on a multi-electrode array. Scientific Reports. 9, 4159 (2019).
- Roll, L., Lessmann, K., Brüstle, O., Faissner, A. Cerebral organoids maintain the expression of neural stem cell-associated glycoepitopes and extracellular matrix. Cells. 11 (5), 760 (2022).
- Yan, Y., Bejoy, J., Marzano, M., Li, Y. The use of pluripotent stem cell-derived organoids to study extracellular matrix development during neural degeneration. Cells. 8 (3), 242 (2019).
- Ma, L., et al. 3D bioprinted hyaluronic acid-based cell-laden scaffold for brain microenvironment simulation. Bio-Design and Manufacturing. 3 (3), 164-174 (2020).
- Liaw, C. -. Y., Ji, S., Guvendiren, M. Engineering 3D hydrogels for personalized in vitro human tissue models. Advanced Healthcare Materials. 7 (4), 1701165 (2018).
- Ma, J., Huang, C. Composition and mechanism of three-dimensional hydrogel system in regulating stem cell fate. Tissue Engineering Part B: Reviews. 26 (6), 498-518 (2020).
- Belfiore, L., et al. Generation and analysis of 3D cell culture models for drug discovery. European Journal of Pharmaceutical Sciences. 163, 105876 (2021).
- Langhans, S. A. Three-dimensional in vitro cell culture models in drug discovery and drug repositioning. Frontiers in Pharmacology. 9, 6 (2018).
- Engel, M., Belfiore, L., Aghaei, B., Sutija, M. Enabling high throughput drug discovery in 3D cell cultures through a novel bioprinting workflow. SLAS Technology. 27 (1), 32-38 (2022).
- Takamura, T., et al. Influence of age on global and regional brain stiffness in young and middle-aged adults. Journal of Magnetic Resonance Imaging. 51 (3), 727-733 (2020).
- Slanzi, A., Iannoto, G., Rossi, B., Zenaro, E., Constantin, G. In vitro models of neurodegenerative diseases. Frontiers in Cell and Developmental Biology. 8, 328 (2020).
- de Souza, N. Organoid variability examined. Nature Methods. 14 (7), 655-655 (2017).
- Hernández, D., et al. Culture variabilities of human iPSC-derived cerebral organoids are a major issue for the modelling of phenotypes observed in Alzheimer’s disease. Stem Cell Review and Reports. 18 (2), 718-731 (2022).
- Li, R., et al. Differentiation of human iPS cells into sensory neurons exhibits developmental stage-specific cryopreservation challenges. Frontiers in Cell and Developmental Biology. 9, 796960 (2021).
- Nishiyama, Y., et al. Safe and efficient method for cryopreservation of human induced pluripotent stem cell-derived neural stem and progenitor cells by a programmed freezer with a magnetic field. Neuroscience Research. 107, 20-29 (2016).
- Uhrig, M., Ezquer, F., Ezquer, M. Improving cell recovery: Freezing and thawing optimization of induced pluripotent stem cells. Cells. 11 (5), 799 (2022).
- Harbom, L. J., et al. The effect of rho kinase inhibition on morphological and electrophysiological maturity in iPSC-derived neurons. Cell and Tissue Research. 375 (3), 641-654 (2019).
- Koh, H. S., Yong, T., Chan, C. K., Ramakrishna, S. Enhancement of neurite outgrowth using nano-structured scaffolds coupled with laminin. Biomaterials. 29 (26), 3574-3582 (2008).
- Tarus, D., et al. Design of hyaluronic acid hydrogels to promote neurite outgrowth in three dimensions. ACS Applied Materials & Interfaces. 8 (38), 25051-25059 (2016).
- Brain Initiative Cell Census Network (BICCN). Initiative Cell Census Network (BICCN). A multimodal cell census and atlas of the mammalian primary motor cortex. Nature. 598 (7879), 86-102 (2021).
- Dauchy, S., et al. Expression and transcriptional regulation of ABC transporters and cytochromes P450 in hCMEC/D3 human cerebral microvascular endothelial cells. Biochemical Pharmacology. 77 (5), 897-909 (2009).
- Herculano-Houzel, S. The glia/neuron ratio: How it varies uniformly across brain structures and species and what that means for brain physiology and evolution. Glia. 62 (9), 1377-1391 (2014).
- von Bartheld, C. S., Bahney, J., Herculano-Houzel, S. The search for true numbers of neurons and glial cells in the human brain: A review of 150 years of cell counting. The Journal of Comparative Neurology. 524 (18), 3865-3895 (2016).
- Sullivan, M. A., et al. 3D bioprinting of stem cell-derived central nervous system cells enables astrocyte growth, vasculogenesis and enhances neural differentiation/function. bioRxiv. , (2022).
- Pawlowski, M., et al. Inducible and deterministic forward programming of human pluripotent stem cells into neurons, skeletal myocytes, and oligodendrocytes. Stem Cell Reports. 8 (4), 803-812 (2017).

