Tredimensionell bioprintning av humana iPSC-härledda neuron-astrocyt-samkulturer för screeningapplikationer
Summary
Här presenterar vi ett protokoll för att producera 3D-bioprintade samkulturer av iPSC-härledda neuroner och astrocyter. Denna samodlingsmodell, genererad i en hydrogelställning i 96- eller 384-brunnsformat, visar hög post-print-viabilitet och neuritutväxt inom 7 dagar och visar uttrycket av mognadsmarkörer för båda celltyperna.
Abstract
För att en cellmodell ska vara användbar för läkemedelsscreening måste systemet uppfylla kraven på genomströmning och homogenitet samtidigt som det har en effektiv utvecklingstid. Många publicerade 3D-modeller uppfyller dock inte dessa kriterier. Detta begränsar därför deras användbarhet i tidiga läkemedelsupptäcktstillämpningar. Tredimensionell (3D) bioprinting är en ny teknik som kan tillämpas på utvecklingen av 3D-modeller för att påskynda utvecklingstiden, öka standardiseringen och öka genomströmningen. Här presenterar vi ett protokoll för att utveckla 3D-bioprintade samodlingsmodeller av humant inducerade pluripotenta stamceller (iPSC)-härledda glutamatergiska neuroner och astrocyter. Dessa samkulturer är inbäddade i en hydrogelmatris av bioaktiva peptider, fullängds extracellulär matris (ECM) proteiner och med en fysiologisk styvhet på 1,1 kPa. Modellen kan snabbt etableras i format med 96 brunnar och 384 brunnar och ger en genomsnittlig post-print-viabilitet på 72 %. Förhållandet mellan astrocyter och neuroner i denna modell visar sig vara 1:1,5, vilket ligger inom det fysiologiska intervallet för den mänskliga hjärnan. Dessa 3D-bioprintade cellpopulationer visar också uttryck av mogna neurala celltypsmarkörer och tillväxt av neurit- och astrocytprojektioner inom 7 dagar efter odling. Som ett resultat är denna modell lämplig för analys med hjälp av cellfärgämnen och immunfärgningstekniker tillsammans med neuritutväxtanalyser. Förmågan att producera dessa fysiologiskt representativa modeller i stor skala gör dem idealiska för användning i screeninganalyser med medelhög till hög genomströmning för neurovetenskapliga mål.
Introduction
Forskningen om sjukdomar i centrala nervsystemet (CNS) inom läkemedelsindustrin expanderar1. Men många vanliga CNS-sjukdomar som epilepsi, schizofreni och Alzheimers sjukdom har fortfarande inga botande behandlingar 2,3,4. Bristen på effektiva terapier för CNS-sjukdomar kan, åtminstone delvis, tillskrivas bristen på exakta in vitro-modeller av hjärnan5. Detta har resulterat i en translationell klyfta mellan nuvarande in vitro-modeller och in vivo-data och en efterföljande flaskhals i forskningsinsatserna.
Drivet av detta translationella gap har det skett en betydande ökning av utvecklingen av nya 3D-cellmodeller under de senaste åren, inklusive neurala organoider, neurosfäroider och ställningsbaserade modeller6. 3D-strukturen i dessa modeller hjälper till att rekapitulera den neurala mikromiljön, inklusive biomekaniska påfrestningar, cell-cellkontakter och hjärnans extracellulära matris (ECM)7. Hjärnans ECM är ett dynamiskt element i neurofysiologin som upptar utrymmet mellan neurala celltyper, inklusive neuroner, astrocyter, oligodendrocyter och den neurovaskulära enheten7. Rekapitulation av hjärnans ECM har visat sig påverka neuronal morfologi och neuronal avfyrning, och många komplexa 3D-modeller av hjärnan har visat avsättning av ECM-proteiner av neurala celltyper 8,9,10,11. Ställningsbaserade modeller består av mogna neurala samkulturer suspenderade i en porös syntetisk eller biologisk hydrogelmatris som representerar hjärnans ECM12. Till skillnad från organoid- och sfäroidsystem tillåter ställningsbaserade 3D-modeller anpassning av närvarande ECM-proteiner och har den extra fördelen att hydrogelstyvheten kan justeras för att efterlikna biomekaniska spänningar13,14.
Även om en överväldigande majoritet av 3D-neurala modeller visar en ökad rekapitulation av hjärnans mikromiljö, är inte alla modeller väl lämpade för att implementera applikationer för läkemedelsupptäckt15. För att en 3D-modell ska kunna implementeras i industriella processer måste systemet uppfylla genomströmningskraven för screeningapplikationer och ha en relativt kort utvecklingstid16. 3D-bioprinting är en ny teknik som erbjuder potential att skapa 3D-stödbaserade neurala modeller med snabb utvecklingstid, ökad genomströmning och högre nivåer av precisionskontroll, tillsammans med avlägsnande av variabilitet orsakad av mänskliga fel17. Detta protokoll presenterar en 3D-samodlingsmodell av humana iPSC-härledda glutamaterga neuroner och astrocyter i en hydrogelställning. Denna hydrogelställning innehåller fysiologiskt representativa bioaktiva peptider (RGD, IKVAV, YIGSR) och ECM-proteiner inom en mimetisk biomekanisk styvhet. Dessa fullängds ECM-proteiner inkluderar fullängdslambinin-211 och hyaluronsyra, som finns rikligt i den mänskliga hjärnbarken, med en styvhet på 1,1 kPa i linje med in vivo-mätningar 18. Denna modell är utformad med praktiska egenskaper för läkemedelsupptäckt och skapas med hjälp av en 3D-bioprinter i ett 96-brunnars eller 384-håls plattformat som är lämpligt för screeninganalys med hjälp av avbildningstekniker med cellfärgämnen och antikroppar, tillsammans med neuritutväxtanalyser. Cellerna visar uttryck av neurala celltypsmarkörer och tillväxt av neurit- och astrocytiska projektioner inom 7 dagar efter odling. Således kommer detta protokoll att presentera metodiken för att utveckla en 3D-modell för neural samkultur med hög genomströmning för användning i läkemedelsupptäcktsapplikationer.
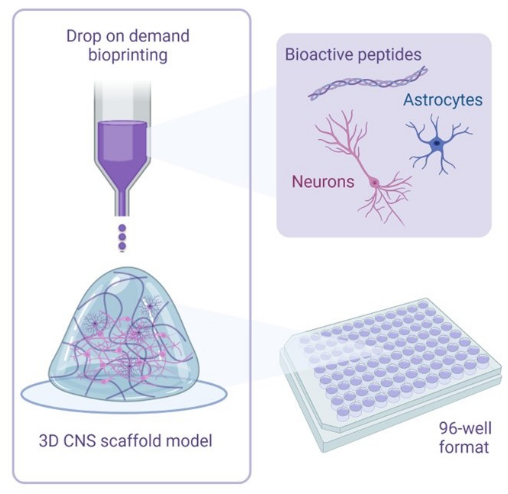
Figur 1: Illustrativ översikt över den metod som används för att 3D-bioprinta samkulturer. Humana iPSC-härledda neuroner och astrocyter kombineras med aktivator- och biobläcklösningar som innehåller bioaktiva peptider och bioprintas till hydrogelställningar i 96-brunnars eller 384-brunnars format med hjälp av drop-on-demand bioprintningsteknik. Klicka här för att se en större version av denna figur.
Protocol
Representative Results
Discussion
Behovet av noggranna modeller av CNS har aldrig varit större, och begränsningar hos tvådimensionella (2D) traditionella cellodlingsmodeller har drivit en generation av komplexa CNS-modeller under de senaste åren19. Många komplexa 3D-modeller som representerar interaktioner mellan neurala celltyper och ECM har dock begränsningar som skulle förhindra tillämpningen av dessa modeller i industriella processer 6,20,21. I detta protokoll utvecklar vi en 3D-samodlingsmodell av humana iPSC-härledda neuroner och astrocyter, som syftar till att lösa några av dessa begränsningar med hjälp av 3D-bioprintningsteknik för att skapa en bioaktiv hydrogelställning i 96-brunnars och 384-brunnars format.
Metodiken för att utveckla dessa modeller har förenklats genom programvaran för design av plåtkartor, automatiskt genererade utskriftsprotokoll och guidad utskriftsprocess från bioprintern. På grund av den känsliga karaktären hos de känsliga iPSC-härledda celltyperna som används i detta protokoll bör dock följande kritiska steg vid upptining och odling vara försiktiga. För det första har införandet av ROCK-hämmare (ROCKi) flera fördelar under hela bioprintningsprocessen och under tidig odling. Cellupptining är en kritisk punkt där neuronerna kan uppleva en stressreaktion, och felaktiga upptiningsprotokoll kan minska chanserna att överleva22. Det rekommenderas vanligtvis att tina celler, tillsätta media och höja cellerna till inkubatortemperatur så effektivt som möjligt23. Under bioprintningsprocessen som beskrivs i detta protokoll är det dock nödvändigt att neuroner och astrocyter återsuspenderas i en aktivatorlösning snarare än media, och cellerna kommer inte att höjas över rumstemperatur förrän i slutet av utskriftskörningen (upp till 30 minuter efter upptining). Således är det absolut nödvändigt att tillsätta ROCKi till mediet omedelbart efter upptining och inkludera detta under de två centrifugeringsstegen (steg 2.1–2.7 och 1.3.15-1.3.20) för att hämma cellstressvägar, vilket skulle resultera i lägre viabilitetsnivåer24. Dessutom har ROCKi visat sig främja neuritutväxt och förbättra neuronal mognad25. Således fortsätter ROCKi-tillskott i 48 timmar efter bioprintning. Det är dock absolut nödvändigt att ta bort ROCKi-tillskott efter 48 timmar för att säkerställa fullständig tvättning under de efterföljande mediebytena innan cellerna används för analys.
Ytterligare ett steg som kräver kritisk uppmärksamhet är vid tillägg av media efter utskrift och byte av media (steg 2.8-2.13). Den bioprintade hydrogelställningen har en motsvarande biomekanisk styvhet på endast 1,1 kPa, vilket motsvarar grå substans. Som beskrivs i steg 2.10 är det viktigt att pipettera försiktigt in i sidan av brunnen under mediatillsats och aspiration för att förhindra störningar. Detta är särskilt relevant för 384-brunnars plattor, där gelnivån tar upp en högre andel av den totala brunnsvolymen. Denna metod bör också användas i 2D-kontrollbrunnar för att förhindra kantlyft av celler och skjuvning av neuritutväxter. Författarna vill också belysa vikten av steril teknik inom bioprintern, som bör behandlas med samma försiktighet som ett biosäkerhetsskåp som används för iPSC-härledda cellkulturer. Detta inkluderar steril filtrering av 70 % EtOH och dH2O som används vid greenlighting och utskrift, att hålla lock på patronerna och plattorna medan du flyttar händerna in och ut ur bioprintern och att dekontaminera ytorna inuti bioprintern med 70 % etanolservetter före och efter utskrift.
Den bioprintade hydrogelställningen, bildad av biobläck och aktivatorlösningar, som valts ut för att utveckla denna modell är utvald från en rad biobläck och aktivatorlösningar som utvecklats av Inventia Life Science för användning i bioprintern RATRUM. Laminin och hyaluronsyra identifierades som molekyler av relevans för iPSC-härledd neuronal mognad på grund av deras roll i axonal vägledning, synapsbildning och bildning av det perineuronala nätet26,27. Dessutom valdes en biomekanisk styvhet på 1,1 kPa, eftersom hydrogeler med lägre densitet har visat sig möjliggöra bättre neuritutväxt från neuroner12. Om ändringar görs i protokollet genom att använda neuroner och astrocyter som har differentierats internt eller från en annan kommersiell leverantör, rekommenderas att göra ett matrisurvalstest för att bestämma den mest stödjande hydrogelställningen15. Dessutom kan celldensiteten också behöva optimeras om förändringar av cellkällor görs för att säkerställa optimal livskraft och förhindra överbeläggning av hydrogeler. För alla modifieringar och felsökningar relaterade till bioprinterfunktionen rekommenderar författarna att man kontaktar tillverkare och hänvisar till tillverkarprotokoll.
CNS innehåller ett brett spektrum av neuronala subtyper och gliaceller, som alla finns i olika hjärnnischer och har specifika roller som bidrar till neural funktion28. Inom ramen för detta breda omfång representerar denna modell endast de två vanligaste celltyperna (astrocyter och excitatoriska glutamaterga neuroner). Viktiga celltyper som mikroglia, oligodendrocyter och blod-hjärnbarriärbildande endotelceller utelämnas från detta system. Inkludering av mikroglia kan vara av relevans i fokus på neuroimmuna interaktioner, och oligodendrocyter kan vara av intresse för sjukdomar som påverkar central myelinisering. Förutom sin roll i patologi utsöndrar celler såsom blod-hjärnbarriärbildande endotelceller läkemedelsmetaboliserande enzymer, vilket kan påverka användningen av denna modell för farmakokinetiska analyser29. En ytterligare begränsning i modellen kan vara förhållandet mellan astrocyter och neuroner; Förhållandet mellan astrocyter och neuroner varierar kraftigt mellan hjärnregioner, med föreslagna värden mellan 1:1 och 1:330,31. Denna modell har ett ungefärligt förhållande på 1:1,5 astrocyter till neuroner; Därför kanske denna modell inte är relevant för att modellera hjärnområden där astrocyter är vanligare, till exempel i områden med vit substans30.
Andra protokoll för att utveckla 3D-bioprintade samkulturmodeller har publicerats under de senaste åren. En publikation av Sullivan et al., 2021, presenterade en 3D-bioprintad neural modell med hjälp av iPSC-härledda neurala stamceller, som visar hög post-print-viabilitet och förbättring av neuronal funktion jämfört med 2D-kulturer32. I detta protokoll användes dock neurala stamceller som cellkälla och hölls i odling i 4 veckor. I detta protokoll användes kommersiellt tillgängliga iPSC-härledda glutamaterga neuroner och astrocyter. Detta gör det möjligt att etablera ett 3D-nätverk av samodlade celler på så lite som 7 dagar; Som framgår av neurittillväxtanalys börjar neuritutväxten inom 24 timmar och fortsätter på ett linjärt sätt under hela den 156-timmarsperiod för vilken celltillväxten övervakades. Den snabba etableringen av dessa nätverk kan delvis tillskrivas användningen av glutamaterga neuroner som använder optimerat doxycyklininducerbart genuttryck av NGN2, som visar uttryck av mogna neuronala subtypmarkörer inom 7 dagar, även i 2D-kultur33. Förkortningen av denna tillväxtperiod med hjälp av denna teknik är viktig för att implementera modeller inom den biofarmaceutiska industrin, eftersom analysutveckling kräver snabb vändning och utveckling av cellmodeller15.
Sammanfattningsvis visar denna modell potential för en 3D-modell av neuroner och astrocyter, som etableras snabbt och bekvämt för screeningändamål. Framtida tillämpningar för denna modelltyp kan vara för läkemedelsutveckling inom olika CNS-sjukdomar, med möjlighet att expandera till olika sjukdomar med hjälp av patient- eller genredigerade sjukdoms-iPSC-linjer. Dessutom gör användningen av doxycyklininducerbara NGN2-uttryck iPSC-härledda glutamaterga neuroner det möjligt för celler att nå mognad på kortare tid, vilket kan användas för att utveckla modeller av den åldrande hjärnan för neurodegenerationsforskning. Detta system skulle också kunna utvidgas genom användning av ytterligare celltyper i samodling, inklusive mikroglia och oligodendrocyter.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna vill tacka Alex Volkerling, Martin Engel och Rachel Bleach för deras hjälp med att utveckla protokollet och återkopplingen på manuskriptet.
Materials
| 2-mercaptoethanol | Thermofisher | 31350010 | |
| 384-well plate | PerkinElmer | 6057300 | |
| 96-well plate | PerkinElmer | 6055300 | |
| Activator fluid F299 | Inventia Life Science | N/A | |
| Activator fluid F3 | Inventia Life Science | N/A | |
| B27 (50x) minus Vit A | Thermofisher | 12587010 | |
| Bioink fluid F261 | Inventia Life Science | N/A | |
| Bioink fluid F32 | Inventia Life Science | N/A | |
| Doxycycline hyclate | Sigma Aldrich | D5207 | |
| GlutaMAX (100x) | Thermofisher | 35050061 | |
| Goat anti-mouse IgG H&L Alexa Fluor 647 | Abcam | ab150115 | |
| Goat anti-rabbit IgG H&L Alexa Fluor 488 | Abcam | ab150077 | |
| Hoechst | Abcam | ab228551 | |
| Human BDNF Recombinant Protein | Thermofisher | PHC7074 | |
| Human NT3 Recombinant Protein | Thermofisher | PHC7036 | |
| iCell Astrocytes | Fujifilm CDI | 1434 | |
| INCell Analyser 6500HS | Molecular Devices | N/A | high content imaging system |
| Incucyte S3 | Sartorius | N/A | |
| ioGlutamatergic Neurons (Large vial) | Bit.bio | e001 | |
| Laminin (1 mg/mL) | Sigma Aldrich | L2020 | |
| Live/dead kit (Calcein-AM, Ethidium homo-dimer-1) | Invitrogen | L3224 | |
| Mouse anti-BIII tubulin NL637 conjugated | R&D systems | SC024 | |
| Neurobasal media | Thermofisher | 21103049 | |
| Normal Donkey Serum | Abcam | ab7475 | |
| NucBlue Live (Hoechst 33342) | Thermofisher | R37605 | |
| Opti-MEM | Thermofisher | 11058021 | |
| Paraformaldehyde | Sigma Aldrich | P6148 | |
| PEI 50% in H2O | Sigma Aldrich | 181978 | |
| Pierce Borate Buffer 20x | Thermofisher | 28341 | |
| Prism | GraphPad | Data analysis software | |
| Rabbit anti-ionotropic glutamatre receptor 2 (GluR2) | Abcam | ab206293 | |
| RASTRUM(TM) Bioprinter | Inventia Life Science | N/A | Bioprinter |
| RASTRUM(TM) Bioprinter Cartridges | Inventia Life Science | N/A | Bioprinter Cartridges |
| RASTRUM(TM) Targeting plate | Inventia Life Science | N/A | Targeting plate |
| Rho kinase (ROCK) inhibitor | Abcam | ab120129 | |
| Sheep anti-GFAP NL493 conjugated | R&D systems | SC024 | |
| Signals Image Artist | PerkinElmer | N/A | Image analysis platform |
| Triton X-100 | Thermofisher | HFH10 | |
| Zeiss Axio Observer | Zeiss | N/A | Inverted microscope platform |
References
- Jung, Y. L., Hwang, J., Yoo, H. S. Disease burden metrics the innovations of leading pharmaceutical companies: a global and regional comparative study. Globalization and Health. 16 (1), 80-80 (2020).
- Potkin, S. G., et al. The neurobiology of treatment-resistant schizophrenia: paths to antipsychotic resistance and a roadmap for future research. npj Schizophrenia. 6, 1 (2020).
- Zahra, W., et al., Keswani, C., et al. The Global Economic Impact of Neurodegenerative Diseases: Opportunities and Challenges. Bioeconomy for Sustainable Development. , (2019).
- Perucca, E. The pharmacological treatment of epilepsy: recent advances and future perspectives. Acta Epileptologica. 3 (1), 22 (2021).
- Nikolakopoulou, P., et al. Recent progress in translational engineered in vitro models of the central nervous system. Brain. 143 (11), 3181-3213 (2020).
- Whitehouse, C., Corbett, N., Brownlees, J. 3D models of neurodegeneration: implementation in drug discovery. Trends in Pharmacological Sciences. 44 (4), 208-221 (2023).
- Rauti, R., Renous, N., Maoz, B. M. Mimicking the brain extracellular matrix in vitro: A review of current methodologies and challenges. Israel Journal of Chemistry. 60 (12), 1141-1151 (2020).
- Fawcett, J. W., Oohashi, T., Pizzorusso, T. The roles of perineuronal nets and the perinodal extracellular matrix in neuronal function. Nature Reviews Neuroscience. 20 (8), 451-465 (2019).
- Lam, D., et al. Tissue-specific extracellular matrix accelerates the formation of neural networks and communities in a neuron-glia co-culture on a multi-electrode array. Scientific Reports. 9, 4159 (2019).
- Roll, L., Lessmann, K., Brüstle, O., Faissner, A. Cerebral organoids maintain the expression of neural stem cell-associated glycoepitopes and extracellular matrix. Cells. 11 (5), 760 (2022).
- Yan, Y., Bejoy, J., Marzano, M., Li, Y. The use of pluripotent stem cell-derived organoids to study extracellular matrix development during neural degeneration. Cells. 8 (3), 242 (2019).
- Ma, L., et al. 3D bioprinted hyaluronic acid-based cell-laden scaffold for brain microenvironment simulation. Bio-Design and Manufacturing. 3 (3), 164-174 (2020).
- Liaw, C. -. Y., Ji, S., Guvendiren, M. Engineering 3D hydrogels for personalized in vitro human tissue models. Advanced Healthcare Materials. 7 (4), 1701165 (2018).
- Ma, J., Huang, C. Composition and mechanism of three-dimensional hydrogel system in regulating stem cell fate. Tissue Engineering Part B: Reviews. 26 (6), 498-518 (2020).
- Belfiore, L., et al. Generation and analysis of 3D cell culture models for drug discovery. European Journal of Pharmaceutical Sciences. 163, 105876 (2021).
- Langhans, S. A. Three-dimensional in vitro cell culture models in drug discovery and drug repositioning. Frontiers in Pharmacology. 9, 6 (2018).
- Engel, M., Belfiore, L., Aghaei, B., Sutija, M. Enabling high throughput drug discovery in 3D cell cultures through a novel bioprinting workflow. SLAS Technology. 27 (1), 32-38 (2022).
- Takamura, T., et al. Influence of age on global and regional brain stiffness in young and middle-aged adults. Journal of Magnetic Resonance Imaging. 51 (3), 727-733 (2020).
- Slanzi, A., Iannoto, G., Rossi, B., Zenaro, E., Constantin, G. In vitro models of neurodegenerative diseases. Frontiers in Cell and Developmental Biology. 8, 328 (2020).
- de Souza, N. Organoid variability examined. Nature Methods. 14 (7), 655-655 (2017).
- Hernández, D., et al. Culture variabilities of human iPSC-derived cerebral organoids are a major issue for the modelling of phenotypes observed in Alzheimer’s disease. Stem Cell Review and Reports. 18 (2), 718-731 (2022).
- Li, R., et al. Differentiation of human iPS cells into sensory neurons exhibits developmental stage-specific cryopreservation challenges. Frontiers in Cell and Developmental Biology. 9, 796960 (2021).
- Nishiyama, Y., et al. Safe and efficient method for cryopreservation of human induced pluripotent stem cell-derived neural stem and progenitor cells by a programmed freezer with a magnetic field. Neuroscience Research. 107, 20-29 (2016).
- Uhrig, M., Ezquer, F., Ezquer, M. Improving cell recovery: Freezing and thawing optimization of induced pluripotent stem cells. Cells. 11 (5), 799 (2022).
- Harbom, L. J., et al. The effect of rho kinase inhibition on morphological and electrophysiological maturity in iPSC-derived neurons. Cell and Tissue Research. 375 (3), 641-654 (2019).
- Koh, H. S., Yong, T., Chan, C. K., Ramakrishna, S. Enhancement of neurite outgrowth using nano-structured scaffolds coupled with laminin. Biomaterials. 29 (26), 3574-3582 (2008).
- Tarus, D., et al. Design of hyaluronic acid hydrogels to promote neurite outgrowth in three dimensions. ACS Applied Materials & Interfaces. 8 (38), 25051-25059 (2016).
- Brain Initiative Cell Census Network (BICCN). Initiative Cell Census Network (BICCN). A multimodal cell census and atlas of the mammalian primary motor cortex. Nature. 598 (7879), 86-102 (2021).
- Dauchy, S., et al. Expression and transcriptional regulation of ABC transporters and cytochromes P450 in hCMEC/D3 human cerebral microvascular endothelial cells. Biochemical Pharmacology. 77 (5), 897-909 (2009).
- Herculano-Houzel, S. The glia/neuron ratio: How it varies uniformly across brain structures and species and what that means for brain physiology and evolution. Glia. 62 (9), 1377-1391 (2014).
- von Bartheld, C. S., Bahney, J., Herculano-Houzel, S. The search for true numbers of neurons and glial cells in the human brain: A review of 150 years of cell counting. The Journal of Comparative Neurology. 524 (18), 3865-3895 (2016).
- Sullivan, M. A., et al. 3D bioprinting of stem cell-derived central nervous system cells enables astrocyte growth, vasculogenesis and enhances neural differentiation/function. bioRxiv. , (2022).
- Pawlowski, M., et al. Inducible and deterministic forward programming of human pluripotent stem cells into neurons, skeletal myocytes, and oligodendrocytes. Stem Cell Reports. 8 (4), 803-812 (2017).

