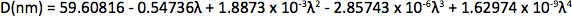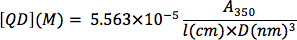Kompakte kvanteprikker for Single-molekylet Imaging
Summary
Vi beskriver fremstillingen av kolloidale kvanteprikker med minimert hydrodynamisk størrelse for single-molekyl fluorescens imaging. Sammenlignet med konvensjonelle kvanteprikker, disse nanopartiklene er omtrent samme størrelse som globular proteiner og er optimalisert for single-molekyl lysstyrke, stabilitet mot fotonedbrytning, og motstand mot uspesifikke binding til proteiner og celler.
Abstract
Enkelt-molekyl imaging er et viktig verktøy for å forstå mekanismene for biomolekylære funksjon og for å visualisere romlige og tidsmessige heterogenitet av molekylære atferd som ligger til grunn cellebiologi 1-4. Å image en enkelt molekyl av interesse, er det vanligvis konjugert til en fluoriserende tag (fargestoff, protein, perle, eller quantum prikk) og observert med epifluorescence eller total intern refleksjon fluorescens (TIRF) mikroskopi. Mens fargestoffer og fluorescerende proteiner har vært bærebjelken i fluorescens bildebehandling i flere tiår, er deres fluorescens ustabil under høye foton flukser er nødvendige for å observere individuelle molekyler, gir bare noen få sekunder av observasjon før fullstendig tap av signal. Lateksperler og dye-merkede perler gir forbedret signal stabilitet, men på bekostning av drastisk større hydrodynamisk størrelse, som kan skadelig endre diffusjon og oppførselen til molekylet under studien.
ntent "> Quantum prikker (QDs) tilbyr en balanse mellom disse to problematiske regimer. Disse nanopartikler består av halvledermaterialer, og kan være konstruert med en hydrodynamisk kompakt størrelse med eksepsjonell motstand mot fotonedbrytning 5. Dermed siste årene QDs har vært medvirkende i slik langsiktig observasjon av komplekse macromolecular oppførsel på ett molekyl-nivå. Men disse partiklene har likevel blitt funnet å utvise nedsatt diffusjon i overfylte molekylære miljøer som mobilnettet cytoplasma og nevrale synaptiske spalten, der deres størrelser er fortsatt for stor 4,6 , 7.Nylig har vi utviklet kjernene og overflatebelegg av QDs for minimal hydrodynamisk størrelse, mens balansere forskyvninger til kolloidal stabilitet, fotostabilitet, lysstyrke og uspesifikke binding som har hindret nytten av kompakte QDs i det siste 8,9. Målet med denne artikkelen er å visesyntesen, modifikasjon og karakterisering av disse optimaliserte nanokrystaller, sammensatt av et legert Hg x CD 1-x Se kjerne belagt med et isolerende Cd y Zn 1-y S skall, videre belagt med en polymer multidentate ligand modifisert med korte polyetylenglykol ( PEG) kjeder (figur 1). Sammenlignet med konvensjonelle CdSe nanokrystaller, Hg x CD 1-x Sé legeringer tilby større quantum utbytter av fluorescens, fluorescens på rødt og nær-infrarøde bølgelengder for forbedret signal-til-støy i celler, og eksitasjon på ikke-cytotoksiske synlige bølgelengder. Multidentate polymer belegg binder seg til nanocrystal overflaten i en lukket og flat konformasjon å minimere hydrodynamisk størrelse, og PEG nøytraliserer overflateladning for å minimere ikke-spesifikke binding til celler og biomolekyler. Sluttresultatet er en lyst fluorescerende nanocrystal med utslipp mellom 550-800 nm og en total hydrodynamisk størrelse nær 12 nm. Dette er i same størrelsesområdet så mange løselig globular proteiner i celler, og betydelig mindre enn konvensjonelle pegylert QDs (25-35 nm).
Protocol
Representative Results
Discussion
Sammenlignet med konvensjonelle CdSe kvanteprikker, kan trefoldig legering Hg x CD 1-x SE nanokrystaller være innstilt på størrelse og fluorescens bølgelengde uavhengig. Størrelsen er første valgt under syntesen av CdSe nanocrystal kjerner, og fluorescensen bølgelengden er valgt på en sekundær kvikksølv kationebytter steg, som ikke i vesentlig grad endre nanocrystal størrelse 9. Det er viktig å tillate det rensede Hg x CD 1-x Sé nanokrystaller inkubere ved romtemp…
Declarações
The authors have nothing to disclose.
Acknowledgements
Forfatterne ønsker å takke dr. Hong Yi ved Emory University Integrert Mikroskopi Kjerne for elektronmikroskopi imaging. Dette arbeidet ble sponset av NIH tilskudd (PN2EY018244, R01 CA108468, U54CA119338, og 1K99CA154006-01).
Materials
| Name of the reagent | Company | Catalogue number | Comments (optional) |
| Selenium | Sigma-Aldrich | 229865 | |
| Tri-n-octylphosphine | Strem | 15-6655 | 97% pure, unstable in air |
| Cadmium oxide | Sigma-Aldrich | 202894 | Highly toxic: use caution |
| Tetradecylphosphonic acid | PCI Synthesis | 4671-75-4 | |
| Octadecene | Alfa Aesar | L11004 | Technical grade |
| Hexadecylamine | Sigma-Aldrich | H7408 | |
| Diphenylphosphine | Sigma-Aldrich | 252964 | Pyrophoric |
| Mercury acetate | Sigma-Aldrich | 456012 | Highly toxic: use caution |
| 1-Octanethiol | Sigma-Aldrich | 471836 | Strong odor |
| Oleic acid | Sigma-Aldrich | W281506 | |
| Zinc acetate | Alfa Aesar | 35792 | |
| Cadmium acetate hydrate | Sigma-Aldrich | 229490 | Highly toxic: use caution |
| Oleylamine | Fisher Scientific | AC12954 | Unstable in air |
| Sulfur | Sigma-Aldrich | 344621 | |
| Trioctylphosphine oxide | Strem | 15-6661 | 99% |
| Pyridine | VWR | EM-PX2012-6 | Anhydrous |
| Thioglycerol | Sigma-Aldrich | M1753 | Strong odor |
| Triethylamine | Sigma-Aldrich | 471283 | Anhydrous |
| Dialysis tubing | Spectrum Labs | 131342 | 20 kDa cutoff |
| Centrifugal filter | Millipore | UFC801024 | 10 kDa cutoff |
| Monoamino-PEG | Rapp Polymere | 12 750-2 | 750 Da |
| DMTMM, 4-(4,6-Dimethoxy-1,3,5-triazin-2-yl)-4-methylmorpholinium chloride hydrate | Alfa Aesar | H26333 | |
| AKTAprime Plus Chromatography System | GE HealthCare | ||
| Superose 6 10/300 GL chromatography column | GE HealthCare | 17-5172-01 | |
| Agarose, OmniPur | VWR | EM-2120 | |
Appendix Synthesis of mercury octanethiolate: Slowly add a methanol solution of mercury acetate (1 eq.) to a stirring solution of 1-octanethiol (3 eq.) and potassium hydroxide (3 eq.) in methanol at room temperature. Isolate the mercury(II) octanethiolate precipitate via filtration, wash two times with methanol and once with ether, and then dry under vacuum. Synthesis of multidentate polymer: Dissolve polyacrylic acid (1 g, 1,773 Da) in 25 ml dimethylformamide (DMF) in a 150 ml three-necked flask and bubble with argon for 30 min. Add an anhydrous solution of cysteamine (374 mg, 4.87 mmol) in 10 ml DMF. At room temperature with vigorous stirring, slowly add anhydrous diisopropylcarbodiimide (DIC, 736 mg, 5.83 mmol) over 30 min, followed by triethylamine (170 μl, 1.22 mmol), and allow the reaction to proceed for 72 hr at 60 °C. Add mercaptoethanol (501 mg, 6.41 mmol) to quench the reaction, and stir for 2 hr at room temperature. Remove DMF via rotary evaporation and isolate the polymer with the addition of a 2:1 mixture of ice-cold acetone:chloroform, followed by centrifugation. Dissolve the polymer in ~5 ml anhydrous DMF, filter, precipitate again with diethyl ether, and repeat. Dry the product under vacuum and store under argon. Determination of CdSe core diameter: From the UV-Vis absorption spectrum determine the wavelength of the first exciton peak (λ, in nm), which is the longest-wavelength peak (e.g. roughly 498 nm for CdSe in Figure 2a), and use the sizing curve of Mulvaney and coworkers 12:
Determination of CdSe nanocrystal concentration: From a background-subtracted UV-Vis spectrum of an optically clear solution of CdSe nanocrystals, determine the absorption at 350 nm wavelength. Serial dilutions can be used to determine if the optical absorption is within the linear range of Beer’s Law. The nanocrystal concentration (QD, in M) can be determined by plugging in the nanocrystal diameter (D, in nm), the optical absorption value (A3sa), and the cuvette path length (l, in cm) into the following equation from the empirical correlation of Bawendi and coworkers 13:
|
Referências
- Toprak, E., Selvin, P. R. New fluorescent tools for watching nanometer-scale conformational changes of single molecules. Annu. Rev. Biophys. Biomol. Struct. 36, 349-369 (2007).
- Joo, C., Balci, H., Ishitsuka, Y., Buranachai, C., Ha, T. J. Advances in single molecule fluorescence methods for molecular biology. Annu. Rev. Biochem. 77, 51-76 (2008).
- Pinaud, F., Clarke, S., Sittner, A., Dahan, M. Probing cellular events, one quantum dot at a time. Nat. Method. 7, 275-285 (2010).
- Smith, A. M., Wen, M. M., Nie, S. M. Imaging dynamic cellular events with quantum dots. Biochemist. 32, 12-17 (2010).
- Smith, A. M., Duan, H. W., Mohs, A. M., Nie, S. M. Bioconjugated quantum dots for in vivo molecular and cellular imaging. Adv. Drug Deliv. Rev. 60, 1226-1240 (2008).
- Smith, A. M., Nie, S. M. Next-generation quantum dots. Nature Biotech. 27, 732-733 (2009).
- Groc, L., Lafourcade, M., Heine, M., Renner, M., Racine, V., Sibarita, J. -. B., Lounis, B., Choquet, D., Cognet, L. Single trafficking of neurotransmitter receptor: comparison between single-molecule/quantum dot strategies. J. Neurosci. 27, 12433-12437 (2007).
- Smith, A. M., Nie, S. M. Minimizing the hydrodynamic size of quantum dots with multifunctional multidentate polymer ligands. J. Am. Chem. Soc. 130, 11278-11279 (2008).
- Smith, A. M., Nie, S. M. Bright and compact alloyed quantum dots with broadly tunable near-infrared absorption and fluorescence spectra through mercury cation exchange. J. Am. Chem. Soc. 133, 24-26 (2011).
- Shriver, D. F., Drezdzon, M. A. . The Manipulation of Air-Sensitive Compounds. , (1986).
- Errington, R. J. . Advanced Practical Inorganic and Metalorganic Chemistry. , (1997).
- Jasieniak, J., Smith, L., van Embden, J., Mulvaney, P., Califano, M. Re-examination of the size-dependent absorption properties of CdSe quantum dots. J. Phys. Chem. C. 113, 19468-19474 (2009).
- Leatherdale, C. A., Woo, W. K., Mikulec, F. V., Bawendi, M. G. On the absorption cross section of CdSe nanocrystal quantum dots. J. Phys. Chem. B. 106, 7619-7622 (2002).
- Smith, A. M., Mohs, A. M., Nie, S. M. Tuning the optical and electronic properties of colloidal nanocrystals by lattice strain. Nature Nanotech. 4, 56-63 (2009).
- Demas, J. N., Crosby, G. A. The measurement of photoluminescence quantum yields. A review. J. Phys. Chem. 75, 991-1024 (1971).
- Van Embden, J., Jasieniak, J., Mulvaney, P. Mapping the optical properties of CdSe/CdS heterostructure nanocrystals: the effects of core size and shell thickness. J. Am. Chem. Soc. 131, 14299-14309 (2009).
- Smith, A. M., Duan, H. W., Rhyner, M. N., Ruan, G., Nie, S. M. A systematic examination of surface coatings on the optical and chemical properties of semiconductor quantum dots. Phys. Chem. Chem. Phys. 8, 3895-3903 (2006).
- Zhang, X., Mohandessi, S., Miller, L. W., Snee, P. T. Efficient functionalization of aqueous CdSe/ZnS nanocrystals using small-molecule chemical activators. Chem. Comm. 47, 3532-3534 (2011).
- Bucio, L., Souza, V., Albores, A., Sierra, A., Chavez, E., Carabez, A., Guiterrez-Ruiz, M. C. Cadmium and mercury toxicity in a human fetal hepatic cell line (WRL-68 cells). Toxicol. 102, 285-299 (1995).
- Han, S. G., Castranova, V., Vallyathan, V. J. Comparative cytotoxicity of cadmium and mercury in a human bronchial epithelial cell line (BEAS-2B) and its role in oxidative stress and induction of heat shock protein 70. J. Toxicol. Environ. Health Part A. 70, 852-860 (2007).
- Strubelt, O., Kremer, J., Tilse, A., Keogh, J., Pentz, R. J. Comparative studies on the toxicity of mercury, cadmium, and copper toward the isolated perfused rat liver. J. Toxicol. Environ. Health Part A. 47, 267-283 (1996).