एक वाणिज्यिक माइक्रोस्कोप में लाइव कोशिका झिल्ली पर आण्विक प्रसार कानून को फास्ट प्रतिदीप्ति इमेजिंग से
Summary
Spatial distribution and temporal dynamics of plasma membrane proteins and lipids is a hot topic in biology. Here this issue is addressed by a spatio-temporal image fluctuation analysis that provides conceptually the same physical quantities of single particle tracking, but it uses small molecular labels and standard microscopy setups.
Abstract
यह स्थानिक वितरण और लिपिड और प्रोटीन की तरह झिल्ली घटकों की गति कई सेलुलर कार्यों के विनियमन में महत्वपूर्ण कारक हैं कि तेजी से स्पष्ट हो गया है. हालांकि, तेजी से गतिशीलता और शामिल छोटे संरचनाओं के लिए, एक बहुत ही उच्च spatio- लौकिक संकल्प अणुओं की वास्तविक व्यवहार को पकड़ने के लिए आवश्यक है. यहाँ हम उच्च spatiotemporal संकल्प के साथ जीवित कोशिकाओं में fluorescently लेबल प्लाज्मा झिल्ली प्रोटीन और लिपिड की गतिशीलता के अध्ययन के लिए प्रयोगात्मक प्रोटोकॉल प्रस्तुत करते हैं. विशेष रूप से, इस दृष्टिकोण प्रत्येक अणु को ट्रैक करने की जरूरत नहीं है, लेकिन यह झिल्ली का एक दिया क्षेत्र के सभी अणुओं का उपयोग कर जनसंख्या व्यवहार खरीदते हैं. शुरुआती बिंदु झिल्ली पर एक दिया क्षेत्र की एक तेजी से इमेजिंग है. बाद में, एक पूर्ण spatio- अस्थायी autocorrelation समारोह उदाहरण के लिए, प्रत्येक 2, 3, एन repetitions समय देरी बढ़ती में अधिग्रहीत छवियों correlating गणना की जाती है. यह चौड़ाई को दिखाना है कि संभव हैकारण प्रसार करने के कण आंदोलन के एक समारोह के रूप में समय की देरी बढ़ाने के स्थानिक autocorrelation समारोह बढ़ जाती है की चोटी की. इसलिए, autocorrelation कार्यों की श्रृंखला की फिटिंग वास्तविक प्रोटीन यहां औसत विस्थापन बनाम स्पष्ट diffusivity के रूप में प्रस्तुत किया, इमेजिंग (iMSD) से वर्ग विस्थापन मतलब निकालने के लिए सक्षम बनाता है. इस नैनोमीटर सटीकता के साथ एकल अणुओं की औसत गतिशीलता का एक मात्रात्मक देखने पैदावार. लेबल transferrin रिसेप्टर (टीएफआर) और एक ATTO488 की एक GFP टैग संस्करण का उपयोग करके 1-palmitoyl-2-hydroxy- एस.एन. -glycero-3-phosphoethanolamine (पीपीई) उस पर प्रोटीन और लिपिड प्रसार के spatiotemporal विनियमन निरीक्षण करने के लिए संभव है माइक्रो करने वाली मिल्ली दूसरी बार सीमा में माइक्रोन आकार झिल्ली क्षेत्रों.
Introduction
सिंगर और निकोल्सन द्वारा मूल "द्रव मोज़ेक" मॉडल से शुरू, सेलुलर प्लाज्मा झिल्ली की तस्वीर लगातार cytoskeleton और लिपिड डोमेन 1,2 की उभरती भूमिका को शामिल करने के क्रम में पिछले दशकों के दौरान अद्यतन किया गया है.
पहली टिप्पणियों झिल्ली प्रोटीन का एक महत्वपूर्ण अंश 3-5 स्थिर है कि (FRAP) अनावरण photobleaching के बाद फ्लोरोसेंट वसूली से प्राप्त किया गया. इन अग्रणी अध्ययन, बहुत जानकारीपूर्ण हालांकि, FRAP setups के अपेक्षाकृत गरीब अंतरिक्ष (माइक्रोन) में संकल्प और समय (सेकंड) से सामना करना पड़ा. इसके अलावा, एक जोड़ा औसत माप किया जा रहा है, FRAP एक अणु व्यवहार के बारे में जानकारी देने में अभाव है.
इस संदर्भ में, संभावना विशेष रूप से (एक समय में प्रसार की प्रक्रिया एक अणु के अध्ययन की अनुमति) बहुत उज्ज्वल टैग के साथ एक अणु लेबल करने के लिए बहुत सफल रहा है. विशेष रूप से, जोर सेएट microseconds timescale, Kusumi, बहुत झिल्ली फिजियोलॉजी 6 में actin आधारित झिल्ली कंकाल की भूमिका की मान्यता के लिए योगदान दिया है कि लिपिड और प्रोटीन की गतिशीलता की अज्ञात सुविधाओं के लिए अल. प्राप्त की पहुँच के लिए एक कण ट्रैकिंग (SPT) दृष्टिकोण का समय संकल्प , 7. इन निष्कर्षों लिपिड और प्रोटीन प्रसार actin आधारित कंकाल द्वारा नियंत्रित किया जाता है, जिसमें 'धरना और बाड़' मॉडल, तथाकथित उत्पन्न. हालांकि, SPT कई प्रयोगात्मक मुद्दों द्वारा उपलब्ध कराई गई जानकारी की विशाल राशि के लिए उपयोग करने के क्रम में संबोधित किया जाना है. विशेष रूप से, लेबलिंग प्रक्रिया आम तौर पर इस प्रणाली में लेबल प्रजातियों के उत्पादन, शोधन और परिचय की तरह कई कदम से बना है. इसके अलावा, बड़े लेबल, क्वांटम डॉट्स या धातु नैनोकणों की तरह, अक्सर उप millisecond timescale और कई मामलों में टाला नहीं जा सकता है लेबल द्वारा लक्ष्य अणुओं की crosslinking तक पहुँचने के लिए आवश्यक हैं. अंत में, कई trajectoriesसांख्यिकीय मापदंड फिट करने के लिए दर्ज हो चुके हैं और समन्वित रूप से लेबल की एक कम घनत्व ट्रैकिंग की अनुमति की आवश्यकता है.
SPT की तुलना में, इन कमियों के कई पर काबू पाने प्रतिदीप्ति सहसंबंध स्पेक्ट्रोस्कोपी (एफसीएस), आणविक गतिशीलता का अध्ययन करने के लिए एक बहुत ही होनहार दृष्टिकोण का प्रतिनिधित्व करता है. वास्तव में, एफसीएस क्षणिक ट्रांसफ़ेक्ट कोशिकाओं में फ्लोरोसेंट प्रोटीन टैग अणुओं की गतिशीलता का अध्ययन करने के लिए सक्षम करने, मंद और घने लेबल के साथ अच्छी तरह भी काम करता है. इसके अलावा, यह समय की एक सीमित मात्रा में उच्च आँकड़े तक पहुँचने की अनुमति देता है. अंत में, लेबल की "" उच्च घनत्व के बावजूद FCS एकल अणुओं जानकारी प्रदान करता है. धन्यवाद इन सभी गुणों को, एफसीएस एक बहुत स्पष्ट दृष्टिकोण का प्रतिनिधित्व करता है और बड़े पैमाने पर मॉडल झिल्ली में और जीवित कोशिकाओं 8-10 में दोनों लिपिड और प्रोटीन गतिशीलता का अध्ययन करने के लिए लागू किया गया है. कई अलग अलग दृष्टिकोण आणविक प्रसार का विवरण प्रकट करने के लिए एफसीएस की क्षमता में वृद्धि करने का प्रस्ताव किया गया है. उदाहरण के लिए, यह श थाखुद को अलग ढंग से आकार अवलोकन क्षेत्रों पर एफसीएस प्रदर्शन से एक आणविक गति 11,12 के एक "एफसीएस प्रसार कानून" शिक्षाप्रद छिपा सुविधाओं परिभाषित कर सकते हैं कि. आकार में विविध होने के अलावा, फोकल क्षेत्र में भी, 13 दोहराया गया था तेजी कैमरों 21,22 के साथ लाइनों 14-20 या संयुग्मित साथ अंतरिक्ष में ले जाया गया. इन 'spatio- लौकिक' सहसंबंध दृष्टिकोण का उपयोग कर, कई झिल्ली घटकों के प्रासंगिक जैविक मापदंडों मात्रात्मक मॉडल झिल्ली और वास्तविक जैविक वाले, झिल्ली स्थानिक संगठन में इस प्रकार उपज अंतर्दृष्टि दोनों पर वर्णित किया गया.
हालांकि, सभी FRAP और FCS अनुप्रयोगों में अब तक वर्णित फोकल क्षेत्र के आकार के दूर नहीं किया जा सकता है कि स्थानिक संकल्प में एक सीमा का प्रतिनिधित्व करता है. कई सुपर संकल्प इमेजिंग तरीकों हाल ही में इस सीमा को बायपास करने के लिए विकसित किया गया है. कुछ ऐसे Stochastic ऑप्टिकल पुनर्निर्माण माइक्रोस्कोपी (तूफान) के रूप में, स्थानीयकरण परिशुद्धता के आधार पर कर रहे हैं <समर्थन> 23,24, photoactivation स्थानीयकरण माइक्रोस्कोपी (पाम) 25, प्रतिदीप्ति पाम (FPALM) 26, और एकल कण ट्रैकिंग पाम (sptPALM) 27: प्रत्येक स्नैपशॉट में आवश्यक फोटॉनों की अपेक्षाकृत बड़ी राशि है, तथापि, के समय संकल्प सीमा कम से कम कई मिसे के लिए इन तरीकों, इस प्रकार vivo में उनकी प्रयोज्यता बाधा.
इसके विपरीत, सुपर संकल्प इमेजिंग के लिए एक आशाजनक विकल्प स्थानिक प्रेरित उत्सर्जन रिक्तीकरण तरीकों (STED या प्रतिवर्ती saturable ऑप्टिकल प्रतिदीप्ति संक्रमण (RESOLFT)) 28,29 के साथ प्रतिदीप्ति उत्सर्जन नियमन से खोल दिया गया है. इन तरीकों में तेजी से स्कैनिंग सूक्ष्मदर्शी और पहचान प्रणाली का उपयोग करने की संभावना के साथ अवलोकन मात्रा का आकार देने में अच्छी तरह से नीचे विवर्तन सीमा गठबंधन. प्रतिदीप्ति अस्थिरता विश्लेषण के साथ संयोजन में, STED माइक्रोस्कोपी सीधे लिपिड और पी के nanoscale spatiotemporal गतिशीलता की जांच करने की अनुमति दीजीवित कोशिका झिल्ली 30,31 में roteins.
STED आधारित माइक्रोस्कोपी का ही भौतिक मात्रा में जीवित कोशिकाओं में fluorescently टैग झिल्ली प्रोटीन और / या लिपिड की गतिशीलता के अध्ययन के लिए उपयुक्त है कि एक संशोधित spatio- अस्थायी छवि सहसंबंध स्पेक्ट्रोस्कोपी (stics 32,33) विधि द्वारा प्राप्त किया जा सकता है और एक वाणिज्यिक माइक्रोस्कोप से. यहाँ प्रस्तुत प्रयोगात्मक प्रोटोकॉल कुछ कदम से बना है. पहले एक झिल्ली पर ब्याज के क्षेत्र की एक तेज इमेजिंग की आवश्यकता है. फिर, छवियों के परिणामस्वरूप ढेर औसत स्थानिक लौकिक सहसंबंध कार्यों की गणना करने के लिए प्रयोग किया जाता है. सहसंबंध कार्यों की श्रृंखला फिटिंग द्वारा, आणविक 'प्रसार कानून' एक स्पष्ट diffusivity (डी एपीपी) के रूप में इमेजिंग से सीधे प्राप्त किया जा सकता है – -average विस्थापन साजिश बनाम. इस साजिश समीक्षकों अणुओं से पता लगाया वातावरण पर निर्भर करता है और सीधे वास्तविक प्रसार मोड पहचानने की अनुमति देता हैब्याज की लिपिड / प्रोटीन की.
पहले 34 के रूप में दिखाया अधिक विवरण में, अधिग्रहीत छवि श्रृंखला की spatio- अस्थायी ऑटो सहसंबंध समारोह समीक्षकों एकत्र छवि श्रृंखला में आगे बढ़ अणुओं की गतिशीलता पर निर्भर करता है (एक ही तर्क एक लाइन अधिग्रहण में लागू किया जा सकता है कि कृपया ध्यान दें अंतरिक्ष में सिर्फ एक आयाम) माना जाता है, जहां. विशेष रूप से, हम सहसंबंध समारोह के रूप में परिभाषित:
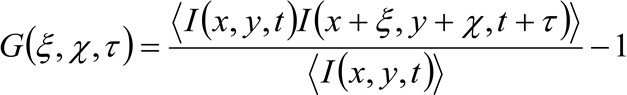 (1)
(1)
जहां 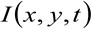 स्थिति एक्स में मापा प्रतिदीप्ति तीव्रता का प्रतिनिधित्व करता है, वाई और समय टी,
स्थिति एक्स में मापा प्रतिदीप्ति तीव्रता का प्रतिनिधित्व करता है, वाई और समय टी, ![]() और
और ![]() का प्रतिनिधित्व करता है एक्स में दूरी औरक्रमशः वाई दिशाओं,
का प्रतिनिधित्व करता है एक्स में दूरी औरक्रमशः वाई दिशाओं, ![]() समय अंतराल का प्रतिनिधित्व करता है, और
समय अंतराल का प्रतिनिधित्व करता है, और ![]() औसत का प्रतिनिधित्व करता है. इस समारोह के रूप में व्यक्त किया जा सकता है:
औसत का प्रतिनिधित्व करता है. इस समारोह के रूप में व्यक्त किया जा सकता है:
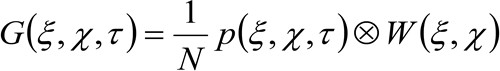 (2)
(2)
'एन' अवलोकन क्षेत्र में अणुओं की औसत संख्या का प्रतिनिधित्व करता है, ![]() अंतरिक्ष में कनवल्शनफ़िल्टर्स ऑपरेशन का प्रतिनिधित्व करता है, और
अंतरिक्ष में कनवल्शनफ़िल्टर्स ऑपरेशन का प्रतिनिधित्व करता है, और 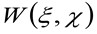 वाद्य कमर के autocorrelation का प्रतिनिधित्व करता है. यह बाद के कारण ऑप्टिकल / रिकॉर्डिंग स्थापना के लिए एक एकल emitter के फोटॉनों अंतरिक्ष में फैल रहे हैं की एक उपाय के रूप में व्याख्या की जा सकती (तथाकथित बात फैल समारोह, पीएसएफ, जीनअच्छी तरह से) एक गाऊसी समारोह द्वारा approximated रैली. अंत में,
वाद्य कमर के autocorrelation का प्रतिनिधित्व करता है. यह बाद के कारण ऑप्टिकल / रिकॉर्डिंग स्थापना के लिए एक एकल emitter के फोटॉनों अंतरिक्ष में फैल रहे हैं की एक उपाय के रूप में व्याख्या की जा सकती (तथाकथित बात फैल समारोह, पीएसएफ, जीनअच्छी तरह से) एक गाऊसी समारोह द्वारा approximated रैली. अंत में, 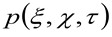 एक दूरी पर एक कण को खोजने के लिए संभावना का प्रतिनिधित्व करता है
एक दूरी पर एक कण को खोजने के लिए संभावना का प्रतिनिधित्व करता है ![]() और
और ![]() एक समय की देरी के बाद
एक समय की देरी के बाद ![]() . हम कणों सभी दिशाओं में बेतरतीब ढंग से ले जाने और शुद्ध अपशिष्टों मौजूद नहीं हैं, जिसमें एक वाचाल गतिशीलता, विचार, इस समारोह में भी अच्छी तरह से विचरण चलती कण का मतलब स्क्वायर विस्थापन (एमएसडी) के रूप में पहचाना जा सकता है जहां एक गाऊसी समारोह द्वारा approximated है . इस प्रकार, सहसंबंध समारोह की कमर (भी रूप में भेजा
. हम कणों सभी दिशाओं में बेतरतीब ढंग से ले जाने और शुद्ध अपशिष्टों मौजूद नहीं हैं, जिसमें एक वाचाल गतिशीलता, विचार, इस समारोह में भी अच्छी तरह से विचरण चलती कण का मतलब स्क्वायर विस्थापन (एमएसडी) के रूप में पहचाना जा सकता है जहां एक गाऊसी समारोह द्वारा approximated है . इस प्रकार, सहसंबंध समारोह की कमर (भी रूप में भेजा ![]() ), कण MSDS की राशि और वाद्य कमर के रूप में परिभाषित किया जा सकता है और एक गाऊसी फिट से मापा जा सकता हैहर बार देरी के लिए सहसंबंध समारोह की ting. मापा मैं एमएसडी आगे बढ़ अणुओं का एक स्पष्ट diffusivity गणना करने के लिए इस्तेमाल किया जा सकता है
), कण MSDS की राशि और वाद्य कमर के रूप में परिभाषित किया जा सकता है और एक गाऊसी फिट से मापा जा सकता हैहर बार देरी के लिए सहसंबंध समारोह की ting. मापा मैं एमएसडी आगे बढ़ अणुओं का एक स्पष्ट diffusivity गणना करने के लिए इस्तेमाल किया जा सकता है ![]() और एक औसत विस्थापन
और एक औसत विस्थापन ![]() के रूप में:
के रूप में:
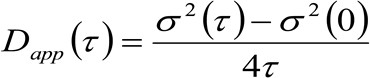 (3)
(3)
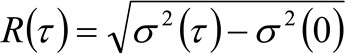 (4)
(4)
निम्न वर्गों भर में पाठक मार्गदर्शन कर सकते हैं इस्तेमाल किया प्रयोगात्मक स्थापना पर कुछ विचार. चुनिंदा एक वाणिज्यिक TIR प्रतिदीप्ति हम कुल आंतरिक प्रतिबिंब (TIR) रोशनी का उपयोग करेगा जीवित कोशिकाओं के बेसल झिल्ली पर fluorophores उत्तेजित करने के लिए आदेश में (TIRF) माइक्रोस्कोप (विवरण सामग्री अनुभाग में पाया जा सकता है). इसके अलावा, आदेश में वें इकट्ठा करने के लिएई प्रतिदीप्ति हम एक उच्च बढ़ाई उद्देश्य का उपयोग करेगा और (चिप 16 माइक्रोन पर पिक्सेल की शारीरिक आकार) एक EMCCD कैमरा (100x NA 1.47, उच्च संख्यात्मक एपर्चर TIRF रोशनी के लिए आवश्यक है). 100 एनएम के एक पिक्सेल आकार तक पहुँचने के लिए हम 1.6x के एक अतिरिक्त बढ़ाई लेंस लागू होते हैं. नीचे चर्चा की, 1 मिसे नीचे एक समय संकल्प ठीक से 100 एनएम से नीचे तेजी से झिल्ली लिपिड की गतिशीलता का वर्णन करने के लिए आवश्यक हो जाएगा. इस अस्थायी समाधान तक पहुँचने के क्रम में हम कैमरा (एक्स 512 512) के पूरे चिप की तुलना में छोटे ब्याज (आरओआई) के एक क्षेत्र का चयन करने की आवश्यकता है. इस तरह, कैमरे समय संकल्प बढ़ती लाइनों की संख्या कम पढ़ा होगा. हालांकि, इस readout शासन में फ्रेम बार कैमरे पर readout चिप के लिए जोखिम से शुल्क में बदलाव करने की जरूरत है और 512 x 512 पिक्सेल EMCCD के लिए मिसे के क्रम में आमतौर पर समय से सीमित हो जाएगा. इस सीमा को हरा करने के लिए, एक उभरती हुई प्रौद्योगिकी डब्ल्यू, रॉय लाइनों केवल बजाय पूरे फ्रेम स्थानांतरण की अनुमति देता है(हमारे EMCCD में फसली सेंसर मोड कहा जाता है) उजागर चिप के आकार का एक व्यावहारिक प्रभावी कमी रबर. इस विन्यास प्रभावी होने के लिए, रॉय के बाहर चिप ऑप्टिकल पथ में घुड़सवार slits के एक जोड़े द्वारा कवर किया जाना चाहिए. एक समय संकल्प नीचे 10 -4 सेकंड के लिए इस सेटअप करने के लिए धन्यवाद प्राप्त किया जा सकता है. 'चर्चा' अनुभाग में समझाया के रूप में इस दृष्टिकोण, कई अलग अलग प्रयोगात्मक setups के साथ मिलकर किया जा सकता है कि, हालांकि, कृपया ध्यान दें.
विधि का प्रदर्शन GFP- एक ATTO488 लेबल दोनों 1-palmitoyl-2-hydroxy- एस.एन. -glycero-3-phosphoethanolamine (ATTO488-पीपीई) और transferrin रिसेप्टर के एक GFP लेबल संस्करण (का उपयोग करके, जीवित कोशिकाओं में प्रदान किया जाएगा टीएफआर). पहले से 30,35 रिपोर्ट के रूप में ATTO488-पीपीई के मामले में इस दृष्टिकोण को सफलतापूर्वक, एक ज्यादातर मुक्त प्रसार का संकेत औसत विस्थापन के एक समारोह के रूप में एक लगभग निरंतर विकास अनुप्रयोग ठीक हो सकता है. इसके विपरीत, टीएफआर-GFP एक घटते विकास से पता चलता है <suआंशिक रूप से सीमित प्रसार 6 सुझाव औसत विस्थापन के एक समारोह के रूप में b> अनुप्रयोग. इसके अलावा, दूसरे मामले में यह स्थानीय प्रसार निरंतर और झिल्ली विमान पर कई माइक्रोन से अधिक औसत कारावास क्षेत्र यों संभव है.
Protocol
Representative Results
Discussion
एक कण ट्रैकिंग (SPT) आणविक गतिशीलता का अध्ययन करने के लिए सबसे आम रणनीतियों में से एक का प्रतिनिधित्व करता है और यह कण trajectories मापने के महान लाभ है. यह बदले में एक जटिल प्रणाली में भी कुछ लेबल कणों के व्यवहार क?…
Declarações
The authors have nothing to disclose.
Acknowledgements
This work is supported in part by NIH-P41 P41-RRO3155 and NIH P50-GM076516 (grant to EG), and Fondazione Monte dei Paschi di Siena (grant to FB).
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| iXon Ultra 897 | Andor | DU-897U-CS0 | |
| Solis | Andor | ||
| CHO-K1 | ATCC | CCL-61 | |
| ATTO 488 labeled PPE | ATTO-TEC GmbH | AD 488-151 | |
| DOPE | Avanti Polar Lipids, Inc. | 850725 | |
| DOTAP | Avanti Polar Lipids, Inc. | 890890 | |
| 100X Penicillin-Streptomycin-Glutamine | Gibco | 10378-016 | |
| DMEM/F-12 | Gibco | 21331 | |
| FBS | Gibco | 10082147 | |
| HEPES | Gibco | 15630-106 | |
| PBS | Gibco | 10010-023 | |
| SimFCS 3.0 | Globals Software | the software can be downloaded here: http://www.lfd.uci.edu/globals/ | |
| DMI6000 with TIRF modulus | Leica | ||
| LAS AF | Leica | ||
| Lipofectamine 2000 | Lipofectamine | 11668019 | |
| Matlab | MathWork | ||
| Imagej | NIH | ||
| C-terminal GFP tagged Tranferrin Receptor | OriGene | RG200980 | |
| Agar | Sigma Aldrich | A5306 | |
| Chloroform | Sigma Aldrich | 528730 | |
| Latex beads, fluorescent yellow-green, 30 nm | Sigma Aldrich | L5155 | |
| SONICA Ultrasonic Cleaners | SOLTEC | ETH S3 | |
| Petri Dishes | Willco | GWSt-3522 | |
| Bio-Format importer for Matlab | http://www.openmicroscopy.org/site/support/bio-formats5/users/matlab/ | ||
| ICS-MatLab Tools | https://www.cellmigration.org/resource/imaging/software/ICSMATLAB_28-02-06.zip | ||
| Simulation by Matlab Tutorial | https://www.cellmigration.org/resource/imaging/icsmatlab/ICSTutorial.html | ||
| Simulation by SimFCS Tutorial | https://www.cellmigration.org/resource/imaging/ppt-pdf/RICS%20Simulations.ppt |
Referências
- Engelman, D. M. Membranes are more mosaic than fluid. Nature. 438 (7068), 578-580 (2005).
- Vereb, G., et al. yet structured: The cell membrane three decades after the Singer-Nicolson model. Proc. Natl. Acad. Sci. U. S. A. 100 (14), 8053-8058 (1073).
- Ishihara, A., Hou, Y., Jacobson, K. The Thy-1 antigen exhibits rapid lateral diffusion in the plasma membrane of rodent lymphoid cells and fibroblasts. 84 (5), 1290-1293 (1987).
- Axelrod, D., et al. Lateral motion of fluorescently labeled acetylcholine receptors in membranes of developing muscle fibers. Proc. Natl. Acad. Sci. U. S. A. 73 (12), 4594-4598 (1976).
- Jacobson, K., Derzko, Z., Wu, E. S., Hou, Y., Poste, G. Measurement of the lateral mobility of cell surface components in single, living cells by fluorescence recovery after photobleaching. J. Supramol. Struct. 5 (4), 10-1002 (1976).
- Kusumi, A., et al. Paradigm shift of the plasma membrane concept from the two-dimensional continuum fluid to the partitioned fluid: high-speed single-molecule tracking of membrane molecules. Annu. Rev. Biophys. Biomol. Struct. 34, 351-378 (2005).
- Kusumi, A., Ike, H., Nakada, C., Murase, K., Fujiwara, T. Single-molecule tracking of membrane molecules: plasma membrane compartmentalization and dynamic assembly of raft-philic signaling molecules. Semin. Immunol. 17 (1), 3-21 (2005).
- Schwille, P., Korlach, J., Webb, W. W. Fluorescence correlation spectroscopy with single-molecule sensitivity on cell and model membranes. Cytometry. 36, 176-182 (1999).
- Gielen, E., et al. Diffusion of sphingomyelin and myelin oligodendrocyte glycoprotein in the membrane of OLN-93 oligodendroglial cells studied by fluorescence correlation spectroscopy. C. R. Biol. 328 (12), 1057-1064 (2005).
- Weiss, M., Hashimoto, H., Nilsson, T. Anomalous protein diffusion in living cells as seen by fluorescence correlation spectroscopy. Biophys. J. 84, 4043-4052 (2003).
- Wawrezinieck, L., Rigneault, H., Marguet, D., Lenne, P. F. Fluorescence correlation spectroscopy diffusion laws to probe the submicron cell membrane organization. Biophys. J. 89 (6), 4029-4042 (2005).
- Lenne, P. F., et al. Dynamic molecular confinement in the plasma membrane by microdomains and the cytoskeleton meshwork. EMBO J. 25 (14), 3245-3256 (2006).
- Ries, J., Schwille, P. Studying slow membrane dynamics with continuous wave scanning fluorescence correlation spectroscopy. Biophys. J. 91 (5), 1915-1924 (2006).
- Ruan, Q., Cheng, M. A., Levi, M., Gratton, E., Mantulin, W. W. Spatial-temporal studies of membrane dynamics: scanning fluorescence correlation spectroscopy (SFCS). Biophys. J. 87 (2), 1260-1267 (2004).
- Berland, K. M., So, P. T., Chen, Y., Mantulin, W. W., Gratton, E. Scanning two-photon fluctuation correlation spectroscopy: particle counting measurements for detection of molecular aggregation. Biophys. J. 71, 410-420 (1996).
- Heinemann, F., Betaneli, V., Thomas, F. A., Schwille, P. Quantifying lipid diffusion by fluorescence correlation spectroscopy: a critical treatise. Langmuir. 28 (37), 13395-13404 (2012).
- Cardarelli, F., Lanzano, L., Gratton, E. Capturing directed molecular motion in the nuclear pore complex of live cells. Proc. Natl. Acad. Sci. U. S. A. 109 (25), 9863-9868 (2012).
- Sanchez, S. A., Tricerri, M. A., Gratton, E. Laurdan generalized polarization fluctuations measures membrane packing micro-heterogeneity in vivo. Proc. Natl. Acad. Sci. U. S. A. 109 (19), 7314-7319 (2012).
- Cardarelli, F., Lanzano, L., Gratton, E. Fluorescence correlation spectroscopy of intact nuclear pore complexes. Biophys. J. 101 (4), 27-29 (2012).
- Di Rienzo, C., et al. Unveiling LOX-1 receptor interplay with nanotopography: mechanotransduction and atherosclerosis onset. Sci. Rep. 3, 10-1038 (2013).
- Unruh, J. R., Gratton, E. Analysis of molecular concentration and brightness from fluorescence fluctuation data with an electron multiplied CCD camera. Biophys. J. 95 (11), 5385-5398 (2008).
- Kannan, B., et al. Electron multiplying charge-coupled device camera based fluorescence correlation spectroscopy. Anal. Chem. 78 (10), 3444-3451 (2006).
- Jones, S. A., Shim, S. H., He, J., Fast Zhuang, X. three-dimensional super-resolution imaging of live cells. Nat. Methods. 8 (6), 499-508 (2011).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy. 3 (10), 793-795 (2006).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313 (5793), 1642-1645 (2006).
- Hess, S. T., Girirajan, T. P., Mason, M. D. Ultra-high resolution imaging by fluorescence photoactivation localization microscopy. Biophys. J. 91 (11), 4258-4272 (2006).
- Manley, S., et al. High-density mapping of single-molecule trajectories with photoactivated localization microscopy. Nat. Methods. 5 (2), 155-157 (2008).
- Hell, S. W. Far-field optical nanoscopy. Science. 316 (5828), 1153-1158 (2007).
- Klar, T. A., Hell, S. W. Subdiffraction resolution in far-field fluorescence microscopy. Opt. Lett. 24 (14), 954-956 (1999).
- Eggeling, C., et al. Direct observation of the nanoscale dynamics of membrane lipids in a living cell. Nature. 457 (7233), 1159-1162 (2009).
- Hedde, P. N., et al. Stimulated emission depletion-based raster image correlation spectroscopy reveals biomolecular dynamics in live cells. Nat. Commun. 4, .
- Hebert, B., Costantino, S., Wiseman, P. W. Spatiotemporal image correlation spectroscopy (STICS) theory, verification, and application to protein velocity mapping in living CHO cells. Biophys. J. 88 (5), 3601-3614 (2005).
- Brown, C. M., et al. Probing the integrin-actin linkage using high-resolution protein velocity mapping. J. Cell Sci. 119, 5204-5214 (2006).
- Di Rienzo, C., Gratton, E., Beltram, F., Cardarelli, F. Fast spatiotemporal correlation spectroscopy to determine protein lateral diffusion laws in live cell membranes. Proc. Natl. Acad. Sci. U. S. A. 110 (30), 12307-12312 (2013).
- Mueller, V., et al. STED nanoscopy reveals molecular details of cholesterol- and cytoskeleton-modulated lipid interactions in living cells. Biophys. J. 101 (7), 1651-1660 (2011).
- Kleusch, C., Hersch, N., Hoffmann, B., Merkel, R., Csiszar, A. Fluorescent lipids: functional parts of fusogenic liposomes and tools for cell membrane labeling and visualization. Molecules. 17 (1), 1055-1073 (2012).
- Ries, J., Chiantia, S., Schwille, P. Accurate determination of membrane dynamics with line-scan FCS. Biophys. J. 96 (5), 1999-2008 (2009).
- Kolin, D. L., Wiseman, P. W. Advances in image correlation spectroscopy: measuring number densities, aggregation states, and dynamics of fluorescently labeled macromolecules in cells. Cell Biochem. Biophys. 49 (3), 141-164 (2007).
- Digman, M. A., et al. Measuring fast dynamics in solutions and cells with a laser scanning microscope. Biophys. J. 89 (2), 1317-1327 (2005).
- Ritchie, K., et al. Detection of non-Brownian diffusion in the cell membrane in single molecule tracking. Biophys. J. 88 (3), 2266-2277 (2005).
- Voie, A. H., Burns, D. H., Spelman, F. A. Orthogonal-plane fluorescence optical sectioning: three-dimensional imaging of macroscopic biological specimens. J. Microsc. 170, 229-236 (1993).
- Huisken, J., Swoger, J., Del Bene, ., Wittbrodt, F., J, E. H., Stelzer, Optical sectioning deep inside live embryos by selective plane illumination microscopy. Science. 305 (5686), 1007-1009 (2004).
- Wohland, T., Shi, X., Sankaran, J., Stelzer, E. H. Single plane illumination fluorescence correlation spectroscopy (SPIM-FCS) probes inhomogeneous three-dimensional environments. Opt. Express. 18 (10), 10627-10641 (2010).

