qPCRTag Analyse - En High Throughput, Real Time PCR-analysen for Sc2.0 Genotypebestemmelse
Summary
Designer chromosomes of the Synthetic Yeast Genome project, Sc2.0, can be distinguished from their native counterparts using a PCR-based genotyping assay called PCRTagging, which has a presence/absence endpoint. Here we describe a high-throughput real time PCR detection method for PCRTag genotyping.
Abstract
Den Syntetisk Gær Genome Project (Sc2.0) har til formål at bygge 16 designer gær kromosomer og kombinere dem til en enkelt gærcelle. Til dato en syntetisk kromosom, synIII 1, og en syntetisk kromosom arm, synIXR 2, er blevet konstrueret, og deres in vivo funktion valideret i fravær af de tilsvarende vildtype kromosomer. Et vigtigt træk i Sc2.0 kromosomer er indførelsen af PCRTags, som er korte, re-kodede sekvenser i åbne læserammer (ORF'er), der muliggør differentiering af syntetiske kromosomer fra deres vildtype modstykker. PCRTag primere annealer selektivt til enten syntetiske eller vildtype kromosomer og tilstedeværelsen / fraværet af hver type DNA kan testes under anvendelse af en simpel PCR-assay. Standard udlæsningen af PCRTag assayet er at vurdere tilstedeværelse / fravær af amplikoner ved agarosegelelektroforese. Men med en gennemsnitlig PCRTag amplicon densitet på en pr 1,5 kb og agenome størrelse ~ 12 Mb, vil den færdige Sc2.0 genom kode omkring 8.000 PCRTags. For at forbedre gennemløb, har vi udviklet et real time PCR-baseret detektion assay for PCRTag genotypebestemmelse, som vi kalder qPCRTag analyse. Arbejdsgangen specificerer 500 nl reaktioner i en 1536 flerbrøndsplade, giver os mulighed for at teste op til 768 PCRTags med både syntetiske og vilde typen primerpar i en enkelt eksperiment.
Introduction
Sc2.0 eller syntetiske Gær Genome Project ( www.syntheticyeast.org ), har sat det mål at designe og bygge en helt syntetisk eukaryot genom. Brug af stærkt curated genom-sekvensen af Saccharomyces cerevisiae 3 som udgangspunkt, idet hver af de seksten lineære kromosomer er blevet re-designet til at opfylde et sæt design principper, der angiver at opretholde celle fitness, forbedre genom stabilitet og øget genetisk fleksibilitet. For eksempel, er destabiliserende elementer som gentagelser slettet fra Sc2.0 kromosomer. Alle forekomster af TAG stopcodoner er re-kodet til TAA at "frigøre" en codon i den endelige belastning for indførelsen af en ikke-genetisk kodet aminosyre. Derudover et inducerbart evolution-system, Scramble, muliggjort af Cre-lox-systemet, tillader hidtil uset evne til at skabe afledte genomer med nye strukturer 4.
<p class="Jove_content"> En anden stor designelement i Sc2.0 genomet er indførelsen af PCRTags, der tjener som DNA-vandmærker at muliggøre sporing af syntetiske og vildtype-DNA. PCRTags er korte, Re-kodede segmenter i ORF på syntetiske kromosomer; mens PCRTag sekvenserne afviger på DNA-niveau mellem syntetiske og vildtype kromosomer, de kodede proteiner er identiske i aminosyresekvens og således formodentlig funktion. PCRTag sekvenser er specielt konstrueret som primer bindingssteder at lette selektiv amplifikation (figur 1A). Design PCRTag udføres under anvendelse af "mest anderledes" algoritme i GeneDesign 5,6, hvor produktet er recoded syntetiske sekvenser, der typisk ~ 60% anderledes end de native sekvenser (minimum 33%) med smeltetemperaturer mellem 58 ° C og 60 ° C og amplikon længder mellem 200-500 basepar 2. Omkodning er ikke tilladt inden de første 100 bp af hver ORF, da disse regioner er kendt for athar særlige præferencer med hensyn til kodonanvendelse 7. Tilsammen udgør disse design regler favoriserer høje ydeevne næsten alle PCRTags under et enkelt sæt PCR betingelser, hvorved syntetiske og vilde typen PCRTag primerpar udelukkende binder og forstærke syntetisk og indfødte DNA, henholdsvis (figur 1B).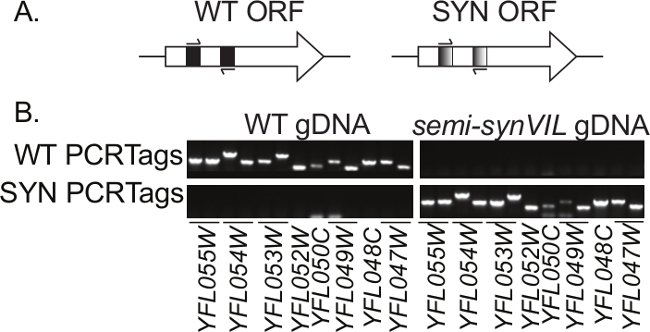
Figur 1:. PCRTag skematiske (A) PCRTags er re-kodede sekvenser i åbne læserammer (ORF) af gener på Sc2.0 kromosomer. (B) Syntetisk (SYN) og vildtype (WT) PCRTag primere udelukkende binde og forstærke syntetisk og genomisk vildtype-DNA (gDNA), henholdsvis. Vist her er en analyse af en ~ 30 kb segment af venstre arm af kromosom seks, teste tretten PCRTag primerpar ved hjælp af enten WT eller semi-synVIL2 gDNA som skabelon. I mange tilfælde et enkelt ORF koder mere end en PCRTag. Tilstedeværelse / fravær af PCRTag amplikoner vurderes via agarosegelelektroforese. PCRTag amplikoner varierer i størrelse fra 200 bp til 500 bp. De hurtigere migrerende arter på bunden af pladerne er primerdimerer.
PCRTag analyse har vist sig at være et vigtigt redskab i samlingen af Sc2.0 kromosomer. I et typisk forsøg 30-50 kb af syntetisk DNA, der koder 20-30 PCRTags, transformeres til gærceller til at erstatte det tilsvarende vildtype-DNA 1,2,8. PCRTag analyse anvendes derefter til at identificere transformanter, som koder for syntetiske, men ikke vildtype PCRTags spænder det segment af DNA, eller såkaldt "vindere". Det er normalt nødvendigt at teste flere transformanter for at identificere "vindere", så gennemløb og omkostningerne ved PCRTag analyse er vigtige overvejelser. Øjeblikket to Sc2.0 kromosomer er afsluttet (synIII 1 og synIXR 2), som repræsenterer mindre end 10% af Sc2.0 genomet, altHough mere end halvdelen af de resterende kromosomer undergår i øjeblikket syntese og samling. Omfanget af PCRTag som kræves for dette projekt er hurtigt hurtigere end evnen til at køre geler og manuelt score tilstedeværelsen af syntetisk DNA og fravær af vildtype-DNA.
For at forbedre gennemløb af PCRTag analysen har vi udviklet et workflow ved hjælp af real time PCR til at omgå anvendelsen af agarosegelelektroforese. Arbejdsgangen gør brug af en bulk væskedispenser at distribuere qPCR mastermiksens i hver brønd i en 1.536 flerbrøndsplade, nanoskala akustisk væskedispenser at overføre template-DNA og primere og en 1.536 qPCR thermocycler, tillader os at miniaturisere reaktioner til 500 nl og maksimere throughput. Desuden analyse kan automatiseres. Denne type af high throughput genotyping protokol bør generaliseres til ethvert projekt, der kræver analyse af mange kloner ved multiple loci.
Protocol
Representative Results
Discussion
Inkorporering af real time PCR detektion i PCRTag genotypebestemmelsesassay er en vigtig udvikling for Sc2.0 projektet, da det giver væsentligt højere gennemløb. Den tidligere arbejdsgang angivne 2,5 pi reaktioner i 384 brønds PCR-plader, 1,5 timer termisk cykling køretid, agarosegelelektroforese, og manuel annotation af gelen.
Arbejdsgangen præsenteres her, kaldet qPCRTag analyse, overvinder flere store flaskehalse. Første, kondenserer en qPCRTag køre 4 x 384 brønds plader i en enkelt eksperiment, der kan behandles, start til slut (plade oprettet plus køretid), i omkring en time. Det er væsentligt at bemærke, at reagenset pris pr godt for qPCRTag analyse er på niveau med den nederste gennemløb agarosegel tilgang. Men ved at omgå gelelektroforese og manuel anmærkning, den qPCRTag workflow giver betydelige besparelser i tid og arbejdskraft, som er de store fordele. Vigtigere at qPCRTag workflow er entirely kompatibel med automatisering.
Et stort problem med brugen af tidstro detektion som udgangssignalet fra PCRTag assayet er antallet af falske positive og falske negative. Da PCRTag primere ikke blev oprindeligt udviklet til brug i real time PCR, forventes det, at ikke alle primerpar vil være egnet til brug med denne udgang. Til dette formål er det vigtigt at validere funktionen og specificiteten af alle PCRTag primerpar til at udelukke den delmængde, der ikke fungerer i realtid assay up front. For eksempel kromosom 3 PCRTag falske positiver og negativer er biprodukter og-large reproducerbar i real time PCR data (figur 2 og 3), og disse kan udelukkes fra yderligere analyser. Endvidere primerpar kendt for at svigte (vurderet ved gelelektroforese og vist i figur S6 og S7 af Annaluru et al. 1) kan også udelukkes. Dette opnås nemt blot excluding defekte primerpar ved oprettelsen af akustiske transfer-protokollen.
Som de fleste analyser med høj kapacitet, vi agter at bruge realtid PCRTag detektion som en primær skærmen for at identificere transformanter, der fortjener yderligere downstream validering. Efterfølgende vil den gyldne standard for sekundær screening forblive PCRTag analyse med gelelektroforese som udlæsning. Ud over anvendelsen af PCRTag analyse for Sc2.0, der kombinerer state-of-the-art nanoskala væske håndteringssystemer med højt gennemløb real time PCR-teknologi muliggør hurtig og automatiseret analyse og har potentiale til at påvirke mange områder. For eksempel kunne denne arbejdsgang anvendes til high throughput screening af biblioteket, infektiøs sygdomsdiagnose, microbiome analyse og banebrydende genom redigering tilgange forsøger at ændre flere loci samtidig.
Declarações
The authors have nothing to disclose.
Acknowledgements
Dette arbejde blev støttet delvist af National Science Foundation Grant MCB-0718846 og Defense Advanced Research Projects Agency Contract N66001-12-C-4020 (til JDB). LAM blev finansieret af en postdoc stipendium fra naturvidenskab og teknik Forskningsråd Canada. Offentliggørelse af denne artikel er sponsoreret af Roche.
Materials
| Yeast gDNA prep | |||
| yeast gDNA | custom | custom | template for real time PCR |
| Acid-washed glass beads (0.5mm) | Sigma | G8772 | yeast cell lysis |
| Ultrapure Phenol:Chloroform:Isoamyl Alcohol (25:24:1, v/v) | Invitrogen | 15593-031 | yeast cell lysis |
| 5432 Mixer | Eppendorf | 5432 | yeast cell lysis |
| Microcentrifuge 5417R | Eppendorf | 22621807 | yeast cell lysis |
| Qubit 3.0 Fluorometer | Life Technologies | Q33216 | gDNA quantification |
| Qubit dsDNA BR Assay Kit | Life Technologies | Q32850 | gDNA quantification |
| Labcyte 384PP plate | Labcyte | P-05525 | gDNA source plate |
| DNA Green Mastermix prep and dispensing | |||
| LightCycler 1536 DNA Green | Roche | 5573092001 | real time PCR mastermix |
| 1.5mL Microfuge Tube Holder | ARI | EST BD060314-1 | microfuge tube holder for deck of Cobra |
| LightCycler 1536 Multiwell Plate | Roche | 5358639001 | |
| Cobra liquid handling system | Art Robbins Instruments | 630-1000-10 | dispense qPCR master mix into 1536 plate |
| PCR Plate Spinner | VWR | 89184-608 | cenrifugation of 1536 plate |
| Template and primer dispensing | |||
| PCRTag primers | IDT | custom | premixed forward and reverse, [50uM] each |
| TempPlate pierceable sealing foil, sterile | USA Scientific | 2923-0110 | temporary seal for PCRTag primer plates |
| Labcyte LDV 384 well plate | Labcyte | LP-0200 | pre-mixed primer source plate |
| Echo 550 Liquid Handler | Labcyte | transfer 2.5nL drops of primer and template DNA into 1536 plate | |
| Plateloc Thermal Microplate Sealer | Agilent | G5402-90001 | heat seal for 1536 plate prior to LC1536 run |
| Clear Permanent Seal | Agilent | 24212-001 | optically clear heat seal for LC1536 multiwell plate |
| PlateLoc Roche/LightCycler 1536 Plate Stage | Agilent | G5402-20008 | can substitute ~2mm thick washers |
| Sorvall Legend XTR | Thermo Scientfic | 75-004-521 | centrifuge heat sealed 1536 plate |
| Industrial Air Compressor | Jun Air | 1795011 | to run the Echo and Heat Sealer |
| Real Time PCR | |||
| LightCycler 1536 | Roche | requires 220V outlet |
Referências
- Annaluru, N., et al. Total synthesis of a functional designer eukaryotic chromosome. Science. 344 (6179), 55-58 (2014).
- Dymond, J. S., et al. Synthetic chromosome arms function in yeast and generate phenotypic diversity by design. Nature. 477 (7365), 471-476 (2011).
- Goffeau, A., et al. Life with 6000 genes. Science. 274 (5287), 546-547 (1996).
- Dymond, J., Boeke, J. The Saccharomyces cerevisiae SCRaMbLE system and genome minimization. Bioeng Bugs. 3 (3), 168-171 (2012).
- Richardson, S. M., Nunley, P. W., Yarrington, R. M., Boeke, J. D., Bader, J. S. GeneDesign 3.0 is an updated synthetic biology toolkit. Nucleic Acids Res. 38 (8), 2603-2606 (2010).
- Richardson, S. M., Liu, S., Boeke, J. D., Bader, J. S. Design-A-Gene with GeneDesign. Methods Mol Biol. 852, 235-247 (2012).
- Lajoie, M. J., et al. Probing the limits of genetic recoding in essential genes. Science. 342 (6156), 361-363 (2013).
- Jovicevic, D., Blount, B. A., Ellis, T. Total synthesis of a eukaryotic chromosome: Redesigning and SCRaMbLE-ing yeast. Bioessays. 36 (9), 855-860 (2014).
- Dymond, J. S. Preparation of genomic DNA from Saccharomyces cerevisiae. Methods Enzymol. 529, 153-160 (2013).
- Brachmann, C. B., et al. Designer deletion strains derived from Saccharomyces cerevisiae S288C: a useful set of strains and plasmids for PCR-mediated gene disruption and other applications. Yeast. 14 (2), 115-132 (1998).

