临床样品RNA病毒的无偏深度测序
Summary
This protocol describes a rapid and broadly applicable method for unbiased RNA-sequencing of viral samples from human clinical isolates.
Abstract
在这里,我们勾勒出下一代RNA测序协议,使从头组件和从临床和生物学来源收集的病毒基因组的帧内主机变种呼叫。该方法是无偏的和普遍的;它采用cDNA合成随机引物,并且需要病毒序列内容的先验知识。图书馆建设之前,选择基于H-RNA酶消化来消耗多余的RNA – 包括聚(RA)载体和核糖体RNA – 从病毒RNA样品。选择性耗尽同时提高数据质量和独特的数目在病毒RNA测序文库的读取。此外,基于转座-'tagmentation'步骤在协议中使用,因为它减少总库施工时间。该协议使快速深度测序超过600拉沙和埃博拉病毒样本,包括来自血液和组织分离,并广泛适用于其它微生物基因组学研究的集合。
Introduction
从临床来源的病毒的新一代测序可以通知传播和感染的流行病学,以及帮助支持新的诊断,疫苗和治疗的发展。使用随机引物合成cDNA已经允许从发散的,共同的侵染的基因组或甚至新的病毒1,2的检测和组装。与其他方式偏见,有害的污染物,会占用大量的测序读取和测序结果产生负面影响。主机和聚(RA)的载体RNA存在于许多现有的病毒样品收集污染物。
该协议描述了基于偏总RNA-SEQ深度测序RNA病毒基因组的高效率和成本效益的方法。该方法利用一种核糖核酸酶H选择性枯竭步骤3,删除不需要的主机核糖体和载体RNA。选择性耗竭丰富了病毒内容( 图1),提高了测序数据的整体质量( 图2)从临床样品。此外,tagmentation被应用到,因为它显著降低了图书馆的建设时间的协议。这些方法已被用于快速产生埃博拉病毒和拉沙病毒基因组2,4,5的大型数据集,并且可以用于研究广泛的RNA病毒。最后,该方法不限于人类样品;选择性消耗的效用已证明来自拉沙感染啮齿动物和非人类灵长类动物疾病模型5,6-收集组织样品。
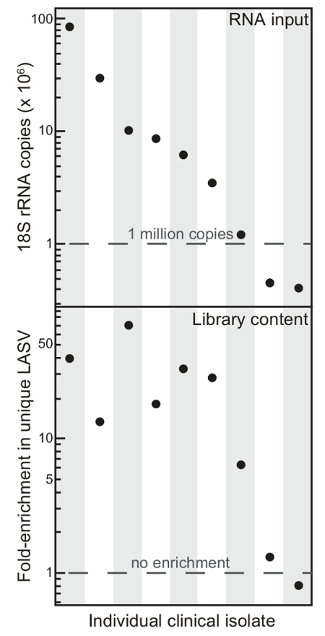
图1.总RNA内容反映拉沙病毒含量采用选择性枯竭的富集。从九个不同的临床分离后,开始枯竭rRNA的整体内容(RNA输入)和独特的拉沙病毒(LASV)富集读取(库内容)。这个数字已经从6修改<em> 点击此处查看该图的放大版本。
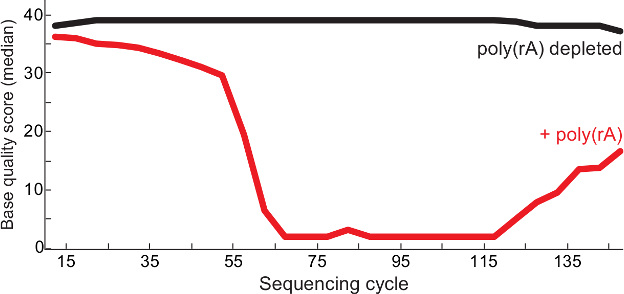
图2.更高质量测序后载体的RNA耗尽。每聚测序循环(RA)中值碱品质-contaminated拉沙病毒库(红色),并从质量控制报告13对照(无载体库观察,黑色)。双方念1,阅读配对末端的2读取合并库中的BAM文件,并在每个基地的质量分数表示。这个数字已经从6修改。 请点击此处查看本图的放大版本。
病毒RNA-SEQ协议的细节建设库直接从提取从临床和生物样品收集的RNA。为了确保人身安全,所有病毒血清,血浆和组织样品应前RNA提取适当的缓冲灭活。在有些失活和提取试剂盒,载体聚(RA)的RNA包括在内;这将在最初的RNA酶H选择性消耗步骤中除去。基于完全恢复,载体RNA的预期浓度为100纳克/微升。在协议中,110纳克/微升寡聚dT的RNA(1.1倍载流子浓度)用于耗竭。如果聚(RA)的载体是不存在于样品中,那么寡(dT)不应之前耗尽加入。
以下协议被设计用于PCR板格式24反应(高达250微升体积)。该协议的早期版本据报道,Matranga 等。6。
Protocol
Representative Results
Discussion
概述的方法能够健壮,通用,快速排序,并用于2014年爆发期间2,4测序埃博拉病毒。通过偶合选择性消耗和cDNA合成用tagmentation文库构建,整个过程的时间是通过从前面的适配器连接方法〜2天缩短。最近,该协议受雇于国际合作者和其他人取得了巨大成功和15,16将被部署到西非的实验室,以支持当地基于基因组学研究的研究和诊断17。
这里所描述的协议使用随机引物来制备cDNA为病毒RNA-SEQ库。不同于以往的病毒RNA-SEQ方法,它不需要序列数据或复杂和费时的引物设计为特定的病毒或分化体的先验知识。该方法可以适用于任何病毒RNA样品。例如,它被用来产生从两个埃博拉病毒内容和拉沙样品6。该协议也可以被用于主机转录,宏基因组和病原体发现测序项目1。
该协议的一个关键步骤是针对核糖核酸酶H消化,高通量,从病毒样本去除多余的载体和宿主RNA低成本的方法。该协议的选择性耗尽步骤使用了许多部件,并需要技巧性和准确性。额外的时间和精力应该在初始设置期间服用。
因为大多数临床血清和血浆样品通常具有非常少的核酸材料,污染和样品损失是常见的。为了避免这些问题,应特别注意使用此协议时作出。首先,RNA是非常容易退化;因此,所有的区域应清洁,无核酸酶。第二,以确定适用于该协议使用的样品,应该用于定量5,6-两种宿主RNA和病毒定量RT-PCR测定</suP>。当从协议测序结果测序成功比较输入量( 即,代全病毒装配足够的数据)与含有至少100pg的总RNA和病毒的1000份样本相关。应避免第三,暴露于核酸环境来源。这里列出的协议是在安全防范生物安全柜和限制环境污染物进行。此外,我们的组和其他已经注意到商业酶可以是低输入样本6,18在污染细菌的核酸的另一个来源。用干净的工作空间( 如 PCR罩,生物安全柜)和阴性对照( 例如 ,水或缓冲液)将有助于减轻分别和跟踪污染。用于与样品<100pg的总RNA,只聚(RA)载体RNA,不rRNA基因,应该被耗尽,以确保高质量的测序结果,同时限制材料的损失。对于非常低输入样本,cDNA的扩增方法可以是更合适的19,虽然聚(RA)载体应之前的cDNA合成中除去。
主机的rRNA的耗尽丰富在测序文库的病毒含量,并适用于不同的样本的集合,包括血清或血浆,和多种类型的来自啮齿类和非人灵长类5,6-组织。在非人类生物,读取对准28S rRNA的仍然耗尽后,提示28S rRNA的是人类和其它物种6,20之间不太保守。当使用这种方法与非人类分离,它可能有必要对特定的主机3,21的发散rRNA序列互补的DNA寡核苷酸来补充。
由于该协议是公正的,病毒会读取仅代表总库内容的一小部分。虽然rRNA基因是宿主RNA品种最丰富,仅rRNA基因的一小部分读取(0; 1%)被发现选择性耗尽之后,所有其它宿主RNA( 例如 ,mRNA)的仍将耗尽后及可能占许多测序从样品中读取。因此,“过采样”( 即 oversequencing)单个图书馆需要,以有足够的覆盖面为病毒组装和变异电话。对于我们的研究中,我们试图序列每个样品〜20000000读取具有用于病毒基因组和相关的变异体的分析深度不够以及宏基因组内容2,5。对于宏基因组和病原体发现研究中,要注意的是污染宿主DNA通过DNA酶消化除去是很重要的。因此,包含的DNA基因组的病毒和其他病原体的过程中会丢失,但是RNA中间体可以仍然进行测序。
Declarações
The authors have nothing to disclose.
Acknowledgements
This work has been funded in part with Federal funds from the National Institutes of Health, Office of Director, Innovator (No.: DP2OD06514) (PCS) and from the National Institute of Allergy and Infectious Diseases, National Institutes of Health, Department of Health and Human Services, under Contracts (No:HHSN272200900018C, HHSN272200900049C and U19AI110818).
Materials
| 96-Well PCR Plates | VWR | 47743-953 | |
| Strips of Eight Caps | VWR | 47745-512 | |
| Nuclease-free water | Ambion | AM9937 | 50 ml bottle |
| TURBO DNase | Ambion | AM2238 | post RNA extraction step, 2 U/µL, buffer included |
| PCR cycler | any PCR cyclers | ||
| Agencourt RNAClean XP SPRI beads | Beckman Coulter Genomics | A63987 | beads for RNA cleanup |
| Real Time qPCR system | any system | ||
| DynaMag-96 Side Skirted Magnet | Invitrogen | 12027 | |
| 70% Ethanol | prepare fresh | ||
| qRT-PCR primers | IDT DNA | see Table 2 | |
| 5M NaCl | Ambion | AM9760G | |
| 1M Tris-HCl pH 7.4 | Sigma | T2663-1L | |
| 1M Tris-HCl pH 7.5 | Invitrogen | 15567-027 | |
| 1M MgCl2 | Ambion | AM9530G | |
| Linear acrylamide | Ambion | AM9520 | |
| DNA oligos covering entire rRNA region | IDT DNA | see Table 3, order lab-ready at 100 µM | |
| Oligo (dT) | IDT DNA | 40 nt long, desalted | |
| Hybridase Thermostable RNase H | Epicentre | H39100 | |
| RNase-free DNase Kit | Qiagen | 79254 | post selective depletion step |
| SUPERase-In RNase Inhibitor | Ambion | AM2694 | |
| Random Primers | Invitrogen | 48190-011 | mostly hexamers |
| 10 mM dNTP mix | New England Biolabs | N0447L | |
| SuperScript III Reverse Transcriptase | Invitrogen | 18080-093 | with first-strand buffer, DTT |
| Air Incubator | any air incubator cyclers | ||
| NEBNext Second Strand Synthesis (dNTP-free) Reaction Buffer | New England Biolabs | B6117S | 10x |
| E. coli DNA Ligase | New England Biolabs | M0205L | 10 U/μl |
| E. coli DNA Polymerase I | New England Biolabs | M0209L | 10 U/μl |
| E. coli RNase H | New England Biolabs | M0297L | 2 U/μl |
| 0.5M EDTA | Ambion | AM9261 | |
| Agencourt AMPure XP SPRI beads | Beckman Coulter Genomics | A63881 | beads for DNA cleanup |
| Elution Buffer | Qiagen | 10 mM Tris HCl, pH 8.5 | |
| Quant-iT dsDNA HS Assay Kit | Invitrogen | Q32854 | |
| Qubit fluorometer | Invitrogen | Q32857 | |
| Nextera XT DNA Sample Prep Kit | Illumina | FC-131-1096 | |
| Nextera XT DNA Index Kit | Illumina | FC-131-1001 | |
| Tapestation 2200 | Agilent | G2965AA | |
| High Sensitivity D1000 reagents | Agilent | 5067-5585 | |
| High Sensitivity D1000 ScreenTape | Agilent | 5067-5584 | |
| BioAnalyzer 2100 | Agilent | G2939AA | |
| High Sensitivity DNA reagents | Agilent | 5067-4626 | |
| Library Quantification Complete kit (Universal) | Kapa Biosystems | KK4824 | alternative to tapestation, bioanalyzer for library quantification |
Referências
- Stremlau, M. H., et al. Discovery of novel rhabdoviruses in the blood of healthy individuals from West Africa. PLoS Negl Trop Dis. 9, e0003631 (2015).
- Gire, S. K., et al. Genomic surveillance elucidates Ebola virus origin and transmission during the 2014 outbreak. Science. 345, 1369-1372 (2014).
- Morlan, J. D., Qu, K., Sinicropi, D. V. Selective depletion of rRNA enables whole transcriptome profiling of archival fixed tissue. PLoS One. 7, e42882 (2012).
- Park, D. J., et al. Ebola Virus Epidemiology, Transmission, and Evolution during Seven Months in Sierra Leone. Cell. 161, 1516-1526 (2015).
- Andersen, K. G., et al. Clinical Sequencing Uncovers Origins and Evolution of Lassa Virus. Cell. 162, 738-750 (2015).
- Matranga, C. B., et al. Enhanced methods for unbiased deep sequencing of Lassa and Ebola RNA viruses from clinical and biological samples. Genome Biol. 15, 519 (2014).
- Tang, F., et al. RNA-Seq analysis to capture the transcriptome landscape of a single cell. Nat Protoc. 5, 516-535 (2010).
- Jiang, L., et al. Synthetic spike-in standards for RNA-seq experiments. Genome Res. 21, 1543-1551 (2011).
- . Kapa Biosystems Available from: https://www.kapabiosystems.com/product-applications/products/next-generation-sequencing-2/library-quantification/ (2015)
- . Illumina Technologies Available from: https://support.illumina.com/content/dam/illumina-support/documents/documentation/system_documentation/miseq/preparing-libraries-for-sequencing-on-miseq-15039740-d.pdf (2015)
- Kircher, M., Sawyer, S., Meyer, M. Double indexing overcomes inaccuracies in multiplex sequencing on the Illumina platform. Nucleic Acids Res. 40, 3 (2012).
- Trombley, A. R., et al. Comprehensive panel of real-time TaqMan polymerase chain reaction assays for detection and absolute quantification of filoviruses, arenaviruses, and New World hantaviruses. Am J Trop Med Hyg. 82, 954-960 (2010).
- Hu, Y., et al. Serial high-resolution analysis of blood virome and host cytokines expression profile of a patient with fatal H7N9 infection by massively parallel RNA sequencing. Clin Microbiol Infect. 21, 713 (2015).
- Simon-Loriere, E., et al. Distinct lineages of Ebola virus in Guinea during the 2014 West African epidemic. Nature. 524, 102-104 (2015).
- Folarin, O. A., Happi, A. N., Happi, C. T. Empowering African genomics for infectious disease control. Genome Biol. 15, 515 (2014).
- Blainey, P. C., Quake, S. R. Digital MDA for enumeration of total nucleic acid contamination. Nucleic Acids Res. 39, 19 (2011).
- Malboeuf, C. M., et al. Complete viral RNA genome sequencing of ultra-low copy samples by sequence-independent amplification. Nucleic Acids Res. 41, 13 (2013).
- Gonzalez, I. L., Sylvester, J. E., Smith, T. F., Stambolian, D., Schmickel, R. D. Ribosomal RNA gene sequences and hominoid phylogeny. Mol Biol Evol. 7, 203-219 (1990).
- Adiconis, X., et al. Comparative analysis of RNA sequencing methods for degraded or low-input samples. Nat Methods. 10, 623-629 (2013).

