De synthese van RGD-gefunctionaliseerde Hydrogels als een instrument voor therapeutische toepassingen
Summary
We present a protocol for the synthesis of RGD-functionalized hydrogels as devices for cell and drug delivery. The procedure involves copper catalyzed alkyne-azide cycloaddition (CuAAC) between alkyne-modified polyacrylic acid (PAA) and a RGD-azide derivative. The hydrogels are formed using microwave-assisted polycondensation and their physicochemical properties are investigated.
Abstract
The use of polymers as biomaterials has provided significant advantages in therapeutic applications. In particular, the possibility to modify and functionalize polymer chains with compounds that are able to improve biocompatibility, mechanical properties, or cell viability allows the design of novel materials to meet new challenges in the biomedical field. With the polymer functionalization strategies, click chemistry is a powerful tool to improve cell-compatibility and drug delivery properties of polymeric devices. Similarly, the fundamental need of biomedicine to use sterile tools to avoid potential adverse-side effects, such as toxicity or contamination of the biological environment, gives rise to increasing interest in the microwave-assisted strategy.
The combination of click chemistry and the microwave-assisted method is suitable to produce biocompatible hydrogels with desired functionalities and improved performances in biomedical applications. This work aims to synthesize RGD-functionalized hydrogels. RGD (arginylglycylaspartic acid) is a tripeptide that can mimic cell adhesion proteins and bind to cell-surface receptors, creating a hospitable microenvironment for cells within the 3D polymeric network of the hydrogels. RGD functionalization occurs through Huisgen 1,3-dipolar cycloaddition. Some PAA carboxyl groups are modified with an alkyne moiety, whereas RGD is functionalized with azido acid as the terminal residue of the peptide sequence. Finally, both products are used in a copper catalyzed click reaction to permanently link the peptide to PAA. This modified polymer is used with carbomer, agarose and polyethylene glycol (PEG) to synthesize a hydrogel matrix. The 3D structure is formed due to an esterification reaction involving carboxyl groups from PAA and carbomer and hydroxyl groups from agarose and PEG through microwave-assisted polycondensation. The efficiency of the gelation mechanism ensures a high degree of RGD functionalization. In addition, the procedure to load therapeutic compounds or biological tools within this functionalized network is very simple and reproducible.
Introduction
Hydrogelen driedimensionale netwerken gevormd door hydrofiele verknoopte polymeren, die natuurlijk of synthetisch, en gekenmerkt door een opvallende driedimensionale structuur. Deze apparaten zijn steeds aantrekkelijker in de biomedische gebied van drug delivery, tissue engineering, gen vervoerders en slimme sensoren 1,2. Inderdaad, het hoge watergehalte, evenals hun reologische en mechanische eigenschappen maken ze geschikte kandidaten zacht weefsel micromilieus nabootsen en ze doeltreffende instrumenten voor in water oplosbare cytokine of groeifactor levering. Een van de meest veelbelovende toepassing is als een injecteerbaar biomateriaal dragende cellen en bioactieve stoffen. Hydrogels kunnen celoverleving en controle stamcellen lot verbeteren door het houden en precies leveren van stamcellen regulerende signalen in een fysiologisch relevante manier, zoals waargenomen in in vitro pt in vivo experimenten 3,4. De belangrijkste voordeel hiervan is de mogelijkheidgeïnjecteerde cellen in de zone van inoculatie (in situ) te handhaven, het minimaliseren van de hoeveelheid cellen die de stippellijn extravasates bladeren in de bloedsomloop stroom, migreren over het hele lichaam en verliest de goalmuur 5. De stabiliteit van de hydrogel driedimensionale netwerken vanwege de verknopingsplaatsen, gevormd door covalente bindingen of cohesieve krachten tussen de polymeerketens 6.
In dit kader, orthogonale selectieve chemie toegepast op polymeerketens is een veelzijdige tool in staat om hydrogel voorstellingen 7 verbeteren. Inderdaad, kan de modificatie van polymeren met geschikte chemische groepen leiden tot goede chemische, fysische en mechanische eigenschappen te verschaffen levensvatbaarheid van de cellen en hun gebruik in weefselvorming verbeteren. Op dezelfde wijze, onder de technieken om cellen of groeifactoren laden in de gelmatrix, het gebruik van de RGD peptide maakt verbeteringen in celadhesie en overleving. RGD tripeptide is bestaandevan arginine, glycine en asparaginezuur, die veruit de meest effectieve en vaak werkzaam tripeptide vanwege zijn vermogen om meerdere celadhesie receptoren richten en de biologische gevolgen cel verankering, en de levensvatbaarheid 8,9. In dit werk, is de synthese van RGD-gefunctionaliseerd hydrogels bestudeerd met als doel het ontwerpen netwerken gekenmerkt door voldoende biochemische eigenschappen voor een gastvrije micro cel.
Het gebruik van microgolfstraling in hydrogel synthese biedt een eenvoudige procedure om nevenreacties te minimaliseren en het verkrijgen van hogere reactiesnelheden en opbrengsten in een kortere tijdsperiode in vergelijking met de conventionele thermische processen 10. Deze methode niet zuiveringsstappen en opbrengsten steriele hydrogels vanwege de interactie van de polymeren en de afwezigheid van organisch oplosmiddel in het 11 reactiesysteem vereisen. Daarom verzekert hoge percentages RGD gekoppeld aan het polymeernetwerk, omdat er geen modcaties nodig zijn om het polymeer chemische groepen die deze gelvorming. Carboxylgroepen van PAA en carbomeer en hydroxylgroepen van PEG en agarose, geven aanleiding tot de hydrogel driedimensionale structuur door een polycondensatiereactie. De genoemde polymeren worden toegepast voor de synthese van hydrogelen in het ruggenmergletsel reparatie 12 behandelingen. Deze apparaten, zoals in eerdere werken 13,14, vertonen een hoge biocompatibiliteit en mechanische en fysisch-chemische eigenschappen die die van vele levende weefsels en thixotrope aard lijken. Bovendien blijven zij gelokaliseerd in situ op het gebied van de injectie.
In dit werk worden PAA carboxylgroepen gemodificeerd met een alkynrest (figuur 1), en een RGD-azide verbinding gesynthetiseerd gebruikmakend van de reactiviteit van het tripeptide eindgroep NH2 met een vervaardigde chemische verbinding met de structuur (CH2) n – N 3 (<strong> Figuur 2). Vervolgens worden de gewijzigde PAA reageert met de RGD-azide vorm via CuAAC click reactie 15-17 (figuur 3). Het gebruik van een koper (I) -katalysator leidt tot belangrijke verbeteringen in zowel de reactiesnelheid en de regioselectiviteit. De CuAAC reactie wordt op grote schaal gebruikt in de organische synthese en in Polymer Science. Combineert een hoge efficiëntie en een hoge tolerantie voor de functionele groepen en het is beïnvloed door het gebruik van organische oplosmiddelen. Een hoge selectiviteit, een snelle reactietijd en een eenvoudige zuivering procedure laat het verkrijgen van stervormige polymeren, blokcopolymeren of kettingen enten gewenste delen 18. Deze klik strategie maakt het mogelijk om polymeren te wijzigen na polymerisatie de fysisch-chemische eigenschappen aanpassen aan biochemische uiteindelijke toepassing. De CuAAC experimentele omstandigheden gemakkelijk reproduceerbaar (de reactie is ongevoelig voor water, terwijl koper oxidatie minimaal optreden) en de aard vangevormd triazool zorgt voor stabiliteit van het product. Het gebruik van koper metaal kan worden beschouwd als een kritisch punt, vanwege de mogelijke toxische effect tegen cellen en in de biologische micro-omgeving, maar dialyse wordt gebruikt als een zuiveringswerkwijze om de volledige verwijdering van katalytische residuen mogelijk. Tenslotte PAA gemodificeerde RGD wordt gebruikt in de synthese hydrogel (figuur 4) en de fysisch-chemische eigenschappen van de resulterende netwerken worden onderzocht, teneinde de mogelijke functies van deze systemen cellen of geneesmiddelen dragers controleren.
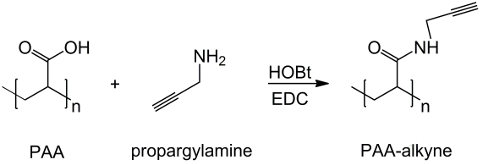
Figuur 1: PAA gemodificeerd alkyn synthese van een schema van PAA functionalisering met alkyngroep;. "n" geeft de monomeren met carboxylgroep reageren met propargylamine. Klik hier om te bekijkeneen grotere versie van deze figuur.
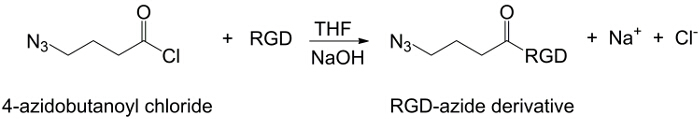
Figuur 2:.. RGD-azide synthese De synthese van RGD-azidederivaat Klik hier om een grotere versie van deze figuur te bekijken.
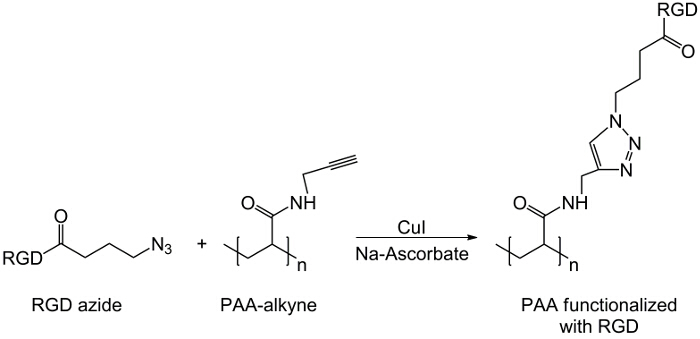
Figuur 3: Klik reactie Scheme of klik reactie tussen RGD-azide derivaat en alkyn-PAA.. Klik hier om een grotere versie van deze figuur te bekijken.
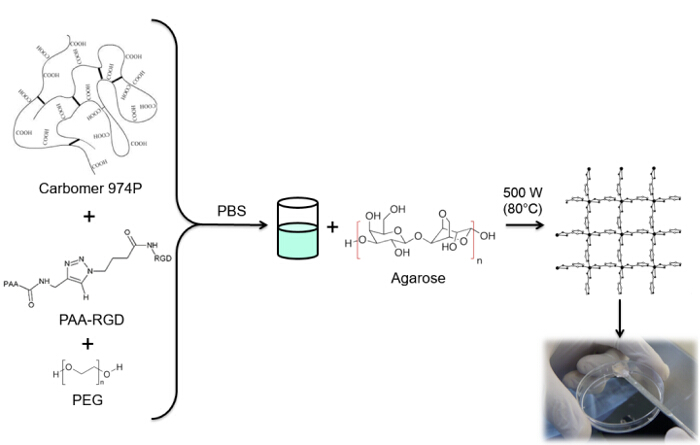
Figuur 4: Hydrogel synthesis. RGD gefunctionaliseerde hydrogel synthese procedure. Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
The PAA post-polymerization modification with alkyne moieties and the RGD functionalization with the azide group guarantee the formation of a stable bond between the polymer and the peptide. Indeed, triazole serves as a rigid linking unit among the carbon atoms, attached to the 1,4 positions of the 1,2,3-triazole ring and it cannot be cleaved hydrolytically or otherwise. In addition, triazole is extremely difficult to oxidize and reduce, unlike other cyclic structures such as benzenoids and related aromatic heterocycles<…
Declarações
The authors have nothing to disclose.
Acknowledgements
Auteurs danken Prof. Maurizio Masi voor een vruchtbare discussie en Miss Chiara Allegretti voor taal bewerken. onderzoek auteurs wordt ondersteund door Bando Giovani Ricercatori 2010 (Ministero della Salute GR-2010- 2312573).
Materials
| Poly(acrylic acid) solution average Mw ~ 100,000, 35 wt % in H2O | Sigma Aldrich | 523925 | CAS 9003-01-4 |
| Poly(ethylene glycol) 2,000 | Sigma Aldrich | 84797 | CAS 25322-68-3 |
| Carbomeer 974P | Fagron | 1387083 | |
| Agarose | Invitrogen Corp. | 16500-500 | UltraPure Agarose |
| RGD peptide | abcam | ab142698 | |
| 4-azidobutanoic acid | Aurum Pharmatech | Z-2421 | CAS 54447-68-6 |
| Oxalyl chloride | Sigma Aldrich | O8801 | CAS 79-37-8 |
| Propargylamine hydrochloride 95% | Sigma Aldrich | P50919 | CAS 15430-52-1 |
| Copper(I) iodide | Sigma Aldrich | 3140 | CAS 7681-65-4 |
| Sodium ascorbate | Sigma Aldrich | Y0000039 | CAS 134-03-2 |
| Phosphate buffered saline | Sigma Aldrich | P4417 | |
| Dialysis Membrane | Spectrum Laboratories, Inc. | 132725 | Spectra/Por 3 Dialysis Membrane Standard RC Tubing MWCO: 3,5 kD |
Referências
- Slaughter, B. V., Khurshid, S. S., Fisher, O. Z., Khademhosseini, A., Peppas, N. A. Hydrogels in Regenerative Medicine. Adv. Mater. 21 (32-33), 3307-3329 (2009).
- Rossi, F., Perale, G., Papa, S., Forloni, G., Veglianese, P. Current options for drug delivery to the spinal cord. Expert Opin. Drug Deliv. 10 (3), 385-396 (2013).
- Huebsch, N., et al. Harnessing traction-mediated manipulation of the cell/matrix interface to control stem-cell fate. Nat. Mater. 9 (6), 518-526 (2010).
- Mothe, A. J., Tam, R. Y., Zahir, T., Tator, C. H., Shoichet, M. S. Repair of the injured spinal cord by transplantation of neural stem cells in a hyaluronan-based hydrogel. Biomaterials. 34 (15), 3775-3783 (2013).
- Khetan, S., et al. Degradation-mediated cellular traction directs stem cell fate in covalently crosslinked three-dimensional hydrogels. Nat. Mater. 12 (5), 458-465 (2013).
- Ashley, G. W., Henise, J., Reid, R., Santi, D. V. Hydrogel drug delivery system with predictable and tunable drug release and degradation rates. Proc. Natl. Acad. Sci. U S A. 110 (6), 2318-2323 (2013).
- Rossi, F., van Griensven, M. Polymer Functionalization as a Powerful Tool to Improve Scaffold Performances. Tissue Eng. Part A. 20 (15-16), 2043-2051 (2014).
- Gould, S. T., Darling, N. J., Anseth, K. S. Small peptide functionalized thiol-ene hydrogels as culture substrates for understanding valvular interstitial cell activation and de novo tissue deposition. Acta Biomater. 8 (9), 3201-3209 (2012).
- Azagarsamy, M. A., Anseth, K. S. Wavelength-Controlled Photocleavage for the Orthogonal and Sequential Release of Multiple Proteins. Angew. Chem. Int. Edit. 52 (51), 13803-13807 (2013).
- Larrañeta, E., et al. Microwave-Assisted Preparation of Hydrogel-Forming Microneedle Arrays for Transdermal Drug Delivery Applications. Macromol. Mater. Eng. 300 (6), 586-595 (2015).
- Cook, J. P., Goodall, G. W., Khutoryanskaya, O. V., Khutoryanskiy, V. V. Microwave-Assisted Hydrogel Synthesis: A New Method for Crosslinking Polymers in Aqueous Solutions. Macromol. Rapid Comm. 33 (4), 332-336 (2012).
- Perale, G., et al. Multiple drug delivery hydrogel system for spinal cord injury repair strategies. J. Control. Release. 159 (2), 271-280 (2012).
- Rossi, F., Perale, G., Storti, G., Masi, M. A Library of Tunable Agarose Carbomer-Based Hydrogels for Tissue Engineering Applications: The Role of Cross-Linkers. J. Appl. Polym. Sci. 123 (4), 2211-2221 (2012).
- Frith, J. E., et al. An injectable hydrogel incorporating mesenchymal precursor cells and pentosan polysulphate for intervertebral disc regeneration. Biomaterials. 34 (37), 9430-9440 (2013).
- Kolb, H. C., Finn, M. G., Sharpless, K. B. Click chemistry: Diverse chemical function from a few good reactions. Angew. Chem. Int. Edit. 40 (11), (2001).
- Sacchetti, A., Mauri, E., Sani, M., Masi, M., Rossi, F. Microwave-assisted synthesis and click chemistry as simple and efficient strategy for RGD functionalized hydrogels. Tetrahedron Lett. 55 (50), 6817-6820 (2014).
- Ossipov, D. A., Hilborn, J. Poly(vinyl alcohol)-based hydrogels formed by "click chemistry". Macromolecules. 39 (5), 1709-1718 (2006).
- Truong, V., Blakey, I., Whittaker, A. K. Hydrophilic and Amphiphilic Polyethylene Glycol-Based Hydrogels with Tunable Degradability Prepared by "Click" Chemistry. Biomacromolecules. 13 (12), 4012-4021 (2012).
- Hou, R. Z., et al. New synthetic route for RGD tripeptide. Prep. Biochem. Biotechnol. 36 (3), 243-252 (2006).
- Rossi, F., Chatzistavrou, X., Perale, G., Boccaccini, A. R. Synthesis and Degradation of Agar-Carbomer Based Hydrogels for Tissue Engineering Applications. J. Appl. Polym. Sci. 123 (1), 398-408 (2012).
- Mauri, E., Rossi, F., Sacchetti, A. Tunable drug delivery using chemoselective functionalization of hydrogels. Mater. Sci. Eng. C. 61, 851-857 (2016).
- Joaquin, A., Peppas, N. A., Zoldan, J. Hydrogel Polymer Library for Developing Induced Pluripotent Stem Cell Derived Cardiac Patches. Tissue Eng. Part A. 20, S55-S55 (2014).
- Rossi, F., et al. Tunable hydrogel-Nanoparticles release system for sustained combination therapies in the spinal cord. Colloids Surf. B Biointerfaces. 108, 169-177 (2013).
- Kolb, H. C., Sharpless, K. B. The growing impact of click chemistry on drug discovery. Drug Discov. Today. 8 (24), 1128-1137 (2003).
- Ossipov, D. A., Yang, X., Varghese, O., Kootala, S., Hilborn, J. Modular approach to functional hyaluronic acid hydrogels using orthogonal chemical reactions. Chem. Commun. 46 (44), 8368-8370 (2010).
- Anderson, S. B., Lin, C. C., Kuntzler, D. V., Anseth, K. S. The performance of human mesenchymal stem cells encapsulated in cell-degradable polymer-peptide hydrogels. Biomaterials. 32 (14), 3564-3574 (2011).
- Caron, I., et al. A new three dimensional biomimetic hydrogel to deliver factors secreted by human mesenchymal stem cells in spinal cord injury. Biomaterials. 75, 135-147 (2016).
- Lee, J. W., Kim, H., Lee, K. Y. Effect of spacer arm length between adhesion ligand and alginate hydrogel on stem cell differentiation. Carbohyd. Polym. 139, 82-89 (2016).
- Liu, Y., Fan, Z., Wang, Y., Yu, L. Controlled Release of Low Molecular Protein Insulin-like Growth Factor-1 through Self-Assembling Peptide Hydrogel with Biotin Sandwich Approach. J.Biomed. Eng. 32 (2), 387-392 (2015).

