Génération de fusions de protéines fluorescentes dans<em> Candida</em> espèces
Summary
La modification du gène à médiation par PCR peut être utilisée pour générer des fusions de protéines fluorescentes dans des espèces de Candida, ce qui facilite la visualisation et la quantification des cellules de levure et les protéines. Ici, nous présentons une stratégie pour la construction d' une protéine de fusion fluorescente (ENO1-FP) dans Candida parapsilosis.
Abstract
Les espèces de Candida, colonisateurs répandues des voies intestinales et génito, sont la cause de la majorité des infections fongiques invasives chez les humains. Ainsi, les outils moléculaires et génétiques sont nécessaires pour faciliter l'étude de leurs mécanismes de pathogénicité. modification génique par PCR est une approche simple et rapide pour générer des protéines de marquage épitopique pour faciliter leur détection. En particulier, la protéine fluorescente (PF), les fusions sont des outils puissants qui permettent la visualisation et la quantification des deux cellules de levure et des protéines par microscopie à fluorescence et immunotransfert, respectivement. Les plasmides contenant des séquences codant pour la PF, ainsi que des gènes marqueurs nutritionnels qui facilitent la transformation des espèces de Candida, ont été produites à des fins de construction et d' expression dans la PF Candida. Ici, nous présentons une stratégie pour la construction d' une fusion FP dans une espèce de Candida. Les plasmides contenant l'antitache nourseothricinence gène marqueur de transformation (en NAT1) , ainsi que des séquences soit pour le vert, le jaune, ou la cerise vps (GFP, YFP, mCherry) sont utilisées conjointement avec des amorces qui comprennent des séquences spécifiques d' un gène dans une réaction en chaîne par polymérase (PCR) pour générer une cassette FP . Cette cassette spécifique du gène a la possibilité d'intégrer dans l'extrémité 3 'du locus du gène correspondant par l'intermédiaire d'une recombinaison homologue. Réussi fusion en cadre de la séquence PF dans le locus du gène d'intérêt est contrôlée génétiquement, suivie d'une analyse de l'expression de la protéine de fusion par microscopie et / ou des méthodes d'immuno-détection. En outre, pour le cas des protéines hautement exprimés, des fusions avec succès peuvent être criblés principalement par les techniques d'imagerie par fluorescence.
Introduction
Les espèces de Candida sont des champignons commensaux qui colonisent le tractus intestinal et génito de tous les humains. Dans des conditions d'immunodéficience, telles que celle se produisent avec une naissance prématurée ou d' effets immunosuppresseurs de traitements pour le cancer, les espèces de Candida peuvent devenir pathogènes opportunistes. Parmi les espèces de Candida, Candida albicans est le colonisateur fongique la plus répandue et provoque la majorité des infections fongiques invasives. D' autres espèces de Candida telles que C. glabrata, C. parapsilosis, C. tropicalis et C. kruseii aussi causer des infections graves chez les patients immunodéprimés, avec une certaine résistance intrinsèque présentant aux antibiotiques couramment utilisés anti-fongiques comme le fluconazole et l' amphotéricine B. Par conséquent, infections avec certaines de ces espèces sont observées plus fréquemment, en particulier chez les patients traités à titre prophylactique avec des agents anti-fongiques. Même avec un approprié et opportuntraitement nti-fongiques, les infections à Candida invasives continuent d'être associée à une morbidité et une mortalité significatives. En raison de l'importance des espèces de Candida dans la santé humaine, il y a un besoin d'outils moléculaires facilement disponibles qui permettent l'étude et l' élucidation de leurs mécanismes de pathogénicité.
Un outil important qui permet aux chercheurs de visualiser et de quantifier les cellules microbiennes et les protéines qu'ils expriment est la technologie de fusion FP. Réaction en chaîne par polymérase (PCR) de modification de gène médiée, tel que décrit dans le présent document, permet la construction de fusions, entre les séquences de PF et une séquence codante d'intérêt à son locus génomique protéine Candida. Une intégration stable de la construction facilite l'analyse de l'expression des protéines ainsi que la dynamique des protéines de localisation. Les plasmides contenant des séquences de PF, optimisés pour l' expression dans Candida albicans et que peuvent être utilisés dans la g médiée par PCRstratégie de modification ène ont été préalablement construits 2, 3, 4, 5. Plasmides contiennent PF transformation «cassettes»: une séquence de FP lié à un gène marqueur nutritionnel qui favorise la transformation de C. albicans et C. parapsilosis 2, 3, 4, 5, 6, 7. À l' heure actuelle plasmides disponibles contiennent une variété de gènes sélectionnables marqueurs nutritionnels (URA3 His1, ARG4) pour la transformation des souches auxotrophes, ainsi qu'un marqueur de résistance aux médicaments dominante (NAT1), ce qui facilite la transformation des souches cliniques dépourvues auxotrophies. En outre, des plasmides contiennent des options pour jusqu'à quatre séquences différentes de PF (vert [GFP], yellow [YFP], cyan [PCP] et de cerise [mCherry]) et soit une séquence de terminaison ADH1 pour la construction d' un carboxy-terminale des protéines de fusion, ou une séquence de promoteur pour la construction d'amino-terminale des protéines de fusion. Les amorces sont conçues avec une homologie avec l'ADN du plasmide entourant la cassette FP. En outre, les amorces contiennent également des séquences 5 ' d' extension portant une homologie avec le gène de levure d'intérêt à marquer, ce qui facilite l' intégration de la cassette dans le locus génomique par recombinaison homologue (figure 1). Spécifique du gène FP cassettes sont générés par PCR et ensuite transformés en cellules de Candida rendues compétentes pour l' absorption de l' ADN par un traitement avec de l' acétate de lithium.
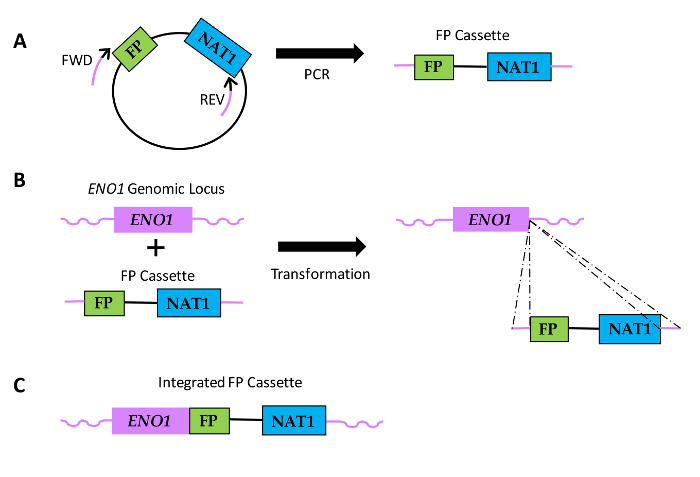
Figure 1: Schéma de la façon dont les fusions de séquences PF sont générées dans les espèces de Candida. (A) L' ADN de plasmide includes une séquence de PF et une séquence codant pour la résistance nourseothricine (NAT1). emplacements relatifs de l'avant (FWD) et inverse (REV) les amorces sont représentées, avec des parties noires des amorces indiquant la région d'homologie à la séquence plasmidique et les portions violet dénotant la région d'homologie spécifique d'un gène ou d'une extension d'amorce. Cassettes (B) PF sont transformées en Candida et à intégrer au sein du locus génomique de ENO1 par recombinaison homologue (lignes en pointillés). (C) résultant séquence de fusion FP à l'extrémité 3 du ENO1. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Ici, nous présentons un exemple de la protéine de fusion (ENO1-FP) constructions dans les espèces de Candida. Nous utilisons le marquage des plasmides contenant le gène marqueur de transformation NAT1 avec des séquences codant pour la GFP, YFP, oumCherry (figure 2). Ces plasmides sont utilisés conjointement avec des amorces de PCR pour générer des cassettes spécifiques de gènes qui facilitent la fusion de PCR à l'extrémité 3 'de ENO1, ayant pour résultat l' expression de ENO1 fusionnée à son extrémité carboxy à MF-terminale.
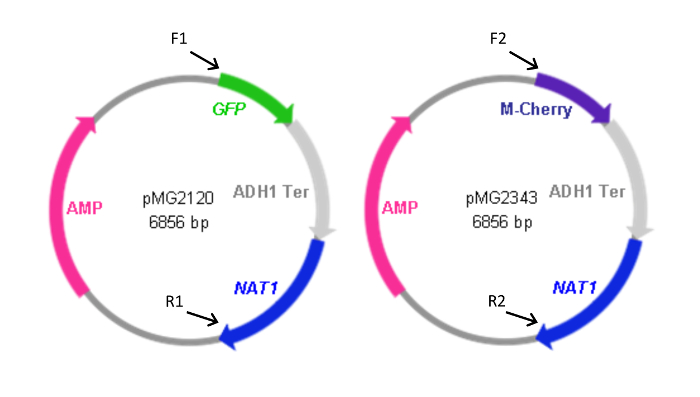
Figure 2: Carte de PF plasmides contenant la cassette. Vers l'avant (F) et arrière (R) des amorces utilisées pour générer les cassettes à partir des plasmides sont indiqués ainsi que la position relative de leur homologie avec les plasmides. Les séquences des amorces sont énumérées dans le tableau 1. F1 et R1 ont également été utilisés pour générer la cassette pYFP- NAT1. Le plasmide contenant la cassette YFP- NAT1 (pMG2263) est identique à pMG2120 à l'exception de la YFP à la place de la séquence de la GFP. Tailles de cassettes: GFP-Nat1, 3,7 kbp; mCherry- NAT1, 3,2 kbp; YFP- NAT1, 3.7 kpb. Ce chiffre a été modifié depuis Gerami-Nejad, et al. 4 S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Protocol
Representative Results
Discussion
Construction d'épitope tagged séquences dans les espèces de Candida en utilisant la stratégie de modification génique par PCR décrit ci – dessus peuvent être résumées comme un processus en trois étapes. Tout d'abord, la cassette est réalisée par PCR qui code à la fois la séquence souhaitée pour l'intégration et des régions homologues au locus d'insertion dans le génome de la levure. D'autre part, les cellules de levure à transformer chimiquement compétentes sont effectué…
Declarações
The authors have nothing to disclose.
Acknowledgements
Nous remercions N. Dean pour fournir la séquence mCherry FP d'origine, M. Gerami-Nejad pour la construction de plasmides, B. Larson pour l'assistance technique, et T. Heisel pour obtenir des conseils utiles lors de l'élaboration de ce projet. JB a été soutenu par le Prix du Conseil européen de la recherche avancée 340087 (RAPLODAPT). systèmes de microscopie et d'imagerie ont été fournis par la Fondation Université de Minnesota Pediatrics et l'Université du Minnesota Imaging Center.
Materials
| 100W mercury lamp | CHIU Technical Corporation | M-100T | |
| 95% Ethanol | Any | NA | |
| Adenine | Any | NA | |
| Ampicillin | Any | NA | |
| Carrier DNA | Ambion | AM9680 | Sheared Salmon Sperm DNA 10 mg/ml |
| CCD Camera | Photometrics | CoolSNAP HQ | |
| Conical Tube | Corning | 430828 | 50ml |
| Culture Tube Rotator | New Brunswick | 2013923 | TC-8, or Any Culture Tube Rotator |
| Deoxynucleotides (dNTP) PCR Grade | Any | NA | |
| Eppendorf Tubes | Eppendorf | 022363719, 022363212 | 0.5ml, 1.5ml |
| Erlenmeyer Flask | Fisher Scientific | 7250089 | 125ml |
| Ethylenediaminetetraacetic Acid (EDTA) | Any | NA | |
| Freezer (-80 °C ) | Thermo Electron Corporation | ULT-1386-9-V | Revco Ultima II |
| GFP, YFP and Texas Red Filter Sets | Chroma Technology Corporation | 49002, 86004v2, 49008 | |
| Glass culture tubes | Fisher Scientific | 1496126 | 75mm |
| HRP goat anti-mouse antibody | Santa Cruz Biotechnology | SC-2005 | |
| HRP goat anti-rabbit antibody | Santa Cruz Biotechnology | SC-2301 | |
| Incubator (30 °C ) | Any | NA | |
| Lithium Acetate | Any | NA | |
| Lysogeny Broth (LB) Media | Any | NA | |
| Magnesium Chloride | Any | NA | |
| Microcentrifuge | Eppendorf | 5415 D | |
| Microscope | Nikon | E600 | Nikon Eclipse E600 |
| Microscope Image Analysis Software | Universal Imaging Corporation | 6.3r7 | MetaMorph Software Series 6.3r7 |
| Mouse anti-GFP antibody | Roche | 11814460001 | |
| Nourseothricin | Fisher Scientific | 50997939 | |
| PCR Thermocycler | Applied Biosystems | 9700 | GeneAmp PCR System |
| PCR tubes | BioExpress, GeneMate | T-3035-1 | 0.2ml |
| Polyethylene Glycol 3350 | Any | NA | |
| Potassium Chloride | Any | NA | |
| Rabbit anti-mCherry antibody | BioVision | 5993-100 | |
| Refrigerator (4°C) | Any | NA | |
| Sodium Acetate | Any | NA | |
| Stereomicroscope | Nikon | SMZ1500 | |
| Table Top Centrifuge | Labnet | Z 400 | Hermle Z 400 |
| Taq DNA Polymerase | Any | NA | |
| Tris(hydroxymethyl)aminomethane (Tris) | Any | NA | |
| Vortex Mixer | Scientific Industries | SI-0236 | Vortex Genie 2 |
| Yeast Extract Peptone Dextrose (YPD) Media | Any | NA |
Referências
- Bendel, C. M. Colonization and epithelial adhesion in the pathogenesis of neonatal candidiasis. Semin. Perinatol. 27 (5), 357-364 (2003).
- Gerami-Nejad, M., Berman, J., Gale, C. A. Cassettes for PCR-mediated construction of green, yellow, and cyan fluorescent protein fusions in Candida albicans. Yeast. 18 (9), 859-864 (2001).
- Gerami-Nejad, M., Dulmage, K., Berman, J. Additional cassettes for epitope and fluorescent fusion proteins in Candida albicans. Yeast. 26 (7), 399-406 (2009).
- Gerami-Nejad, M., Forche, A., McClellan, M., Berman, J. Analysis of protein function in clinical C. albicans isolates. Yeast. 29 (8), 303-309 (2012).
- Gerami-Nejad, M., Hausauer, D., McClellan, M., Berman, J., Gale, C. Cassettes for the PCR-mediated construction of regulatable alleles in Candida albicans. Yeast. 21 (5), 429-436 (2004).
- Gonia, S., Larson, B., Gale, C. A. PCR-mediated gene modification strategy for construction of fluorescent protein fusions in Candida parapsilosis. Yeast. 33 (2), 63-69 (2016).
- Milne, S. W., Cheetham, J., Lloyd, D., Aves, S., Bates, S. Cassettes for PCR- mediated gene tagging in Candida albicans utilizing nourseothricin resistance. Yeast. 28 (12), 833-841 (2011).
- Ausubel, F. M., et al. . Current Protocols in Molecular Biology. , (1995).
- Wilson, R. B., Davis, D., Mitchell, A. P. Rapid hypothesis testing with Candida albicans through gene disruption with short homology regions. J. Bacteriol. 181 (6), 1868-1874 (1999).
- Pulver, R., et al. Rsr1 focuses Cdc42 activity at hyphal tips and promotes maintenance of hyphal development in Candida albicans. Eukaryotic Cell. 12 (4), 482-495 (2013).
- Falgier, C., et al. Candida species differ in their interactions with immature human gastrointestinal epithelial cells. Pediatr. Res. 69 (5), 384-389 (2011).
- Nosek, J., et al. Genetic manipulation of the pathogenic yeast Candida parapsilosis. Curr. Genet. 42 (1), 27-35 (2002).
- Zemanova, J., Nosek, J., Tomaska, L. High-efficiency transformation of the pathogenic yeast Candida parapsilosis. Curr. Genet. 45 (3), 183-186 (2004).
- Benjamin, D. K., et al. Neonatal candidiasis among extremely low birth weight infants: risk factors, mortality rates, and neurodevelopmental outcomes at 18 to 22 months. Pediatrics. 117 (1), 84-92 (2006).
- Kullberg, B. J., Arendrup, M. C. Invasive Candidiasis. N Engl J Med. 373 (15), 1445-1456 (2015).

