Amplificazione del vicino full-length provirus di HIV-1 per il sequenziamento di nuova generazione
Summary
Full-Length individuo proviral sequenziamento (Flip) fornisce un metodo efficiente e ad alta produttività per l’amplificazione e sequenziamento del singolo, vicino a full-length provirus di HIV-1 (intatto e difettoso) e permette per la determinazione del loro potenziale replica-competenza. Salti mortali supera i limiti delle precedenti analisi progettate per sequenziare il serbatoio latente di HIV-1.
Abstract
Il dosaggio di Full-Length individuali Proviral Sequencing (Flip) è un metodo efficiente e ad alta velocità progettato per amplificare e la sequenza singola, nei pressi di provirus di HIV-1 (intatto e difettoso), full-length. RIBALTA permette di determinare la composizione genetica di HIV-1 integrato all’interno di una popolazione delle cellule. Attraverso l’identificazione di difetti all’interno di sequenze provirale di HIV-1 che si verificano durante la trascrizione d’inversione, come grandi omissioni interne, fermata deleteri codoni/hypermutation, mutazioni frameshift e mutazioni/delezioni in cis elementi sostituti necessari salti mortali, per maturazione del virione, è in grado di identificare integrato provirus incapace di replica. Il dosaggio di salti mortali possa essere utilizzato per identificare provirus di HIV-1 che mancano di questi difetti e sono quindi potenzialmente replica-competente. Il protocollo di salti mortali coinvolge: lisi delle cellule di infezione da HIV-1, nested PCR di vicino a full-length provirus di HIV-1 (utilizzando primers mirati al HIV-1 5′ e 3′ LTR), purificazione del DNA e quantificazione, preparazione libreria per Next-generation Sequencing (NGS), NGS, Assemblea de novo di contigs proviral e un semplice processo di eliminazione per l’identificazione di provirus replica-competente. Salti mortali fornisce vantaggi rispetto ai tradizionali metodi progettati per sequenza integrato provirus di HIV-1, come singolo-proviral sequenziamento. Salti mortali amplifica e sequenze vicino a full-length provirus abilitazione competenza di replica deve essere determinato e utilizza anche meno primer di amplificazione, prevenire le conseguenze di mancate corrispondenze primer. Flip è uno strumento utile per la comprensione del panorama genetico dell’integrato provirus di HIV-1, soprattutto all’interno del serbatoio latente, tuttavia, il suo utilizzo può estendere a qualsiasi applicazione in cui è necessaria la composizione genetica di HIV-1 integrato.
Introduction
Caratterizzazione genetica del bacino di HIV-1 latente, che persiste in individui sulla terapia antiretrovirale a lungo termine (arte), è stato fondamentale per la comprensione che la maggioranza di provirus integrato sono difettosi e replica-incompetente1 , 2. durante il processo di trascrizione inversa, gli errori vengono introdotti nella sequenza proviral integrata. Alcuni meccanismi che generano difettosi sequenze proviral includono il soggetta a errori di enzima trascrittasi inversa dell’HIV-13, modello di commutazione4, e/o indotta da APOBEC hypermutation5,6. Due recenti studi hanno trovato che circa il 5% del provirus di HIV-1 isolato da individui sull’arte a lungo termine sono geneticamente intatti e potenzialmente replica-competente e può contribuire a rimbalzo rapido nei livelli del plasma HIV-1 al momento della cessazione dell’arte 1 , 2 , 7. gli studi precedenti hanno identificato che replica-competente provirus di HIV-1 persistere nelle ingenuo e riposo memoria CD4+ T cell sottoinsiemi (compresi central, transitorio e cellule effettrici T di memoria), che indica l’importanza di targeting per queste cellule in futuro strategie di eradicazione2,8,9.
Primi approfondimenti la distribuzione, la dinamica e la manutenzione del serbatoio latente di HIV-1 sono stati ottenuti attraverso l’utilizzo di metodi di sequenziamento singolo-proviral (SPS) che caratterizzano geneticamente sub-regioni del genoma dell’HIV-110 ,11,12,13. SPS è uno strumento versatile, in grado di sequenziare un singolo provirus di HIV-1 all’interno di una singola cellula infettata. Tuttavia, SPS è in grado di determinare la replica-competenza del provirus, poiché solo sequenze sub-genomica provirus regioni e manca che contengono grandi omissioni all’interno di siti di legame del primer. Uno studio precedente ha dimostrato che SPS sopravvaluta le dimensioni del serbatoio replica-competente di 13 – 17 volte tramite sequenziamento selettivamente intatte regioni sub-genomiche2.
Per affrontare le limitazioni di SPS, Ho et al. 4 e Bruner et al. 1 sviluppato analisi di sequenza vicino a full-length provirus di HIV-1. Questo ha permesso la frequenza di geneticamente intatti e potenzialmente replica-competente, provirus di HIV-1 in individui sull’arte a lungo termine deve essere determinato. Queste analisi amplificato ed ordinato (via Sanger sequenziamento) regioni sub-genomiche che sono stati poi assemblate per ottenere un provirus di HIV-1 sequenza di (intatto o difettoso). Tre limiti di questo approccio sono: 1) l’uso del primer di sequenziamento più aumenta il rischio di introdurre inavvertitamente difetti nella sequenza proviral, 2) primer disadattamento può impedire l’amplificazione del provirus particolare e 3) spesso i proviral intera sequenza non può essere risolto a causa della tecnicità di questi metodi.
Per superare le limitazioni delle esistenti analisi di sequenziamento proviral HIV-1 Full-Length, abbiamo sviluppato il Full –Length hondividual Proviral Sequencing (Flip) saggio. Flip è un sequenziamento di nuova generazione (NGS)-analisi di base che amplifica e sequenze vicino provirus di HIV-1 (intatto o difettosi) Full-Length in maniera efficiente e ad alta velocità. Salti mortali offre vantaggi rispetto le analisi precedenti, poiché limita il numero dei primer utilizzati; di conseguenza, diminuisce la probabilità di primer disadattamento, che può limitare la popolazione di provirus catturato o involontariamente introdurre difetti in una sequenza virale. Flip è anche tecnicamente meno impegnativo di saggi precedenti e prevede 6 passaggi principali: cellule Lisi 1) di infezione da HIV-1, 2) amplificazione del singolo provirus di HIV-1 tramite nested PCR eseguita a limitare la diluizione usando gli iniettori specifici per altamente conservato HIV-1 5′ e 3′ U5 LTR regione (Figura 1A), 3) purificazione e quantificazione dei prodotti amplificati, 4) preparazione della biblioteca di provirus amplificato per NGS, 5) NGS e 6) montaggio de novo di provirus in sequenza per ottenere contigs di ciascuno provirus individuali.
Sequenze generate da salti mortali possono subire un processo rigoroso di eliminazione per identificare quelli che sono geneticamente intatti e potenzialmente replica-competente (Figura 1)2. Provirus geneticamente intatti mancano tutti i difetti noti che provocare la generazione di un provirus replica-incompetente. Questi difetti comprendono: sequenze di inversione, ampie delezioni interne, codoni di stop hypermutation/deleteri, frameshift o mutazioni in 5′ imballaggio segnale o principali della giuntura sito donatore (MSD).
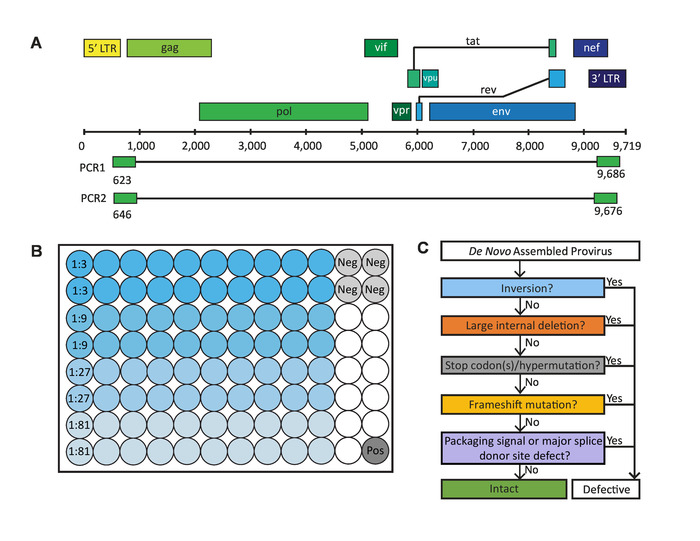
Figura 1: fasi critiche nell’analisi di sequenziamento proviral individuali Full-Length (Flip). (A) genoma di HIV-1 DNA con siti di legame del primer 5′ e 3′ regioni U5 LTR utilizzato da salti mortali per amplificare vicino a full-length provirus di HIV-1 (difettoso e intatto) tramite PCR annidata. (B) Layout di una piastra PCR a 96 pozzetti contenenti 80 pozzetti dei campioni (20 pozzi per ogni diluizione), 4 pozzi di controllo negativo e positivo 1 controllo bene. (C) processo di eliminazione utilizzato per identificare geneticamente intatti e potenzialmente replica-competente, provirus di HIV-1. Questa figura è stata modificata da Hiener et al. 2 . Clicca qui per visualizzare una versione più grande di questa figura.
Protocol
Representative Results
Discussion
Il dosaggio di salti mortali è un metodo efficiente e ad alta resa di amplificazione e sequenziamento singolo, vicino a full-length provirus di HIV-1. I fattori multipli e passaggi critici nel protocollo che influenzano il numero e la qualità delle sequenze ottenute sono state identificate. In primo luogo, il numero delle cellule e la frequenza di infezione di HIV-1 della popolazione cellulare influenzano il numero di provirus amplificato. Ad esempio, in una precedente pubblicazione, circa la metà come molte sequenze sono state ottenute dallo stesso numero di ingenuo CD4+ T cellule rispetto alla memoria effettrici CD4+ T cellule. Questo è perché le cellule naive in genere hanno una frequenza più bassa di infezione che di cellule effettrici memoria2. In secondo luogo, la lisi cellulare sono preferibile ai metodi di estrazione basata su colonne per l’ottenimento del DNA genomico non c’è alcun rischio di perdere del DNA nel processo di estrazione. Infine, come con qualsiasi analisi PCR-basata, impedendo la contaminazione è fondamentale. Zone separate pulite dovrebbero essere designate per la preparazione di mix master, manipolazione del DNA di genomic, aggiunta di controlli positivi, purificazione del DNA e quantificazione e preparazione di biblioteca. Ciò è particolarmente importante per singola copia saggi come quello qui presentato.
Implementazione del dosaggio FLIPS prima dovrebbe includere in esecuzione di un controllo positivo ad esempio plasmidi pNL4-3 piuttosto che campioni partecipanti. Questo permetterà per qualsiasi risoluzione dei problemi prima che l’uso di cellule positive del HIV-1, come le sequenze ottenute possono essere paragonate alle sequenze di riferimento disponibili per questi plasmidi. Quando si utilizza cellule positive del HIV-1, è importante considerare il sottotipo di HIV-1 (primer disegnati per salti mortali sono specifici al sottotipo B) e la frequenza di infezione della popolazione cellulare se poco o nessun provirus vengono amplificato. Sequenze dell’iniettore possono essere per volta/ridisegnato per abbinare altri sottotipi. Inoltre, un bene che contiene un controllo positivo dovrebbe essere incluso in ogni PCR eseguita.
Salti mortali ha superato i limiti della precedente analisi di sequenziamento, compreso SPS. FLIPS, attraverso amplificazione e sequenziamento vicino a full-length provirus di HIV-1, è in grado di determinare la potenziale replica-competenza del provirus di HIV-1. Questo non era possibile utilizzando SPS, che solo regioni sub-genomiche in sequenza e quindi selezionati per le sequenze con siti di legame del primer intatto. Inoltre, FLIPS supera i limiti associati all’utilizzo più amplificazione e primer di sequenziamento, come è stato impiegato da precedente full-length sequenziamento saggi1,4. Attraverso due cicli di PCR indirizzando le regioni LTR di HIV-1 combinate con NGS, FLIPS diminuisce il numero e la complessità degli iniettori richiesto. Salti mortali è quindi meno suscettibile alle conseguenze del primer disadattamento, vale a dire l’identificazione erronea del provirus difettoso e un’incapacità di amplificare alcune provirus all’interno di una popolazione. Il protocollo di FLIPS è anche più efficiente e consente un throughput più elevato del sequenziamento rispetto ai metodi precedenti.
Evidentemente, FLIPS fornisce vantaggi rispetto ai metodi esistenti che determinano la composizione genetica di provirus di HIV-1. Tuttavia, è importante riconoscere i limiti di lanci. In primo luogo, il dosaggio di salti mortali non è stato sviluppato come uno strumento per misurare le dimensioni del bacino di HIV-1 latente, come analisi per determinare se FLIPS amplifica ogni provirus di HIV-1 presenti in una popolazione delle cellule non sono state completate. Salti mortali è invece utile per effettuare confronti relativi della composizione del serbatoio tra cellulari differenti popolazioni2. In secondo luogo, la replica-competenza del intatta provirus di HIV-1 non può essere determinata con certezza senza analisi in vivo , ad esempio quelle eseguite da Ho et al. 4. in terzo luogo, salti mortali non è progettato per determinare il sito di integrazione del provirus di HIV-1.
Piccole variazioni al protocollo FLIPS possono aumentare la sua applicazione. Ad esempio, le variazioni di primer sequenze possono consentire diverse e molteplici sottotipi di HIV-1 ad essere amplificato ed ordinato. Sequenziamento dei virions del plasma HIV-1 è possibile attraverso l’aggiunta di sintesi del cDNA prima del PCR annidata. Futuro utilizzo dei metodi di sequenziamento di singola molecola eliminerà la necessità per l’assemblaggio de novo .
Sequenziamento genetico di integrato provirus di HIV-1 ha aumentato la nostra comprensione del bacino latente di HIV-1. Flip è uno strumento importante per gli studi futuri delucidando la composizione e la distribuzione del serbatoio latente. Tuttavia, l’applicazione di lanci può estendersi oltre il serbatoio. Gli studi futuri possono utilizzare i salti mortali per determinare obiettivi particolari per tecnologia CRISPR-Cas, o contribuire all’identificazione di codifica e regioni non codificanti, che rendono il virus più reattivo alla latenza agenti di retromarcia. Ricombinazione virale può essere meglio compresa guardando i siti di giunzione di ampie delezioni interne.
Declarações
The authors have nothing to disclose.
Acknowledgements
Questo lavoro è stato supportato Delaney AIDS ricerca Enterprise (DARE) per trovare una cura (1U19AI096109 e 1UM1AI126611-01); un amfAR Consorzio di ricerca su HIV eradicazione (ARCHE) Collaborative Research Grant della Fondazione per la ricerca sull’AIDS (amfAR 108074-50-RGRL); Australian Centre for HIV ed epatite virologia ricerca (ACH2); UCSF-GIVI centro per la ricerca sull’AIDS (P30 AI027763); e l’Australian National Health and Medical Research Council (AAP1061681). Vorremmo ringraziare Dr. Joey Lai, genomica Facility Manager presso l’Istituto di Westmead ricerca medica per la sua formazione in libreria preparazione e uso del suo impianto e il centro di Ramaciotti per genomica (Università del New South Wales, Sydney, Australia) per lo svolgimento di sequenziamento. Riconosciamo con gratitudine i partecipanti che hanno donato i campioni per questo studio.
Materials
| UltraPure 1 M Tris-HCI, pH 8.0 | Invitrogen | 15568025 | Dilute to 5 mM for nested PCR |
| Nonidet P 40 Substitute solution | Sigma | 98379 | |
| Tween-20 | Sigma | P9416 | |
| Proteinase K Solution (20 mg/mL) | Promega | AM2548 | |
| 96 well thermocycler | Any 96 well thermocycler can be used | ||
| Platinum Taq DNA Polymerase High Fidelity | Invitrogen | 11304011 | |
| 10X High Fidelity Buffer [600 mM Tris-SO4 (pH 8.9), 180 mM (NH4)2SO4] | Invitrogen | 11304011 | |
| 50 mM MgSO4 | Invitrogen | 11304011 | |
| PCR Nucleotide Mix, 10 mM | Promega | C1141 | |
| Ultrapure H2O | Invitrogen | 10977023 | |
| PCR1 and PCR2 Primers | Desalted. Dilute to (100 M) with H2O | ||
| PCR Plate 96 Well, Half Skirt, Single Notch Corner, Clear | Axygen | PCR-96M2-HS-C | |
| Microseal 'B' Adhesive Seals | BioRad | MSB1001 | Required to seal 96 well PCR plates |
| HIV-1 NL4-3 Infectious Molecular Clone (pNL4-3) | The following reagent was obtained through the NIH AIDS Reagent Program, Division of AIDS, NIAID, NIH: HIV-1 NL4-3 Infectious Molecular Clone (pNL4-3) from Dr. Malcolm Martin (Cat# 114). | Diluted to 10^5 copies/mL and used as positive control | |
| PCR plate spinner or benchtop centrifuge | |||
| E-GEL 48 1% Agarose | Invitrogen | G800801 | Precast 1% agarose gels (two gels used per 96 well plate). Any 1% agarose gel can be substituted. Contains ethidium bromide. |
| DirectLoad Wide Range DNA Marker | Sigma | D7058 | Any ladder with a range up to 10 kb can be substituted |
| Mother E-Base device | Invitrogen | EBM03 | Required for running precast 48 well 1% agarose gels |
| Gel Doc EZ Gel Documentation System | BioRad | 1708270 | Any visualisation system for ethidium bromide containing agarose gels can be used |
| PlateMax Peelable Heat Sealing | Axygen | HS-200 | Heat sealing film for long term storage |
| 96 Well 0.8 mL Storage Plate | ThermoFisher Scientific | AB0765 | 0.8 mL 96 well plate required for magnetic bead based PCR purification |
| Agencourt AMPure XP (PCR purification kit) | Beckman Coulter | A63880 | Magnetic bead based PCR purification kit. Other PCR purification kits can be substitued here (e.g. QIAquick PCR Purification Kit (Qiagen Cat#28106) |
| Ethyl alcohol, Pure. 200 proof, for molecular biology | Sigma | E7023 | |
| Magnetic Stand-96 | Invitrogen | AM10027 | |
| Microplate shaker | Optional | ||
| Buffer EB | Qiagen | 19086 | Elution buffer |
| Quant-iT PicoGreen dsDNA Assay Kit | Invitrogen | P11496 | A fluorescence based stain for measuring dsDNA concentration |
| Microplate reader | |||
| Nextera XT DNA Library Preparation Kit | Illumina | FC-131-1096 | |
| Nextera XT Index Kit | Illumina | FC-131-2001 | |
| Hard-Shell 96-Well PCR Plates | Biorad | HSP9601 | Required for Nextera XT DNA library preparation kit |
| Library Quantification Kit – Illumina/Universal | Kapa Biosystems | KK4824 | Other library quantification kits can be substitued (e.g. JetSeq DNA Library Quantification Lo-Rox Kit (Bioline Cat#BIO-68029) |
| 2100 Bioanalyzer | Agilent Technology | Automated electrophoresis system . Use in conjunction with a High Sensistivity DNA kit | |
| High Sensistivty DNA kit | Agilent Technology | 5067-4626 | |
| Illumina MiSeq Platform | Illumina |
Referências
- Bruner, K. M., et al. Defective proviruses rapidly accumulate during acute HIV-1 infection. Nature Medicine. 22 (9), 1043-1049 (2016).
- Hiener, B., et al. Identification of Genetically Intact HIV-1 Proviruses in Specific CD4(+) T Cells from Effectively Treated Participants. Cell Reports. 21 (3), 813-822 (2017).
- Abram, M. E., Ferris, A. L., Shao, W., Alvord, W. G., Hughes, S. H. Nature, position, and frequency of mutations made in a single cycle of HIV-1 replication. Journal of Virology. 84 (19), 9864-9878 (2010).
- Ho, Y. C., et al. Replication-competent noninduced proviruses in the latent reservoir increase barrier to HIV-1 cure. Cell. 155 (3), 540-551 (2013).
- Harris, R. S., et al. DNA deamination mediates innate immunity to retroviral infection. Cell. 113 (6), 803-809 (2003).
- Lecossier, D., Bouchonnet, F., Clavel, F., Hance, A. J. Hypermutation of HIV-1 DNA in the absence of the Vif protein. Science. 300 (5622), 1112 (2003).
- Chun, T. W., et al. Rebound of plasma viremia following cessation of antiretroviral therapy despite profoundly low levels of HIV reservoir: implications for eradication. AIDS. 24 (18), 2803-2808 (2010).
- Chomont, N., et al. HIV reservoir size and persistence are driven by T cell survival and homeostatic proliferation. Nature Medicine. 15 (8), 893-900 (2009).
- Soriano-Sarabia, N., et al. Quantitation of replication-competent HIV-1 in populations of resting CD4+ T cells. Journal of Virology. 88 (24), 14070-14077 (2014).
- Josefsson, L., et al. The HIV-1 reservoir in eight patients on long-term suppressive antiretroviral therapy is stable with few genetic changes over time. Proceedings of the National Academy of Sciences USA. 110 (51), E4987-E4996 (2013).
- Evering, T. H., et al. Absence of HIV-1 evolution in the gut-associated lymphoid tissue from patients on combination antiviral therapy initiated during primary infection. Public Library of Science Pathogens. 8 (2), e1002506 (2012).
- von Stockenstrom, S., et al. Longitudinal Genetic Characterization Reveals That Cell Proliferation Maintains a Persistent HIV Type 1 DNA Pool During Effective HIV Therapy. Journal of Infectious Diseases. 212 (4), 596-607 (2015).
- Palmer, S., et al. Multiple, linked human immunodeficiency virus type 1 drug resistance mutations in treatment-experienced patients are missed by standard genotype analysis. Journal of Clinical Microbiology. 43 (1), 406-413 (2005).
- . CLC Genomics Version 10 Available from: https://www.qiagenbioinformatics.com/products/clc-genomics-workbench (2018)
- . FastQC: a quality control tool for high throughput sequence data Available from: https://www.bioinformatics.babraham.ac.uk/projects/fastqc/ (2010)
- Bolger, A. M., Lohse, M., Usadel, B. Trimmomatic: a flexible trimmer for Illumina sequence data. Bioinformatics. 30 (15), 2114-2120 (2014).
- Martin, M. Cutadapt removes adapter sequences from high-throughput sequencing reads. EMBnet.journal. 17 (1), (2011).
- Magoc, T., Salzberg, S. L. FLASH: fast length adjustment of short reads to improve genome assemblies. Bioinformatics. 27 (21), 2957-2963 (2011).
- Langmead, B., Salzberg, S. L. Fast gapped-read alignment with Bowtie 2. Nature Methods. 9 (4), 357-359 (2012).
- Bankevich, A., et al. SPAdes: a new genome assembly algorithm and its applications to single-cell sequencing. Journal of Computational Biology. 19 (5), 455-477 (2012).
- Kumar, S., Stecher, G., Tamura, K. MEGA7: Molecular Evolutionary Genetics Analysis Version 7.0 for Bigger Datasets. Molecular Biology and Evolution. 33 (7), 1870-1874 (2016).
- Katoh, K., Standley, D. M. MAFFT multiple sequence alignment software version 7: improvements in performance and usability. Molecular Biology and Evolution. 30 (4), 772-780 (2013).
- . HIV Sequence Database – Gene Cutter tool Available from: https://www.hiv.lanl.gov/content/sequence/GENE_CUTTER/cutter.html (2018)
- Foster, J. L., Garcia, J. V. Role of Nef in HIV-1 replication and pathogenesis. Advances in Pharmacology. 55, 389-409 (2007).
- . HIV Sequence Database – Consensus Maker tool Available from: https://www.hiv.lanl.gov/content/sequence/CONSENSUS/consensus.html (2018)
- . HIV Sequence Database – Hypermut tool Available from: https://www.hiv.lanl.gov/content/sequence/HYPERMUT/hypermut.html (2018)
- Yu, G., Smith, D. K., Zhu, H., Guan, Y., Lam, T. T. Y. ggtree: an r package for visualization and annotation of phylogenetic trees with their covariates and other associated data. Methods in Ecology and Evolution. , (2016).

