Korrelationsmaalinger lys Elektron Mikroskopi (CLEM) til sporing og Imaging Viral Protein associeret strukturer i Cryo-immobiliserede celler
Summary
En korrelationsmaalinger lys elektronmikroskopi (CLEM) metode kan anvendes på billedet virus-induceret intracellulære strukturer via elektronmikroskopi (EM) i celler, der er tidligere vælges ved lysmikroskopi (LM). LM og EM er kombineret som en hybrid imaging tilgang til at opnå en integreret visning af virus-værtssammenspil.
Abstract
På grund af sin høje opløsning er elektronmikroskopi (EM) et uundværligt redskab for virologer. En af de største problemer når du analyserer virus-inficerede eller transfekteret celler via EM er dog de lave effektivitet af infektion eller Transfektion, hindrer behandlingen af disse celler. For at overvinde denne vanskelighed, kan lysmikroskopi (LM) blive udført først for at allokere delpopulation af inficerede eller transfekteret celler. Således at drage fordel af brugen af fluorescerende proteiner (FPs) smeltet til virusproteiner, LM bruges her til at registrere positioner “positive-transfekteret” celler, udtrykker en FP og vokser på en støtte med en alfanumerisk mønster. Efterfølgende celler behandles yderligere til EM via højtryk frysning (HPF), fryse substitution (FS) og harpiks indlejring. Den ultra-hurtig nedfrysning trin sikrer fremragende membran bevarelsen af de markerede celler, der kan analyseres derefter på ultrastrukturelle niveau af transmissions Elektron Mikroskopi (TEM). Her tilbydes en trinvis korrelationsmaalinger lys elektronmikroskopi (CLEM) arbejdsproces, der beskriver prøveforberedelse, billedbehandling og korrelation i detaljer. Den eksperimentelle design kan også anvendes for at løse mange celle biologi spørgsmål.
Introduction
Idé om at kombinere to mikroskopi metoder til at få et bedre billede af en bestemte biologiske proces er temmelig gammel. Således, den første undersøgelse om virus ved hjælp af “korrelationsmaalinger mikroskopi” udkom i 1960 som to særskilte publikationer1,2. I denne undersøgelse analyserede forfatterne ændringer i morfologi af kernen induceret af adenovirus ved hjælp af to mikroskopi-teknikker. I den første publikation var elektronmikroskopi (EM) bemærkninger beskriver de morfologiske oplysninger tilknyttet adenovirus infektion rapporteret1. I en anden publikation, var de forskellige strukturer observeret af EM korreleret med lysmikroskopi (LM) billeder af histokemiske farvning mønstre, til at definere karakteren af de strukturer, tidligere observeret af EM2.
I disse tidlige studier, var deres observationer imidlertid udføres, ved hjælp af forskellige inficerede celler forberedt som uafhængige forsøg. “Korrelation” var, ja, ment som kombinationen af oplysninger fra to billeddiagnostiske modaliteter til at forstå et bestemt fænomen, sammenligne alle de resultater, der er opnået med forskellige assays for at forstå en given biologiske proces.
I dag er anvendes udtrykket korrelationsmaalinger mikroskopi, også kendt som korrelationsmaalinger lys og elektronmikroskopi (CLEM), til et stigende antal metoder (gennemgik i referencer3,4,5), med fællestrækkene at både Billeddannende teknikker (LM og EM) er udført på samme prøve. Kombinationen af begge metoder resulterer derved i et multimodalt, multi-skala og multi-dimensional analyse af at prøve3. Fordelene er, at LM kan give et bredt overblik over mange forskellige celler, muliggør identifikation af celle delpopulationer udtryk for et protein eller proteiner af interesse inden for en heterogen celle population. EM overvinder opløsning grænsen for LM, hvilket giver en højere opløsning billede af en bestemt intracellulære begivenhed. Derudover EM giver mulighed for visualisering af ikke-fluorescerende subcellulært sammenhæng, herunder alle membran bundet organeller, store makromolekylære komplekser (fx ribosomer, centrioler, etc.) og cytoskeletal elementer, således giver yderligere geografisk information, den såkaldte “refererer til rum”6, og giver forbindelse til fluorescerende stedet opdaget af LM.
I løbet af de sidste par år, CLEM er blevet et stærkt værktøj for celle biologer5, men også for virologer (gennemgik i reference7) villig til at forstå de komplekse virus-celle interaktioner, der fører til en vellykket virus formering. Dermed, forståelse af hvordan virus ændre cellemembraner og organeller til deres egen fordel er vigtigt at udvikle antivirale lægemidler for at udrydde lavpatogen virus.
Her, er en CLEM metode beskrevet der giver mulighed for påvisning af LM af celler, der udtrykker virusproteiner smeltet til en fluorescerende proteiner (FP). Disse celler er efterfølgende cryo-immobiliseret og yderligere rede for ultrastrukturelle analyse via transmissions Elektron Mikroskopi (TEM) at få ny indsigt i hvordan udtryk for disse proteiner omarrangere intracellulære membraner (figur 1). CLEM er udført med kemisk fast celler i de fleste af de virologi undersøgelser offentliggjort til dato8,9,10,11,12,13,14 ,15,16,17,18,19. Dette er hovedsagelig på grund af behovet for at inaktivere smitsomme materiale for Biosikkerhed grunde i biosikkerhed niveau-2 og -3 (BSL-2 og BSL-3) laboratorier, hvor cryo-immobilisering af celler ikke er normalt muligt. For disse spørgsmål, der kræver en optimal bevarelse af cellemembraner, vitrifikation via højtryk frysning (HPF), dog anbefales20. I disse tilfælde kan CLEM protokollen beskrevet her anvendes. Interessant, især når du arbejder med smitsomme prøver, kan HPF udføres på prøver, der har været tidligere kemisk inaktiveret, for eksempel i BSL-2 og BSL-3 laboratorier. Kombinationen af kemisk fiksering efterfulgt af HPF er en mulighed for at profit i det mindste delvist fra fordelene ved cryo-bevarelse metoder21,22.
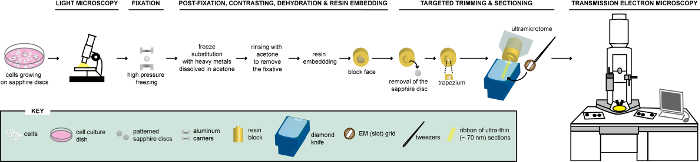
Figur 1 : Skematisk fremstilling af arbejdsgangen for analysen af celler via CLEM. Celler vokser på mønstrede safir diske analyseres først af LM til at lokalisere celler, der udtrykker FPs før deres forarbejdning til EM. Når fundet, fast celler straks af HPF og FS at være efterfølgende indkapslet i harpiks. Efter polymerisering af harpiks, støtte hvor celler voksende (= safir diske) skal fjernes fra harpiks blok. Blokken indeholder de indlejrede celler er trimmet til en lille trapez, hvorfra de resterende celler, udtrykker FPs, er delt med en diamant kniv. Ultratynde sektioner er indsamlet på slot gitre og yderligere undersøgt af TEM ultrastrukturelle oplysninger af disse celler. Dette tal er tilpasset og ændret med tilladelse fra reference29. Venligst klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Metoden CLEM præsenteret her for at studere virkningerne af en viral protein udtryk på cellemembraner har held været anvendt inden for at belyse HCV replikation-associerede strukturer, især dobbelt membran vesikler (DMVs)21, samt at bestemme de kritiske byggesten kræves for at danne disse HCV-induceret strukturer23. Bemærk, at i vores første arbejde ved hjælp af CLEM for at studere HCV replikering21, en let ændret udgave af protokollen beskrevet her blev anvendt. I denne undersøgelse, konventionelle 0,05 mm tyk safir diske, uden alfanumeriske mønster, blev brugt som en reference mønstret blev skabt af kulstof belægning dem med et finder gitter på toppen (Se Tabel af materialer). Denne version af den aktuelle protokol kan anvendes til sidst, med den fordel, at “A” transportøren for HPF kan anvendes direkte, uden behov for at skære det som i figur 3A. Alternativt, som nævnt i protokollen, en tykkere “A” transportør kan udnyttes (Se Tabel af materialer) med mønstrede safir diske, uden brug af en “B” luftfartsselskab.
Interessant, kan denne protokol anvendes ikke kun til at studere BSL-1 prøver, som celler transfekteret med virale proteiner som beskrevet her og andetsteds19,23, men også at studere virus-inficerede celler. Selv om arbejdet med menneskers patogener er normalt begrænset til BSL-2 og BSL-3 laboratorier, i nogle lande er det stadig muligt at udføre cryo-immobilisering disse biosikkerhed betingelser. I disse BSL-2 og BSL-3 laboratorier hvor vitrifikation ikke er mulig på grund af de lokale regler eller fraværet af en HPF maskine, kan virus-inficerede celler stadig forberedes ved hjælp af denne metode hvis kemisk fiksering med aldehyder udføres på forhånd nemlig inden de forlader BSL-2 eller BSL-3 faciliteterne. Endvidere skal aldehyder være slukkes straks efter fiksering at holde fluorescens, mens resten af protokollen er identisk med den, der er beskrevet her. Denne teknik kan betragtes som overflødig, fordi cellerne er fast to gange, kemisk og via vitrifikation. Men denne dobbelt fiksering protokol fører faktisk til en meget bedre bevarelse af HCV-induceret DMVs i forhold til DMVs fundet i celler udsat for kemisk fiksering alene21.
For yderligere ændringer og fejlfinding læseren henvises til noter i hele protokol del af dette manuskript. Disse noter beskrive faldgruber for at undgå, såvel som alternativer til at overvinde formodede vanskeligheder, der måtte opstå, når du udfører denne metode.
Den vigtigste forudsætning for at anvende denne teknik er en HPF maskine. Hvornår cryo-immobilisere celler via HPF er ikke mulig (på grund af manglende en HPF maskine) eller ikke påkrævet (når membranen bevarelse ikke behøver at være optimale), celler kan være kemisk fast og efterfølgende udarbejdet og analyseret af EM8, 9,10,11,12,13,14,15,16,17,18 ,19. Denne indstilling kræver ikke brug af safir diske, men celle kultur retter med inddelte mønstre for at flytte celler eller celle klynger. Den største fordel ved brugen af disse retter er deres større diameter sammenlignet med safir diske, tillade screening af større overfladearealer. Således har CLEM protokollens anvendelse været anvendt med succes til at studere effekten af et antiviralt stof mod HCV15 eller at visualisere membran rearrangementer induceret af de strukturmaessige proteiner af norovira19. Et andet spørgsmål, der kan begrænse effektiviteten af denne metode er fraværet af en kommerciel FS enhed. I dette tilfælde kan grundlæggende hjemmelavet FS systemer udnyttes i stedet. Selv om automatiske FS enheder kan reducere håndtering uheld, er hjemmelavede anordninger anvendt med succes for eksempel på Kent Mcdonald’s30 og Paul Walther labs.
Med hensyn til kemisk fiksering sikrer protokollen beskrevet her en optimal bevarelse af den intracellulære strukturer20. Derfor, i tilfælde af den ovennævnte HPF og FS hjælpemidler er tilgængelige, vitrifying celler af interesse vil blive foretrukket.
Fremtidige alternativer til denne CLEM tilgang omfatter mulighed for at anvende denne metode ikke blot at erhverve 2D oplysninger på ultrastrukturelle niveau, men også at få 3D-oplysninger om arkitekturen af membranen og organelle ændringer forårsaget af virus. De 3D-EM metoder, herunder elektron tomografi (ET) og fokuseret ion beam-scanning elektronmikroskopi (FIB-SEM) (udførligt beskrevet i29), kunne også anvendes til celler, der er udarbejdet efter denne aktuelle protokol21, 31. Derudover kan 3D-oplysninger også fås ved henvendelse til LM niveau, når ved hjælp af en Konfokal mikroskop, som giver mulighed for erhvervelse af z-stakke. Denne indstilling er i virkeligheden, anbefales når en præcis sammenhæng mellem LM og EM datasæt er ønskede (Se for eksempel17). Oplysningerne i 3D z-stakke aids at forbedre sammenhængen med 2D TEM billeder. Således, i et sådant scenario, de bedste montering LM og EM billeder kan vælges og derefter udsat for en af de korrelation software til rådighed, som EF-CLEM plugin af ICY (http://icy.bioimageanalysis.org/)32 eller Landmark korrespondancer plugin af Billede Jørgensen (http://imagej.net/Landmark_Correspondences), hvilket resulterer i generation af overlappende LM-EM billeder.
Når tidsmæssige oplysninger er nødvendige for at forstå kinetik af en bestemt begivenhed, kan time-lapse billedbehandling bruges til at overvåge dynamikken i levende celler i kombination med EM. Under arrangementet af interesse rettes celler straks, generere en “frossen snapshot”, der efterfølgende kan analyseres via EM, der giver detaljerede ultrastrukturelle oplysninger om det pågældende tidspunkt på tidspunktet for immobilisering. For at opnå den “frosne snapshot”, efter observation i realtid, kan celler være enten kemisk fast33 eller cryo-immobiliseret6. Da mange cellulære processer forekomme hurtigere end diffusion processer af kemisk fiksering, hvis det er muligt, skal ultra-hurtig nedfrysning udføres. Det er dog vigtigt at tage i betragtning at HPF maskiner adskiller sig i deres effektive tid beslutning34.
Desuden, selv om denne protokol har været designet til integrering af celler i en epoxy-harpiks, celler kan også integreres i lav viskositet harpikser, såsom Lowicryls, LR hvid eller LR guld. Brugen af disse indlejring medier gør det muligt for at bevare antigenicity35,36, samt fluorescens37,38 , og derfor bruges mest til post indlejring på afsnit immunolabeling39 , 40 og på afsnit CLEM41,42,43,44, hvor LM er gjort efter integrering. Begge tilgange (immuno-EM og på afsnit CLEM) skal være afgørende for de eksperimenter, hvor ikke-karakteristiske strukturer kan nemt findes via TEM og/eller som en kontrol mod miscorrelation mellem LM og EM signaler. Ligeledes, mærkning med antistoffer, der kan visualiseres ved begge billeddiagnostiske modaliteter (LM og EM) kan transporteres ud af45 for at, for eksempel, identificere transfekteret celler i LM (pre indlejring fase) og opnå en mere nøjagtig lokalisering af den Normal god landbrugspraksis signal via sin særlige mærkning af immuno-EM (post indlejring fase). Det skal tages i betragtning, dog at permeabilization foregår før LM til at tillade adgang for antistoffer mod det intracellulære rum, som kan resultere i en optimal bevarelse af celle arkitektur på EM-niveau. Interessant, denne protokol er også velegnet for multi-farve eksperimenter der kan opnås med brugen af andre fluorescerende tags, end normal god landbrugspraksis (som vist her). Afslutningsvis er der mange formodede mulighederne for tilpasning af denne protokol, både LM og/eller EM sider, afhængigt af de spørgsmål, der behandles. En omfattende beskrivelse af andre alternative protokoller henvises læseren til5,46. Uanset hvordan mikroskopi metoder kombineres, er resultatet sammen en gevinst på information, giver mulighed for os til bedre at forstå hvordan vira og deres proteiner sammen med deres værter i det virkelige liv.
Det mest afgørende skridt inden for denne metode er samlingen af seriel afsnit fra celler af interesse. Som fremhævet i afsnittet repræsentative resultater kræver dette ekspert personale, samt en masse tålmodighed. Vigtigere, er dette trin vigtigt at finde cellerne tilbage på niveauet EM af to grunde. Først, i denne slags CLEM protokol bruger pre indlejring LM, koordinater er kun synlige på LM-niveau og på harpiks blok ansigt efter integrering. Dog vil de ikke være synlig på sektioner af TEM. Derfor skal målrettet trimning i blok ansigtet ned til områder af interesse (ROIs) udføres omhyggeligt med et barberblad til at sikre, at de dele, der er efterfølgende indhentet indeholder de celler, der udtrykker en bestemt FP. For det andet er “scanning” flere sektioner nødvendigt at finde den bedste overlay mellem LM og EM erhvervelser. I modsætning til metoder hvor LM er udført på stadiet post indlejring, er i dette tilfælde LM-EM overlay ikke så præcis. Lav overlay nøjagtighed skyldes forskelle i aksial beslutning mellem LM og EM, svind under prøve behandling af EM og komprimering ved skæring42. Ikke desto mindre hjælpe effektiv sporingsmetoder, såsom brugen af landemærker, med at finde cellerne tilbage. Dette omfatter én celle til en anden position og form af celler og deres kerne. I denne forbindelse som anført i protokollen, give DIC billeder “anatomiske” information af de celler, der er afgørende for at forbedre sammenhængen. Alternativt, kerner eller andre godt-genkendelige celle organeller (mitokondrier eller lipid dråber) kan farves før LM og anvendes som vartegn.
Endelig er det værd at nævne, at selvom dette manuskript er fokuseret på anvendelsen af denne teknik for virologi undersøgelser, omfanget af denne eksperimentelle design kan udvides for at løse mere almindelige biologiske spørgsmål.
Declarações
The authors have nothing to disclose.
Acknowledgements
Vi er meget taknemmelige for medarbejdere af elektronmikroskopi Core faciliteter (EFMS ‘s) på EMBL (Heidelberg) og på Universitet i Heidelberg. Vi også gerne takke Ulrike Herian, Stephanie Kallis og Andrea Hellwig (Heidelberg Universitet), samt Eberhardt Schmidt og Renate Kunz (Universitet i Ulm) til teknisk ekspertbistand. Arbejde ved R.B. og hans team (U.H. og I.R.-B.) blev støttet af Deutsche Forschungsgemeinschaft, SFB1129, TP11 og TRR83, TP13.
Materials
| UV Crosslinker | Stratagene | 400072 | Stratalinker 1800, 230Vac, equipped with 254-nm UV light bulbs, 8-watts/each. |
| Patterned sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 627 | They have a 0.3-mm diameter and are 0.16-mm thick, as well as an an etched alphanumeric pattern to allow for re-location of the cells. They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Slim and long tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | 72919-SS | "Style SS", for handling sapphire discs. |
| Cell culture medium | Thermo Fisher Scientific, Waltham, MA, USA | 41965-062 | Dulbecco's modified Eagle medium (DMEM) supplemented with 2 mM L-glutamine, nonessential amino acids, 100 units penicillin per ml, 100 µg streptomycin per ml and 10% fetal calf serum (DMEM complete, see below). Package containing 10 bottles, 500 ml/each. |
| L-glutamine | Thermo Fisher Scientific, Waltham, MA, USA | 25030-123 | Package containing 20 bottles of 100 ml/each. |
| Nonessential amino acids | Thermo Fisher Scientific, Waltham, MA, USA | 11140-068 | Package containing 20 bottles of 100 ml/each. |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Waltham, MA, USA | 15140-163 | Package containing 20 bottles of 100 ml/each. |
| Fetal calf serum | Sigma Aldrich, St. Louis, MI, USA | F7524 | Bottle of 50 ml. |
| Inverted microscope | Olympus Deutschland, Hamburg, Germany | CKX41 | It is an inverted microscope with trinocular head options and fluorescence upgrade capability. |
| Huh7-Lunet cells stably expressing the T7 RNA-polymerase | Avaliable at Prof. Dr. Ralf Bartenschlager laboratory | Not available | Contact Prof. Bartenschlager at: ralf.bartenschlager@med.uni-heidelberg.de. |
| Mirus TransIT-LT1 Transfection Reagent | Mirus Bio LLC, Madison, USA | MIR 2304 | Broad spectrum, low toxicity, DNA transfection reagent. Vial of 0.4 ml. |
| Inverted widefield fluorescence microscope | Carl Zeiss Microscopy GmbH, Germany | Zeiss Observer.Z1 | Inverted fluorescence microscope for experiments involving living cell cultures. |
| 1-hexadecene | Merck, Darmstadt, Germany | 8220640100 | Bottle of 100 ml. |
| "A" aluminium holders for high pressure frezing (HPF) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 241 | This is the holder that has been used for this protocol and has 2 different depths of 0.1 and 0.2-mm. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "B" aluminium holders for HPF | Engineering Office M. Wohlwend, Sennwald, Switzerland | 242 | This is the holder that has been used for this protocol.It is 0.3-mm thick.They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "A" aluminium holder for HPF (special for working with patterned sapphire discs) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 737 | This is the holder than can be used alone with the patterned sapphire disc (as an alternative to the current protocol), without the need of a "B" holder or the edition of the "A" holder. It is 0.84-mm thick. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 405 | These sapphires discs are the "conventional" one, with a 0.3-mm diameter and a thickness of 0.05 mm . They can be also used for CLEM as an alternative instead of patterned sapphire discs. |
| Finder grids | Electron Microscopy Sciences, Hatfield, Philadelphia, USA | LF135-Cu | These 135 mesh grids are used to create an alphanumeric pattern on "conventional" sapphire discs (described above) via carbon coating, so that they can be used for CLEM. 100 grids/vial. |
| HPF machine | ABRA Fluid AG, Widnau, Switzerland | HPM 01 | This HPF machine has been used for this protocol. |
| HPF machine | Leica Microsystems, Vienna, Austria | EMPACT 2 | "EMPACT 2", as an alternative to the use of the HPM machine that it has been used in this protocol (described above). |
| Cryo-tubes | Thermo Fisher Scientific, Waltham, MA, USA | Z763667-500EA | For long term-storage of cryo-immobilized samples in liquid nitrogen. Package containing 500 cryovials. |
| Liquid nitrogen dewar | Cole-Parmer GmbH, Wertheim, Germany | GZ-05094-60 | For long term-storage of cryo-immobilized samples in liquid nitrogen, equipped with cryo-racks with a capacity of 1600 cryo-tubes. |
| Automatic freeze substitution (AFS) machine | Leica Microsystems, Vienna, Austria | EM AFS2 | This machine performs freeze substitution and progressive lowering of temperature (PLT) techniques and allows low temperature embedding and polymerization of resins. |
| Osmium tetroxide (OsO4) | Electron Microscopy Sciences, Hatfield, PA, USA | 19150 | 4% aqueous solution, one box containing 10 x 2 ml ampules. |
| Uranyl-Acetate (UA) | Serva, Heidelberg, Germany | 77879.01 | Bottle containing 25 grs of (UA)-2 H2O. |
| Sonicator | Bandelin Electronic, Berlin, Germany | 329 | "Sonorex Super RK 31" is a high-power ultrasonic cleaning bath for aqueous cleaning solution that is used in this protocol to mix OsO4 and Ua when preparing the FS medium. |
| Glass-distilled acetone | Electron Microscopy Sciences, Hatfield, PA, USA | 10015 | Bottle of 100 ml. |
| Stereomicroscope | Leica Microsystems, Vienna, Austria | Leica M80 | Routine stereomicroscope for daily inspections, equipped with a camera for capturing images. |
| Epoxy resin | Electron Microscopy Sciences, Hatfield, PA, USA | 14120 | Embed 812 is a kit containing several components that must be mix together in the proportions given by the manufacturers. |
| Flow through rings | Leica Microsystems, Vienna, Austria | 16707157 | Package containing 100 pieces. |
| Reagent baths | Leica Microsystems, Vienna, Austria | 16707154 | Package containing 100 pieces. |
| Ultramicrotome | Leica Microsystems, Vienna, Austria | Leica EM UC7 | Ultramicrotome for preparation of semi- and ultrathin sections at room temperature. |
| Ultra 35° diamond knife | Diatome Ltd., Nidau Switzerland |
AGG339-735 | This knife have an edge length of 3 mm. |
| Ultra fine tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | E78318 | "Style 3X", for handling EM grids. |
| EM slot grids | Electron Microscopy Sciences, Hatfield, PA, USA | G2010-Cu | 100 grids/vial. |
| EM grid storage box | Electron Microscopy Sciences, Hatfield, PA, USA | 71155 | It has capacity for 100 grids. |
Referências
- Morgan, C., Godman, G. C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. I. Electron microscopy. Journal of Experimental Medicine. 112, 373-382 (1960).
- Godman, G. C., Morgan, C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. II. Light microscopy. Journal of Experimental Medicine. 112, 383-402 (1960).
- Caplan, J., Niethammer, M., Taylor, R. M., Czymmek, K. J. The power of correlative microscopy: multi-modal, multi-scale, multi-dimensional. Current Opinion in Structural Biology. 21, 686-693 (2011).
- de Boer, P., Hoogenboom, J. P., Giepmans, B. N. Correlated light and electron microscopy: ultrastructure lights up. Nature Methods. 12, 503-513 (2015).
- Müller-Reichert, T., Verkade, P. . Correlative light and electron microscopy III, First edition. , (2017).
- Brown, E., Mantell, J., Carter, D., Tilly, G., Verkade, P. Studying intracellular transport using high-pressure freezing and Correlative Light Electron Microscopy. Seminars in Cell and Developmental Biology. 20, 910-919 (2009).
- Bykov, Y. S., Cortese, M., Briggs, J. A., Bartenschlager, R. Correlative light and electron microscopy methods for the study of virus-cell interactions. FEBS Letters. , (2016).
- Spuul, P., et al. Assembly of alphavirus replication complexes from RNA and protein components in a novel trans-replication system in mammalian cells. Journal of Virology. 85, 4739-4751 (2011).
- Nagel, C. H., Dohner, K., Binz, A., Bauerfeind, R., Sodeik, B. Improper tagging of the non-essential small capsid protein VP26 impairs nuclear capsid egress of herpes simplex virus. PLoS One. 7, 44177 (2012).
- Sharma, M., Kamil, J. P., Coughlin, M., Reim, N. I., Coen, D. M. Human cytomegalovirus UL50 and UL53 recruit viral protein kinase UL97, not protein kinase C, for disruption of nuclear lamina and nuclear egress in infected cells. Journal of Virology. 88, 249-262 (2014).
- Kallio, K., et al. Template RNA length determines the size of replication complex spherules for Semliki Forest virus. Journal of Virology. 87, 9125-9134 (2013).
- Martinez, M. G., Snapp, E. L., Perumal, G. S., Macaluso, F. P., Kielian, M. Imaging the alphavirus exit pathway. Journal of Virology. 88, 6922-6933 (2014).
- Lebrun, M., et al. Varicella-zoster virus induces the formation of dynamic nuclear capsid aggregates. Virology. 454-455, 311-327 (2014).
- Madela, K., et al. A simple procedure to analyze positions of interest in infectious cell cultures by correlative light and electron microscopy. Methods in Cell Biology. 124, 93-110 (2014).
- Berger, C., et al. Daclatasvir-like inhibitors of NS5A block early biogenesis of hepatitis C virus-induced membranous replication factories, independent of RNA replication. Gastroenterology. 147, 1094-1105 (2014).
- van der Schaar, H. M., et al. Illuminating the Sites of Enterovirus Replication in Living Cells by Using a Split-GFP-Tagged Viral Protein. mSphere. 1, (2016).
- Vale-Costa, S., et al. Influenza A virus ribonucleoproteins modulate host recycling by competing with Rab11 effectors. Journal of Cell Science. 129, 1697-1710 (2016).
- Wang, L., et al. Visualization of HIV T Cell Virological Synapses and Virus-Containing Compartments by Three-Dimensional Correlative Light and Electron Microscopy. Journal of Virology. 91, (2017).
- Doerflinger, S. Y., et al. Membrane alterations induced by nonstructural proteins of human norovirus. PLOS Pathogens. 13, 1006705 (2017).
- Dahl, R., Staehelin, L. A. High-pressure freezing for the preservation of biological structure: theory and practice. Journal of Electron Microscopy Technique. 13, 165-174 (1989).
- Romero-Brey, I., et al. Three-dimensional architecture and biogenesis of membrane structures associated with hepatitis C virus replication. PLOS Pathogens. 8, 1003056 (2012).
- Sosinsky, G. E., et al. The combination of chemical fixation procedures with high pressure freezing and freeze substitution preserves highly labile tissue ultrastructure for electron tomography applications. Journal of Structural Biology. 161, 359-371 (2008).
- Romero-Brey, I., et al. NS5A Domain 1 and Polyprotein Cleavage Kinetics Are Critical for Induction of Double-Membrane Vesicles Associated with Hepatitis C Virus Replication. MBio. 6, 00759 (2015).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36, 280-290 (2003).
- Jou, M. J., Jou, S. B., Guo, M. J., Wu, H. Y., Peng, T. I. Mitochondrial reactive oxygen species generation and calcium increase induced by visible light in astrocytes. Annals of the New York Academy of Sciences. 1011, 45-56 (2004).
- McDonald, K. L., Morphew, M., Verkade, P., Muller-Reichert, T. Recent advances in high-pressure freezing: equipment- and specimen-loading methods. Methods in Molecular Biology. 369, 143-173 (2007).
- Walther, P., Ziegler, A. Freeze substitution of high-pressure frozen samples: the visibility of biological membranes is improved when the substitution medium contains water. Journal of Microscopy. 208, 3-10 (2002).
- White, J. G., Southgate, E., Thomson, J. N., Brenner, S. The structure of the nervous system of the nematode Caenorhabditis elegans. Philosophical Transactions of the Royal Society B: Biological Sciences. 314, 1-340 (1986).
- Romero-Brey, I., Bartenschlager, R. Viral Infection at High Magnification: 3D Electron Microscopy Methods to Analyze the Architecture of Infected Cells. Viruses. 7, 6316-6345 (2015).
- McDonald, K. L., Webb, R. I. Freeze substitution in 3 hours or less. Journal of Microscopy. 243, 227-233 (2011).
- Villinger, C., Neusser, G., Kranz, C., Walther, P., Mertens, T. 3D Analysis of HCMV Induced-Nuclear Membrane Structures by FIB/SEM Tomography: Insight into an Unprecedented Membrane Morphology. Viruses. 7, 5686-5704 (2015).
- Paul-Gilloteaux, P., et al. eC-CLEM: flexible multidimensional registration software for correlative microscopies. Nature Methods. 14, 102-103 (2017).
- Polishchuk, R. S., Mironov, A. A. Correlative video light/electron microscopy. Current Protocols in Cell Biology Supplement. , 8 (2001).
- McDonald, K. L. A review of high-pressure freezing preparation techniques for correlative light and electron microscopy of the same cells and tissues. Journal of Microscopy. 235, 273-281 (2009).
- Newman, G. R., Jasani, B., Williams, E. D. A simple post-embedding system for the rapid demonstration of tissue antigens under the electron microscope. The Histochemical Journal. 15, 543-555 (1983).
- Schwarz, H., Humbel, B. M. Influence of fixatives and embedding media on immunolabelling of freeze-substituted cells. Scanning Microscopy. 3, 57-63 (1989).
- Luby-Phelps, K., Ning, G., Fogerty, J., Besharse, J. C. Visualization of identified GFP-expressing cells by light and electron microscopy. Journal of Histochemistry and Cytochemistry. 51, 271-274 (2003).
- Nixon, S. J., et al. A single method for cryofixation and correlative light, electron microscopy and tomography of zebrafish embryos. Traffic. 10, 131-136 (2009).
- McDonald, K. L. Rapid embedding methods into epoxy and LR White resins for morphological and immunological analysis of cryofixed biological specimens. Microscopy and Microanalysis. 20, 152-163 (2014).
- Webster, P., Schwarz, H., Griffiths, G. Preparation of cells and tissues for immuno EM. Methods in Cell Biology. 88, 45-58 (2008).
- Kukulski, W., et al. Correlated fluorescence and 3D electron microscopy with high sensitivity and spatial precision. Journal of Cell Biology. 192, 111-119 (2011).
- Peddie, C. J., et al. Correlative and integrated light and electron microscopy of in-resin GFP fluorescence, used to localise diacylglycerol in mammalian cells. Ultramicroscopy. 143, 3-14 (2014).
- Hampoelz, B., et al. Pre-assembled Nuclear Pores Insert into the Nuclear Envelope during Early Development. Cell. 166, 664-678 (2016).
- Lemercier, N., et al. Microtome-integrated microscope system for high sensitivity tracking of in-resin fluorescence in blocks and ultrathin sections for correlative microscopy. Scientific Reports. 7, 13583 (2017).
- Takizawa, T., Powell, R. D., Hainfeld, J. F., Robinson, J. M. FluoroNanogold: an important probe for correlative microscopy. Journal of Biological Chemistry. 8, 129-142 (2015).
- Romero-Brey, I., Yamauchi, Y. 3D electron microscopy (EM) and correlative light electron microscopy (CLEM) methods to study virus-host interactions. Methods in Molecular Biology: Influenza Virus Methods & Protocols. , (2018).

