Corrélatives microscopie électronique léger (CLEM) de suivi et d’imagerie protéine virale associés Structures des cellules immobilisées Cryo
Summary
Une méthode de microscopie corrélative électron (CLEM) est appliquée aux structures intracellulaires Viro-induite d’image par microscopie électronique (EM) dans les cellules qui sont préalablement sélectionnés par microscopie photonique (LM). LM et EM sont combinés en une approche d’imagerie hybride pour obtenir une vision intégrée des interactions virus-hôte.
Abstract
En raison de sa haute résolution, microscopie électronique (me) est un outil indispensable pour les virologues. Cependant, une des principales difficultés lors de l’analyse de cellules transfectées ou infectés par un virus par l’intermédiaire de EM sont les gains d’efficacité faibles d’infection ou de transfection, empêchant l’examen de ces cellules. Afin de surmonter cette difficulté, microscopie photonique (LM) peut être effectuée tout d’abord pour allouer la sous-population de cellules transfectées ou infectés. Ainsi, en profitant de l’utilisation des protéines fluorescentes (FPs) fusionnée à protéines virales, LM est utilisé ici pour enregistrer la position des cellules transfectées « positif », exprimant un FP et ça grimpe sur un support avec un modèle alphanumérique. Par la suite, les cellules sont traitées ultérieurement pour EM par haute pression gel (HPF), gel de substitution (FS) et l’incorporation de résine. L’étape de congélation ultra rapide assure membrane excellente préservation des cellules sélectionnées qui peuvent ensuite être analysées au niveau ultrastructural par microscopie électronique à transmission (TEM). Ici, un flux de travail étape par étape microscopie lumineuse corrélative (CLEM) est fourni, qui décrit la préparation de l’échantillon, l’imagerie et corrélation en détail. Le dispositif expérimental peut être également appliqué pour résoudre de nombreuses questions de biologie cellulaire.
Introduction
L’idée de combiner les deux modalités de microscopie pour obtenir une meilleure image d’un processus biologique spécifique est plutôt vieux. Ainsi, la toute première étude sur les virus « microscopie corrélative » a été publiée en 1960 comme deux publications distinctes1,2. Dans cette étude, les auteurs ont analysé les changements dans la morphologie du noyau induite par adénovirus au moyen de deux techniques de microscopie. Dans la première publication, les observations au microscope électronique (EM) décrivant les détails morphologiques associés à l’infection à adénovirus ont été signalés1. Dans une seconde publication, les différentes structures observées par EM étaient corrélés avec des images de microscopie photonique (LM) de colorations histochimiques, à définir la nature des structures observées précédemment par EM2.
Dans ces premières études, cependant, leurs observations ont été effectuées à l’aide de différentes cellules infectées préparés comme expériences indépendantes. La « corrélation » était, en effet, signifiait que la combinaison des informations provenant des deux modalités d’imagerie pour comprendre un certain phénomène, en comparant toutes les constatations qui ont été obtenues avec différentes épreuves afin de comprendre une donnée biologique processus.
De nos jours, la microscopie corrélative de terme, également connu sous le nom corrélatif microscopie photonique et électronique (CLEM), est appliquée à un nombre croissant de méthodes (révisé dans les références3,4,,5), avec les composants communs que les deux techniques d’imagerie (LM et EM) sont réalisées sur le même échantillon. La combinaison de ces deux méthodes entraîne, par conséquent, une analyse multimodale, multi-échelle et multidimensionnelle de cet échantillon3. Les avantages sont que LM peut fournir une vue d’ensemble de plusieurs cellules différentes, permettant d’identifier les sous-populations de cellules exprimant une protéine ou des protéines d’intérêt au sein d’une population hétérogène de cellules. EM permet de surmonter la limite de résolution de LM, fournissant une image de résolution plus élevée d’un événement particulier intracellulaire. En outre, EM permet la visualisation du contexte subcellulaire non fluorescent, y compris tous les organites liés à la membrane, grands complexes macromoléculaires (p. ex., ribosomes, centrioles, etc.) et des éléments du cytosquelette, ainsi fournissant des informations spatiales supplémentaires, le soi-disant « espace de référence »6et donnant le contexte à la tache fluorescente détectée par LM.
Au cours de ces dernières années, CLEM est devenu un outil puissant, non seulement pour la cellule biologistes5, mais aussi pour les virologues (revus en référence7) désireux de comprendre les interactions virus-cellules complexes qui conduisent à une propagation de virus avec succès. Ainsi, comprendre comment les virus modifient les membranes cellulaires et des organites à leur profit est essentiel de développer des médicaments antiviraux pour éradiquer les virus pathogènes.
Ici, CLEM on décrit une méthode qui permet la détection par LM de cellules exprimant des protéines virales fusionnés à une protéine fluorescente (FP). Ces cellules sont par la suite cryo-immobilisé et autrement préparés pour les analyses ultrastructurales par microscopie électronique à transmission (TEM) à acquérir de nouvelles connaissances dans l’expression de ces protéines Comment réorganiser les membranes intracellulaires (Figure 1). CLEM a été exécuté avec les cellules chimiquement fixes dans la plupart des études virologie publiées à la date8,9,10,11,12,13,14 ,15,16,17,18,19. C’est principalement en raison de la nécessité d’inactiver les matières infectieuses pour des raisons de biosécurité de niveau de biosécurité-2 et -3 (BSL-2 et niveau de biosécurité 3) laboratoires, où la cryo-immobilisation des cellules n’est généralement pas possible. Pour ces questions qui nécessitent une conservation optimale des membranes cellulaires, vitrification par haute pression gel (HPF) est, cependant, fortement recommandée de20. Dans ces cas, le protocole de CLEM décrit ici peut être appliqué. Fait intéressant, surtout si vous travaillez avec des échantillons infectieux, HPF peut être pratiquée sur les échantillons qui ont été précédemment chimiquement inactivés, par exemple dans les laboratoires BSL-2 et de niveau de biosécurité 3. La combinaison de fixation chimique suivie d’HPF est une possibilité de tirer profit au moins en partie des avantages de cryoconservation méthodes21,22.
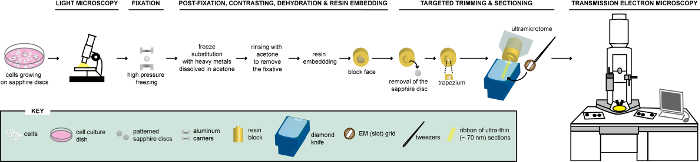
Figure 1 : Représentation schématique du flux de travail pour l’analyse des cellules via CLEM. Cellules qui croissent sur des disques saphir à motifs sont d’abord analysés par LM de localiser les cellules exprimant FPs avant leur traitement pour EM. Une fois localisé, les cellules sont immédiatement fixés par HPF et FS pour être par la suite incorporé dans la résine. Lors de la polymérisation de la résine, l’appui où sont développaient des cellules (= disques saphir) doivent être enlevés du bloc de résine. Le bloc contenant les cellules embarqués est réduit à un petit trapèze dont les cellules restantes, exprimant des FPs, sont sectionnés avec un couteau de diamant. Ultraminces sont recueillies sur des grilles de fente et examinées par TEM se renseigner ultrastructurale de ces cellules. Ce chiffre est adapté et modifié avec la permission de référence29. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
Protocol
Representative Results
Discussion
La méthodologie de CLEM présentée ici pour étudier l’impact d’une expression de la protéine virale sur les membranes cellulaires a été utilisée avec succès avant afin d’élucider le VHC réplication associées aux structures, principalement double membrane des vésicules (DMV)21, ainsi que pour déterminer les blocs de construction essentiels nécessaires à la formation de ces structures induite par le VHC23. Notez que dans notre premier travail à l’aide de CLEM pour étudier le VHC réplication21, une version légèrement modifiée du protocole décrit ici a été appliquée. À cet étude, épais disques saphir classique de 0,05 mm, sans modèle alphanumérique, servaient, dans laquelle un modèle de référence a été créé par carbone revêtement avec une grille de finder sur le dessus (voir Table des matières). Cette version du protocole actuel peut être éventuellement appliquée, avec l’avantage que le « A » transporteur pour HPF peut servir directement, sans avoir besoin de le couper vers le bas comme dans la Figure 3A. Sinon, comme mentionné dans le protocole, un épais « A » transporteur peuvent être utilisé (voir Table des matières) avec motifs disques saphir, sans avoir besoin d’un transporteur « B ».
Fait intéressant, ce protocole peut être appliqué non seulement d’étudier des échantillons de BSL-1, tels que les cellules transfectées avec des protéines virales comme décrit ici et d’ailleurs19,23, mais aussi pour étudier les cellules infectées par le virus. Bien que travailler avec des agents pathogènes humains est habituellement limitée aux laboratoires BSL-2 et de niveau de biosécurité 3, dans certains pays, il est toujours possible d’effectuer la cryo-immobilisation dans ces conditions de biosécurité. Dans ces BSL-2 et les laboratoires de niveau de biosécurité 3 où la vitrification n’est pas possible, en raison de la réglementation locale ou de l’absence d’une machine de HPF, les cellules infectées par le virus peuvent être toujours préparés en utilisant cette méthode, si la fixation chimique avec des aldéhydes est effectuée à l’avance, à savoir avant de quitter les installations BSL-2 ou de niveau de biosécurité 3. Par ailleurs, aldéhydes doivent être éteint immédiatement après fixation de garder la fluorescence, tandis que le reste du protocole est identique à celle décrite ici. Cette technique peut être considéré comme superflue parce que les cellules sont fixées deux fois, chimiquement et par l’intermédiaire de vitrification. Toutefois, ce protocole de double fixation entraîne en effet une bien meilleure conservation des DMV induite par le VHC en comparaison des DMV trouvés chez les cellules soumises à fixation chimique seul21.
Des modifications supplémentaires et dépannage le lecteur est renvoyé aux notes tout au long de la partie du protocole de ce manuscrit. Ces notes décrivent les pièges à éviter, ainsi que des solutions de rechange pour surmonter des difficultés qui pourraient surgir lors de l’exécution de cette méthode.
La condition principale pour l’application de cette technique est une machine de HPF. Cryo-immobiliser les cellules par l’intermédiaire de HPF n’est pas possible (à cause de l’absence d’une machine de HPF) ou n’est requise (pour la préservation de la membrane n’a pas besoin d’être optimale), lorsque les cellules peuvent être chimiquement fixe et par la suite préparé et analysés par EM8, 9,10,11,12,13,14,15,16,17,18 ,,19. Cette option ne requiert pas l’utilisation de disques saphir, mais Pétri de cellules avec des motifs maillées pour le déplacement de cellules ou agrégats cellulaires. Le principal avantage de l’utilisation de ces plats est leur plus grand diamètre par rapport aux disques saphir, permettant la projection de plus grandes surfaces. Ainsi, l’application du présent protocole de CLEM a été appliquée avec succès pour étudier l’effet d’un composé antiviral contre le VHC15 ou pour visualiser les réarrangements de membrane induites par les protéines non structurales du Norovirus19. Une autre question qui peut limiter les performances de cette méthode est l’absence d’un appareil commercial de FS. Dans ce cas, systèmes FS de base fait maison peuvent être utilisés à la place. Bien que les automatismes FS pourraient réduire les accidents de manutention, des dispositifs sont utilisés avec succès par exemple à30 de Kent McDonald et laboratoires de Paul Walther.
En ce qui concerne la fixation chimique, le protocole décrit ici garantit une conservation optimale des structures intracellulaires20. Par conséquent, dans le cas où les dispositifs HPF et FS susmentionnées sont disponibles, vitrification les cellules d’intérêt serait préférable.
Les alternatives à cette approche de CLEM incluent la possibilité d’utiliser cette méthode non seulement d’acquérir des informations 2D au niveau ultrastructural, mais aussi pour obtenir des informations sur l’architecture 3D d’altérations membranaires et organelle causées par des virus. Les méthodes 3D-EM, y compris la tomographie électronique (HE) et ionique focalisé faisceau-microscopie électronique (FIB-SEM) (largement décrit dans29), pourraient être également appliqués à des cellules qui ont été préparés en suivant ce protocole actuel21, 31. En outre, des informations 3D pourraient être également obtenues au niveau LM, lorsque vous utilisez un microscope confocal, qui permet l’acquisition de z-piles. En fait, cette option est fortement recommandée quand une corrélation précise entre les ensembles de données LM et EM est souhaitée (voir par exemple17). L’information incluse dans 3D z-piles du sida afin d’améliorer la corrélation avec les images 2D de TEM. Ainsi, dans un tel scénario, le meilleur montage images LM et EM peut être sélectionné et ensuite soumis à l’un des logiciels disponibles, comme le plugin d’ec-CLEM ICY (http://icy.bioimageanalysis.org/)32 ou le plugin de Landmark correspondances de corrélation Image J (http://imagej.net/Landmark_Correspondences), ayant pour résultat la génération de chevauchement des images LM-EM.
Lorsque l’information temporelle est nécessaire pour comprendre la cinétique d’un certain événement, Time-lapse imagerie peut être utilisé pour surveiller la dynamique de cellules vivantes en combinaison avec EM. Durant la manifestation d’intérêt, les cellules sont fixées immédiatement, générant un « instantané congelé » qui peut être analysé par la suite via EM, fournissant des informations détaillées et ultrastructurales sur ce moment particulier au moment de l’immobilisation. Afin d’obtenir cet « gelé instantané », après l’observation en temps réel, les cellules peuvent être chimiquement fixe33 ou cryo-immobilisé6. Puisque de nombreux processus cellulaires se produisent plus rapidement que les processus de diffusion de fixation chimique, si possible, la congélation ultra rapide doit être effectuée. Cependant, il est important de tenir compte du fait que les machines de HPF se différencient dans leur temps effectif résolution34.
En outre, bien que ce protocole a été conçu pour l’intégration des cellules dans une résine époxy, les cellules peuvent être incorporés aussi dans les résines de faible viscosité, tels que Lowicryls, LR blanc ou or LR. L’utilisation de ces médias encastrement permet de préserver l’antigénicité35,36, ainsi que de37,de fluorescence38 et, par conséquent, sont surtout utilisés pour l’enrobage après immunomarquage sur-section39 , 40 et sur-section CLEM41,42,43,44, où le LM s’effectue après l’incorporation. Les deux approches (immuno-EM et sur-section CLEM) doivent être cruciales pour ces expériences dans lesquelles des structures non caractéristiques peuvent être facilement trouvés via TEM et/ou comme témoin contre miscorrelation entre LM et EM signaux. De même, marquage avec des anticorps qui peuvent être visualisées par les deux modalités d’imagerie (LM et EM) peut être effectué45 afin, par exemple, identifier les cellules transfected dans LM (enrobage préalable d’étape) et d’atteindre une localisation plus précise de la Signal GFP via son étiquetage spécifique par immuno-EM (stade post-encastrement). Il doit être pris en compte, toutefois, cette perméabilisation a lieu avant LM pour permettre l’accès des anticorps à l’espace intracellulaire, ce qui pourrait entraîner une préservation optimale de l’architecture cellulaire au niveau de l’EM. Fait intéressant, ce protocole est également bien adapté pour multicolore des expériences qui peuvent être obtenus avec l’utilisation d’autres étiquettes fluorescentes, autre que GFP (comme illustré ici). En conclusion, il y a beaucoup de possibilités putatif d’adapter ce protocole, tant sur le LM, et/ou sur les côtés de l’EM, selon les questions qui sont abordées. Pour une description complète des autres protocoles alternatifs se reportera à5,46. Quelle que soit la façon dont les modalités de microscopie sont combinées, ensemble le résultat est un gain d’information, ce qui nous permet de mieux comprendre comment les virus et leurs protéines interagissent avec leurs hôtes dans la vraie vie.
L’étape la plus importante au sein de cette méthode est la collection de coupes sériées des cellules d’intérêt. Comme l’a souligné dans la section résultats représentatifs, cela nécessite de personnel spécialisé, ainsi que beaucoup de patience. Ce qui est important, cette étape est essentielle pour trouver les cellules retour au niveau de l’EM pour deux raisons. Tout d’abord, dans ce genre de protocole de CLEM avec incorporation des LM, les coordonnées ne sont visibles au niveau du LM et sur la face du bloc résine après l’incorporation. Toutefois, ils ne seront pas visibles sur les sections de TEM. Par conséquent, parage ciblée sur la face du bloc vers le bas aux régions d’intérêt (ROIs) doit être effectuée soigneusement avec une lame de rasoir pour s’assurer que les sections que l’on obtient par la suite contiennent les cellules exprimant un FP donnée. Deuxièmement, la « numérisation » plusieurs sections est nécessaire de trouver la meilleure superposition entre le LM et les acquisitions de l’EM. Contrairement aux méthodes où LM est effectuée à l’étape de l’incorporation, dans ce cas la superposition de LM-EM n’est pas si précise. La précision faible recouvrement est due aux différences dans la résolution axiale entre LM et EM, rétrécissement lors du traitement d’échantillon des EM et compression au cours de la section42. Néanmoins, des méthodes de suivi efficaces, telles que l’utilisation des points de repère, aident à isoler les cellules à l’arrière. Cela inclut la position d’une cellule à l’autre, ainsi que la forme des cellules et leur noyau. À cet égard, comme cela est expliqué dans le protocole, DIC images fournissent des informations « anatomique » des cellules qui sont essentiels pour améliorer la corrélation. Alternativement, les noyaux ou autres organites de la cellule bien reconnaissable (comme les mitochondries ou lipides gouttelettes) peuvent être colorées avant LM et utilisés comme points de repère.
Enfin, il convient de mentionner que, bien que ce manuscrit est axé sur l’utilisation de cette technique pour les études de la virologie, la portée de ce dispositif expérimental peut être étendue pour répondre à des questions biologiques plus générales.
Declarações
The authors have nothing to disclose.
Acknowledgements
Nous sommes très reconnaissants aux membres du personnel de la microscopie électronique Core installations (FECOM) à l’EMBL (Heidelberg) et à l’Université de Heidelberg. Nous avons également voudrais remercier Ulrike Herian, Stephanie Kallis et Andrea Hellwig (Université de Heidelberg), ainsi que Eberhardt Schmidt et Renate Kunz (Université d’Ulm) pour l’assistance technique d’experts. Travail par R.B. et son équipe (C.H.U et I.R.-B.) a été soutenu par la Deutsche Forschungsgemeinschaft, TP11 et SFB1129, TRR83, TP13.
Materials
| UV Crosslinker | Stratagene | 400072 | Stratalinker 1800, 230Vac, equipped with 254-nm UV light bulbs, 8-watts/each. |
| Patterned sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 627 | They have a 0.3-mm diameter and are 0.16-mm thick, as well as an an etched alphanumeric pattern to allow for re-location of the cells. They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Slim and long tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | 72919-SS | "Style SS", for handling sapphire discs. |
| Cell culture medium | Thermo Fisher Scientific, Waltham, MA, USA | 41965-062 | Dulbecco's modified Eagle medium (DMEM) supplemented with 2 mM L-glutamine, nonessential amino acids, 100 units penicillin per ml, 100 µg streptomycin per ml and 10% fetal calf serum (DMEM complete, see below). Package containing 10 bottles, 500 ml/each. |
| L-glutamine | Thermo Fisher Scientific, Waltham, MA, USA | 25030-123 | Package containing 20 bottles of 100 ml/each. |
| Nonessential amino acids | Thermo Fisher Scientific, Waltham, MA, USA | 11140-068 | Package containing 20 bottles of 100 ml/each. |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Waltham, MA, USA | 15140-163 | Package containing 20 bottles of 100 ml/each. |
| Fetal calf serum | Sigma Aldrich, St. Louis, MI, USA | F7524 | Bottle of 50 ml. |
| Inverted microscope | Olympus Deutschland, Hamburg, Germany | CKX41 | It is an inverted microscope with trinocular head options and fluorescence upgrade capability. |
| Huh7-Lunet cells stably expressing the T7 RNA-polymerase | Avaliable at Prof. Dr. Ralf Bartenschlager laboratory | Not available | Contact Prof. Bartenschlager at: ralf.bartenschlager@med.uni-heidelberg.de. |
| Mirus TransIT-LT1 Transfection Reagent | Mirus Bio LLC, Madison, USA | MIR 2304 | Broad spectrum, low toxicity, DNA transfection reagent. Vial of 0.4 ml. |
| Inverted widefield fluorescence microscope | Carl Zeiss Microscopy GmbH, Germany | Zeiss Observer.Z1 | Inverted fluorescence microscope for experiments involving living cell cultures. |
| 1-hexadecene | Merck, Darmstadt, Germany | 8220640100 | Bottle of 100 ml. |
| "A" aluminium holders for high pressure frezing (HPF) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 241 | This is the holder that has been used for this protocol and has 2 different depths of 0.1 and 0.2-mm. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "B" aluminium holders for HPF | Engineering Office M. Wohlwend, Sennwald, Switzerland | 242 | This is the holder that has been used for this protocol.It is 0.3-mm thick.They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "A" aluminium holder for HPF (special for working with patterned sapphire discs) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 737 | This is the holder than can be used alone with the patterned sapphire disc (as an alternative to the current protocol), without the need of a "B" holder or the edition of the "A" holder. It is 0.84-mm thick. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 405 | These sapphires discs are the "conventional" one, with a 0.3-mm diameter and a thickness of 0.05 mm . They can be also used for CLEM as an alternative instead of patterned sapphire discs. |
| Finder grids | Electron Microscopy Sciences, Hatfield, Philadelphia, USA | LF135-Cu | These 135 mesh grids are used to create an alphanumeric pattern on "conventional" sapphire discs (described above) via carbon coating, so that they can be used for CLEM. 100 grids/vial. |
| HPF machine | ABRA Fluid AG, Widnau, Switzerland | HPM 01 | This HPF machine has been used for this protocol. |
| HPF machine | Leica Microsystems, Vienna, Austria | EMPACT 2 | "EMPACT 2", as an alternative to the use of the HPM machine that it has been used in this protocol (described above). |
| Cryo-tubes | Thermo Fisher Scientific, Waltham, MA, USA | Z763667-500EA | For long term-storage of cryo-immobilized samples in liquid nitrogen. Package containing 500 cryovials. |
| Liquid nitrogen dewar | Cole-Parmer GmbH, Wertheim, Germany | GZ-05094-60 | For long term-storage of cryo-immobilized samples in liquid nitrogen, equipped with cryo-racks with a capacity of 1600 cryo-tubes. |
| Automatic freeze substitution (AFS) machine | Leica Microsystems, Vienna, Austria | EM AFS2 | This machine performs freeze substitution and progressive lowering of temperature (PLT) techniques and allows low temperature embedding and polymerization of resins. |
| Osmium tetroxide (OsO4) | Electron Microscopy Sciences, Hatfield, PA, USA | 19150 | 4% aqueous solution, one box containing 10 x 2 ml ampules. |
| Uranyl-Acetate (UA) | Serva, Heidelberg, Germany | 77879.01 | Bottle containing 25 grs of (UA)-2 H2O. |
| Sonicator | Bandelin Electronic, Berlin, Germany | 329 | "Sonorex Super RK 31" is a high-power ultrasonic cleaning bath for aqueous cleaning solution that is used in this protocol to mix OsO4 and Ua when preparing the FS medium. |
| Glass-distilled acetone | Electron Microscopy Sciences, Hatfield, PA, USA | 10015 | Bottle of 100 ml. |
| Stereomicroscope | Leica Microsystems, Vienna, Austria | Leica M80 | Routine stereomicroscope for daily inspections, equipped with a camera for capturing images. |
| Epoxy resin | Electron Microscopy Sciences, Hatfield, PA, USA | 14120 | Embed 812 is a kit containing several components that must be mix together in the proportions given by the manufacturers. |
| Flow through rings | Leica Microsystems, Vienna, Austria | 16707157 | Package containing 100 pieces. |
| Reagent baths | Leica Microsystems, Vienna, Austria | 16707154 | Package containing 100 pieces. |
| Ultramicrotome | Leica Microsystems, Vienna, Austria | Leica EM UC7 | Ultramicrotome for preparation of semi- and ultrathin sections at room temperature. |
| Ultra 35° diamond knife | Diatome Ltd., Nidau Switzerland |
AGG339-735 | This knife have an edge length of 3 mm. |
| Ultra fine tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | E78318 | "Style 3X", for handling EM grids. |
| EM slot grids | Electron Microscopy Sciences, Hatfield, PA, USA | G2010-Cu | 100 grids/vial. |
| EM grid storage box | Electron Microscopy Sciences, Hatfield, PA, USA | 71155 | It has capacity for 100 grids. |
Referências
- Morgan, C., Godman, G. C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. I. Electron microscopy. Journal of Experimental Medicine. 112, 373-382 (1960).
- Godman, G. C., Morgan, C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. II. Light microscopy. Journal of Experimental Medicine. 112, 383-402 (1960).
- Caplan, J., Niethammer, M., Taylor, R. M., Czymmek, K. J. The power of correlative microscopy: multi-modal, multi-scale, multi-dimensional. Current Opinion in Structural Biology. 21, 686-693 (2011).
- de Boer, P., Hoogenboom, J. P., Giepmans, B. N. Correlated light and electron microscopy: ultrastructure lights up. Nature Methods. 12, 503-513 (2015).
- Müller-Reichert, T., Verkade, P. . Correlative light and electron microscopy III, First edition. , (2017).
- Brown, E., Mantell, J., Carter, D., Tilly, G., Verkade, P. Studying intracellular transport using high-pressure freezing and Correlative Light Electron Microscopy. Seminars in Cell and Developmental Biology. 20, 910-919 (2009).
- Bykov, Y. S., Cortese, M., Briggs, J. A., Bartenschlager, R. Correlative light and electron microscopy methods for the study of virus-cell interactions. FEBS Letters. , (2016).
- Spuul, P., et al. Assembly of alphavirus replication complexes from RNA and protein components in a novel trans-replication system in mammalian cells. Journal of Virology. 85, 4739-4751 (2011).
- Nagel, C. H., Dohner, K., Binz, A., Bauerfeind, R., Sodeik, B. Improper tagging of the non-essential small capsid protein VP26 impairs nuclear capsid egress of herpes simplex virus. PLoS One. 7, 44177 (2012).
- Sharma, M., Kamil, J. P., Coughlin, M., Reim, N. I., Coen, D. M. Human cytomegalovirus UL50 and UL53 recruit viral protein kinase UL97, not protein kinase C, for disruption of nuclear lamina and nuclear egress in infected cells. Journal of Virology. 88, 249-262 (2014).
- Kallio, K., et al. Template RNA length determines the size of replication complex spherules for Semliki Forest virus. Journal of Virology. 87, 9125-9134 (2013).
- Martinez, M. G., Snapp, E. L., Perumal, G. S., Macaluso, F. P., Kielian, M. Imaging the alphavirus exit pathway. Journal of Virology. 88, 6922-6933 (2014).
- Lebrun, M., et al. Varicella-zoster virus induces the formation of dynamic nuclear capsid aggregates. Virology. 454-455, 311-327 (2014).
- Madela, K., et al. A simple procedure to analyze positions of interest in infectious cell cultures by correlative light and electron microscopy. Methods in Cell Biology. 124, 93-110 (2014).
- Berger, C., et al. Daclatasvir-like inhibitors of NS5A block early biogenesis of hepatitis C virus-induced membranous replication factories, independent of RNA replication. Gastroenterology. 147, 1094-1105 (2014).
- van der Schaar, H. M., et al. Illuminating the Sites of Enterovirus Replication in Living Cells by Using a Split-GFP-Tagged Viral Protein. mSphere. 1, (2016).
- Vale-Costa, S., et al. Influenza A virus ribonucleoproteins modulate host recycling by competing with Rab11 effectors. Journal of Cell Science. 129, 1697-1710 (2016).
- Wang, L., et al. Visualization of HIV T Cell Virological Synapses and Virus-Containing Compartments by Three-Dimensional Correlative Light and Electron Microscopy. Journal of Virology. 91, (2017).
- Doerflinger, S. Y., et al. Membrane alterations induced by nonstructural proteins of human norovirus. PLOS Pathogens. 13, 1006705 (2017).
- Dahl, R., Staehelin, L. A. High-pressure freezing for the preservation of biological structure: theory and practice. Journal of Electron Microscopy Technique. 13, 165-174 (1989).
- Romero-Brey, I., et al. Three-dimensional architecture and biogenesis of membrane structures associated with hepatitis C virus replication. PLOS Pathogens. 8, 1003056 (2012).
- Sosinsky, G. E., et al. The combination of chemical fixation procedures with high pressure freezing and freeze substitution preserves highly labile tissue ultrastructure for electron tomography applications. Journal of Structural Biology. 161, 359-371 (2008).
- Romero-Brey, I., et al. NS5A Domain 1 and Polyprotein Cleavage Kinetics Are Critical for Induction of Double-Membrane Vesicles Associated with Hepatitis C Virus Replication. MBio. 6, 00759 (2015).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36, 280-290 (2003).
- Jou, M. J., Jou, S. B., Guo, M. J., Wu, H. Y., Peng, T. I. Mitochondrial reactive oxygen species generation and calcium increase induced by visible light in astrocytes. Annals of the New York Academy of Sciences. 1011, 45-56 (2004).
- McDonald, K. L., Morphew, M., Verkade, P., Muller-Reichert, T. Recent advances in high-pressure freezing: equipment- and specimen-loading methods. Methods in Molecular Biology. 369, 143-173 (2007).
- Walther, P., Ziegler, A. Freeze substitution of high-pressure frozen samples: the visibility of biological membranes is improved when the substitution medium contains water. Journal of Microscopy. 208, 3-10 (2002).
- White, J. G., Southgate, E., Thomson, J. N., Brenner, S. The structure of the nervous system of the nematode Caenorhabditis elegans. Philosophical Transactions of the Royal Society B: Biological Sciences. 314, 1-340 (1986).
- Romero-Brey, I., Bartenschlager, R. Viral Infection at High Magnification: 3D Electron Microscopy Methods to Analyze the Architecture of Infected Cells. Viruses. 7, 6316-6345 (2015).
- McDonald, K. L., Webb, R. I. Freeze substitution in 3 hours or less. Journal of Microscopy. 243, 227-233 (2011).
- Villinger, C., Neusser, G., Kranz, C., Walther, P., Mertens, T. 3D Analysis of HCMV Induced-Nuclear Membrane Structures by FIB/SEM Tomography: Insight into an Unprecedented Membrane Morphology. Viruses. 7, 5686-5704 (2015).
- Paul-Gilloteaux, P., et al. eC-CLEM: flexible multidimensional registration software for correlative microscopies. Nature Methods. 14, 102-103 (2017).
- Polishchuk, R. S., Mironov, A. A. Correlative video light/electron microscopy. Current Protocols in Cell Biology Supplement. , 8 (2001).
- McDonald, K. L. A review of high-pressure freezing preparation techniques for correlative light and electron microscopy of the same cells and tissues. Journal of Microscopy. 235, 273-281 (2009).
- Newman, G. R., Jasani, B., Williams, E. D. A simple post-embedding system for the rapid demonstration of tissue antigens under the electron microscope. The Histochemical Journal. 15, 543-555 (1983).
- Schwarz, H., Humbel, B. M. Influence of fixatives and embedding media on immunolabelling of freeze-substituted cells. Scanning Microscopy. 3, 57-63 (1989).
- Luby-Phelps, K., Ning, G., Fogerty, J., Besharse, J. C. Visualization of identified GFP-expressing cells by light and electron microscopy. Journal of Histochemistry and Cytochemistry. 51, 271-274 (2003).
- Nixon, S. J., et al. A single method for cryofixation and correlative light, electron microscopy and tomography of zebrafish embryos. Traffic. 10, 131-136 (2009).
- McDonald, K. L. Rapid embedding methods into epoxy and LR White resins for morphological and immunological analysis of cryofixed biological specimens. Microscopy and Microanalysis. 20, 152-163 (2014).
- Webster, P., Schwarz, H., Griffiths, G. Preparation of cells and tissues for immuno EM. Methods in Cell Biology. 88, 45-58 (2008).
- Kukulski, W., et al. Correlated fluorescence and 3D electron microscopy with high sensitivity and spatial precision. Journal of Cell Biology. 192, 111-119 (2011).
- Peddie, C. J., et al. Correlative and integrated light and electron microscopy of in-resin GFP fluorescence, used to localise diacylglycerol in mammalian cells. Ultramicroscopy. 143, 3-14 (2014).
- Hampoelz, B., et al. Pre-assembled Nuclear Pores Insert into the Nuclear Envelope during Early Development. Cell. 166, 664-678 (2016).
- Lemercier, N., et al. Microtome-integrated microscope system for high sensitivity tracking of in-resin fluorescence in blocks and ultrathin sections for correlative microscopy. Scientific Reports. 7, 13583 (2017).
- Takizawa, T., Powell, R. D., Hainfeld, J. F., Robinson, J. M. FluoroNanogold: an important probe for correlative microscopy. Journal of Biological Chemistry. 8, 129-142 (2015).
- Romero-Brey, I., Yamauchi, Y. 3D electron microscopy (EM) and correlative light electron microscopy (CLEM) methods to study virus-host interactions. Methods in Molecular Biology: Influenza Virus Methods & Protocols. , (2018).

