Potensering af Anticancer antistof effektivitet af antineoplastiske stoffer: påvisning af antistof-drug synergi med kombination indeks ligning
Summary
Denne protokol beskriver hvordan man vurdere synergi mellem en anticancer antistof og antineoplastiske stoffer i prækliniske modeller ved hjælp af kombination indeks ligning af Chou og Talalay.
Abstract
Potensering af fjendtlige monoklonale antistoffer (mAb) af kemoterapeutiske stoffer udgør en værdifuld strategi til design effektiv og sikker behandling mod kræft. Her giver vi en protokol for at identificere en rationel kombination på den prækliniske trin. Først, vi beskriver en celle-baseret analyse for at vurdere den synergi mellem anticancer mAb og cytotoksiske stoffer, der bruger kombination indeks ligning af Chou og Talalay1. Dette omfatter måling af tumor celle stof og antistof-følsomhed ved hjælp af en MTT assay, efterfulgt af en automatiseret computer analyse til at beregne kombination indeks (CI) værdier. CI værdier i < 1 angive synergi mellem testet mAbs og cytotoksiske agenser1. For at underbygge den in vitro- resultaterne i vivo, vi yderligere at beskrive en metode til at vurdere kombination regime effektiviteten i en xenograft tumor model. I denne model forsinker den kombinerede regime betydeligt tumorvækst, hvilket resulterer i en betydelig udvidet overlevelse i forhold til single-agent kontrol. Vigtigere, afslører i vivo forsøg, at kombination regime er veltolereret. Denne protokol giver mulighed for en effektiv evaluering af anticancer narkotika kombinationer i prækliniske modeller og identifikation af rationel kombination at evaluere i kliniske forsøg.
Introduction
Den konventionelle tilgang til behandling af et stort antal forskellige typer kræft var baseret på monoterapi. Selv hvis det bruges stadig i mange tilfælde, mødte denne metode flere forhindringer fører til vælger kombinerede terapier2. Navnlig, er kræftceller mere modtagelige for at udvikle resistens når behandlet med en enkelt drug ved at inducere alternative overlevelse mekanismer3, hvilket resulterer i behandlingssvigt i patienter4. Derudover i monoterapi, er narkotika normalt administreres på en høj dosis. Denne situation ofte resulterer i forekomsten af stærk dosisafhængig bivirkninger, der kan være uacceptabel og tvinge læger til at stoppe behandling2. Af disse grunde, Sammenslutningen af anticancer molekyler er nu foretrukket at monoterapi.
Ideel drug kombinationer vil være dem, som handle i synergi mod tumorceller, uden øget toksicitet mod normale celler. Synergi refererer til samspillet mellem to eller flere stoffer, der producerer en terapeutisk effekt større end summen af hver enkelt drug handler separat. Sådanne interaktioner kan resultere i forbedrede kliniske terapeutiske virkning2. Det begrænser behandling modstand, øger effektiviteten og kan også reducere toksicitet2. I virkeligheden, kan dosis af hvert stof reduceres til at sænke deres bivirkninger ved at målrette forskellige veje. Desuden kan en af molekylerne også tjene som en sensibiliserende agens mod kræftceller. Effekten af den anden medicin kan forbedres på overfølsomme over celler og færre doser kan være brugt5.
Kombineret behandling kan indeholde to eller flere kemoterapeutiske stoffer og/eller biologiske lægemidler, såsom monoklonale antistoffer6. Disse mAbs målrettet mod celler, der udtrykker en celle overflade antigen af interesse og er i stand til at dræbe tumorceller gennem immunologiske veje herunder antistof-afhængige celle-medieret cytotoksicitet (ADCC), med inddragelse af immun effektor celler 7, og komplement-afhængig cytotoksicitet (CDC)6. De kan også handle via en ikke-immunologiske mekanisme medieret apoptose8,9,10,11. I dette tilfælde kan induktion af programmeret celledød processen bevidstgøre kræftceller svække deres funktion og effektivisere den tilknyttede kemoterapeutiske stof ved en lavere dosering. Som sådan proapoptotic mAb er gode kandidater til at designe kombination regimer med antineoplastiske stoffer.
Forskellige matematiske modeller er blevet beskrevet til at vurdere stoffet synergi; en af dem er baseret på kombination indeks metode1. Denne metode er baseret på median-effekt princippet udviklet af Chou1. Median-effekt ligning korrelerer stof dosis og narkotika virkning som følger.
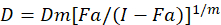
Her, er D stof dosis; DM er den dosis, median-effekt; FA er den fraktion, påvirket af dosis; m er en eksponent, der angiver formen af dosis-effekt plot1. Median-effekt dosis bruges til at beregne dosis Dx af et stof, der hæmmer eller dræber “x” procent af celler. CI værdien beregnes derefter for at vurdere stoffet kombination, som følger1additiv virkning.
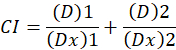
CI værdien 1 angiver en additiv effekt og et CI værdien af 1 angiver antagonisme1. Anvendelsen af denne metode er yderligere fremmet af tilgængeligheden af et edb-program, CompuSyn, der bestemmer synergi og antagonisme på alle doser eller effekt niveauer simuleret automatisk12.
Vores gruppe har udviklet mAb 8B6 specifikke for O-acetyl-GD2 ganglioside (OAcGD2) neuroblastoma antigen13 og yderligere vist at denne mAb er i stand til at fremkalde celledød med attributter af apoptose11. For at teste, om mAb 8B6 kan bevidstgøre neuroblastoma celler til antineoplastisk agent topotecan, tilpasset vi den ovennævnte metode udviklet af Chou1. Først, vi bestemme de effektive dosis 50 (ED50) værdier af mAb 8B6 og topotecan. Næste, neuroblastoma celler med equipotent forhold mellem de to forbindelser baseret på ED50 værdier er udsat for at bestemme de CI værdier ved hjælp af ovennævnte simulation software. Denne metode gør det muligt for os at demonstrere synergi mellem mAb 8B6 og topotecan in vitro. Næste, vi beskriver en protokol for at yderligere vurdere styrken og sikkerheden af denne kombination regime i vivo. Denne protokol kan nemt anvendes for at markere potente og sikre anticancer mAb og kemoterapeutiske agent kombinationer i prækliniske studier. En skematisk gengivelse af denne undersøgelse er fastsat i figur 1.
Protocol
Representative Results
Discussion
For at forudsige effekten af lægemiddelinteraktioner, der kan anvendes tre metoder: isobologram metode17, ikke-lineære blanding model18og kombinationen indeks1. Kombination indeks analyse er de mest almindeligt anvendte fordi dens anvendelse er forenklet af tilgængeligheden af et brugervenligt computerprogram. Til dette formål karakteriseret vi først dosis-effekt svar af hver agent, anvendt alene eller i kombination, ved at udføre en MTT assay<…
Declarações
The authors have nothing to disclose.
Acknowledgements
Yde støtte: Fondation de Projet de L ‘Université de Nantes, les Bagouz’ à Manon, La Ligue contre le Cancer comité de Loire-Atlantique, comité du Morbihan og comité de Vendée, une steg hæld S.A.R.A.H, L’Etoile de Martin og la Société Française de Lutte contre les Kræftformer et les leucémies de L’Enfant et de L’adolescent (SFCE). M.B. og J.F. understøttes af La Ligue Contre Le Cancer. Forfatterne takke UTE-facilitet i struktur Fédérative de Recherche François Bonamy. Forfatterne også takke Dr. S. Suzin (Inserm, Paris) for at give IMR5 cellerne og Ms. H. Estéphan for hendes teknisk bistand.
Materials
| Cell Proliferation kit (MTT) | Roche | 11-465-007-001 | |
| CompuSyn software | ComboSyn | Combosyn can be downloaded for free at http://www.combosyn.com | |
| Electric shaver | Bioseb | BIO-1556 | |
| Fetal calf serum | Eurobio | CVFSVFF00-01 | 10% heat-inactivated fetal calf serum in RPMI 1640 |
| Firefox | Mozilla Corporation | Firefox can be downloaded for free at http://www.mozilla.org/en-US/firefox/ | |
| Heat lamp | Verre&Quartz | 4003/1R | |
| Human neuroblastoma IMR-5 cell line | Accegen Biotechnology | ABC-TC0450 | IMR-5 is a clone of the human neuroblastoma cell line IMR32 5459762. IMR-5 cells were generously provided by Dr. Santos Susin (U.872, Paris, France) |
| L-glutamine | Gibco | 25030-024 | 2 mM in RPMI 1640 |
| Lysis solution | Roche | 11-465-007-001 | |
| mAb 8B6 | University of Nantes | N/A | |
| Matrigel | Corning | 354248 | |
| Multiskan FC | Thermofischer Scientific | N08625 | |
| Needle 21G 1 ½ | BD Microlance | 304432 | |
| Needle 25G 1 | Terumo | NN-2525R | |
| NSG mice | Charles River Laboratories | 5557 | |
| Nunc MicroWell 96-well microplates | Thermofisher | 167008 | |
| PBS | VWR | L182-10 | |
| PBS, 0,05% EDTA | Sigma-Aldrich | E9884 | |
| PC that runs windows 7 | Microsoft | Windows 7 can be purchased at http://www.microsoft.com/en-gb/software-download/windows7 | |
| Penicillin-Streptomycin | Gibco | 15140-122 | 100 units/mL penicillin and 100 mg/mL streptomycin in RPMI 1640 |
| Reagent reservoir | Thermofischer Scientific | 8094 | |
| Rodent restrainer | Bioseb | TV-150-SM | |
| RPMI 1640 | Gibco | 31870-025 | |
| Syringe 1 mL | Henke Sass Wolf | 5010.200V0 | |
| Topotecan | Sigma-Aldrich | T2705 |
Referências
- Chou, T. C. Theoretical basis, experimental design, and computerized simulation of synergism and antagonism in drug combination studies. Pharmacological Reviews. 58 (3), 621-681 (2006).
- Bayat Mokhtari, R., et al. Combination therapy in combating cancer. Oncotarget. 8 (23), 38022-38043 (2017).
- Zahreddine, H., Borden, K. L. Mechanisms and insights into drug resistance in cancer. Frontiers in Pharmacology. 4, 28 (2013).
- Martin, T. P., Baguley, D., et al. Re: “Postoperative validation of bone-anchored implants in the single-sided deafness population.” Snapp et al. Otol Neurotol 2012: 33;291-6. Otol Neurotol. 34 (4), 777-778 (2013).
- Choi, B., et al. Sensitization of lung cancer cells by altered dimerization of HSP27. Oncotarget. 8 (62), 105372-105382 (2017).
- Weiner, L. M., Surana, R., Wang, S. Monoclonal antibodies: versatile platforms for cancer immunotherapy. Nature Reviews Immunology. 10 (5), 317-327 (2010).
- Mellor, J. D., Brown, M. P., Irving, H. R., Zalcberg, J. R., Dobrovic, A. A critical review of the role of Fc gamma receptor polymorphisms in the response to monoclonal antibodies in cancer. Journal of Hematology & Oncology. 6, 1 (2013).
- Kowalczyk, A., et al. The GD2-specific 14G2a monoclonal antibody induces apoptosis and enhances cytotoxicity of chemotherapeutic drugs in IMR-32 human neuroblastoma cells. Cancer Letters. 281 (2), 171-182 (2009).
- Retter, M. W., et al. Characterization of a proapoptotic antiganglioside GM2 monoclonal antibody and evaluation of its therapeutic effect on melanoma and small cell lung carcinoma xenografts. Pesquisa do Câncer. 65 (14), 6425-6434 (2005).
- Nakamura, K., et al. Apoptosis induction of human lung cancer cell line in multicellular heterospheroids with humanized antiganglioside GM2 monoclonal antibody. Pesquisa do Câncer. 59 (20), 5323-5330 (1999).
- Cochonneau, D., et al. Cell cycle arrest and apoptosis induced by O-acetyl-GD2-specific monoclonal antibody 8B6 inhibits tumor growth in vitro and in vivo. Cancer Letters. 333 (2), 194-204 (2013).
- Chou, T. C., Martin, N. . CompuSyn for drug combinations: PC software and user’s guide: a computer program for quantitation of synergism and antagonism in drug combinations, and the determination of IC50 and ED50 and LD50 values. , (2005).
- Alvarez-Rueda, N., et al. A monoclonal antibody to O-acetyl-GD2 ganglioside and not to GD2 shows potent anti-tumor activity without peripheral nervous system cross-reactivity. PLoS One. 6 (9), e25220 (2011).
- Faraj, S., et al. Neuroblastoma chemotherapy can be augmented by immunotargeting O-acetyl-GD2 tumor-associated ganglioside. Oncoimmunology. 7 (1), e1373232 (2017).
- Ishikawa, F., et al. Development of functional human blood and immune systems in NOD/SCID/IL2 receptor {gamma} chain(null) mice. Blood. 106 (5), 1565-1573 (2005).
- Ullman-Cullere, M. H., Foltz, C. J. Body condition scoring: a rapid and accurate method for assessing health status in mice. Laboratory Animal Science. 49 (3), 319-323 (1999).
- Teicher, B. A. Assays for in vitro and in vivo synergy. Methods in Molecular Medicine. 85, 297-321 (2003).
- White, D. B., Slocum, H. K., Brun, Y., Wrzosek, C., Greco, W. R. A new nonlinear mixture response surface paradigm for the study of synergism: a three drug example. Current Drug Metabolism. 4 (5), 399-409 (2003).
- Mosmann, T. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. Journal of Immunological Methods. 65 (1-2), 55-63 (1983).
- Huyck, L., Ampe, C., Van Troys, M. The XTT cell proliferation assay applied to cell layers embedded in three-dimensional matrix. Assay and Drug Development Technologies. 10 (4), 382-392 (2012).
- Thompson, J., et al. Synergy of topotecan in combination with vincristine for treatment of pediatric solid tumor xenografts. Clinical Cancer Research. 5 (11), 3617-3631 (1999).
- Tan, M., Fang, H. B., Tian, G. L., Houghton, P. J. Experimental design and sample size determination for testing synergism in drug combination studies based on uniform measures. Statistic in Medicine. 22 (13), 2091-2100 (2003).
- Tang, X. X., et al. Implications of EPHB6, EFNB2, and EFNB3 expressions in human neuroblastoma. Proceding of the National Academy of Sciences of the United States of America. 97 (20), 10936-10941 (2000).
- Mehta, R. R., Graves, J. M., Hart, G. D., Shilkaitis, A., Das Gupta, T. K. Growth and metastasis of human breast carcinomas with Matrigel in athymic mice. Breast Cancer Research and Treatment. 25 (1), 65-71 (1993).
- Mullen, P., Ritchie, A., Langdon, S. P., Miller, W. R. Effect of Matrigel on the tumorigenicity of human breast and ovarian carcinoma cell lines. International Journal of Cancer. 67 (6), 816-820 (1996).
- Feng, C., Tang, S., Wang, J., Liu, Y., Yang, G. Topotecan plus cyclophosphamide as maintenance chemotherapy for children with high-risk neuroblastoma in complete remission: short-term curative effects and toxicity. Nan Fang Yi Ke Da Xue Xue Bao. 33 (8), 1107-1110 (2013).
- Cheung, N. K., et al. Ganglioside GD2 specific monoclonal antibody 3F8: a phase I study in patients with neuroblastoma and malignant melanoma. Journal of Clininical Oncology. 5 (9), 1430-1440 (1987).
- Nair, A. B., Jacob, S. A simple practice guide for dose conversion between animals and human. Journal of Basic Clinical Pharmacy. 7 (2), 27-31 (2016).
- Dayde, D., et al. Tumor burden influences exposure and response to rituximab: pharmacokinetic-pharmacodynamic modeling using a syngeneic bioluminescent murine model expressing human CD20. Blood. 113 (16), 3765-3772 (2009).
- Racki, W. J., et al. NOD-scid IL2rgamma(null) mouse model of human skin transplantation and allograft rejection. Transplantation. 89 (5), 527-536 (2010).
- Sherif, A., Winerdal, M., Winqvist, O. Immune Responses to Neoadjuvant Chemotherapy in Muscle Invasive Bladder Cancer. Bladder Cancer. 4 (1), 1-7 (2018).

