Elektromechanische beoordeling van optogenetisch gemoduleerde cardiomyocyteactiviteit
Summary
We presenteren een protocol voor de evaluatie van de elektromechanische effecten van GtACR1 activering bij konijnencardiomyocyten. We geven gedetailleerde informatie over celisolatie, kweek- en adenovirale transductie, en over functionele experimenten met de patch-clamp en koolstofvezel technieken.
Abstract
In de afgelopen twee decennia zijn optogenetische instrumenten opgericht als krachtige middelen om cel-type specifieke activiteit in prikkelbare weefsels, waaronder het hart, te moduleren. Terwijl Channelrhodopsin-2 (ChR2) is een gemeenschappelijk instrument om het membraan potentieel in cardiomyocyten (CM) depolariseren, potentieel uitlokken actie potentials (AP), een effectief instrument voor betrouwbare uitschakeling van CM activiteit is ontbreekt. Er is voorgesteld om anion channelrhodopsins (ACR) te gebruiken voor optogenetische remming. Hier beschrijven we een protocol om de effecten van het activeren van de natuurlijke ACR GtACR1 van Guillardia theta in gekweekt konijn CM te beoordelen. Het protocol omvat CM isolatie van konijnenhart, zaaien en kweken van de cellen voor maximaal 4 dagen, transductie via adenovirus codering voor de licht-gated chloride kanaal, voorbereiding van patch-klem en koolstofvezel setups, data verzameling en analyse. Met behulp van de patch-clamp techniek in hele cel configuratie kan men licht geactiveerde stromen (in spanning-klem modus, V-klem) en AP (huidige-klem modus, I-klem) op te nemen in real time. Naast patch-clamp experimenten, voeren we contractility metingen voor functionele beoordeling van CM activiteit zonder verstoring van de intracellulaire milieu. Om dit te doen, cellen zijn mechanisch voorgeladen met behulp van koolstofvezels en contracties worden geregistreerd door het bijhouden van veranderingen in sarcomere lengte en koolstofvezel afstand. Data-analyse omvat de beoordeling van de AP-duur van I-klem opnames, piekstromen van V-klem opnames en krachtberekening van koolstofvezelmetingen. Het beschreven protocol kan worden toegepast op het testen van biofysische effecten van verschillende optogenetische actuatoren op CM-activiteit, een voorwaarde voor de ontwikkeling van een mechanistisch begrip van optogenetische experimenten in hartweefsel en hele harten.
Introduction
ChR-gemedieerde fotostromen werden voor het eerst opgenomen in de oogvlek van eencellige groene algen1,2. Kort na genetische klonen en heterologe expressie van Chlamydomonas reinhardtii ChR1 en ChR2, chr werden gebruikt als instrumenten om het membraan potentieel in Xenopus eicellen en zoogdiercellen te veranderen door licht3,4. Kation niet-selectieve ChR depolariseren het membraan van cellen met een rustmembraan potentieel dat negatief is voor de omkering potentieel van ChR. Ze kunnen dus worden gebruikt om AP uit te lokken in prikkelbare cellen, waaronder neuronen en CM, waardoor optische pacing5,6.
Aanvullend op kation ChR, licht aangedreven proton, chloride en natriumpompen7,8,9 zijn gebruikt om neuronale activiteit te remmen10,11,12. Deze laatste hebben echter beperkingen, die hoge lichtintensiteiten en aanhoudende verlichting vereisen, omdat één ion per geabsorbeerd foton wordt vervoerd. In 2014 beschreven twee onafhankelijke studies van Wietek et al. en Berndt et al. de omzetting van kation-geleidende ChR in ACR via mutaties in het kanaal porie13,14. Een jaar later werd natuurlijke ACR ontdekt in de cryptophyte Guillardia theta (GtACR)15. Zoals ontworpen ACR toonde resterende kation geleiding, werden ze vervangen door natuurlijke ACR, gekenmerkt door een grote single-channel geleiding en hoge lichtgevoeligheid15. GtACR werden gebruikt om neuronale activiteit het zwijgen op te leggen door het membraanpotentieel te polariseren naar het omkeringspotentieel van chloride16,17. Govorunova et al. toegepast GtACR1 op gekweekte rat ventriculaire CM en toonde efficiënte fotoremming bij lage lichtintensiteit niveaus die niet voldoende waren om eerder beschikbare remming tools te activeren, zoals de protonpomp Arch18. Onze groep meldde onlangs dat GtACR1-gemedieerde fotoinhibitie van CM is gebaseerd op depolarisatie en dat GtACR1 kan ook worden gebruikt, dus voor optische pacing van CM19.
Hier presenteren we een protocol voor het bestuderen van de elektrofysiologische en mechanische effecten van GtACR1 fotoactivatie op gekweekte konijn ventriculaire CM. We beschrijven eerst celisolatie, kweek en transductie. Elektrofysiologische effecten worden gemeten met behulp van hele cel patch-klem opnames. Lichtgemedieerde stromen bij een bepaalde membraanspanning worden beoordeeld in V-klemmodus. Membraan potentiële dynamiek worden gemeten tijdens het elektrisch of optisch pacing CM (I-klem modus). Optische remming van elektrisch geactiveerde AP wordt getest met behulp van aanhoudende lichttoepassing. Mechanische effecten worden gemeten met behulp van koolstofvezels in combinatie met beeldvorming-gebaseerde tracking van sarcomere lengte. Om dit te doen, worden optisch paceable cellen mechanisch voorgeladen door twee koolstofvezels aan het plasmamembraan dichtbij tegenovergestelde celeinden te bevestigen. Sarcomere lengte veranderingen worden geregistreerd tijdens optische of elektrische pacing. Ten slotte wordt fotoinhibitie gemeten tijdens elektrische veldstimulatie van de cellen en worden gegenereerde krachten geanalyseerd.
Het protocol bevat de volgende stappen in het stroomdiagram in figuur 1:konijnendiepe anesthesie, thiopentale overdosisinjectie, hartexcisie, Langendorff-perfusie en weefselvertering, mechanische dissociatie van het weefsel om cellen vrij te geven, microscopische analyse van CM-opbrengst, kweek van CM, transductie met adenovirus type 5, gevolgd door incubatie en functionele experimenten.
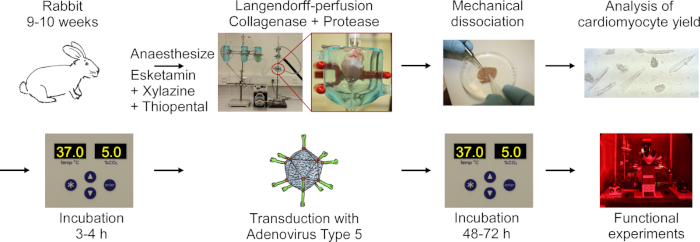
Figuur 1: Stroomschema van het protocol dat wordt gebruikt om elektrisch en optisch paceable CM te verkrijgen. Harten worden verwijderd van konijnen 9-10 weken oud, en hartweefsel wordt verteerd terwijl ze geperfundeerd met behulp van een Langendorff setup. Cellen worden vrijgegeven door mechanische agitatie. De CM-opbrengst wordt onder een microscoop geteld. CM worden gekweekt, getranstmet adenovirus type 5 en functionele experimenten worden uitgevoerd 48-72 uur na transductie. Klik hier om een grotere versie van dit cijfer te bekijken.
Protocol
Representative Results
Discussion
Terwijl optogenetische hulpmiddelen modulatie van prikkelbare celelektrofysiologie op een niet-invasieve manier mogelijk maken, hebben ze een grondige karakterisering in verschillende celtypen (bijvoorbeeld CM) nodig om het beste beschikbare instrument te kunnen kiezen voor een specifiek experimenteel ontwerp. De patch-clamp techniek is een standaard methode voor de beoordeling van cellulaire elektrofysiologie. In de hele cel configuratie, het maakt het mogelijk om foto-geactiveerde stromen op te nemen over het plasmamembraan of tijdelijke veranderingen in membraanspanning na lichtstimulatie / remming. Optogenetische manipulatie van elektrische excitatie beïnvloedt ook CM-contracties. We gebruiken sarcomere tracking en koolstofvezel-ondersteunde kracht metingen om de effecten van optische ondervraging op de mechanische activiteit van myocyten te kwantificeren.
We beschrijven een protocol om de basiseffecten van een lichtgatchloridekanaal, GtACR1, in CM te karakteriseren. Als modelsysteem kozen we voor konijn CM, omdat hun elektrofysiologische kenmerken (bijvoorbeeld AP-vorm en vuurvaste periode) beter lijken op die waargenomen in menselijke CM dan knaagdier CM. Bovendien kan konijn CM meerdere dagen gekweekt worden, lang genoeg voor adenovirale levering en expressie van GtACR1-eGFP. Met name geïsoleerde CM veranderen hun structurele eigenschappen in de cultuur in de tijd, met inbegrip van afronding van cel eindes en geleidelijk verlies van kruis-striatie, T-buisvormige systeem en caveolae23,24. In overeenstemming hiermee zijn functionele veranderingen gemeld in gekweektcm: depolarisatie van het rustmembraanpotentieel, verlenging van de AP en veranderingen in cellulaire Ca2+ handling. Voor herziening van cellulaire aanpassingen in cultuur, zie Louch et al.25. Aanvullende figuur 2 toont voorbeeldige AP en contractie metingen van vers geïsoleerde CM voor vergelijking met die waargenomen in gekweekte CM (Figuur 6, Figuur 7) met behulp van de hier gepresenteerde protocol.
Opnamen van hele celpatchklemmen maken directe metingen van fotostromende eigenschappen (bijvoorbeeld amplitudes en kinetiek) en lichtgeïnduceerde veranderingen in membraanpotentieel of AP-kenmerken bij hoge temporele resolutie mogelijk. Dergelijke opnames hebben echter verschillende beperkingen: Ten eerste wordt de cytosol vervangen door de pipetoplossing in whole-cell opnames, wat voordelig is voor de controle van ionische elektrochemische gradiënten, maar het intrinsieke nadeel heeft van het uitwassen van cellulaire organellen, eiwitten en andere verbindingen, waardoor cellulaire elektrische reacties mogelijk worden beïnvloed. Ten tweede zijn bijwerkingen zoals activering van extra ionenkanalen als gevolg van niet-fysiologisch lange depolarisatie (bijvoorbeeld langzame tijdconstanten van lichtgatige ionenkanalen) moeilijk in te schatten omdat onze methode slechts een methode toestaat om veranderingen in APD te detecteren, maar geen directe metingen van ionische concentraties in elektrofysiologisch relevante celcompartimenten uit te voeren. Dit kan worden gedaan met fluorescerende indicatoren (bijvoorbeeld Ca2+ sensoren) of ionenselectieve elektroden. Verdere karakterisering kan bestaan uit lichtintensiteit titraties, bepaling van pH-afhankelijkheid, fotostroom kinetiek op verschillende membraan potentials, en herstel kinetiek tijdens repetitieve lichtstimulatie.
In tegenstelling tot patch-klem opnames, single-cell kracht metingen mogelijk analyse van cellulaire samentrekkingen van intacte myocyten zonder dat hun intracellulaire milieu. Secundaire effecten op ionconcentraties (bijvoorbeeld Ca2+) kunnen indirect worden beoordeeld door het bepalen van gegenereerde krachtamplitude en -dynamiek (bijvoorbeeld maximale snelheid van contractie en ontspanning; hier niet geanalyseerd). Krachtmetingen met de koolstofvezeltechniek hebben een voordeel ten opzichte van vrij aanbestedende cellen, omdat ze directe informatie geven over passieve en actieve krachten in vooraf geladen cellen (d.w.z. in omstandigheden die meer lijken op de in situ of in vivo instellingen). Mechanische preloading is vooral belangrijk bij het analyseren van cellulaire contractiliteit, omdat stretch van invloed is op krachtproductie en ontspanning26,27.
Optogenetische benaderingen zorgen voor spatiotemporally nauwkeurige manipulatie van het cellulaire membraan potentieel, zowel in enkele CM en intact hartweefsel. Klassiek, ChR2, een licht-gated kation niet-selectief kanaal, is gebruikt voor depolarisatie van het membraan potentieel, terwijl licht-aangedreven proton en / of chloride pompen werden gebruikt voor membraan hyperpolarisatie. Beide groepen van optogenetische actuatoren vereisen hoge expressieniveaus, omdat ChR2 wordt gekenmerkt door een intrinsiek lage single-channel geleiding28 en lichtaangedreven pompen maximaal één ion per geabsorbeerd foton vervoeren. Bovendien kan langdurige activering van ChR2 in CM leiden tot Na+ en/of Ca2+ overbelasting, en lichtaangedreven pompen kunnen trans-sarcolemmale H+ of Cl veranderen– hellingen29,30. Op zoek naar alternatieve instrumenten voor optogenetische controle van CM-activiteit, hebben we onlangs de natuurlijke anion kanaalrhodopsin GtACR1 getest, gekenmerkt door een superieure single-channel geleiding en een hogere lichtgevoeligheid in vergelijking met kation ChR zoals ChR2. We vonden dat GtACR1 activering cm depolariseert en kan worden gebruikt voor optische pacing en remming, afhankelijk van de lichtpulstiming en duur. Een bijkomend voordeel van het gebruik van ACR in plaats van kation ChR zou de meer negatieve omkering potentieel van Cl– in vergelijking met Na+, het verminderen van kunstmatig geïntroduceerde ionenstromen. Zoals we eerder hebben aangetoond, kan optische pacing met GtACR1 leiden tot AP verlenging als gevolg van de langzame component van GtACR1 kanaal sluiting, die kan worden overwonnen door het gebruik van snellere GtACR1 mutanten19. De verlenging van de AP is echter veel minder uitgesproken bij het gebruik van een lagere, meer fysiologische intracellulaire Cl– concentratie (zie figuur 6). Bovendien resulteert gtacr1-gemedieerde remming door langdurige verlichting in een diepgaande membraandepolarisatie, die opnieuw secundaire Na+ en Ca2+ instroom kan activeren, waardoor de activiteit van voltage-gated kanalen verandert. In onze metingen zien we dat AP- en contractieparameters zich herstellen tot de basislijn binnen 40 s na een lichtgeïnduceerde remming gedurende 1 min (zie Kopton et al. 2018, figuur 6, figuur 7). Lichtgatige K+ kanalen bieden een krachtig alternatief voor het uitschakelen van CM zonder dat dit het CM rustmembraanpotentieel31aantast.
In de toekomst willen we verschillende optogenetische hulpmiddelen kwantitatief vergelijken voor hun potentieel om hartactiviteit te remmen. Hiertoe testen we een verscheidenheid aan lichtgatige ionenkanalen, waaronder ACR, ChR2 en roodverschoven ChR-varianten32, evenals hyperpolariserende actuatoren zoals halorhodopsine of het licht gated adenylyl cyclase bPAC in combinatie met het kaliumkanaal SthK (PAC-K)31.
Het hier gepresenteerde protocol kan worden gebruikt voor diepgaande karakterisering van de elektromechanische eigenschappen van CM. Het is hoofdzakelijk ook toepasselijk op CM van andere soorten, en aan CM die van ziek myocardium worden geïsoleerd. Optische stimulatie maakt het mogelijk om CM tempo op verschillende frequenties, en verschillende preloads kunnen worden getest tijdens koolstofvezel contractieexperimenten. Een interessant experiment zou zijn om verlichting met lage intensiteit te gebruiken voor subdrempeldepolarisatie, om geleidelijke toename van het rustmembraanpotentieel na te bootsen, zoals kan worden waargenomen tijdens de ontwikkeling van het remodelleren van hartweefsel tijdens de progressie van de ziekte. Ten slotte kunnen functionele metingen worden gecombineerd met Ca2+ beeldvorming voor verder inzicht in excitatie-contractiekoppeling, of met farmacologische interventies om de effecten van verschillende geneesmiddelen op cm-activiteit te evalueren.
Declarações
The authors have nothing to disclose.
Acknowledgements
Wij danken Stefanie Perez-Feliz voor uitstekende technische assistentie, Dr. Jonas Wietek (Humboldt-University, Berlijn, Duitsland) voor het verstrekken van de pUC57-GtACR1 plasmid, Prof. Dr. Michael Schupp (Charité- Universitätsmedizin Berlin, Institut für Pharmakologie, Berlijn) voor de adenovirusproductie en Dr. Anastasia Khokhlova (Ural Federal University) voor het delen van haar expertise om het celisolatieprotocol te verbeteren en de pipetbuiginstallatie opnieuw te ontwerpen. Het project werd gefinancierd door de Duitse Research Foundation (SPP1926: SCHN 1486/1-1; Emmy-Noether fellowship: SCHN1486/2-1) en de ERC Advanced Grant CardioNECT.
Materials
| Equipment – Cell isolation/Culturing/Transduction | |||
| Adeno-X Adenoviral System 3 CMV | TaKaRa, Clontech Laboratories, Inc., Mountain View, California, USA | ||
| Aortic cannula | Radnoti | 4.8 OD x 3.6 ID x 8-9 L mm | |
| Coverslips ø 16 mm, Thickness No. 0 | VWR International GmbH, Leuven, Belgium | 631-0151 | Borosilicate Glass |
| Griffin Silk, Black, 2 m Length, Size 3, 0.5 mm | Samuel Findings, London, UK | TSGBL3 | |
| Incubator | New Brunswick, Eppendorf, Schönenbuch, Switzerland | Galaxy 170S | |
| Langendorff-perfusion set-up | Zitt-Thoma Laborbedarf Glasbläserei, Freiburg, Germany | Custom-made | |
| Langendorff-pump | Ismatec, Labortechnik-Analytik, Glattbrugg-Zürich, Switzerland | ISM444 | |
| Mesh: Nylon Monodur filter cloth | Cadisch Precision Meshes Ltd | 800 µm holes, 1 m wide | |
| Neubauer chamber | VWR International GmbH, Leuven, Belgium | 717806 | |
| Rabbit, New Zealand White | Charles River | Strain Code: 052 | |
| Scissors | Aesculap AG, Tuttlingen, Germany | BC774R | Bauchdeckenschere ger. 18cm |
| Sterile filter, 0.22 µm | Merck, Darmstadt, Germany | SLGP033RB | |
| Equipment – Patch-clamp | |||
| Amplfier | AxonInstruments, Union City, CA, United States | Axopatch 200B | |
| Coverslip ø 50 mm, Thickness No. 1 | VWR International GmbH, Leuven, Belgium | 631-0178 | Borosilicate Glass |
| Digitizer Axon Digidata | Molecular Devices, San José, CA, United States | 1550A | |
| Filter (530/20) | Leica Microsystems, Wetzlar, Germany | 11513878 | BZ:00 |
| Filter (630/20) | Chroma Technology, Bellows Falls, Vermont, United States | 227155 | |
| Headstage | AxonInstruments, Union City, CA, United States | CV203BU | |
| Interface | Scientifica, Uckfield, UK | 1U Rack, 352036 | |
| LED 525 nm | Luminus Devices, Sunnyvale, CA, United States | PT-120-G | |
| LED control software | Essel Research and Development, Toronto, Canada | ||
| LED control system | custom-made | ||
| Micropipette Puller | Narishige Co., Tokyo, Japan | PP-830 | |
| Microscope inverted | Leica Microsystems, Wetzlar, Germany | DMI4000B | |
| Motorised Micromanipulator | Scientifica, Uckfield, UK | PatchStar | |
| Optical power meter | Thorlabs, Newton, NJ, United States | PM100D | |
| Silicone Grease | RS Components, Corby, UK | 494-124 | |
| Silver wire | A-M Systems, Sequim, WA, United States | 787500 | Silver, Bare 0.015'', Coated 0.0190'', Length 25 Feet |
| Soda lime glass capillaries | Vitrex Medical A/S, Vasekaer, Denmark | 160213 BRIS, ISO12772 | 1.55 OD x 1.15 ID x 75 L mm |
| Software Axon pClamp | Molecular Devices, San José, CA, United States | Version 10.5 | |
| Software MatLab2017 | The MathWorks, Inc. | ||
| Stage micrometer | Graticules Optics LTD, Tonbridge, UK | 1 mm | |
| Equipment – Carbon fiber | |||
| Carbon fibers | provided from Prof. Jean-Yves Le Guennec | BZ:00 | |
| Digitizer Axon Digidata | Molecular Devices, Sunnyvale, CA, United States | 1550B | |
| Filter (530/20) | Leica Microsystems, Wetzlar, Germany | 11513878 | |
| Filter (630/20) | Chroma Technology, Bellows Falls, Vermont, United States | 227155 | |
| Fluorescence System Interface | IonOptix, Milton, MA United States | FSI-800 | 2.0 OD x 1.16 ID x 100 L mm |
| Force Transducer System | Aurora Scientific Inc., Ontario, Canada | 406A | |
| Glass capillaries for force measurements | Harvard Apparatus, Holliston, Massachusetts, United States | GC200F-10 | |
| Interface National Instruments | National Instruments, Budapest, Hungary | BNC-2110 | |
| LED 525 nm | Luminus Devices, Sunnyvale, CA, United States | PT-120-G | |
| LED control box | Essel Research and Development, Toronto, Canada | ||
| LED control system | custom-made | ||
| Microcontroller | Parallax Inc., Rocklin, California, United States | Propeller | |
| Micropipette Puller | Narishige Co., Tokyo, Japan | PC-10 | |
| Microscope inverted | Leica Microsystems, Wetzlar, Germany | DMI4000B | |
| MyoCam-S camera | IonOptix, Dublin, Ireland | ||
| MyoCam-S camera Power | IonOptix, Milton, MA, United States | MCS-100 | |
| MyoPacer Field Stimulator | IonOptix Cooperation, Milton, MA, United States | MYP100 | |
| Piezo Motor | Physik Instrumente (PI) GmbH & Co. KG, Karlsruhe, Germany | E-501.00 | |
| Silicone Grease | RS Components, Corby, UK | 494-124 | |
| Software Axon pClamp | Molecular Devices, San José, CA, United States | Version 10.5 | |
| Software IonWizard | IonOptix, Dublin, Ireland | Version 6.6.10.125 | |
| Software MatLab2017 | The MathWorks, Inc. | ||
| Stage micrometer | Graticules Optics LTD, Tonbridge, UK | 1 mm | |
| Chemicals | |||
| Adenosine | Sigma-Aldrich, St. Louis, Missouri, United States | A9251-100G | |
| Bovine serum albumin | Sigma-Aldrich, St. Louis, Missouri, United States | A7030-50G | |
| CaCl2 | Honeywell Fluka, Muskegon, MI, USA | 21114-1L | |
| L-Carnitine hydrochloride | Sigma-Aldrich, St. Louis, Missouri, United States | C9500-25G | |
| Collagenase type 2, 315 U/mg | Worthington, Lakewood, NJ, USA | LS004177 | |
| Creatine | Sigma-Aldrich, St. Louis, Missouri, United States | C0780-50G | |
| Cytosine-β-D-arabinofuranoside | Sigma-Aldrich, St. Louis, Missouri, United States | C1768-100MG | |
| EGTA | Carl Roth GmbH + Co. KG, Karlsruhe, Germany | 3054.3 | |
| Esketamine hydrochloride, Ketanest S 25 mg/mL | Pfizer Pharma PFE GmbH, Berlin, Germany | PZN-07829486 | |
| Fetal Bovine Serum | Sigma-Aldrich, St. Louis, Missouri, United States | F9665 | |
| Gentamycin 50 mg/mL | Gibco, Life Technologies, Waltham, MA, USA | 15750-037 | |
| Glucose | Sigma-Aldrich, St. Louis, Missouri, United States | G7021-1KG | |
| Heparin-Sodium, 5,000 IU/mL | Braun Melsungen AG, Melsungen, Germany | PZN-03029843 | |
| HEPES | Sigma-Aldrich, St. Louis, Missouri, United States | H3375-1KG | |
| Insulin (bovine pancreas) | Sigma-Aldrich, St. Louis, Missouri, United States | I6634-50MG | |
| K-aspartate | Sigma-Aldrich, St. Louis, Missouri, United States | A6558-25G | |
| KCl | VWR International GmbH, Leuven, Belgium | 26764.260 | 1 mg/mL |
| KOH | Honeywell Fluka, Muskegon, MI, USA | 35113-1L | |
| Laminin from Engelbreth-Holm-Swarm murine sarcoma basement membrane | Sigma-Aldrich, St. Louis, Missouri, United States | L2020-1MG | |
| M199-Medium | Sigma-Aldirch, St. Louis, Missouri, United States | M4530 | |
| Mg-ATP | Sigma-Aldrich, St. Louis, Missouri, United States | A9187-1G | |
| MgCl2 | Sigma-Aldrich, St. Louis, Missouri, United States | 63069-500ML | |
| NaCl | Fisher Scientific, Loughborough, Leics., UK | 10428420 | |
| NaCl-Solution 0.9%, Isotone Kochsalz-Lösung 0.9% | Braun Melsungen AG, Melsungen, Germany | 3200950 | |
| NaOH | AppliChem GmbH, Darmstadt, Germany | A6579 | without Ca2+/Mg2+ |
| Na-pyruvat | Sigma-Aldrich, St. Louis, Missouri, United States | P2256-100MG | |
| Phosphate Buffered Saline | Sigma-Aldrich, St. Louis, Missouri, United States | D1408-500ML | |
| Poly(2-hydroxyethyl methacrylate) | Sigma, Poole, UK | 192066 | |
| Protease XIV from Streptomyces griseus | Sigma-Aldrich, St. Louis, Missouri, United States | P5147-1G | |
| Taurine | Sigma-Aldrich, St. Louis, Missouri, United States | T0625-500G | |
| Thiopental Inresa 0.5 g | Inresa Arzneimittel GmbH, Freiburg, Germany | PZN-11852249 | |
| Xylazine hydrochloride, Rompun 2% | Bayer Vital GmbH, Leverkusen, Germany | PZN-01320422 |
Referências
- Harz, H., Hegemann, P. Rhodopsin-regulated calcium currents in Chlamydomonas. Nature. 351, 489-491 (1991).
- Litvin, F. F., Sineshchekov, O. A., Sineshchekov, V. A. Photoreceptor electric potential in the phototaxis of the alga Haematococcus pluvialis. Nature. 271, 476-478 (1978).
- Nagel, G., et al. Channelrhodopsin-1: A Light-Gated Proton Channel in Green Algae. Science. 296 (5577), 2395-2398 (2002).
- Nagel, G., et al. Channelrhodopsin-2, a directly light-gated cation-selective membrane channel. Proceedings of the National Academy of Sciences of the United States of America. 100 (24), 13940-13945 (2003).
- Boyden, E. S., Zhang, F., Bamberg, E., Nagel, G., Deisseroth, K. Millisecond-timescale, genetically targeted optical control of neural activity. Nature Neuroscience. 8 (9), 1263-1268 (2005).
- Bruegmann, T., et al. Optogenetic control of heart muscle in vitro and in vivo. Nature Methods. 7 (11), 897-900 (2010).
- Lozier, R. H., Bogomolni, R. A., Stoeckenius, W. Bacteriorhodopsin: a light-driven proton pump in Halobacterium Halobium. Biophysical journal. 15 (9), 955-962 (1975).
- Schobert, B., Lanyi, J. K. Halorhodopsin is a light-driven chloride pump. Journal of Biological Chemistry. 257 (17), 10306-10313 (1982).
- Inoue, K., et al. A light-driven sodium ion pump in marine bacteria. Nature Communications. 4, 1678 (2013).
- Han, X., et al. A High-Light Sensitivity Optical Neural Silencer: Development and Application to Optogenetic Control of Non-Human Primate Cortex. Frontiers in Systems Neuroscience. 5, 18 (2011).
- Zhang, F., et al. Multimodal fast optical interrogation of neural circuitry. Nature. 446 (7136), 633-639 (2007).
- Grimm, C., Silapetere, A., Vogt, A., Bernal Sierra, Y. A., Hegemann, P. Electrical properties, substrate specificity and optogenetic potential of the engineered light-driven sodium pump eKR2. Scientific Reports. 8, 9316 (2018).
- Wietek, J., et al. Conversion of channelrhodopsin into a light-gated chloride channel. Science. 344 (6182), 409-412 (2014).
- Berndt, A. Structure-Guided Transformation. Science. 344 (6182), 420-424 (2014).
- Govorunova, E. G., Sineshchekov, O. A., Janz, R., Liu, X., Spudich, J. L. Natural light-gated anion channels: A family of microbial rhodopsins for advanced optogenetics. Science. 349 (6248), 647-650 (2015).
- Mohamed, G. A., et al. Optical inhibition of larval zebrafish behaviour with anion channelrhodopsins. BMC Biology. 15 (1), 103 (2017).
- Mauss, A. S., Busch, C., Borst, A. Optogenetic Neuronal Silencing in Drosophila during Visual Processing. Scientific Reports. 7, 13823 (2017).
- Govorunova, E. G., Cunha, S. R., Sineshchekov, O. A., Spudich, J. L. Anion channelrhodopsins for inhibitory cardiac optogenetics. Scientific Reports. 6, 33530 (2016).
- Kopton, R. A., et al. Cardiac Electrophysiological Effects of Light-Activated Chloride Channels. Frontiers in Physiology. 9, 1806 (2018).
- Peyronnet, R., et al. Load-dependent effects of apelin on murine cardiomyocytes. Progress in Biophysics and Molecular Biology. 130, 333-343 (2017).
- Wang, K., et al. Cardiac tissue slices: preparation, handling, and successful optical mapping. American Journal of Physiology-Heart and Circulatory Physiology. 308 (9), 1112-1125 (2015).
- Nishimura, S., et al. Single cell mechanics of rat cardiomyocytes under isometric, unloaded, and physiologically loaded conditions. American Journal of Physiology-Heart and Circulatory Physiology. 287 (1), 196-202 (2004).
- Mitcheson, J. S., Hancox, J. C., Levi, A. J. Action potentials, ion channel currents and transverse tubule density in adult rabbit ventricular myocytes maintained for 6 days in cell culture. Pflugers Archiv European Journal of Physiology. 43 (6), 814-827 (1996).
- Burton, R. A. B., et al. Caveolae in Rabbit Ventricular Myocytes: Distribution and Dynamic Diminution after Cell Isolation. Biophysical Journal. 113 (5), 1047-1059 (2017).
- Louch, W. E., Sheehan, K. A., Wolska, B. M. Methods in cardiomyocyte isolation, culture, and gene transfer. Journal of Molecular and Cellular Cardiology. 51 (3), 288-298 (2011).
- Janssen, P. M., Hunter, W. C. Force, not sarcomere length, correlates with prolongation of isosarcometric contraction. The American Journal of Physiology. 269 (2), 676-685 (1995).
- Monasky, M. M., Varian, K. D., Davis, J. P., Janssen, P. M. L. Dissociation of force decline from calcium decline by preload in isolated rabbit myocardium. Pflugers Archiv European Journal of Physiology. 456 (2), 267-276 (2008).
- Kleinlogel, S., et al. Ultra light-sensitive and fast neuronal activation with the Ca 2+-permeable channelrhodopsin CatCh. Nature Neuroscience. 14 (4), 513-518 (2011).
- Schneider-Warme, F., Ravens, U. Using light to fight atrial fibrillation. Cardiovascular Research. 114 (5), 635-637 (2018).
- Chow, B. Y., et al. High-performance genetically targetable optical neural silencing by light-driven proton pumps. Nature. 463 (7277), 98-102 (2010).
- Bernal Sierra, Y. A., et al. Potassium channel-based optogenetic silencing. Nature Communications. 9 (1), 4611 (2018).
- Oda, K., et al. Crystal structure of the red light-activated channelrhodopsin Chrimson. Nature Communications. 9 (1), 3949 (2018).

