Evaluación electromecánica de la actividad de cardiomiocitos moduladas optogenéticamente
Summary
Presentamos un protocolo para evaluar los efectos electromecánicos de la activación de GtACR1 en cardiomiocitos de conejo. Proporcionamos información detallada sobre el aislamiento celular, el cultivo y la transducción adenoviral, y sobre experimentos funcionales con las técnicas de abrazadera de parche y fibra de carbono.
Abstract
En las últimas dos décadas, las herramientas optogenéticas se han establecido como medios potentes para modular la actividad específica del tipo celular en los tejidos excitables, incluido el corazón. Mientras que Channelrhodopsin-2 (ChR2) es una herramienta común para despolarizar el potencial de membrana en cardiomiocitos (CM), potencialmente provocando potenciales de acción (AP), una herramienta eficaz para el silenciamiento confiable de la actividad de CM ha faltado. Se ha sugerido utilizar aniones canalrhodopsins (ACR) para la inhibición optogenética. Aquí, describimos un protocolo para evaluar los efectos de la activación del ACR GtACR1 natural de Guillardia theta en conejo cultivado CM. Las lecturas primarias son grabaciones electrofisiológicas de abrazaderas de parche y seguimiento óptico de las contracciones de CM, ambas realizadas mientras se aplican diferentes patrones de estimulación de la luz. El protocolo incluye aislamiento CM del corazón del conejo, sembración y cultivo de las células durante un máximo de 4 días, transducción a través de la codificación de adenovirus para el canal de cloruro cerrado a la luz, preparación de configuraciones de abrazaderas de parche y fibra de carbono, recopilación y análisis de datos. El uso de la técnica de abrazadera de parche en la configuración de células enteras permite grabar corrientes activadas por la luz (en modo de abrazadera de voltaje, abrazadera en V) y AP (modo de abrazadera de corriente, I-clamp) en tiempo real. Además de los experimentos con abrazaderas de parches, realizamos mediciones de contractilidad para la evaluación funcional de la actividad de CM sin alterar el entorno intracelular. Para ello, las células se precargan mecánicamente utilizando fibras de carbono y las contracciones se registran mediante el seguimiento de los cambios en la longitud del sarcomere y la distancia de la fibra de carbono. El análisis de datos incluye la evaluación de la duración de AP a partir de grabaciones de abrazaderas I, corrientes máximas de grabaciones de abrazadera en V y cálculo de fuerza a partir de mediciones de fibra de carbono. El protocolo descrito se puede aplicar a las pruebas de efectos biofísicos de diferentes actuadores optogenéticos en la actividad de CM, un requisito previo para el desarrollo de una comprensión mecanicista de experimentos optogenéticos en tejido sorcardíaco y corazones enteros.
Introduction
Las fotocorrientes mediadas por ChR se registraron por primera vez en la mancha ocular de las algas verdes unicelulares1,2. Poco después de la clonación genética y la expresión heteróloga de Chlamydomonas reinhardtii ChR1 y ChR2, se utilizaron ChR como herramientas para alterar el potencial de membrana en los ovocitos de Xenopus y las células de mamíferos por la luz3,4. Cación chR no selectivo despolarizar la membrana de las células con un potencial de membrana en reposo que es negativo al potencial de inversión de ChR. Por lo tanto, se pueden utilizar para obtener AP en células excitables, incluyendo neuronas y CM, permitiendo el ritmo óptico5,6.
Complementarios a la cación ChR, protones accionados por la luz, bombas de cloruro y sodio7,8,9 se han utilizado para inhibir la actividad neuronal10,11,12. Sin embargo, estos últimos tienen limitaciones, que requieren altas intensidades de luz e iluminación sostenida, ya que un ion se transporta por fotón absorbido. En 2014, dos estudios independientes de Wietek et al. y Berndt et al. describieron la conversión de ChR conductor catiónico en ACR a través de mutaciones en el poro del canal13,14. Un año más tarde, el ACR natural fue descubierto en el criptofito Guillardia theta (GtACR)15. Como el ACR de ingeniería mostró conductividad catiónica residual, fueron reemplazados por ACR natural, caracterizado por una gran conductancia de un solo canal y alta sensibilidad a la luz15. GtACR se utilizaron para silenciar la actividad neuronal polarizando el potencial de membrana hacia el potencial de reversión del cloruro16,17. Govorunova et al. aplicaron GtACR1 a la rata cultivada ventricular CM y mostraron fotoinhibición eficiente a niveles de intensidad de luz bajos que no eran suficientes para activar las herramientas de inhibición previamente disponibles, como la bomba de protones Arch18. Nuestro grupo informó recientemente que la fotoinhibición mediada por GtACR1 de CM se basa en la despolarización y que GtACR1 también se puede utilizar, por lo tanto, para el ritmo óptico de CM19.
Aquí, presentamos un protocolo para estudiar los efectos electrofisiológicos y mecánicos de la fotoactivación GtACR1 en el cm ventricular del conejo cultivado. Primero describimos el aislamiento celular, el cultivo y la transducción. Los efectos electrofisiológicos se miden utilizando grabaciones de abrazaderas de parche de células enteras. Las corrientes mediadas por luz a una tensión de membrana determinada se evalúan en modo de abrazadera en V. La dinámica del potencial de membrana se mide mientras se pisa eléctrica u ópticamente CM (modo I-clamp). La inhibición óptica de AP activado eléctricamente se prueba utilizando una aplicación de luz sostenida. Los efectos mecánicos se miden utilizando fibras de carbono en combinación con el seguimiento basado en imágenes de la longitud del sarcomere. Para ello, las células ópticamente pacebles se precargan mecánicamente mediante la fijación de dos fibras de carbono a la membrana plasmática cerca de los extremos de las células opuestas. Los cambios en la longitud de Sarcomere se registran durante el ritmo óptico o eléctrico. Finalmente, la fotoinhibición se mide durante la estimulación eléctrica del campo de las células, y se analizan las fuerzas generadas.
El protocolo incluye los siguientes pasos que se muestran en el diagrama de flujo en la Figura 1:anestesia profunda de conejo, inyección de sobredosis tiopental, escisión cardíaca, digestión de langendorff y tejido, disociación mecánica del tejido para liberar células, análisis microscópico del rendimiento de CM, cultivo de CM, transducción con adenovirus tipo 5, seguido de incubación y experimentos funcionales.
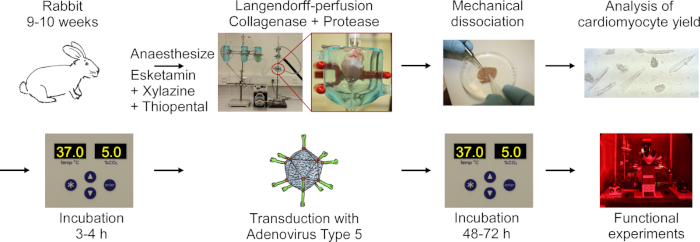
Figura 1: Diagrama de flujo del protocolo utilizado para obtener CM eléctrica y ópticamente paceble. Los corazones se extirpan de conejos de 9-10 semanas de edad, y el tejido cardíaco se digiere mientras se perfunde usando una configuración de Langendorff. Las células se liberan por agitación mecánica. El rendimiento CM se cuenta bajo un microscopio. CM son cultivados, transducidos con adenovirus tipo 5 y los experimentos funcionales se realizan 48-72 horas después de la transducción. Haga clic aquí para ver una versión más grande de esta figura.
Protocol
Representative Results
Discussion
Mientras que las herramientas optogenéticas permiten la modulación de la electrofisiología celular excitable de una manera no invasiva, necesitan una caracterización exhaustiva en diferentes tipos de células (por ejemplo, CM) para permitir que uno elija la mejor herramienta disponible para un diseño experimental específico. La técnica de abrazadera de parche es un método estándar para evaluar la electrofisiología celular. En la configuración de células enteras, permite grabar corrientes fotoactivadas a través de la membrana plasmática o cambios temporales en el voltaje de la membrana después de la estimulación/inhibición de la luz. La manipulación optogenética de la excitación eléctrica también afecta a las contracciones de CM. Utilizamos el seguimiento de sarcomere y las mediciones de fuerza asistida por fibra de carbono para cuantificar los efectos del interrogatorio óptico en la actividad mecánica de los miocitos.
Describimos un protocolo para caracterizar los efectos básicos de un canal de cloruro ligero, GtACR1, en CM. Como sistema modelo, elegimos el conejo CM, ya que sus características electrofisiológicas (por ejemplo, forma AP y período refractario) se asemejan más a las observadas en CM humano más cercano que a los roedores CM. Además, el conejo CM se puede cultivar durante varios días, el tiempo suficiente para la administración adenoviral y la expresión de GtACR1-eGFP. En particular, el CM aislado cambia sus propiedades estructurales en el cultivo a lo largo del tiempo, incluyendo el redondeo de terminaciones celulares y la pérdida gradual de estrías cruzadas, sistema T-tubular y caveolas23,24. En línea con esto, se han reportado alteraciones funcionales en CM cultivado: despolarización del potencial de membrana en reposo, prolongación de la AP y cambios en el manejo celular De2+. Para una revisión de las adaptaciones celulares en la cultura, consulte Louch et al.25. La Figura Suplementaria 2 muestra las mediciones ejemplares DE AP y de contracción de CM recién aislado para la comparación con las observadas en CM cultivado(Figura 6, Figura 7)utilizando el protocolo aquí presentado.
Las grabaciones de abrazaderas de parche de células enteras permiten mediciones directas de las propiedades fotocorrientes (por ejemplo, amplitudes y cinética) y cambios inducidos por la luz en el potencial de membrana o las características de AP a alta resolución temporal. Sin embargo, tales grabaciones tienen varias limitaciones: En primer lugar, el citosol es reemplazado por la solución de pipeta en grabaciones de células enteras, lo que es ventajoso para controlar gradientes electroquímicos iónicos, pero tiene la desventaja intrínseca de lavar orgánulos celulares, proteínas y otros compuestos, lo que potencialmente afecta a las respuestas eléctricas celulares. En segundo lugar, los efectos secundarios como la activación de canales iónicos adicionales resultantes de la despolarización no fisiológicamente larga (por ejemplo, constantes de tiempo lento de los canales iónicos bloqueados por la luz) son difíciles de evaluar, ya que nuestro método sólo permite detectar cambios en el TPA, pero no realizar mediciones directas de las concentraciones iónicas en compartimentos celulares electrofisiológicamente relevantes. Esto podría hacerse con indicadores fluorescentes (por ejemplo, sensores Ca2+) o electrodos selectivos de iones. La caracterización adicional puede incluir valoraciones de intensidad de la luz, determinación de la dependencia del pH, cinética fotocorriente en diferentes potenciales de membrana y cinética de recuperación durante la estimulación de la luz repetitiva.
A diferencia de las grabaciones de abrazaderas de parche, las mediciones de fuerza de una sola célula permiten el análisis de las contracciones celulares de los miocitos intactos sin afectar su entorno intracelular. Los efectos secundarios sobre las concentraciones iónicas (por ejemplo, Ca2+) pueden evaluarse indirectamente determinando la amplitud y la dinámica de fuerza generadas (por ejemplo, la velocidad máxima de contracción y relajación; aquí no analizada). Las mediciones de fuerza con la técnica de fibra de carbono tienen una ventaja sobre las células que se contraen libremente, ya que proporcionan información directa sobre las fuerzas pasivas y activas en las células precargadas (es decir, en condiciones más similares a las configuraciones in situ o in vivo). La precarga mecánica es especialmente importante a la hora de analizar la contractilidad celular, ya que el estiramiento afecta a la producción de fuerza y la relajación26,27.
Los enfoques optogenéticos permiten una manipulación naturalmente precisa del potencial de la membrana celular, tanto en un solo CM como en el tejido cardíaco intacto. Clásicamente, ChR2, un canal no selectivo de cationes ligeros, se ha utilizado para la despolarización del potencial de membrana, mientras que las bombas de protones y/o cloruro impulsadas por la luz se utilizaron para la hiperpolarización de membranas. Ambos grupos de actuadores optogenéticos requieren altos niveles de expresión, ya que ChR2 se caracteriza por una conductividad de un solo canal intrínsecamente baja28 y bombas accionadas por luz transportan al máximo un ion por fotón absorbido. Además, la activación prolongada de ChR2 en CM puede dar lugar a sobrecarga Na+ y/o Ca2+, y las bombas accionadas por luz pueden cambiar trans-sarcolem H+ o Cl– gradientes29,30. En busca de herramientas alternativas para el control optogenético de la actividad de CM, recientemente probamos el anión natural channelrhodopsin GtACR1, caracterizado por una conductancia de un solo canal superior y una mayor sensibilidad a la luz en comparación con el Catión ChR como ChR2. Encontramos que la activación GtACR1 despolariza CM y se puede utilizar para el ritmo óptico y la inhibición, dependiendo de la sincronización del pulso de luz y la duración. Una ventaja adicional de usar ACR en lugar de cation ChR podría ser el potencial de inversión más negativo de Cl– en comparación con Na+, reduciendo las corrientes iónicas introducidas artificialmente. Como hemos demostrado anteriormente, el ritmo óptico con GtACR1 puede conducir a la prolongación de AP como resultado del componente lento del cierre del canal GtACR1, que podría ser superado mediante el uso de mutantes GtACR1 más rápidos19. Sin embargo, la prolongación de AP es mucho menos pronunciada cuando se utiliza unaconcentración de Cl intracelular más baja y fisiológica (ver Figura 6). Por otra parte, la inhibición mediada por GtACR1 por iluminación prolongada da como resultado una profunda despolarización de la membrana, que de nuevo podría activar la afluencia secundaria Na+ y Ca2+, alterando así la actividad de los canales cerrados por voltaje. En nuestras mediciones, encontramos que los parámetros AP y de contracción se recuperan a la línea de base dentro de 40 s después de una inhibición inducida por la luz durante 1 min (véase Kopton et al. 2018, Figura 6, Figura 7). Los canales K+ con cierre ligero ofrecen una potente alternativa para silenciar CM sin afectar al potencial de membrana de reposo DE CM31.
En el futuro nos gustaría comparar cuantitativamente diferentes herramientas optogenéticas por su potencial para inhibir la actividad cardíaca. Con este fin, probamos una variedad de canales de iones con luz, incluyendo ACR, ChR2 y variantes ChR de cambio rojo32,así como actuadores hiperpolarizantes como halorhodopsin o el bPAC adenil cyclase cerrado con luz en combinación con el canal de potasio SthK (PAC-K)31.
El protocolo aquí presentado se puede utilizar para la caracterización en profundidad de las propiedades electromecánicas de CM. Es principalmente aplicable también a CM de otras especies, y a CM aislado de miocardio enfermo. La estimulación óptica permite que uno tome el ritmo CM a diferentes frecuencias, y se pueden probar diferentes precargas durante los experimentos de contracción de fibra de carbono. Un experimento interesante sería utilizar la iluminación de baja intensidad para la despolarización de los subumbrales, para imitar el aumento gradual en el potencial de la membrana en reposo, como se puede observar durante el desarrollo de la remodelación del tejido cardíaco durante la progresión de la enfermedad. Por último, las mediciones funcionales podrían combinarse con imágenes Ca2+ para obtener más información sobre el acoplamiento excitación-contracción, o con intervenciones farmacológicas para evaluar los efectos de diferentes fármacos en la actividad de CM.
Declarações
The authors have nothing to disclose.
Acknowledgements
Agradecemos a Stefanie Perez-Feliz por su excelente asistencia técnica, Dr. Jonas Wietek (Universidad DeHumboldt, Berlín, Alemania) por proporcionar el plásmido pUC57-GtACR1, el Prof. Dr. Michael Schupp (Charité- Universidad de Berlín, Instituto de Farmacia, Berlín) para la producción de adenovirus y la Dra. Anastasia Khokhlova (Universidad Federal de los Urales) por compartir su experiencia para mejorar el protocolo de aislamiento celular y rediseñar la El proyecto fue financiado por la Fundación Alemana de Investigación (SPP1926: SCHN 1486/1-1; Beca Emmy-Noether: SCHN1486/2-1) y el ERC Advanced Grant CardioNECT.
Materials
| Equipment – Cell isolation/Culturing/Transduction | |||
| Adeno-X Adenoviral System 3 CMV | TaKaRa, Clontech Laboratories, Inc., Mountain View, California, USA | ||
| Aortic cannula | Radnoti | 4.8 OD x 3.6 ID x 8-9 L mm | |
| Coverslips ø 16 mm, Thickness No. 0 | VWR International GmbH, Leuven, Belgium | 631-0151 | Borosilicate Glass |
| Griffin Silk, Black, 2 m Length, Size 3, 0.5 mm | Samuel Findings, London, UK | TSGBL3 | |
| Incubator | New Brunswick, Eppendorf, Schönenbuch, Switzerland | Galaxy 170S | |
| Langendorff-perfusion set-up | Zitt-Thoma Laborbedarf Glasbläserei, Freiburg, Germany | Custom-made | |
| Langendorff-pump | Ismatec, Labortechnik-Analytik, Glattbrugg-Zürich, Switzerland | ISM444 | |
| Mesh: Nylon Monodur filter cloth | Cadisch Precision Meshes Ltd | 800 µm holes, 1 m wide | |
| Neubauer chamber | VWR International GmbH, Leuven, Belgium | 717806 | |
| Rabbit, New Zealand White | Charles River | Strain Code: 052 | |
| Scissors | Aesculap AG, Tuttlingen, Germany | BC774R | Bauchdeckenschere ger. 18cm |
| Sterile filter, 0.22 µm | Merck, Darmstadt, Germany | SLGP033RB | |
| Equipment – Patch-clamp | |||
| Amplfier | AxonInstruments, Union City, CA, United States | Axopatch 200B | |
| Coverslip ø 50 mm, Thickness No. 1 | VWR International GmbH, Leuven, Belgium | 631-0178 | Borosilicate Glass |
| Digitizer Axon Digidata | Molecular Devices, San José, CA, United States | 1550A | |
| Filter (530/20) | Leica Microsystems, Wetzlar, Germany | 11513878 | BZ:00 |
| Filter (630/20) | Chroma Technology, Bellows Falls, Vermont, United States | 227155 | |
| Headstage | AxonInstruments, Union City, CA, United States | CV203BU | |
| Interface | Scientifica, Uckfield, UK | 1U Rack, 352036 | |
| LED 525 nm | Luminus Devices, Sunnyvale, CA, United States | PT-120-G | |
| LED control software | Essel Research and Development, Toronto, Canada | ||
| LED control system | custom-made | ||
| Micropipette Puller | Narishige Co., Tokyo, Japan | PP-830 | |
| Microscope inverted | Leica Microsystems, Wetzlar, Germany | DMI4000B | |
| Motorised Micromanipulator | Scientifica, Uckfield, UK | PatchStar | |
| Optical power meter | Thorlabs, Newton, NJ, United States | PM100D | |
| Silicone Grease | RS Components, Corby, UK | 494-124 | |
| Silver wire | A-M Systems, Sequim, WA, United States | 787500 | Silver, Bare 0.015'', Coated 0.0190'', Length 25 Feet |
| Soda lime glass capillaries | Vitrex Medical A/S, Vasekaer, Denmark | 160213 BRIS, ISO12772 | 1.55 OD x 1.15 ID x 75 L mm |
| Software Axon pClamp | Molecular Devices, San José, CA, United States | Version 10.5 | |
| Software MatLab2017 | The MathWorks, Inc. | ||
| Stage micrometer | Graticules Optics LTD, Tonbridge, UK | 1 mm | |
| Equipment – Carbon fiber | |||
| Carbon fibers | provided from Prof. Jean-Yves Le Guennec | BZ:00 | |
| Digitizer Axon Digidata | Molecular Devices, Sunnyvale, CA, United States | 1550B | |
| Filter (530/20) | Leica Microsystems, Wetzlar, Germany | 11513878 | |
| Filter (630/20) | Chroma Technology, Bellows Falls, Vermont, United States | 227155 | |
| Fluorescence System Interface | IonOptix, Milton, MA United States | FSI-800 | 2.0 OD x 1.16 ID x 100 L mm |
| Force Transducer System | Aurora Scientific Inc., Ontario, Canada | 406A | |
| Glass capillaries for force measurements | Harvard Apparatus, Holliston, Massachusetts, United States | GC200F-10 | |
| Interface National Instruments | National Instruments, Budapest, Hungary | BNC-2110 | |
| LED 525 nm | Luminus Devices, Sunnyvale, CA, United States | PT-120-G | |
| LED control box | Essel Research and Development, Toronto, Canada | ||
| LED control system | custom-made | ||
| Microcontroller | Parallax Inc., Rocklin, California, United States | Propeller | |
| Micropipette Puller | Narishige Co., Tokyo, Japan | PC-10 | |
| Microscope inverted | Leica Microsystems, Wetzlar, Germany | DMI4000B | |
| MyoCam-S camera | IonOptix, Dublin, Ireland | ||
| MyoCam-S camera Power | IonOptix, Milton, MA, United States | MCS-100 | |
| MyoPacer Field Stimulator | IonOptix Cooperation, Milton, MA, United States | MYP100 | |
| Piezo Motor | Physik Instrumente (PI) GmbH & Co. KG, Karlsruhe, Germany | E-501.00 | |
| Silicone Grease | RS Components, Corby, UK | 494-124 | |
| Software Axon pClamp | Molecular Devices, San José, CA, United States | Version 10.5 | |
| Software IonWizard | IonOptix, Dublin, Ireland | Version 6.6.10.125 | |
| Software MatLab2017 | The MathWorks, Inc. | ||
| Stage micrometer | Graticules Optics LTD, Tonbridge, UK | 1 mm | |
| Chemicals | |||
| Adenosine | Sigma-Aldrich, St. Louis, Missouri, United States | A9251-100G | |
| Bovine serum albumin | Sigma-Aldrich, St. Louis, Missouri, United States | A7030-50G | |
| CaCl2 | Honeywell Fluka, Muskegon, MI, USA | 21114-1L | |
| L-Carnitine hydrochloride | Sigma-Aldrich, St. Louis, Missouri, United States | C9500-25G | |
| Collagenase type 2, 315 U/mg | Worthington, Lakewood, NJ, USA | LS004177 | |
| Creatine | Sigma-Aldrich, St. Louis, Missouri, United States | C0780-50G | |
| Cytosine-β-D-arabinofuranoside | Sigma-Aldrich, St. Louis, Missouri, United States | C1768-100MG | |
| EGTA | Carl Roth GmbH + Co. KG, Karlsruhe, Germany | 3054.3 | |
| Esketamine hydrochloride, Ketanest S 25 mg/mL | Pfizer Pharma PFE GmbH, Berlin, Germany | PZN-07829486 | |
| Fetal Bovine Serum | Sigma-Aldrich, St. Louis, Missouri, United States | F9665 | |
| Gentamycin 50 mg/mL | Gibco, Life Technologies, Waltham, MA, USA | 15750-037 | |
| Glucose | Sigma-Aldrich, St. Louis, Missouri, United States | G7021-1KG | |
| Heparin-Sodium, 5,000 IU/mL | Braun Melsungen AG, Melsungen, Germany | PZN-03029843 | |
| HEPES | Sigma-Aldrich, St. Louis, Missouri, United States | H3375-1KG | |
| Insulin (bovine pancreas) | Sigma-Aldrich, St. Louis, Missouri, United States | I6634-50MG | |
| K-aspartate | Sigma-Aldrich, St. Louis, Missouri, United States | A6558-25G | |
| KCl | VWR International GmbH, Leuven, Belgium | 26764.260 | 1 mg/mL |
| KOH | Honeywell Fluka, Muskegon, MI, USA | 35113-1L | |
| Laminin from Engelbreth-Holm-Swarm murine sarcoma basement membrane | Sigma-Aldrich, St. Louis, Missouri, United States | L2020-1MG | |
| M199-Medium | Sigma-Aldirch, St. Louis, Missouri, United States | M4530 | |
| Mg-ATP | Sigma-Aldrich, St. Louis, Missouri, United States | A9187-1G | |
| MgCl2 | Sigma-Aldrich, St. Louis, Missouri, United States | 63069-500ML | |
| NaCl | Fisher Scientific, Loughborough, Leics., UK | 10428420 | |
| NaCl-Solution 0.9%, Isotone Kochsalz-Lösung 0.9% | Braun Melsungen AG, Melsungen, Germany | 3200950 | |
| NaOH | AppliChem GmbH, Darmstadt, Germany | A6579 | without Ca2+/Mg2+ |
| Na-pyruvat | Sigma-Aldrich, St. Louis, Missouri, United States | P2256-100MG | |
| Phosphate Buffered Saline | Sigma-Aldrich, St. Louis, Missouri, United States | D1408-500ML | |
| Poly(2-hydroxyethyl methacrylate) | Sigma, Poole, UK | 192066 | |
| Protease XIV from Streptomyces griseus | Sigma-Aldrich, St. Louis, Missouri, United States | P5147-1G | |
| Taurine | Sigma-Aldrich, St. Louis, Missouri, United States | T0625-500G | |
| Thiopental Inresa 0.5 g | Inresa Arzneimittel GmbH, Freiburg, Germany | PZN-11852249 | |
| Xylazine hydrochloride, Rompun 2% | Bayer Vital GmbH, Leverkusen, Germany | PZN-01320422 |
Referências
- Harz, H., Hegemann, P. Rhodopsin-regulated calcium currents in Chlamydomonas. Nature. 351, 489-491 (1991).
- Litvin, F. F., Sineshchekov, O. A., Sineshchekov, V. A. Photoreceptor electric potential in the phototaxis of the alga Haematococcus pluvialis. Nature. 271, 476-478 (1978).
- Nagel, G., et al. Channelrhodopsin-1: A Light-Gated Proton Channel in Green Algae. Science. 296 (5577), 2395-2398 (2002).
- Nagel, G., et al. Channelrhodopsin-2, a directly light-gated cation-selective membrane channel. Proceedings of the National Academy of Sciences of the United States of America. 100 (24), 13940-13945 (2003).
- Boyden, E. S., Zhang, F., Bamberg, E., Nagel, G., Deisseroth, K. Millisecond-timescale, genetically targeted optical control of neural activity. Nature Neuroscience. 8 (9), 1263-1268 (2005).
- Bruegmann, T., et al. Optogenetic control of heart muscle in vitro and in vivo. Nature Methods. 7 (11), 897-900 (2010).
- Lozier, R. H., Bogomolni, R. A., Stoeckenius, W. Bacteriorhodopsin: a light-driven proton pump in Halobacterium Halobium. Biophysical journal. 15 (9), 955-962 (1975).
- Schobert, B., Lanyi, J. K. Halorhodopsin is a light-driven chloride pump. Journal of Biological Chemistry. 257 (17), 10306-10313 (1982).
- Inoue, K., et al. A light-driven sodium ion pump in marine bacteria. Nature Communications. 4, 1678 (2013).
- Han, X., et al. A High-Light Sensitivity Optical Neural Silencer: Development and Application to Optogenetic Control of Non-Human Primate Cortex. Frontiers in Systems Neuroscience. 5, 18 (2011).
- Zhang, F., et al. Multimodal fast optical interrogation of neural circuitry. Nature. 446 (7136), 633-639 (2007).
- Grimm, C., Silapetere, A., Vogt, A., Bernal Sierra, Y. A., Hegemann, P. Electrical properties, substrate specificity and optogenetic potential of the engineered light-driven sodium pump eKR2. Scientific Reports. 8, 9316 (2018).
- Wietek, J., et al. Conversion of channelrhodopsin into a light-gated chloride channel. Science. 344 (6182), 409-412 (2014).
- Berndt, A. Structure-Guided Transformation. Science. 344 (6182), 420-424 (2014).
- Govorunova, E. G., Sineshchekov, O. A., Janz, R., Liu, X., Spudich, J. L. Natural light-gated anion channels: A family of microbial rhodopsins for advanced optogenetics. Science. 349 (6248), 647-650 (2015).
- Mohamed, G. A., et al. Optical inhibition of larval zebrafish behaviour with anion channelrhodopsins. BMC Biology. 15 (1), 103 (2017).
- Mauss, A. S., Busch, C., Borst, A. Optogenetic Neuronal Silencing in Drosophila during Visual Processing. Scientific Reports. 7, 13823 (2017).
- Govorunova, E. G., Cunha, S. R., Sineshchekov, O. A., Spudich, J. L. Anion channelrhodopsins for inhibitory cardiac optogenetics. Scientific Reports. 6, 33530 (2016).
- Kopton, R. A., et al. Cardiac Electrophysiological Effects of Light-Activated Chloride Channels. Frontiers in Physiology. 9, 1806 (2018).
- Peyronnet, R., et al. Load-dependent effects of apelin on murine cardiomyocytes. Progress in Biophysics and Molecular Biology. 130, 333-343 (2017).
- Wang, K., et al. Cardiac tissue slices: preparation, handling, and successful optical mapping. American Journal of Physiology-Heart and Circulatory Physiology. 308 (9), 1112-1125 (2015).
- Nishimura, S., et al. Single cell mechanics of rat cardiomyocytes under isometric, unloaded, and physiologically loaded conditions. American Journal of Physiology-Heart and Circulatory Physiology. 287 (1), 196-202 (2004).
- Mitcheson, J. S., Hancox, J. C., Levi, A. J. Action potentials, ion channel currents and transverse tubule density in adult rabbit ventricular myocytes maintained for 6 days in cell culture. Pflugers Archiv European Journal of Physiology. 43 (6), 814-827 (1996).
- Burton, R. A. B., et al. Caveolae in Rabbit Ventricular Myocytes: Distribution and Dynamic Diminution after Cell Isolation. Biophysical Journal. 113 (5), 1047-1059 (2017).
- Louch, W. E., Sheehan, K. A., Wolska, B. M. Methods in cardiomyocyte isolation, culture, and gene transfer. Journal of Molecular and Cellular Cardiology. 51 (3), 288-298 (2011).
- Janssen, P. M., Hunter, W. C. Force, not sarcomere length, correlates with prolongation of isosarcometric contraction. The American Journal of Physiology. 269 (2), 676-685 (1995).
- Monasky, M. M., Varian, K. D., Davis, J. P., Janssen, P. M. L. Dissociation of force decline from calcium decline by preload in isolated rabbit myocardium. Pflugers Archiv European Journal of Physiology. 456 (2), 267-276 (2008).
- Kleinlogel, S., et al. Ultra light-sensitive and fast neuronal activation with the Ca 2+-permeable channelrhodopsin CatCh. Nature Neuroscience. 14 (4), 513-518 (2011).
- Schneider-Warme, F., Ravens, U. Using light to fight atrial fibrillation. Cardiovascular Research. 114 (5), 635-637 (2018).
- Chow, B. Y., et al. High-performance genetically targetable optical neural silencing by light-driven proton pumps. Nature. 463 (7277), 98-102 (2010).
- Bernal Sierra, Y. A., et al. Potassium channel-based optogenetic silencing. Nature Communications. 9 (1), 4611 (2018).
- Oda, K., et al. Crystal structure of the red light-activated channelrhodopsin Chrimson. Nature Communications. 9 (1), 3949 (2018).

