Preparación de muestras en Mediciones de microbalance de cristal de cuarzo de adsorción de proteínas y mecánica de polímeros
Summary
El microbalance de cristal de cuarzo puede proporcionar propiedades precisas de masa y viscoelástica para películas en el rango de micras o submicrones, lo que es relevante para investigaciones en detección biomédica y ambiental, recubrimientos y ciencia de polímeros. El espesor de la muestra influye en qué información se puede obtener del material en contacto con el sensor.
Abstract
En este estudio, presentamos varios ejemplos de cómo la preparación de película delgada para experimentos de microbalanza de cristal de cuarzo informa el modelado adecuado de los datos y determina qué propiedades de la película se pueden cuantificar. El microbalance de cristal de cuarzo ofrece una plataforma únicamente sensible para medir los cambios finos en las propiedades mecánicas y/o de masa de una película aplicada observando los cambios en la resonancia mecánica de un cristal de cuarzo que oscila a alta frecuencia. Las ventajas de este enfoque incluyen su versatilidad experimental, la capacidad de estudiar los cambios en las propiedades en una amplia gama de longitudes de tiempo experimentales y el uso de pequeños tamaños de muestra. Demostramos que, en base al espesor y el módulo de cizallamiento de la capa depositada en el sensor, podemos adquirir información diferente del material. Aquí, este concepto se explota específicamente para mostrar parámetros experimentales que resultan en cálculos de masa y viscoelástica de colágeno adsorbida en complejos de oro y polielectrolitos durante la hinchazón en función de la concentración de sal.
Introduction
El microbalance de cristal de cuarzo (QCM) aprovecha el efecto piezoeléctrico de un cristal de cuarzo para controlar su frecuencia resonante, que depende de la masa adherida a la superficie. La técnica compara la frecuencia resonante y el ancho de banda de un sensor de cristal de cuarzo cortado AT (normalmente en el rango de 5 MHz)1 en aire o un fluido con la frecuencia y el ancho de banda del sensor después de la deposición de una película. Hay varios beneficios para el uso del QCM para estudiar las propiedades e interfaces de película delgada, incluyendo la alta sensibilidad a la masa y potencialmente a los cambios de propiedad viscoelástica (dependiendo de la uniformidad y el grosor de la muestra), la capacidad de realizar estudios en el lugar2,y la capacidad de sondear una escala de tiempo reológica mucho más corta que la reología de cizallamiento tradicional o el análisis mecánico dinámico (DMA). Sondear una escala temporal reológica corta permite la observación de cómo la respuesta en este intervalo de tiempo cambia tanto en tiempos extremadamente cortos (ms)3 y largas (años) duraciones4. Esta capacidad es beneficiosa para el estudio de una variedad de procesos cinéticos y también es una extensión útil de las técnicas reométricas tradicionales5,6.
La alta sensibilidad del QCM también ha llevado a su uso intensivo en aplicaciones biológicas que estudian las interacciones fundamentales de biomoléculas extremadamente pequeñas. Una superficie de sensor no recubierta o funcionalizada se puede utilizar para investigar la adsorción de proteínas; aún más, el bioensión a través de eventos de unión complejos entre enzimas, anticuerpos y aptámeros se puede examinar en función de los cambios en la masa7,8,9. Por ejemplo, la técnica se ha utilizado para entender la transformación de las vesículas a una bicapa lipídica plana como un proceso bifásico bifásico de adsorción de vesículas que contienen líquidos a una estructura rígida observando cambios correlacionados en la frecuencia y la viscoelasticidad10. En los últimos años, el QCM ha ofrecido además una plataforma robusta para monitorear la administración de fármacos por vesículas o nanopartículas11. En la intersección de la ingeniería de materiales y la biología molecular y celular, podemos utilizar el QCM para dilucidar interacciones clave entre materiales y componentes bioactivos como proteínas, ácidos nucleicos, liposomas y células. Por ejemplo, la adsorción de proteínas a un biomaterial media respuestas celulares aguas abajo como la inflamación y a menudo se utiliza como un indicador positivo de biocompatibilidad, mientras que en otros casos la unión de proteína extracelular a recubrimientos que interactúan con la sangre podría inducir coagulación peligrosa en los vasos12,13. Por lo tanto, el QCM se puede utilizar como una herramienta para seleccionar candidatos óptimos para diferentes necesidades.
Dos enfoques comunes para realizar experimentos qCM recopilan datos análogos del experimento: el primer enfoque registra el cambio de frecuencia y la mitad del ancho de banda() del pico de conductividad. El segundo enfoque, QCM con disipación (QCM-D), registra el cambio de frecuencia y el factor de disipación, que es directamente proporcional a la ecuación 1,14
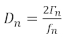 (1)
(1)
donde D es el factor de disipación y es la frecuencia. Tanto D como é están relacionados con el efecto de amortiguación que la película tiene en el sensor, lo que indica la rigidez de la película. El subíndice n denota el armónico o armónico de frecuencia, que son las frecuencias resonantes impares del sensor de cuarzo (n a 1, 3, 5, 7…). Más discusión de modelos utilizando múltiples armónicos para obtener la masa y las propiedades viscoelásticas de una película se puede encontrar en una revisión de Johannsmann14 y documentos anteriores del grupo Shull15,16,17,18.
Una consideración clave para preparar muestras QCM es cómo aplicar la película delgada en la superficie del sensor. Algunos métodos comunes incluyen recubrimiento de espín, recubrimiento por inmersión, recubrimiento de gotas o adsorción de la película en la superficie del sensor durante el experimento19,20. Hay cuatro regiones para las muestras qCM: el límite de Sauerbrey, el régimen viscoelástico, el régimen a granel y el régimen sobreamplificado. Para películas suficientemente delgadas, se aplica el límite de Sauerbrey, donde el cambio de frecuencia(o)proporciona la densidad de masa de la superficie de la película. Dentro del límite de Sauerbrey, las escalas de cambio de frecuencia linealmente con el armónico resonante, n, y los cambios en el factor de amortiguación (D o )son generalmente pequeños. En este régimen no se dispone de suficiente información para determinar de forma exclusiva las propiedades reológicas de la capa sin hacer suposiciones adicionales. Los datos de este régimen se utilizan para calcular la densidad de masa superficial (o el grosor si la densidad se conoce a priori)de la película. En el régimen a granel en el que el medio en contacto con el cristal es lo suficientemente grueso, la onda cortante evanescente se propaga en el medio antes de ser completamente amortiguada. Aquí, no se puede obtener ninguna información de masa utilizando. Sin embargo, en esta región, las propiedades de viscoelástica se determinan de forma fiable utilizando la combinación delos números 15,18. En el régimen a granel, si el medio es demasiado rígido, la película amortiguará la resonancia del sensor, evitando la recopilación de datos fiables del QCM. El régimen viscoelástico es el régimen intermedio donde la película es lo suficientemente delgada como para que la onda cortante se propague completamente a través de la película, así como para tener valores fiables para el factor de amortiguación. A continuación, se puede utilizar el factor de amortiguación yel factor de amortiguación para determinar las propiedades viscoelásticas de la película, así como su masa. Aquí, las propiedades viscoelásticas son dadas por el producto de la densidad y la magnitud del módulo de cizallamiento complejo . G* p y el ángulo de fase dado por el valor de arctan(G” / G’). Cuando las películas se preparan en el límite de Sauerbrey, la masa por unidad de área se puede calcular directamente sobre la base de la ecuación de Sauerbrey que se muestra a continuación21,
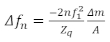 (2)
(2)
Donde el n es el cambio en la frecuencia resonante, n es el tono de interés, 1es la frecuencia resonante del sensor,m / A es la masa por área de la película, y Zq es la impedancia acústica del cuarzo, que para el cuarzo cortado AT es Zq a 8,84 x 106kg / m2s. El régimen viscoelástico es más adecuado para el estudio de películas poliméricas, y el límite a granel es útil para el estudio de polímero viscoso22 o soluciones proteicas16. Los diferentes regímenes dependen de las propiedades del material de interés, con el espesor óptimo para la caracterización viscoelástica completa y de masa sin aumentar generalmente con la rigidez de la película. La Figura 1 describe las cuatro regiones con respecto a la densidad areal de la película, el módulo de cizallamiento complejo y el ángulo de fase, donde hemos asumido una relación específica entre el ángulo de fase y la rigidez de la película que se ha demostrado que es relevante para los materiales de este tipo. Muchas películas de interés práctico son demasiado gruesas para estudiar las propiedades viscoelásticas con QCM, como ciertas biopelículas, donde los espesores están en el orden de decenas a cientos de micras23. Estas películas gruesas generalmente no son apropiadas para estudiar usando el QCM, pero pueden medirse usando resonadores de frecuencia mucho más baja (como resonadores torsionales)23,permitiendo que la onda cortante se propague aún más en la película.
Para determinar qué régimen es relevante para una muestra QCM determinada, es importante entender el parámetro d /n, que es la relación entre el espesor de la película (d) y la longitud de onda de cizallamiento de la oscilación mecánica del sensor de cristal de cuarzo(n)15,16,18. El régimen viscoelástico ideal es d /n á 0,05 – 0,218, donde los valores por debajo de 0,05 están dentro del límite de Sauerbrey y los valores por encima de 0,2 se acercan al régimen a granel. En otros lugaresseproporciona una descripción más rigurosa de d /n, pero es un parámetro cuantitativo que desentraña el límite de Sauerbrey y el límite viscoelástico. Los programas de análisis utilizados a continuación proporcionan este parámetro directamente.
Hay algunas limitaciones adicionales para analizar películas delgadas con el QCM. Los cálculos Sauerbrey y viscoelástico suponen que la película es homogénea tanto en todo el espesor de la película como lateralmente a través de la superficie del electrodo del QCM. Si bien esta suposición hace difícil estudiar películas que tienen vacíos o rellenos presentes, ha habido algunas investigaciones de QCM sobre películas consistentes en nanopartículas injertadas6. Si las heterogeneidades son pequeñas en comparación con el espesor total de la película, todavía se pueden obtener propiedades viscoelásticas fiables del sistema compuesto. Para sistemas más heterogéneos, los valores obtenidos a partir de un análisis viscoelástico siempre deben ser vistos con mucha precaución. Idealmente, los resultados obtenidos de sistemas con heterogeneidad desconocida deben validarse contra sistemas que se sabe que son homogéneos. Este es el enfoque que hemos adoptado en el sistema de ejemplo descrito en este documento.
Un punto importante que ilustramos en este documento es la correspondencia exacta entre las mediciones de QCM realizadas en el dominio de frecuencia (donde se informa de la palabra ) y los experimentos de dominio de tiempo (donde se informa D). Se describen los resultados de dos experimentos QCM diferentes, un dominio de tiempo y un dominio de frecuencia, cada uno de los que implica un sistema de modelo diferente pero conceptualmente relacionado. El primer sistema es un ejemplo simple de fijación de colágeno al sensor para ilustrar la cinética de unión representativa y el equilibrio de adsorción a lo largo del tiempo durante una medición de dominio de tiempo (QCM-D). El colágeno es la proteína más abundante en el cuerpo, conocida por su versatilidad de comportamientos de unión y morfología. La solución de colágeno utilizada aquí no requiere funcionalización adicional de la superficie de oro del sensor para inducir la adsorción9. El segundo sistema experimental es un complejo de polielectrolitos (PEC) compuesto por sulfonato de poliestireno aniónico (PSS) y policatiónico catiónico (diallyldimethylammonium) (PDADMA) preparado de la misma manera que Sadman et al.22. Estos materiales se hinchan y se vuelven suaves en soluciones de sal (KBr en este caso), ofreciendo una plataforma simple para el estudio de la mecánica de polímeros utilizando un enfoque de dominio de frecuencia (QCM-Z). Para cada protocolo, el proceso de preparación, toma y análisis de una medición se muestra en la Figura 2. El esquema muestra que la principal diferencia entre los enfoques QCM-Z y QCM-D está en el paso de recopilación de datos y la instrumentación utilizada en el experimento. Todas las técnicas de preparación de muestras mencionadas son compatibles con ambos enfoques, y cada enfoque puede analizar muestras en las tres regiones representadas en la Figura 1.
Nuestros datos demuestran que la preparación de muestras, ya sea mediante recubrimiento de sensor antes o durante una medición, dicta la capacidad de extraer las propiedades viscoelásticas de un sistema. Al diseñar las primeras etapas de un experimento adecuadamente, podemos determinar qué información podemos recopilar con precisión durante el paso de análisis.
Protocol
Representative Results
Discussion
Los resultados de la adsorción de colágeno abarcan los regímenes de Sauerbrey y viscoelástico. Al trazar los cambios de frecuencia normalizados al número armónico correspondiente, observamos que el límite de Sauerbrey se mantiene fiel para aproximadamente las primeras 2 h de la medición. Con el aumento de la masa de adcejo al sensor, sin embargo, los cambios de frecuencia normalizados para el tercer y quinto armónicos comienzan a desviarse unos de otros(t > 2 h), lo que indica una capacidad para determi…
Declarações
The authors have nothing to disclose.
Acknowledgements
Este trabajo fue apoyado por el NSF (DMR-1710491, OISE-1743748). J.R. y E.S. reconocen el apoyo de la NSF (DMR-1751308).
Materials
| Acetic acid | Sigma-Aldrich | A6283 | For collagen adsorption |
| Ammonium hydroxide solution | Sigma-Aldrich | 221228 | For collagen adsorption |
| Aqueous QCM probe | AWSensors | CLS 00050 A | For polyelectrolyte swelling |
| Collagen I Rat Protein, Tail | Thermo Fisher Scientific | A1048301 | For collagen adsorption |
| Distilled water | Sigma-Aldrich | EM3234 | For polyelectrolyte swelling; generally easy to acquire in research labs, but there is a catalog number in case it is not accessible |
| Ethanol | Sigma-Aldrich | 793175-1GA-PB | For polyelectrolyte swelling |
| Gibco Phosphate Buffered Saline | Thermo Fisher Scientific | 20012-027 | For collagen adsorption |
| Hellmanex III | Sigma-Aldrich | Z805939 | For collagen adsorption |
| Hydrogen peroxide solution | Sigma-Aldrich | 216763 | For collagen adsorption |
| Kimberly-Clark Professional Kimtech Science Kimwipes Delicate Task Wipers, 1-Ply | Fisher Scientific | 06-666A | For polyelectrolyte swelling |
| NP2K VNA | Makarov Instruments | For polyelectrolyte swelling | |
| Poly(diallyldimethylammonium chloride), MW 200,000 | Sigma-Aldrich | 409022 | For polyelectrolyte swelling; for full synthesis procedure see Sadman et al. |
| Poly(styrene-sulfonate) sodium salt 30% weight in water | Sigma-Aldrich | 561967-500G | For polyelectrolyte swelling; for full synthesis procedure see Sadman et al. |
| Potassium Bromide | Sigma-Aldrich | 793604-1KG | For polyelectrolyte swelling |
| QSense QCM Explorer System | Biolin Scientific | For collagen adsorption | |
| Sodium acetate, anhydrous | Sigma-Aldrich | S2889 | For collagen adsorption |
| Spin coater, Model WS-650MZ-23NPP | Laurell technologies | For polyelectrolyte swelling |
Referências
- Marx, K. A. Quartz crystal microbalance: A useful tool for studying thin polymer films and complex biomolecular systems at the solution – Surface interface. Biomacromolecules. 4 (5), 1099-1120 (2003).
- Kleber, C., Hilfrich, U., Schreiner, M. In situ QCM and TM-AFM investigations of the early stages of degradation of silver and copper surfaces. Applied Surface Science. 253 (7), 3712-3721 (2007).
- Yeh, C. J., Hu, M., Shull, K. R. Oxygen Inhibition of Radical Polymerizations Investigated with the Rheometric Quartz Crystal Microbalance. Macromolecules. 51 (15), 5511-5518 (2018).
- Sturdy, L. F., Yee, A., Casadio, F., Shull, K. R. Quantitative characterization of alkyd cure kinetics with the quartz crystal microbalance. Polymer. 103, 387-396 (2016).
- Delgado, D. E., Sturdy, L. F., Burkhart, C. W., Shull, K. R. Validation of quartz crystal rheometry in the megahertz frequency regime. Journal of Polymer Science, Part B: Polymer Physics. , 1-9 (2019).
- Bilchak, C. R., Huang, Y., Benicewicz, B. C., Durning, C. J., Kumar, S. K. High-Frequency Mechanical Behavior of Pure Polymer-Grafted Nanoparticle Constructs. ACS Macro Letters. 8 (3), 294-298 (2019).
- Hook, F., Rodahl, M., Brzezinski, P., Kasemo, B. Energy dissipation kinetics for protein and antibody-antigen adsorption under shear oscillation on a quartz crystal microbalance. Langmuir. 14, 729-734 (1998).
- Liss, M., Petersen, B., Wolf, H., Prohaska, E. An aptamer-based quartz crystal protein biosensor. Analytical Chemistry. 74 (17), 4488-4495 (2002).
- Felgueiras, H. P., Murthy, N. S., Sommerfeld, S. D., Brás, M. M., Migonney, V., Kohn, J. Competitive Adsorption of Plasma Proteins Using a Quartz Crystal Microbalance. ACS Applied Materials and Interfaces. 8 (21), 13207-13217 (2016).
- Keller, C. A., Kasemo, B. Surface specific kinetics of lipid vesicle adsorption measured with a quartz crystal microbalance. Biophysical Journal. 75, 1397-1402 (1998).
- Olsson, A. L. J., Quevedo, I. R., He, D., Basnet, M., Tufenkji, N. Using the quartz crystal microbalance with dissipation monitoring to evaluate the size of nanoparticles deposited on surfaces. ACS Nano. 7 (9), 7833-7843 (2013).
- Xu, X., Zhang, C., Zhou, Y., Cheng, Q. L. J., Yao, K., Chen, Q. Quartz crystal microbalance study of protein adsorption on chitosan, chitosan/poly(vinyl pyrrolidone) blends and chitosan-graft-poly(vinyl pyrrolidone) surfaces. Journal of Bioactive and Compatible Polymers. 22, 195-206 (2007).
- Weber, N., Pesnell, A., Bolikal, D., Zeltinger, J., Kohn, J. Viscoelastic properties of fibrinogen adsorbed to the surface of biomaterials used in blood-contacting medical devices. Langmuir. 23, 3298-3304 (2007).
- Johannsmann, D. Viscoelastic, mechanical, and dielectric measurements on complex samples with the quartz crystal microbalance. Physical Chemistry Chemical Physics. 10 (31), 4516-4534 (2008).
- Denolf, G. C., Sturdy, L. F., Shull, K. R. High-frequency rheological characterization of homogeneous polymer films with the quartz crystal microbalance. Langmuir. 30 (32), 9731-9740 (2014).
- Martin, E. J., Mathew, M. T., Shull, K. R. Viscoelastic properties of electrochemically deposited protein/metal complexes. Langmuir. 31 (13), 4008-4017 (2015).
- Sturdy, L., Casadio, F., Kokkori, M., Muir, K., Shull, K. R. Quartz crystal rheometry: A quantitative technique for studying curing and aging in artists’ paints. Polymer Degradation and Stability. 107, 348-355 (2014).
- Sadman, K., Wiener, C. G., Weiss, R. A., White, C. C., Shull, K. R., Vogt, B. D. Quantitative Rheometry of Thin Soft Materials Using the Quartz Crystal Microbalance with Dissipation. Analytical Chemistry. 90 (6), 4079-4088 (2018).
- Wasilewski, T., Szulczyński, B., Kamysz, W., Gębicki, J., Namieśnik, J. Evaluation of three peptide immobilization techniques on a qcm surface related to acetaldehyde responses in the gas phase. Sensors (Switzerland). 18 (11), 1-15 (2018).
- Lvov, Y., Ariga, K., Kunitake, T., Ichinose, I. Assembly of Multicomponent Protein Films by Means of Electrostatic Layer-by-Layer Adsorption. Journal of the American Chemical Society. 117 (22), 6117-6123 (1995).
- Sauerbrey, G. Verwendung von Schwingquarzen zur Wägung dünner Schichten und zur Mikrowägung. Zeitschrift für Physik. 155 (2), 206-222 (1959).
- Sadman, K., Wang, Q., Chen, Y., Keshavarz, B., Jiang, Z., Shull, K. R. Influence of Hydrophobicity on Polyelectrolyte Complexation. Macromolecules. 50 (23), 9417-9426 (2017).
- Sievers, P., Moß, C., Schröder, U., Johannsmann, D. Use of torsional resonators to monitor electroactive biofilms. Biosensors and Bioelectronics. 110, 225-232 (2018).
- Ringberg, J. Q-Sense Explorer Operator Manual. Biolin Scientific. , (2017).
- Ringberg, J. Q-Sense User Guide: Instrument care and sensor pre-cleaning. Biolin Scientific. , (2015).
- Kern, W. The Evolution of Silicon Wafer Cleaning Technology. Journal of The Electrochemical Society. 137 (6), 1887 (1990).
- Sadman, K. . sadmankazi/QCM-D-Analysis-GUI: QCMD-Analyze. , (2018).

