Studie van eiwitdynamica via neutronenspinechospectroscopie
Summary
Het huidige protocol beschrijft methoden voor het onderzoeken van de structuur en dynamiek van twee modeleiwitten die een belangrijke rol spelen in de menselijke gezondheid. De techniek combineert bench-top biofysische karakterisering met neutronenspinechospectroscopie om toegang te krijgen tot de dynamiek op tijd- en lengteschalen die relevant zijn voor eiwitinterdomeinbewegingen.
Abstract
De activiteit en functionaliteit van de meeste menselijke lichaamseiwitten zijn gerelateerd aan configuratieveranderingen van hele subdomeinen binnen de eiwitkristalstructuur. De kristalstructuren vormen de basis voor elke berekening die de structuur of dynamiek van een eiwit beschrijft, meestal met sterke geometrische beperkingen. Deze beperkingen van de kristalstructuur zijn echter niet aanwezig in de oplossing. De structuur van de eiwitten in de oplossing kan verschillen van het kristal als gevolg van herschikkingen van lussen of subdomeinen op de pico- naar nanosecondetijdschaal (d.w.z. het interne tijdsregime van de eiwitdynamica). Het huidige werk beschrijft hoe slow motions op tijdschalen van enkele tientallen nanoseconden toegankelijk zijn met behulp van neutronenverstrooiing. In het bijzonder wordt de dynamische karakterisering van twee belangrijke menselijke eiwitten, een intrinsiek ongeordend eiwit dat een goed gedefinieerde secundaire structuur en een klassiek antilichaameiwit mist, aangepakt door neutronenspinechospectroscopie (NSE) in combinatie met een breed scala aan laboratoriumkarakteriseringsmethoden. Verdere inzichten in eiwitdomeindynamica werden verkregen met behulp van wiskundige modellering om de experimentele neutronengegevens te beschrijven en de cross-over tussen gecombineerde diffusieve en interne eiwitbewegingen te bepalen. De extractie van de interne dynamische bijdrage aan de intermediaire verstrooiingsfunctie verkregen van NSE, inclusief de tijdschaal van de verschillende bewegingen, maakt verder zicht mogelijk op de mechanische eigenschappen van afzonderlijke eiwitten en de zachtheid van eiwitten in hun bijna natuurlijke omgeving in de overvolle eiwitoplossing.
Introduction
Indringende dynamiek van zachte materie met neutronen
Het onderzoeken van de dynamische eigenschappen van eiwitten en peptiden is een belangrijk onderdeel van biofysisch onderzoek, en er bestaan tegenwoordig veel goed ontwikkelde methoden om toegang te krijgen tot een breed scala aan energielandschappen1. Het relateren van de experimenteel onthulde dynamiek van de eiwitten aan hun biologische functie is een veel moeilijkere taak, waarvoor complexe wiskundige modellen en computerondersteunde dynamicasimulaties nodig zijn. Het belang van neutronenspectroscopie voor de analyse van eiwitbewegingen is benadrukt in verschillende goed ontvangen en algemeen erkende studies 1,2,3,4,5. Alvorens het diverse energielandschap van interne eiwitdynamica te verkennen, is een kort overzicht nodig van de dynamische processen in zachte materie en hoe neutronen er toegang toe kunnen krijgen.
De gevoeligheid van neutronen voor isotopische configuratie en het type interacties dat ze vertonen met zachte materie maakt neutronenverstrooiing een van de meest veelzijdige onderzoekstechnieken6. Er is een breed spectrum van correlatielengteschalen en correlatietijden waartoe neutronen toegang hebben, van nucleaire excitaties en atomaire trillingen tot collectieve bewegingen en langzame ontspanningsprocessen zoals isotrope rotaties en diffusieve bewegingen. Bij het onderzoeken van de verstrooide neutronen op hun energieoverdracht kunnen drie hoofdinteracties worden onderscheiden: de elastische verstrooiing, waarbij er geen energie-uitwisseling plaatsvindt tussen inkomend neutron en deeltje in het monster; de inelastische verstrooiing, met een grote, kwantificeerbare energie-uitwisseling tussen neutron en deeltje; en het eigenaardige geval van quasi-elastische verstrooiing dat een zeer kleine energieoverdracht aanduidt in vergelijking met de invallende neutronenenergie 1,7. Deze interacties geven nauwkeurige informatie over het onderzochte materiaal en vormen de theoretische basis van een breed scala aan neutronenverstrooiingstechnieken.
Bij elastische verstrooiing registreert de detector de richtingen van de neutronen als een diffractiepatroon, dat de positie van de monsteratomen ten opzichte van elkaar weergeeft. Informatie over de correlaties van atomaire posities wordt verkregen (d.w.z. geïntegreerde intensiteit S(Q) met betrekking tot de impulsoverdracht Q, die alleen betrekking heeft op structurele informatie). Dit principe vormt de basis van neutronendiffractie8.
Complexiteit ontstaat wanneer de energieoverdracht niet langer nul is als gevolg van excitaties en interne fluctuaties in het monstermateriaal. Dit vormt de basis van neutronenspectroscopie, waarbij de verstrooide neutronen worden onderzocht als functie van zowel de energieoverdracht E als de impulsoverdracht Q. Dynamische en structurele informatie wordt verkregen. Neutronenspectroscopie meet dezelfde geïntegreerde intensiteit S(Q) voor energieoverdracht (d.w.z. snelheidsverandering van de neutronen als gevolg van monsterverstrooiing, S(Q,ω) = S(Q, E), die ook wel de dynamische structuurfactor wordt genoemd)9.
Voor het berekenen van de verstrooiing van een materiaal is het adequater om de paarcorrelatiefunctie 7,10 te gebruiken. In het geval van diffractie geeft de statische paarcorrelatiefunctie G(r) de kans om het centrum van een deeltje op een bepaalde afstand r van het centrum van een ander deeltje te vinden. De spectroscopie generaliseert de statische paarcorrelatiefunctie en neemt energie/ frequentie / tijd op in de verstrooiingsvergelijking. De paarcorrelatiefunctie G(r) wordt een functie van tijd G(r, t), die kan worden ontleed in een afzonderlijke atoompaarcorrelatiefunctie GD(r, t) en een zelfcorrelatiefunctie GS(r, t). Deze beschrijven twee soorten correlaties: paar-gecorreleerde bewegingen van atomen die de coherente verstrooiing regelen, en zelfcorrelatie die de onsamenhangende verstrooiing regelt10.
Coherente verstrooiing is de verstrooiing van “het gemiddelde” en is afhankelijk van de relatieve fase van de verstrooide golven. In het verstrooiingsregime met een kleine hoek interfereren de verstrooide neutronengolven uit verschillende verstrooiingscentra (verschillende atomen) constructief (hebben vergelijkbare fasen) en de collectieve beweging van de atomen wordt waargenomen met een sterke intensiteitsverbetering. Coherente verstrooiing beschrijft in wezen de verstrooiing van een enkel neutron uit alle kernen in het monster10.
Wanneer er geen constructieve interferentie optreedt tussen de verstrooide neutronengolven uit verschillende centra, wordt een enkel atoom in de tijd gevolgd en wordt de zelfcorrelatie tussen de positie van het atoom op tijdstip t = 0 en hetzelfde atoom op tijdstip t waargenomen. Zo gaat de informatie over de relatieve posities van atomen verloren en ligt de focus alleen op lokale fluctuaties. Verstrooiing door lokale fluctuaties regeert onsamenhangende verstrooiing. Onsamenhangende verstrooiing is isotroop, draagt bij aan het achtergrondsignaal en degradeert de signaal-naar-ruis 10,11.
Door al het bovenstaande te combineren, onderscheiden we vier belangrijke neutronenverstrooiingsprocessen10: (1) elastisch coherent (meet de correlaties van atomaire posities), (2) inelastisch coherent (meet collectieve bewegingen van atomen), (3) elastische onsamenhangende (draagt bij aan de achtergrond, vermindert de verstrooiingsintensiteit door Debye-Waller-factor (DWF) en meet elastische onsamenhangende structuurfactor (EISF), waarbij de geometrie van diffusieve bewegingen in beperkte geometrie wordt beschreven, en (4) inelastisch onsamenhangend (meet de dynamiek van één atoom en zelfcorrelatie).
Dynamische processen waartoe neutronen in de biologie toegang hebben, variëren van de demping van laagfrequente atomaire en moleculaire trillingen, de interactie van oplosmiddelmoleculen met biooppervlakken en diffusieprocessen in de hydratatielaag van macromoleculen en beperkte geometrie, tot translatie-, rotatie- en tuimelende diffusieve bewegingen op korte afstand, en eiwitdomeinen en allosterische bewegingen1 . De grote diversiteit aan neutronenmethoden en -instrumenten voor het meten van eiwitdynamica is gebaseerd op hoe de achromatisatie van de invallende of uitgaande neutronenbundel wordt bereikt en hoe de energieanalyse van de verstrooide neutronen wordt uitgevoerd. Van drie-as tot time-of-flight, backscattering en spin-echo spectrometers, men kan dynamische processen verkennen met karakteristieke tijden tussen 1 x 10-14 s en 1 x 10-6 s (femtoseconden tot microseconden)12.
Oak Ridge National Laboratory, met zijn twee gerenommeerde neutronenbronnen, de Spallation Neutron Source – SNS13 en de High Isotope Flux Reactor – HFIR14, heeft een van de beste suites van spectrometers voor het onderzoeken van dynamica in biomaterialen. Enkele van de meest sprekende voorbeelden zijn het gebruik van de koude neutronenhakspectrometer (CNCS) bij SNS15 om de dynamische verstoring van hydratatiewater rond groen fluorescerend eiwit in oplossing16 of de sub-picoseconde collectieve trillingen van verschillende eiwittente onderzoeken 17. Een terugkerend probleem van inelastisch neutronenverstrooiingsonderzoek is dat sommige biologische processen te traag zijn om te worden waargenomen. Zonder extreme opstellingen die leiden tot een enorm verlies van neutronenintensiteit, zijn time-of-flight spectrometers beperkt tot een energieresolutie van 10 μeV, wat overeenkomt met een maximale tijdschaal van ~ 200 ps10,11. Dit is niet voldoende om grootschalige bewegingen in eiwitten waar te nemen. Daarom zijn instrumenten met een hogere energieresolutie zoals de backscattering spectrometers vaak nodig. Het combineren van de time-of-flight en backscattering-technieken is krachtig gebleken voor het onderzoeken van de verandering in interne dynamiek van Cytochrome P450cam (CYP101), een enzym dat de hydroxylering kamfer18 katalyseert.
Microscopische diffusiviteit gemeten door de backscattering spectrometer op SNS-BASIS19 was verrassend goed gedefinieerd en kon worden gescheiden in de diffusiviteit van water (hydratatie, cytoplasmatisch en bulkachtig water) en de diffusiviteit van celbestanddelen in planaire platwormen, het eerste levende dier dat werd bestudeerd door neutronenverstrooiing20 . Backscattering is een spectroscopische techniek met hoge resolutie, maar het is ook beperkt tot meerdere μeV = enkele nanoseconden, terwijl de langzame dynamiek in biomaterialen zich ook manifesteert als de overlevingstijd van correlatie tussen atomaire positie of spinoriëntaties (bijvoorbeeld ontspanningsprocessen, die regelmatig plaatsvinden in het tijdsbereik van tien tot honderden nanoseconden).
Neutronenspinechospectroscopie (NSE) is de enige neutronenverstrooiingstechniek die zo’n hoge resolutie bereikt. In tegenstelling tot andere neutronentechnieken vereist NSE geen achromatisatie van de bundel, omdat het de kwantummechanische fase van de neutronen gebruikt, wat hun magnetische momenten zijn. De manipulatie van magnetische momenten maakt het gebruik van een brede neutronenbundelgolflengteverdeling mogelijk, terwijl de techniek gevoelig is voor zeer kleine neutronensnelheidsveranderingen in de orde van 1 x 10-4. NSE is met succes gebruikt om de langzame dynamiek van eiwitten in oplossing voor veel eiwitten te onderzoeken. Onder deze vele pioniersstudies erkennen we de studie van de segmentale flexibiliteit van varkensimmunoglobuline21; de gekoppelde domeinbewegingen in Taq polymerase22; de domeinbewegingen in het tetrameer van gistalcoholdehydrogenase23; de verandering van conformatie in fosfoglyceraatkinase op substraatbinding3; de activering van domeinbewegingen en de dynamische voortplanting van allosterische signalen in de Na+/H+ exchange regulatory cofactor 1 (NHERF1) eiwit 4,24,25; de dynamiek van een compacte toestand van mercurische ionenreductase26; en de diffusie van hemoglobine in rode bloedcellen27. Twee meer recente studies in eiwitdynamica hebben de flexibiliteit van humaan antilichaam Immunoglobuline G (IgG) als een entropische lenteblootgelegd 28 en de kenmerken van oplosmiddelbijdrage aan de dynamiek van intrinsiek ongeordend myeline-basiseiwit (MBP)5.
In dit artikel worden de basisprincipes van NSE uitgelegd, de meerdere voorbereidende methoden die worden aanbevolen voor een grondig eiwitdynamica-onderzoek, evenals de methodologie en het experimentele protocol voor NSE-gegevensverzameling bij de NSE-spectrometer bij SNS, SNS-NSE. Het protocol karakteriseert twee eiwitten: IgG, een regulier menselijk antilichaameiwit, en het intrinsiek ongeordende eiwit MBP. De biofysische implicaties, de onderzoeksrelevantie van de voorbeelden en de beperkingen van de techniek worden kort besproken.
NSE-spectroscopie, de methode voor langzame dynamicametingen
NSE is een gepolariseerde techniek die de neutronentijd van de vlucht gebruikt om de uitwisseling van energie (verlies van polarisatie) te meten als gevolg van de quasi-elastische interactie tussen neutronen en atomen in een monster. In de kern van NSE-spectroscopie liggen twee basisprincipes: (1) het vermogen van de neutronenspin om in het magnetisch veld te precesseren met een frequentie die evenredig is met de magnetische sterkte 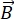 , namelijk de Larmor-frequentie29, en (b) de spin-echo of Hann-echo, die de manipulatie en heroriëntatie van het polarisatiesignaal vertegenwoordigt bij het toepassen van een reeks radiofrequente pulsen30.
, namelijk de Larmor-frequentie29, en (b) de spin-echo of Hann-echo, die de manipulatie en heroriëntatie van het polarisatiesignaal vertegenwoordigt bij het toepassen van een reeks radiofrequente pulsen30.
De basisprincipes van het NSE-proces kunnen worden samengevat in een paar eenvoudige stappen 6,11 met behulp van figuur 1. (1) De neutronenbundel geproduceerd door de bron (positie 1) is gepolariseerd (positie 2), geleid en getransporteerd (positie 3) en komt aan bij de ingang van de NSE-spectrometer, waar deze 90° wordt gedraaid door de eerste pi-halve flipper (positie 4). (2) De gepolariseerde bundel (bijv. magnetische neutronenmomenten) wordt loodrecht op de magnetische veldlijnen van de eerste magneet (eerste precessiezone, positie 5) en begint te precesseren. (3) Aan het einde van de magneet accumuleren neutronenspins een bepaalde precessiehoek die evenredig is met de magnetische veldsterkte en de tijd van de vlucht die erin wordt doorgebracht (in principe omgekeerd evenredig met de neutronensnelheid). De individuele neutronensnelheden worden gecodeerd binnen hun precessiehoek aan het einde van de eerste precessiezone. (4) Dicht bij de monsterpositie keert de pi-flipper (positie 6) de oriëntatie van de spin met 180° om, waardoor het teken van de precessiehoek verandert. (5) De neutronen interageren met de moleculen van het monster (positie 7) en raken verstrooid. (6) De verstrooide neutronen komen binnen en precesseren in de tweede precessiezone (positie 8), maar worden omgekeerd georiënteerd. (7) Een andere pi-halve flipper (positie 9) wordt gebruikt om de oriëntatie van de spin loodrecht op de horizontale richting te draaien. Dit zal de precessie stoppen, waardoor de precessiehoek φ wordt vertaald in polarisatie evenredig met cos(φ). (8) De analysator (positie 10) selecteert de neutronen op basis van één oriëntatie. Als de interactie met het monster elastisch is, zal de snelheid van het neutron niet veranderen. De neutronen zullen een identieke hoeveelheid tijd doorbrengen met vliegen in de eerste en tweede precessiezones en de geaccumuleerde precessiehoeken zijn volledig hersteld. De volledige polarisatie wordt hersteld op de detector (positie 11) als een echo van de oorspronkelijke polarisatie (d.w.z. spin-echo). (9) In NSE is de verstrooiing echter quasi-elastisch, zodat een kleine energie-uitwisseling tussen neutronen en monstermoleculen leidt tot verschillende neutronensnelheden na verstrooiing door het monster. Door de verschillende snelheden zullen de neutronen een extra tijd door de tweede precessiezone vliegen en hun precessiehoek niet goed hebben hersteld. Een gedeeltelijke polarisatie wordt op de detector opgehaald en het verlies van polarisatie als gevolg van spinrelaxatie is evenredig met de cos-Fourier-transformatie van de spectrale functie S(Q, ω), de tussenliggende verstrooiingsfunctie F(Q, t). (10) De tijdparameter van de functie F(Q, t) is evenredig met de magnetische veldsterkte van de precessie. Het scannen van het verlies van polarisatie als functie van de magnetische veldsterkte levert daarom een ontspanningsfunctie op die afhankelijk is van de dynamische processen in het monster.

Figuur 1: Foto van de NSE spectrometer bij SNS (SNS-NSE) en neutronenvliegpad schematisch met de belangrijkste functionele componenten. Van rechts naar links: 1 = neutronenbron; 2 = choppers-bender-polarisator-secundair sluitersysteem; 3 = balktransportgeleiders; 4 = pi/2 flipper voor de eerste 90° spin-turn; 5 = eerste precessiezone; 6 = pi flipper voor 180° spin-turn; 7 = monstergebied en monsteromgeving (hier wordt de cryo-oven getoond); 8 = tweede precessiezone; 9 = pi/2 flipper voor tweede 90° spin-turn; 10 = analyser; 11 = detector. (Merk op dat delen van 3, evenals 2 en 1, zich achter de blauwe muur binnen de afscherming bevinden; de choppers worden vervangen door een snelheidskeuzeschakelaar voor reactorgebaseerde NSE). Klik hier om een grotere versie van deze figuur te bekijken.
Protocol
Representative Results
Discussion
NSE-spectroscopie levert een uniek en gedetailleerd beeld van de dynamiek van eiwitten, die andere spectroscopische technieken niet kunnen produceren. Metingen over een uitgebreide tijdschaal bieden waarnemingen van zowel de translationele als de rotatiediffusie van de eiwitten, zoals hier gepresenteerd. De segmentale dynamica en andere interne oscillaties openbaren zich als een sterk verval van de coherente verstrooiingsfunctie S(Q, t) op een korte tijdschaal en zijn goed gescheiden van de algehele diffusionale…
Declarações
The authors have nothing to disclose.
Acknowledgements
Dit onderzoek gebruikte middelen bij de Spallation Neutron Source (BL-15, BL-6, Biology and Chemistry labs), een DOE Office of the Science User Facility beheerd door het Oak Ridge National Laboratory. Dit onderzoek maakte ook gebruik van middelen in de MLZ-FRM2-reactor Garching (KWS-2, Phoenix-J-NSE) en de JCNS1 in Forschungszentrum Jülich GmbH, Duitsland. De auteur erkent Dr. Ralf Biehl en Dr. Andreas Stadler voor hun hulp bij het modelleren en hun bijdrage aan zowel IgG- als MBP-eiwitonderzoek, Dr. Piotr A. Żołnierczuk voor ondersteuning van NSE-gegevensreductie, Dr. Changwoo Do voor ondersteuning met SANS-metingen en Rhonda Moody en Dr. Kevin Weiss voor SNS biochemische laboratoriumondersteuning.
Materials
| Bovine MBP protein solution | Sigma-Aldrich | M1891 | lyophilized powder reconstituted in D2O |
| D2O – heavy water | Sigma-Aldrich | Product No. 151882 | liquid |
| Dionized water | in house | – | for washing / cleanning cells |
| DLS instrument | Zetasizer Nano ZS, FZ-Jülich | – | dynamic light scattering instrument |
| Elastic scattering standards | SNS-NSE, ORNL | – | Al2O3 and Graphite powders |
| Ethanol | Sigma-Aldrich | 65350-M | 70% ethanol for cleaning cells |
| IgG protein solution | Sigma-Aldrich | I4506 | lyophilized powder reconstituted in D2O |
| KWS-2 instrument | JCNS outstation at the MLZ, Garching, Germany | – | small angle neutron instrument |
| Liquinox dish detergent | Alconox | – | Phosphate-free liquid lab glassware cleaner |
| Na2HPO4·7H2O | Sigma-Aldrich | Product No.S9390 | disodium phosphate heptahydrate salt |
| NaCl | Sigma-Aldrich | Product No.S9888 | sodium chloride salt |
| NaH2PO4·H2O | Sigma-Aldrich | Product No. S9638 | monosodium phosphate monohydrate salt |
| Nanodrop spectrophotometer | Thermo Scientific | Catalog number: ND-2000 | NanoDrop 2000/2000c Spectrophotometer |
| Neutron alignment camera | NeutronOptics, Grenoble | NOG210222 | 100 x 100 mm camera with Sony IMX249 CMOS sensor |
| Parafilm M – wax parafilm | Bemis | Parafilm M – 5259-04LC PM996 | all-purpose laboratory film in cardboard dispenser |
| Phoenix-J-NSE Spectrometer | JCNS outstation at the MLZ, Garching, Germany | – | neutron spectrometer |
| SasView | https://www.sasview.org/ | ||
| SAXSpace, Anton Paar instrument | FZ-Jülich | – | small angle x-ray instrument |
| Slide-A-Lyzer dialysis membranes | Thermo Scientific | 88400-88405 | Slide-A-Lyzer mini dialysis devices tubes of 3.5 K MWCO |
| SNS Remote Analysis Cluster | Neutron Science Remote Analysis (sns.gov) | https://analysis.sns.gov | |
| SNS-NSE spectrometer | ORNL, Oak Ridge, TN, USA | – | neutron spectrometer |
| Sterile syringe filters | VWR | N.A. PN:28145-501 | 0.2 µm pore size filters |
| Temperature Forcing System (TFS) | SP Scientific | Part Number 100004055 | sample environment equipment |
| Urea -d4 | Sigma-Aldrich | Product No. 176087 | deuterated Urea salt |
| Viscometer | FZ-Jülich | – | falling ball viscometer |
Referências
- Fitter, J., Gutberlet, T., Katsaras, J. . Neutron Scattering in Biology: Techniques and Applications. , (2006).
- Stadler, A., Monkenbusch, M., Biehl, R., Richter, D., Ollivier, J. Neutron spin-echo and TOF reveals protein dynamics in solution. Journal of the Physical Society of Japan. 82, (2013).
- Inoue, R. Large domain fluctuations on 50-ns timescale enable catalytic activity in phosphoglycerate kinase. Biophysical Journal. 99 (7), 2309-2317 (2010).
- Callaway, D. J. E., et al. Controllable activation of nanoscale dynamics in a disordered protein alters binding kinetics. Journal of Molecular Biology. 429 (7), 987-998 (2017).
- Stingaciu, L. R., Biehl, R., Changwoo, D., Richter, D., Stadler, A. M. Reduced internal friction by osmolyte interaction in intrinsically disordered myelin basic protein. Journal of Physical Chemistry Letters. 11 (1), 292-296 (2020).
- Monkenbusch, M., Richter, D. High resolution neutron spectroscopy-a tool for the investigation of dynamics of polymers and soft matter. Comptes Rendus Physique. , (2007).
- Richter, D., Monkenbusch, M., Schwahn, D. Neutron Scattering. Polymer Science: A Comprehensive Reference, 10 Volume Set. , (2012).
- Wilson, C. C. . Single Crystal Neutron Diffraction From Molecular Materials. , (2000).
- Marshall, W. . Theory of thermal neutron scattering. , (1971).
- . Roger Pynn Introduction & Neutron Scattering "Theory" Available from: https://neutrons.ornl.gov/sites/default/files/intro_to_neutron_scattering.pdf (2004)
- Richter, D. Neutron scattering in polymer physics. Physica B: Condensed Matter. 276-278, 22-29 (2000).
- Harroun, T. A., Wignall, G. D., Katsaras, J. Neutron scattering for biology. Neutron Scattering in Biology. , (2006).
- . SNS Available from: https://neutrons.ornl.gov/sna (2020)
- . HFIR Available from: https://neutrons.ornl.gov/hfir (2020)
- . CNCS Available from: https://neutrons.ornl.gov/cncs (2020)
- Perticaroli, S., et al. Description of hydration water in protein (green fluorescent protein) solution. Journal of the American Chemical Society. 139 (3), 1098-1105 (2017).
- Perticaroli, S., Nickels, J. D., Ehlers, G., Sokolov, A. P. Rigidity, secondary structure, and the universality of the boson peak in proteins. Biophysical Journal. 106 (12), 2667-2674 (2014).
- Miao, Y., et al. Coupled flexibility change in cytochrome p450cam substrate binding determined by neutron scattering, NMR, and molecular dynamics simulation. Biophysical Journal. 103 (10), 2167-2176 (2012).
- Mamontov, E., Zamponi, M., Hammons, S., Keener, W. S., Hagen, M., Herwig, K. W. BASIS: A new backscattering spectrometer at the SNS. Neutron News. 19 (3), 22-24 (2008).
- Mamontov, E. Microscopic diffusion processes measured in living planarians. Scientific Reports. 9, 8708 (2018).
- Alpert, Y., Cser, L., Faragó, B., Franěk, F., Mezei, F., Ostanevich, Y. M. Segmental flexibility in pig immunoglobulin G studied by neutron spin-echo technique. Biopolymers. 24 (9), 1769-1784 (1985).
- Bu, Z., Biehl, R., Monkenbusch, M., Richter, D., Callaway, D. J. E. Coupled protein domain motion in Taq polymerase revealed by neutron spin-echo spectroscopy. Proceedings of the National Academy of Sciences of the United States of America. 102 (49), 17646-17651 (2005).
- Biehl, R., et al. Direct observation of correlated interdomain motion in alcohol dehydrogenase. Physical Review Letters. 101, 138102 (2008).
- Farago, B., Li, J., Cornilescu, G., Callaway, D. J. E., Bu, Z. Activation of nanoscale allosteric protein domain motion revealed by neutron spin echo spectroscopy. Biophysical Journal. 99 (10), 3473-3482 (2010).
- Bu, Z., Callaway, D. J. E. Dynamic propagation of long-range allosteric signals by nanoscale protein domain motion revealed by neutron spin echo spectroscopy. Biophysical Journal. 100 (3), 223 (2011).
- Hong, L., et al. Structure and dynamics of a compact state of a multidomain protein, the mercuric ion reductase. Biophysical Journal. 107 (2), 393-400 (2014).
- Longeville, S., Stingaciu, L. -. R. Hemoglobin diffusion and the dynamics of oxygen capture by red blood cells. Scientific Reports. 7, 10448 (2017).
- Stingaciu, L. R., Ivanova, O., Ohl, M., Biehl, R., Richter, D. Fast antibody fragment motion: Flexible linkers act as entropic spring. Scientific Reports. 6, 22148 (2016).
- Hahn, E. L. Nuclear induction due to free larmor precession. Physical Review. 77, 297 (1950).
- Hahn, E. L. Spin echoes. Physical Review. 80, 580 (1950).
- Svergun, D. I., Koch, M. H. J. Small-angle scattering studies of biological macromolecules in solution. Reports on Progress in Physics. 66 (10), 1735-1782 (2003).
- . Sasview Available from: https://www.sasview.org (2020)
- Zhao, J. K., Gao, C. Y., Liu, D. The extended Q-range small-angle neutron scattering diffractometer at the SNS. Journal of Applied Crystallography. 43, 1068-1077 (2010).
- Ohl, M., et al. The high-resolution neutron spin-echo spectrometer for the SNS with τ ≥ 1 µs. Physica B: Condensed Matter. 350, 147-150 (2004).
- . SNS-NSE web page Available from: https://neutrons.ornl.gov/nse (2022)
- Ohl, M., et al. The spin-echo spectrometer at the Spallation Neutron Source (SNS). Nuclear Instruments and Methods in Physics Research, Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 696, 85-99 (2012).
- Zolnierczuk, P. A., Holderer, O., Pasini, S., Kozielewski, T., Stingaciu, L. R., Monkenbusch, M. Efficient data extraction from neutron time-of-flight spin-echo raw data. Journal of Applied Crystallography. 52 (5), 1022-1034 (2019).
- . Dr Spine hub Available from: https://jugit.fz-juelich.de/nse/drspine (2022)
- Stadler, A. M., et al. Internal nanosecond dynamics in the intrinsically disordered myelin basic protein. Journal of the American Chemical Society. 136 (19), (2014).
- . FZJ Available from: https://www.fz-juelich.de/portal/EN/AboutUs (2022)
- . KWS2 Available from: https://miz-garching.de/kws-2 (2022)
- Moorhouse, M., Barry, P. The protein databank. Bioinformatics Biocomputing and Perl. , (2005).
- Tria, G., Mertens, H. D. T., Kachala, M., Svergun, D. I. Advanced ensemble modelling of flexible macromolecules using X-ray solution scattering. IUCrJ. 2 (2), 207-217 (2015).
- Holderer, O., Monkenbusch, M., Schätzler, R., Kleines, H., Westerhausen, W., Richter, D. The JCNS neutron spin-echo spectrometer J-NSE at the FRM II. Measurement Science and Technology. 90 (4), 043107 (2008).
- Biehl, R., Monkenbusch, M., Richter, D. Exploring internal protein dynamics by neutron spin echo spectroscopy. Soft Matter. 7 (4), 1299-1307 (2011).
- Stingaciu, L. R., Ivanova, O., Ohl, M., Biehl, R., Richter, D. Fast antibody fragment motion: Flexible linkers act as entropic spring. Scientific Reports. 6, 22148 (2016).
- Stadler, A. M., et al. Internal nanosecond dynamics in the intrinsically disordered myelin basic protein. Journal of the American Chemical Society. 136 (19), 6987-6994 (2014).
- Biehl, R., Richter, D. Slow internal protein dynamics in solution. Journal of Physics: Condensed Matter. 26 (50), 503103 (2014).
- Hinsen, K. The molecular modeling toolkit: A new approach to molecular simulations. Journal of Computational Chemistry. 21 (2), 79-85 (2000).
- Uhlenbeck, G. E., Ornstein, L. S. On the theory of the Brownian motion. Physical Review. 36 (5), 823 (1930).
- Wang, M. C., Uhlenbeck, G. E. On the theory of the Brownian motion II. Reviews of Modern Physics. 17, 323 (1945).
- Callaway, D. J. E., Bu, Z. Nanoscale protein domain motion and long-range allostery in signaling proteins-a view from neutron spin echo spectroscopy. Biophysical Reviews. 7 (2), 165-174 (2015).
- Liu, Y. Intermediate scattering function for macromolecules in solution probed by neutron spin echo. Physical Review E. 95, 020501 (2017).
- Liu, Y. Short-time dynamics of proteins in solutions studied by neutron spin echo. Current Opinion in Colloid & Interface Science. 42, 147-156 (2019).

