In vitro time-lapse live-cell imaging om celmigratie naar het orgaan van Corti te verkennen
Summary
In deze studie presenteren we een real-time beeldvormingsmethode met confocale microscopie om cellen te observeren die naar beschadigd weefsel bewegen door ex vivo incubatie met het cochleaire epitheel dat het orgaan van Corti bevat.
Abstract
Om de effecten van mesenchymale stamcellen (MSC’s) op celregeneratie en -behandeling te bestuderen, volgt deze methode MSC-migratie en morfologische veranderingen na co-cultuur met cochleair epitheel. Het orgaan van Corti werd geïmmobiliseerd op een plastic deklip door een deel van het membraan van de Reissner te drukken dat tijdens de dissectie werd gegenereerd. MSC’s die door een glazen cilinder werden opgesloten, migreerden naar cochleair epitheel toen de cilinder werd verwijderd. Hun overheersende lokalisatie werd waargenomen in de modiolus van het orgaan van Corti, uitgelijnd in een richting die vergelijkbaar is met die van de zenuwvezels. Sommige MSC’s werden echter gelokaliseerd in het limbusgebied en vertoonden een horizontaal langwerpige vorm. Bovendien werd de migratie naar het haarcelgebied verhoogd en veranderde de morfologie van de MSC’s in verschillende vormen na de behandeling met kanamycine. Concluderend geven de resultaten van deze studie aan dat de cocultuur van MSC’s met cochleair epitheel nuttig zal zijn voor de ontwikkeling van therapieën via celtransplantatie en voor studies naar celregeneratie die verschillende aandoeningen en factoren kunnen onderzoeken.
Introduction
Gehoorverlies kan aangeboren optreden of kan geleidelijk worden veroorzaakt door verschillende factoren, waaronder veroudering, medicijnen en lawaai. Gehoorverlies is vaak moeilijk te behandelen omdat het zeer uitdagend is om een verminderde functie te herstellen zodra de haarcellen die verantwoordelijk zijn voor het gehoor zijn beschadigd1. Volgens de Wereldgezondheidsorganisatie hebben naar schatting 461 miljoen mensen wereldwijd gehoorverlies, wat verantwoordelijk is voor 6,1% van de wereldbevolking. Van degenen met gehoorverlies is 93% volwassen en 7% kinderen.
Er is geprobeerd gehoorverlies te behandelen; met name een regeneratiebenadering met behulp van MSC’s is een veelbelovende behandeling gebleken. Wanneer weefsel beschadigd is, worden MSC’s van nature vrijgegeven in de bloedsomloop en migreren ze naar de plaats van verwondingen waar ze verschillende moleculen afscheiden om een micromilieu te vormen dat regeneratiebevordert 2. Daarom is het belangrijk om een methode te ontwikkelen om beschadigde weefsels te behandelen door de migratie van extern geïmplanteerde MSC’s om organen te targeten en hun daaropvolgende afscheiding van moleculen die krachtige immuunregulatie, angiogenese en anti-apoptose veroorzaken om het herstel van beschadigde celfunctie3,4,5te verbeteren .
Het homing-proces waarbij MSC’s migreren naar beschadigde weefsels kan het belangrijkste obstakel zijn om te overwinnen. MSC ‘s hebben een systemisch homingmechanisme met opeenvolgende stappen van tethering/rolling, activering, arrestatie, transmigratie/diapedese en migratie6,7,8. Momenteel worden er inspanningen geleverd om manieren te vinden om deze stappen te verbeteren. Verschillende strategieën, waaronder genetische modificatie, celoppervlaktechniek, in vitro priming en magnetische geleiding, zijn getest6,7. Daarnaast zijn verschillende pogingen gedaan om de bescherming en regeneratie van auditieve haarcellen te bevorderen door MSC’s naar de plaats van beschadigd slakkenhuis te brengen. Het volgen van MSC’s in vivo is echter tijdrovend en arbeidsintensief en vereist zeer gespecialiseerde vaardigheden9.
Om dit probleem op te lossen, werd een methode ontwikkeld om de homing van MSC’s in het slakkenhuis te observeren door middel van time-lapse confocale microscopie die de migratie van cellen gedurende meerdere uren fotografeert (Figuur 1). Het werd ontwikkeld in het begin van de 20e eeuw en is onlangs uitgegroeid tot een krachtig hulpmiddel voor het bestuderen van migratie van specifieke cellen.
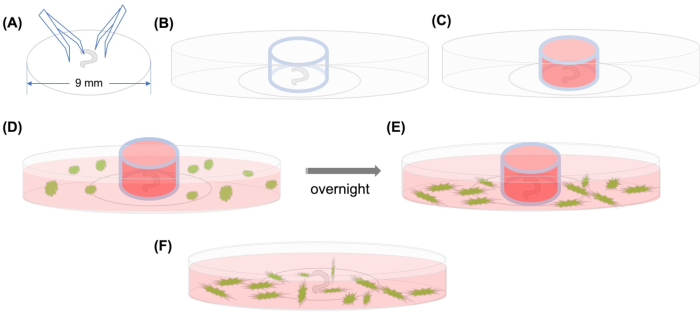
Figuur 1: Grafische samenvatting. (A) Nadat het ontlede orgaan van Corti met behulp van een tang op een plastic afdeklip is gehecht, wordt de afdeklip op een confocale microscopische schaal met glazen bodem van 35 mm geplaatst en (B) de glazen cilinder is geplaatst. (C) Na het vullen van de binnenkant van de glazen cilinder met medium, (D) GFP-gelabelde MSC’s met medium worden zorgvuldig toegevoegd buiten de cilinder. (E) Na incubatie ‘s nachts, (F) wordt de glazen cilinder verwijderd en worden beelden gemaakt met een confocale microscoop. Afkortingen: GFP = groen fluorescerend eiwit; MSC’s = mesenchymale stamcellen. Klik hier om een grotere versie van deze afbeelding te bekijken.
Protocol
Representative Results
Discussion
Transplantatie van MSC’s naar beschadigde locaties om de regeneratie van beschadigde cellen te bevorderen is uitgebreid bestudeerd en het therapeutische effect is duidelijk. De transplantatie en daaropvolgende differentiatie van MSC’s zijn gemeld om het gehoor te herstellen bij ratten met gehoorverlies veroorzaakt door 3-nitropropioninezuur13. Hoewel Lee c.s. MSC’s trans-veneus op mensen toepasten, bereikten zij geen significante verbetering in het gehoor14. Tot voor kort w…
Declarações
The authors have nothing to disclose.
Acknowledgements
Dit werk werd ondersteund door onderzoeksbeurzen (NRF-2018-R1D1A1B07050175, HURF-2017-66) van de National Research Foundation (NRF) of Korea en Hallym University Research Fund.
Materials
| 10X PBS Buffer | GenDEPOT | P2100-104 | |
| 4% Formalin | T&I | BPP-9004 | |
| Ampicillin | sigma | A5354-10ml | |
| BSA | sigma | A4503-100G | |
| confocal dish | SPL | 200350 | |
| confocal microscope | ZEISS | LSM800 | |
| coverslip | SPL | 20009 | |
| DMEM/F12 | Gibco | 10565-018 | |
| Fetal Bovine Serum | Thermo Fisher scientific | 16140071 | |
| Fluorsheild with DAPI | sigma | F6057 | |
| Forcep | Dumont | 0508-L5-P0 | |
| HBSS | Thermo Fisher scientific | 14065056 | |
| HEPES | Thermo Fisher scientific | 15630080 | |
| N2 supplement | Gibco | 17502-048 | |
| Phalloidin-iFluor 647 Reagent | abcam | ab176759 | |
| Stage Top Incubator | TOKAI HIT | WELSX | |
| Strain C57BL/6 mouse messenchymal stem cells with GFP | cyagen | MUBMX-01101 | |
| Triton X-100 | sigma | T8787 |
Referências
- Brown, C. S., Emmett, S. D., Robler, S. K., Tucci, D. L. Global hearing loss prevention. Otolaryngologic Clinics of North America. 51 (3), 575-592 (2018).
- Chamberlain, G., Fox, J., Ashton, B., Middleton, J. Concise review: mesenchymal stem cells: their phenotype, differentiation capacity, immunological features, and potential for homing. Stem Cells. 25 (11), 2739-2749 (2007).
- Fu, X., et al. Mesenchymal stem cell migration and tissue repair. Cells. 8 (8), (2019).
- Uder, C., Brückner, S., Winkler, S., Tautenhahn, H. M., Christ, B. Mammalian MSC from selected species: Features and applications. Cytometry A. 93 (1), 32-49 (2018).
- Rojewski, M. T., et al. Translation of a standardized manufacturing protocol for mesenchymal stromal cells: A systematic comparison of validation and manufacturing data. Cytotherapy. 21 (4), 468-482 (2019).
- Ullah, M., Liu, D. D., Thakor, A. S. Mesenchymal stromal cell homing: Mechanisms and strategies for improvement. iScience. 15, 421-438 (2019).
- Ahn, Y. J., et al. Strategies to enhance efficacy of SPION-labeled stem cell homing by magnetic attraction: a systemic review with meta-analysis. International Journal of Nanomedicine. 14, 4849-4866 (2019).
- Alon, R., Ley, K. Cells on the run: shear-regulated integrin activation in leukocyte rolling and arrest on endothelial cells. Current Opinion in Cell Biology. 20 (5), 525-532 (2008).
- Sykova, E., Jendelova, P. In vivo tracking of stem cells in brain and spinal cord injury. Progress in Brain Research. 161, 367-383 (2007).
- Landegger, L. D., Dilwali, S., Stankovic, K. M. Neonatal murine cochlear explant technique as an in vitro screening tool in hearing research. Journal of Visualized Experiments. (124), e55704 (2017).
- Pijuan, J., et al. In vitro cell migration, invasion, and adhesion assays: From cell imaging to data analysis. Frontiers in Cell and Developmental Biology. 7, 107 (2019).
- Rask-Andersen, H., et al. Human cochlea: anatomical characteristics and their relevance for cochlear implantation. The Anatomical Record. 295 (11), 1791-1811 (2012).
- Kamiya, K., et al. Mesenchymal stem cell transplantation accelerates hearing recovery through the repair of injured cochlear fibrocytes. The American Journal of Pathology. 171 (1), 214-226 (2007).
- Lee, H. S., Kim, W. J., Gong, J. S., Park, K. H. Clinical safety and efficacy of autologous bone marrow-derived mesenchymal stem cell transplantation in sensorineural hearing loss patients. Journal of Audiology and Otology. 22 (2), 105-109 (2018).
- Vanden Berg-Foels, W. S. In situ tissue regeneration: chemoattractants for endogenous stem cell recruitment. Tissue Engineering Part B: Reviews. 20 (1), 28-39 (2014).
- Parker, M., Brugeaud, A., Edge, A. S. Primary culture and plasmid electroporation of the murine organ of Corti. Journal of Visualized Experiments. (36), e1685 (2010).
- Ogier, J. M., Burt, R. A., Drury, H. R., Lim, R., Nayagam, B. A. Organotypic culture of neonatal murine inner ear explants. Frontiers in Cellular Neuroscience. 13, 170 (2019).
- Oshima, K., et al. Mechanosensitive hair cell-like cells from embryonic and induced pluripotent stem cells. Cell. 141 (4), 704-716 (2010).

