Werkzeuge zur Echtzeitbewertung eines Pseudomonas aeruginosa-Infektionsmodells
Summary
Synthetisches Mukoviszidose-Sputummedium (SCFM2) kann in Kombination mit konfokaler Laserscanning-Mikroskopie und fluoreszenzaktivierter Zellsortierung verwendet werden, um bakterielle Aggregate mit hoher Auflösung zu beobachten. Dieser Artikel beschreibt Methoden zur Bewertung aggregierter Populationen während der antimikrobiellen Behandlung als Plattform für zukünftige Studien.
Abstract
Pseudomonas aeruginosa (Pa) ist einer der häufigsten opportunistischen Erreger im Zusammenhang mit Mukoviszidose (CF). Sobald die Pa-Besiedlung etabliert ist, bildet ein großer Teil der infizierenden Bakterien Biofilme im Atemwegssputum. Pa-Biofilme, die aus CF-Sputum isoliert wurden, wachsen nachweislich in kleinen, dichten Aggregaten von ~ 10-1.000 Zellen, die räumlich organisiert sind und klinisch relevante Phänotypen wie antimikrobielle Toleranz aufweisen. Eine der größten Herausforderungen bei der Untersuchung, wie Pa-Aggregate auf die sich verändernde Sputumumgebung reagieren, ist das Fehlen ernährungsrelevanter und robuster Systeme, die die Aggregatbildung fördern. Mit einem synthetischen CF-Sputummedium (SCFM2) kann die Lebensgeschichte von Pa-Aggregaten mittels konfokaler Laserscanning-Mikroskopie (CLSM) und Bildanalyse mit der Auflösung einer einzelnen Zelle beobachtet werden. Dieses In-vitro-System ermöglicht die Beobachtung von Tausenden von Aggregaten unterschiedlicher Größe in Echtzeit, drei Dimensionen und im Mikrometerbereich. Auf Individueller und Populationsebene ermöglicht die Fähigkeit, Aggregate nach Phänotyp und Position zu gruppieren, die Beobachtung von Aggregaten in verschiedenen Entwicklungsstadien und deren Reaktion auf Veränderungen in der Mikroumgebung, wie z.B. Antibiotikabehandlung, präzise zu differenzieren.
Introduction
Pseudomonas aeruginosa (Pa) ist ein opportunistischer Erreger, der chronische Infektionen bei immungeschwächten Personen hervorruft. Bei Menschen mit der Erbkrankheit Mukoviszidose (CF) können diese Infektionen den Verlauf eines Lebens umfassen. CF verursacht den Aufbau eines viskosen, nährstoffreichen Auswurfs in den Atemwegen, der im Laufe der Zeit von einer Vielzahl mikrobieller Krankheitserreger besiedelt wird. Pa ist einer der häufigsten CF-Erreger, der die Atemwege in der frühen Kindheit besiedelt und schwer zu behandelnde Infektionen etabliert1. Pa bleibt ein signifikantes klinisches Problem und gilt als eine der häufigsten Todesursachen bei Menschen mit CF, trotz verbesserter Therapieschemata in den letzten Jahren2,3. Dieser Persistenzphänotyp und die zunehmende Antibiotikatoleranz haben Pa einen Platz in einer Gruppe von Krankheitserregern eingebracht, die sowohl von den Centers for Disease Control (CDC) als auch von der Weltgesundheitsorganisation (WHO) als Forschungsprioritäten für die Entwicklung neuer therapeutischer Strategien identifiziert wurden – die ESKAPE-Erreger4.
Wie bei anderen ESKAPE-Erregern ist die erworbene Antibiotikaresistenz bei Paüblich, aber es gibt auch viele intrinsische Eigenschaften, die zur antimikrobiellen Toleranz von Pa beitragen. Dazu gehört die Fähigkeit von Pa, Aggregate zu bilden – hochdichte Cluster von ~ 10-1.000 Zellen, die bei mehreren Infektionen beobachtet werden können, einschließlich CF-Patienten-Sputum5,6. Ähnlich wie Pa, das in anderen Biofilmsystemen untersucht wurde, zeigen Pa-Aggregate klinisch relevante Phänotypen wie erhöhte Antibiotikaresistenz und Aktivierung der Zell-Zell-Kommunikation (Quorum Sensing (QS)). Zum Beispiel wurde gezeigt, dass Aggregate von Pa QS-reguliertes Verhalten verwenden, um andere Mikroben zu bekämpfen und antimikrobielle Behandlungen wie die Produktion von Pyocyanin7zu tolerieren. Die Fähigkeit, solche Verhaltensweisen zu untersuchen, bietet einen spannenden Einblick in bakterielle Ökosysteme in einer Umgebung, die derjenigen ähnelt, in der sie im menschlichen Körper vorkommen.
Eine der größten Herausforderungen bei der Untersuchung, wie Pa-Aggregate auf die sich verändernde Sputumumgebung reagieren, ist das Fehlen ernährungsrelevanter und robuster Systeme, die die Aggregatbildung fördern. Vieles von dem, was über Pa bekannt ist, wurde mit In-vitro-Systemen entdeckt, in denen Zellen planktonisch oder in einer charakteristischen oberflächengebundenen “Pilz”-Architektur wachsen, die in vivo8nicht beobachtet wurde. Während klassische Biofilm-Wachstumsmodelle wie Flusszellen oder fester Agar umfangreiches und wertvolles Wissen über bakterielles Verhalten und Mechanismen der Antibiotikatoleranz gewonnen haben, lassen sich diese Ergebnisse nicht immer in vivo übersetzen. Viele In-vitro-Modelle haben eine begrenzte Fähigkeit, die Wachstumsumgebung der menschlichen Infektionsstelle nachzuahmen, was kostspielige In-vivo-Studien erfordert. Im Gegenzug fehlt vielen In-vivo-Modellen die Flexibilität und Auflösung, die In-vitro-Techniken bieten.
Synthetischer Mukoviszidose-Sputum (SCFM2) wurde entwickelt, um eine Umgebung für das Pa-Wachstum zu schaffen, die der bei chronischen Infektionen in der CF-Lunge ähnelt. SCFM2 umfasst Nährstoffquellen, die in schleimlöserter CF-Sputa zusätzlich zu Mucin, Lipiden und DNA identifiziert wurden. Das Pa-Wachstum in SCFM2 erfordert ein nahezu identisches Gen, das für das Wachstum im tatsächlichen Sputum erforderlich ist, und unterstützt die natürlichePa-Aggregatbildung 9,10. Nach der Impfung bilden planktonische Zellen Aggregate, die durch Expansion an Größe zunehmen. Einzelne Zellen (als Migranten bezeichnet) werden aus Aggregaten freigesetzt, wandern in unbesilumisierte Gebiete und bilden neue Aggregate10. Diese Lebensgeschichte kann mittels CLSM und Bildanalyse bei der Auflösung einer einzelnen Zelle beobachtet werden. Die in SCFM2 gebildeten Pa-Aggregate sind ähnlich groß wie die in der CF-Lunge10beobachteten. Dieses Modell ermöglicht die Beobachtung mehrerer Aggregate unterschiedlicher Größe in Echtzeit und in drei Dimensionen im Mikrometerbereich. Die Zeitraffermikroskopie ermöglicht die Verfolgung von Tausenden (~ 50.000) aggregaten in einem Experiment. Die Verwendung von Bildanalysesoftware ermöglicht die Quantifizierung von aggregierten Phänotypen aus Mikroaufnahmen, einschließlich Aggregatvolumen, Oberfläche und Position in drei Dimensionen auf die nächsten 0,1 μm, sowohl auf der Ebene des einzelnen Aggregats als auch der Population. Die Fähigkeit, Aggregate nach Phänotyp und Position zu gruppieren, ermöglicht die präzise Differenzierung von Aggregaten in verschiedenen Entwicklungsstadien sowie ihre Reaktion auf eine sich verändernde Mikroumgebung6,11.
Die Anwendung von SCFM2 zur Untersuchung von Pa-Aggregaten in Assays mit geringem Volumen und hohem Durchsatz macht es zu einem flexiblen, kostengünstigen Modell. Als definiertes Medium bietet SCFM2 Einheitlichkeit und Reproduzierbarkeit über mehrere Plattformen hinweg und bietet eine ernährungsphysiologisch und physikalisch relevante Methode zur Untersuchung von Pa-Aggregaten in vitro9. Zu den Anwendungen gehört die Verwendung in Kombination mit CLSM zur Beobachtung der räumlichen Organisation und antibiotikatoleranz bei hoher Auflösung (wie in diesem Methodenpapier beschrieben). Die Fähigkeit, Experimente durchzuführen, die Echtzeitdaten im Mikrometerbereich liefern, ermöglicht die Untersuchung von Interaktionen innerhalb und zwischen Spezies, wie sie in vivoauftreten können. Zum Beispiel wurde SCFM2 zuvor verwendet, um die räumliche Dynamik der Zell-Zell-Kommunikation in aggregierten Populationen über ein Netzwerk von Systemen zu untersuchen, die von Pa verwendet werden, um mehrere Gene zu regulieren, die zur Virulenz und Pathogenese beitragen6.
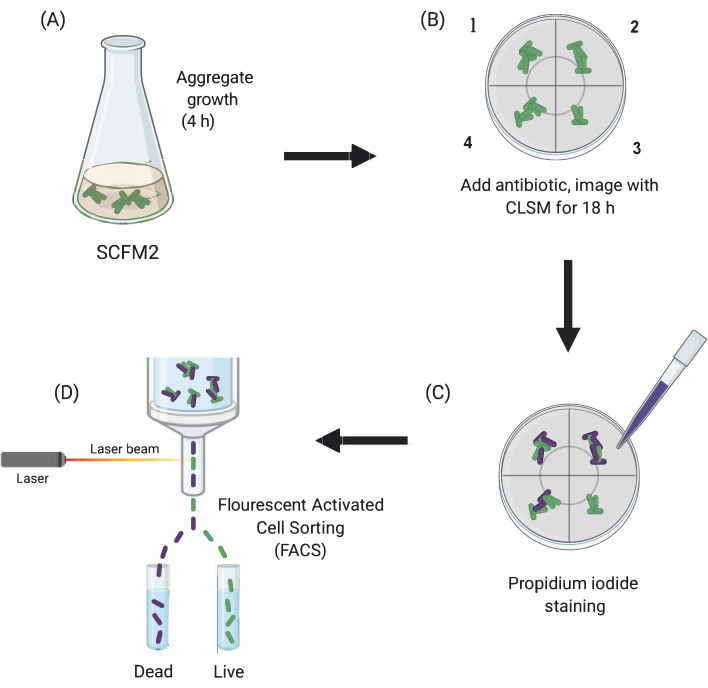
Abbildung 1: Grafische Darstellung der wichtigsten experimentellen Schritte. (A) SCFM2 wird mit Pa-Zellen geimpft und darf in einer Kulturschale mit Glasboden Aggregate bilden. (B) Aggregate werden auf das konfokale Mikroskop übertragen und Antibiotika hinzugefügt. Dargestellt sind drei technische Replikate (Kammern 1-3) und eine Kontrollbohrung (4) von geimpften SCFM2 ohne antibiotikafreie Behandlung. Aggregate werden mit CLSM im Laufe von 18 h abgebildet. (C) Nach der ersten 18-h-Bildgebung werden Aggregate mit Propidieniodid behandelt, um tote Zellen zu visualisieren, und mit CLSM abgebildet (D) Aggregate mit gewünschtem Phänotyp werden mitHILFE VON FACS von SCFM2 getrennt. Abkürzungen: SCFM2 = synthetisches Mukoviszidose-Sputummedium; Pa = Pseudomonas aeruginosa; CLSM = konfokale Laserscanning-Mikroskopie; FACS = fluoreszenzaktivierte Zellsortierung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Hier wird der Nutzen von SCFM2 zur Untersuchung der Auswirkungen der Antibiotikabehandlung auf Pa-Aggregate in Echtzeit demonstriert, gefolgt von der Verwendung eines Zellsortierungsansatzes zur Isolierung von Populationen von Aggregaten mit unterschiedlichen Phänotypen für die nachgelagerte Analyse (Abbildung 1).
Protocol
Representative Results
Discussion
Diese Arbeit hat Methoden eingeführt, die kombiniert werden können, um bakterielle Aggregatpopulationen in Gegenwart und Abwesenheit von Antibiotikabehandlung zu untersuchen. Hochauflösendes CLSM ermöglicht die Visualisierung von Veränderungen der aggregierten Biomasse und der strukturellen Orientierung von Aggregaten in Echtzeit, wenn sie Antibiotika ausgesetzt sind. Darüber hinaus können physikalische und strukturelle Merkmale der Biomasse, die nach der Behandlung mit Antibiotika übrig bleiben, quantifiziert we…
Declarações
The authors have nothing to disclose.
Acknowledgements
S.E.D wird durch Start-up-Fonds des Department of Molecular Medicine, der University of South Florida, sowie ein CFF-Forschungsstipendium (DARCH19G0), das N.I.H (5R21AI147654 – 02 (PI, Chen)) und das USF Institute on Microbiomes unterstützt. Wir danken dem Whiteley-Labor für die kontinuierliche Zusammenarbeit mit Datensätzen zu diesem Manuskript. Wir danken Dr. Charles Szekeres für die Erleichterung der FACS-Sortierung. Die Figuren wurden von A.D.G und S.E.D mit Biorender.com erstellt.
Materials
| Amino acids | |||
| Alanine | Acr s Organics s Organics |
56-41-7 | |
| Arginine HCl | MP | 1119-34-2 | |
| Asparagine | Acr s Organics s Organics |
56-84-8 | Prepared in 0.5 M NaOH |
| Cystine HCl | Alfa Aesar | L06328 | |
| Glutamic acid HCl | Acr s Organics s Organics |
138-15-8 | |
| Glycine | Acr s Organics s Organics |
56-40-6 | |
| Histidine HCl H2O | Alfa Aesar | A17627 | |
| Isoleucine | Acr s Organics s Organics |
73-32-5 | |
| Leucine | Alfa Aesar | A12311 | |
| Lysine HCl | Alfa Aesar | J62099 | |
| Methionine | Acr s Organics s Organics |
63-68-3 | |
| Ornithine HCl | Alfa Aesar | A12111 | |
| Phenylalanine | Acr s Organics s Organics |
63-91-2 | |
| Proline | Alfa Aesar | A10199 | |
| Serine | Alfa Aesar | A11179 | |
| Threonine | Acr s Organics s Organics |
72-19-5 | |
| Tryptophan | Acr s Organics s Organics |
73-22-3 | Prepared in 0.2 M NaOH |
| Tyrosine | Alfa Aesar | A11141 | Prepared in 1.0 M NaOH |
| Valine | Acr s Organics s Organics |
72-18-4 | |
| Antibiotic | |||
| Carbenicillin | Alfa Aesar | J6194903 | |
| Day-of Stocks | |||
| CaCl2 * 2H2O | Fisher Chemical | C79-500 | |
| Dextrose (D-glucose) | Fisher Chemical | 50-99-7 | |
| 1,2-dioleoyl-sn-glycero-3-phosphocholine (DOPC) | Fisher (Avanti Polar Lipids) | 4235-95-4 | shake 15-20 min at 37 °C to evaporate chloroform |
| FeSO4 * 7H2O | Acr s Organics s Organics |
7782-63-0 | this stock equals 1 mg/mL, MUST make fresh |
| L-lactic acid | Alfa Aesar | L13242 | pH stock to 7 with NaOH |
| MgCl2 * 6H2O | Acr s Organics s Organics |
7791-18-6 | |
| N-acetylglucosamine | TCI | A0092 | |
| Prepared solids | |||
| Porcine mucin | Sigma | M1778-100G | UV-sterilize |
| Salmon sperm DNA | Invitrogen | 15632-011 | |
| Stain | |||
| Propidium iodide | Alfa Aesar | J66764MC | |
| Salts | |||
| K2SO4 | Alfa Aesar | A13975 | |
| KCl | Alfa Aesar | J64189 | add solid directly to buffered base |
| KNO3 | Acr s Organics s Organics |
7757-79-1 | |
| MOPS | Alfa Aesar | A12914 | add solid directly to buffered base |
| NaCl | Fisher Chemical | S271-500 | add solid directly to buffered base |
| Na2HPO4 | RPI | S23100-500.0 | |
| NaH2PO4 | RPI | S23120-500.0 | |
| NH4Cl | Acr s Organics s Organics |
12125-02-9 | add solid directly to buffered base |
| Consumables | |||
| Conical tubes (15 mL) | Olympus plastics | 28-101 | |
| Conical tubes (50 mL) | Olympus plastics | 28-106 | |
| Culture tubes w/air flow cap | Olympus plastics | 21-129 | |
| 35 mm four chamber glass-bottom dish | CellVis | NC0600518 | |
| Luria Bertani (LB) broth | Genessee Scientific | 11-118 | |
| Phosphate-buffered saline (PBS) | Fisher Bioreagents | BP2944100 | |
| Pipet tips (p200) | Olympus plastics | 23-150RL | |
| Pipet tips (p1000) | Olympus plastics | 23-165RL | |
| Serological pipets (5 mL) | Olympus plastics | 12-102 | |
| Serological pipets (25 mL) | Olympus plastics | 12-106 | |
| Serological pipets (50 mL) | Olympus plastics | 12-107 | |
| Ultrapure water (RNAse/DNAse free); nanopure water | Genessee Scientific | 18-194 | Nanopure water used for preparation of solutions in Table 1 |
| Syringes (10 mL) | BD | 794412 | |
| Syringes (50 mL) | BD | 309653 | |
| 0.22 mm PES syringe filter | Olympus plastics | 25-244 | |
| PS cuvette semi-mico | Olympus plastics | 91-408 | |
| Software | |||
| Biorender | To prepare the figures | ||
| FacsDiva6.1.3 | Becton Dickinson, San Jose, CA | ||
| Imaris | Bitplane | version 9.6 | |
| Zen Black | |||
| Equipment | |||
| FacsAriallu | Becton Dickinson, San Jose, CA | ||
| LSM 880 confocal laser scanning microscope | Zeiss |
Referências
- Ramsay, K. A., et al. The changing prevalence of pulmonary infection in with fibrosis: A longitudinal analysis. Journal of Cystic Fibrosis. 16 (1), 70-77 (2017).
- Bessonova, L., et al. Data from the US and UK cystic fibrosis registries support disease modification by CFTR modulation with ivacaftor. Thorax. 73 (8), 731-740 (2018).
- Breuer, O., et al. Changing prevalence of lower airway infections in young children with cystic fibrosis. American Journal of Respiratory and Critical Care Medicine. 200 (5), 590-599 (2019).
- O’Donnell, J. N., Bidell, M. R., Lodise, T. P. Approach to the treatment of patients with serious multidrug-resistant Pseudomonas aeruginosa infections. Pharmacotherapy. 40 (9), 952-969 (2020).
- Bjarnsholt, T., et al. The in vivo biofilm. Trends in Microbiology. 21 (9), 466-474 (2013).
- Darch, S. E., et al. Spatial determinants of quorum signaling in a Pseudomonas aeruginosa infection model. Proceedings of the National Academy of Sciences of the United States of America. 115 (18), 4779-4784 (2018).
- Zhu, K., Chen, S., Sysoeva, T. A., You, L. Universal antibiotic tolerance arising from antibiotic-triggered accumulation of pyocyanin in Pseudomonas aeruginosa. PLoS Biology. 17 (12), 3000573 (2019).
- Ciofu, O., Tolker-Nielsen, T. Tolerance and resistance of Pseudomonas aeruginosa biofilms to antimicrobial agents-how P. aeruginosa can escape antibiotics. Frontiers in Microbiology. 10, 913 (2019).
- Turner, K. H., Wessel, A. K., Palmer, G. C., Murray, J. L., Whiteley, M. Essential genome of Pseudomonas aeruginosa in cystic fibrosis sputum. Proceedings of the National Academy of Sciences of the United States of America. 112 (13), 4110-4115 (2015).
- Darch, S. E., et al. Phage inhibit pathogen dissemination by targeting bacterial migrants in a chronic infection model. MBio. 8 (2), 00240 (2017).
- Jorth, P., et al. Regional isolation drives bacterial diversification within cystic fibrosis lungs. Cell Host & Microbe. 18 (3), 307-319 (2015).
- Palmer, K. L., Aye, L. M., Whiteley, M. Nutritional cues control Pseudomonas aeruginosa multicellular behavior in cystic fibrosis sputum. Journal of Bacteriology. 189 (22), 8079-8087 (2007).
- Davies, D. G., et al. The involvement of cell-to-cell signals in the development of a bacterial biofilm. Science. 280 (5361), 295-298 (1998).
- Hartmann, R., et al. Quantitative image analysis of microbial communities with BiofilmQ. Nature Microbiology. 6 (2), 151-156 (2021).
- Stacy, A., et al. Bacterial fight-and-flight responses enhance virulence in a polymicrobial infection. Proceedings of the National Academy of Sciences of the United States of America. 111 (21), 7819-7824 (2014).

