Tredimensionel in vitro biomimetisk model af neuroblastom ved hjælp af kollagenbaserede stilladser
Summary
Dette papir viser de trin, der kræves for at frø neuroblastomcellelinjer på tidligere beskrevne tredimensionelle kollagenbaserede stilladser, opretholde cellevækst i en forudbestemt tidsramme og hente stilladser til flere cellevækst- og celleadfærdsanalyser og downstream-applikationer, der kan tilpasses til at tilfredsstille en række eksperimentelle mål.
Abstract
Neuroblastom er den mest almindelige ekstrakranielle solide tumor hos børn, der tegner sig for 15% af de samlede pædiatriske kræftdødsfald. Det indfødte tumorvæv er et komplekst tredimensionelt (3D) mikromiljø, der involverer lag af kræftceller og ikke-kræftceller omgivet af en ekstracellulær matrix (ECM). ECM giver fysisk og biologisk støtte og bidrager til sygdomsprogression, patientprognose og terapeutisk respons.
Dette papir beskriver en protokol til samling af et 3D-stilladsbaseret system til efterligning af neuroblastommikromiljøet ved hjælp af neuroblastomcellelinjer og kollagenbaserede stilladser. Stilladserne suppleres med enten nanohydroxyapatit (nHA) eller glycosaminoglycaner (GAG’er), der naturligt findes i høje koncentrationer i knogle og knoglemarv, de mest almindelige metastatiske steder for neuroblastom. Den 3D porøse struktur af disse stilladser tillader neuroblastom cellebinding, proliferation og migration og dannelse af celleklynger. I denne 3D-matrix afspejler celleresponsen på terapi mere in vivo-situationen .
Det stilladsbaserede kultursystem kan opretholde højere celletætheder end konventionel todimensionel (2D) cellekultur. Derfor er optimeringsprotokoller for indledende såcellenumre afhængige af de ønskede eksperimentelle tidsrammer. Modellen overvåges ved at vurdere cellevækst via DNA-kvantificering, cellelevedygtighed via metaboliske assays og cellefordeling i stilladserne via histologisk farvning.
Denne models anvendelser omfatter vurdering af gen- og proteinekspressionsprofiler samt cytotoksicitetstest ved hjælp af konventionelle lægemidler og miRNA’er. 3D-kultursystemet giver mulighed for præcis manipulation af celle- og ECM-komponenter, hvilket skaber et miljø, der mere fysiologisk ligner naturligt tumorvæv. Derfor vil denne 3D in vitro-model fremme forståelsen af sygdomspatogenesen og forbedre sammenhængen mellem resultater opnået in vitro, in vivo i dyremodeller og mennesker.
Introduction
Neuroblastom er en pædiatrisk kræft i det sympatiske nervesystem, der opstår under embryonal udvikling eller tidligt postnatalt liv på grund af transformationen af neurale kamceller1. Det er den mest almindelige solide ekstrakranielle tumor hos børn, der repræsenterer 8% af de maligniteter, der diagnosticeres hos patienter under 15 år og er ansvarlig for 15% af alle dødsfald hos børnekræft. Sygdommen viser meget heterogen klinisk adfærd på grund af specifikke kromosomale, genetiske og epigenetiske ændringer og histopatologiske træk.
Disse ændringer bidrager til aggressiviteten af neuroblastom og dårlige resultater hos pædiatriske patienter. Derfor viser de nuværende behandlinger sig ineffektive på lang sigt for næsten 80% af patienterne med den klinisk aggressive sygdom2, hvilket understreger, at behandling for denne gruppe patienter fortsat er udfordrende. Dette skyldes sandsynligvis, at mekanismerne for neuroblastom, heterogenitet og metastaser stadig ikke forstås fuldt ud. Imidlertid antages tumormikromiljøet (TME) nu bredt at spille en rolle i udviklingen af mange kræftformer; Alligevel er det stadig underundersøgt i neuroblastom 3,4.
Den oprindelige TME er et komplekst 3D-mikromiljø, der involverer kræftceller og ikke-kræftceller omgivet af en ECM. ECM refererer til den acellulære komponent i et væv, der giver strukturel og biokemisk støtte til dets cellulære beboere og bidrager til sygdomsprogression, patientprognose og terapeutisk respons5. Denne fremme af sygdomsprogression skyldes “dynamisk gensidighed” eller løbende tovejskommunikation mellem celler og ECM 6,7,8. Efterhånden som kræft skrider frem, omorganiseres stromalkollagen ofte i lineære mønstre vinkelret på stroma-cancer-grænsefladen, som kræftceller bruger som migrationsrute til metastase 9,10,11.
Hovedkomponenterne i dette indfødte funktionelle biologiske stillads inkluderer et fibrøst netværk af kollagener type I og II og andre proteiner, herunder elastin, glycoproteiner såsom laminin samt en række proteoglycaner og andre opløselige komponenter12,13. Disse proteiner fra den oprindelige ECM er nu blevet attraktive naturlige biomolekyler til udvikling af 3D in vitro modeller3. Anvendelsen af 3D-stilladser til in vitro-cellekultur er stigende i popularitet på grund af dens større fysiologiske repræsentation af TME sammenlignet med traditionel 2D-monolagskultur. De fremstillede 3D-stilladser hjælper cellebinding, spredning, migration, metabolisme og respons på stimuli set i in vivo biologiske systemer.
Hovedkomponenten i disse 3D-stilladser er kollagen, som er en nøglespiller i mange normale biologiske processer, herunder vævsreparation, angiogenese, vævsmorfogenese, celleadhæsion og migration11. Kollagenbaserede 3D-matricer har vist deres robuste funktionalitet til at modellere ECM, der fungerer som et in vitro biomimetisk mikromiljø, samtidig med at de muliggør celle-ECM-interaktioner samt cellemigration og invasion. Disse 3D-matricer giver også en mere nøjagtig analyse af cellerespons på kemoterapeutiske lægemidler end traditionel 2D eller “flad” kultur i mange kræftmodeller 14,15,16, herunder neuroblastom 17,18. Genetisk analyse af 3D-cellekulturer har rapporteret en højere korrelation med den humane vævsprofil, selv sammenlignet med dyremodeller19. Samlet set er hjørnestenen i disse 3D-stilladser at give celler et passende in vitro-miljø, som rekapitulerer den oprindelige vævsarkitektur og letter tovejs molekylær krydstale8.
For at øge kompleksiteten af kollagenbaserede modeller inkorporeres andre almindelige ECM-komponenter i vævsteknologiprocessen, hvilket skaber mere fysiologisk relevante modeller til at afspejle niche-TME’er i forskellige væv. For eksempel letter GAG’er, negativt ladede polysaccharider, der findes i alle pattedyrvæv20, cellebinding, migration, proliferation og differentiering. Chondroitinsulfat er en specifik type GAG, der findes i knogle og brusk, som tidligere har været anvendt i vævstekniske applikationer til knoglereparation 21,22,23,24,25. Nanohydroxyapatit (nHA) er den vigtigste uorganiske bestanddel af mineralsammensætningen i humant knoglevæv, der udgør op til 65 vægtprocent af knoglen26 og derfor i vid udstrækning anvendes til knogleudskiftning og regenerering27. GAG’er og nHA er således attraktive kompositter til rekonstruktion af det primære neuroblastom ECM og modellering af de mest almindelige metastatiske steder for neuroblastom, knoglemarv (70,5%) og knogle (55,7%)28.
Stilladser, der indeholder disse ECM-komponenter, blev oprindeligt udviklet til knoglevævstekniske applikationer med omfattende analyse af deres biokompatibilitet, toksicitet og osteokonduktive og osteoinduktive egenskaber29,30. De er porøse, kollagenbaserede matricer produceret ved hjælp af frysetørringsteknikker til at kontrollere deres fysiske og biologiske egenskaber. Kollagenstilladserne suppleret med enten nHA (Coll-I-nHA) eller chondroitin-6-sulfat (Coll-I-GAG) viste succes med at efterligne den primære TME i brystkræft31 og metastase til knogle i prostatacancer15 samt neuroblastom17. Den frysetørringsteknik, der anvendes til fremstilling af disse sammensatte stilladser, giver reproducerbar homogenitet i porestørrelse og porøsitet inden for stilladserne22,23,24. Kort fortalt fremstilles en kollagensopslæmning (0,5 vægt%) ved at blande fibrillært kollagen med 0,05 M eddikesyre. For Coll-I-GAG tilsættes 0,05 vægt% chrondoitin-6-sulfat isoleret fra hajbrusk til kollagenopslæmningen under blanding. Til de sammensatte Coll-I-nHA-stilladser syntetiseres hydroxyapatitpartikler i nanostørrelse som tidligere beskrevet27 og tilsættes til kollagensopslæmningen i forholdet 2: 1 til vægten af kollagen under blandingsprocessen. Alle stilladser er fysisk tværbundet og steriliseret ved hjælp af en dehydrotermisk behandling ved 105 °C i 24 timer25. Cylindriske stilladser (6 mm diameter, 4 mm højde) opnås ved hjælp af en biopsistans og kan kemisk tværbindes med 3 mM N-(3-dimethylaminopropyl)-N’-ethylcarbodiimidhydrochlorid og 5,5 mM N-hydroxysuccinimid (EDAC / NHS) i destilleret vand (dH2O) for at forbedre konstruktionernes mekaniske egenskaber30. Denne veloptimerede fremstillingsproces af to kollagenstilladser skaber stilladser med reproducerbare mekaniske egenskaber, herunder porestørrelse, porøsitet og stivhed (kPa). Både Coll-I-GAG og Coll-I-nHA stilladser har forskellige fysiske egenskaber, hvilket skaber forskellige miljøforhold. Egenskaberne for hvert stillads er vist i tabel 1.
| Coll-I-GAG | Coll-I-nHA | |
| Stillads størrelse (diameter [mm] x højde [mm]) |
6 x 4 17 | 6 x 4 17 |
| Kollagenkoncentration (vægtprocent) | 0.5 17 | 0.5 17 |
| Substratkoncentration (vægtprocent) [baseret på vægten af kollagen] |
0,05 15,17 | 200 17 |
| Gennemsnitlig porestørrelse (mm) | 96 22 | 96 – 120 29 |
| Porøsitet (%) | 99,5 23 | 98,9 – 99,4 27 |
| Stivhed (kPa) | 1.5 27 | 5,5 – 8,63 29 |
Tabel 1: Oversigt over de mekaniske egenskaber af de to stilladser, der er vedtaget til undersøgelse af neuroblastombiologi.
Dette papir beskriver en protokol til samling af et 3D-stilladsbaseret system for bedre at efterligne neuroblastommikromiljøet ved hjælp af neuroblastomcellelinjer og tidligere beskrevne kollagenbaserede stilladser suppleret med enten nHA (Coll-I-nHA) eller chondroitin-6-sulfat (Coll-I-GAG). Protokollen inkluderer downstream-metoder til at analysere neuroblastomcellernes vækstmekanismer i et mere fysiologisk relevant miljø ved hjælp af tidligere optimerede billige metoder tilpasset fra 2D-monolagskultur figur 1.
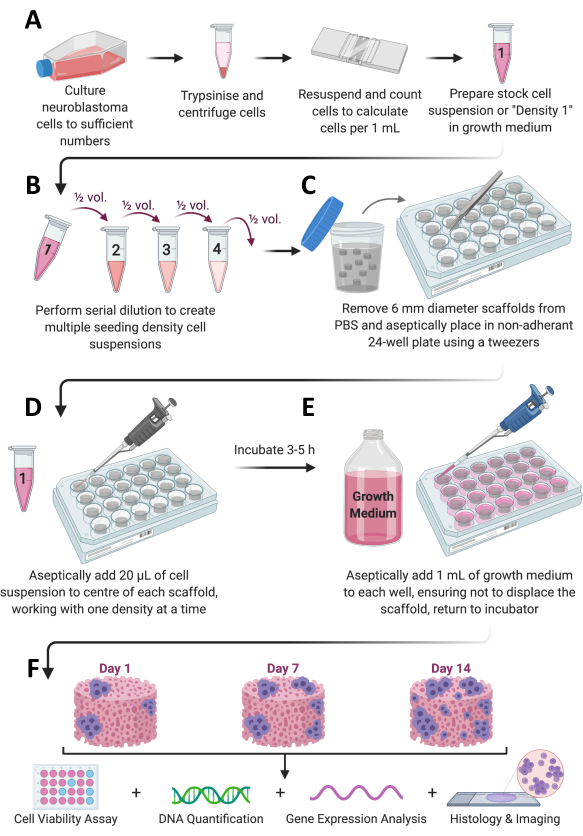
Figur 1: Samlet protokolarbejdsgang. (A) Celler dyrkes til tilstrækkeligt antal, opdeles, tælles og resuspenderes i et passende volumen medium. (B) Denne cellestamme gennemgår derefter seriel fortynding for at fremstille i alt 4 cellesuspensioner med forskellige densiteter. (C) Kollagenbaserede stilladser er sterilt belagt i ikke-klæbende plader med 24 brønde, og (D) 20 μL cellesuspension tilsættes til midten af hvert stillads og efterlades til inkubation ved 37 ° C, 5% CO2 og 95% fugtighed i 3-5 timer. (E) Komplet vækstmedium (1 ml) tilsættes derefter langsomt til hvert stillads, og pladerne placeres tilbage i inkubatoren for at tillade cellevækst i den ønskede tidsramme. (F) På hvert forudbestemt tidspunkt hentes flere stilladser til cellelevedygtighed og vækstvurdering, genekspressionsanalyse og histologisk farvning. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
3D-stilladskræftcellemodellen har vist sig at være et værdifuldt og alsidigt værktøj til at opnå mekanistisk indsigt i neuroblastomcellevækst, levedygtighed og infiltration af celler i en forenklet TME32. 3D-neuroblastommodellen, der er beskrevet her, efterligner den minimale TME og giver mere fysiologisk relevante data end en 2D-monolagskultur. En stor ulempe ved 3D-cellekultur er øget eksperimentel kompleksitet og længere tidsrammer. Beskrevet her er en optimeret protokol til såning, vækst og vedligeholdelse af neuroblastomceller på kollagenbaserede stilladser efterfulgt af downstream-analyser og applikationer, hvilket giver robust karakterisering af cellevækst. Vi havde til formål at få indsigt i den optimale cellesåtæthed for stilladserne for at skabe et forudsigeligt og kontrollerbart miljø til vurdering af kræftbehandlinger i et hurtigt 14-dages eksperimentelt vindue. Kombinationen af alle disse beskrevne enkle protokoller giver en velafrundet vurdering af neuroblastomcellevækst i det stilladsbaserede in vitro-kultursystem .
De kritiske punkter i protokolopsætningen er blevet understreget for at give forskere mulighed for hurtigt at etablere det samme i deres laboratorier. For eksempel tillader de angivne inkubationstider for bedre ydeevne af den kolorimetriske cellelevedygtighedsanalyse dybere penetration af reagenset i stilladsporerne for at nå alle celler. Desuden er den fluorescerende dsDNA-farvningsteknik robust og ligetil; DNA-frigivelse fra stilladserne kræver imidlertid kraftig cellelyse, da cellerne er ‘fanget’ i kollagenfibre.
Ved hjælp af det beskrevne enkle DNA-kvantificeringsassay kan vi identificere logvækstfasen på kollagenbaserede stilladser til screening af kræftlægemidler ved hjælp af denne model. I den beskrevne eksperimentelle indstilling blev der anvendt 4 indledende cellesåningstætheder med en samlet 14-dages periode og analysetidspunkter på dag 1, 7 og 14. Vi identificerede, at KellyLuc-celler podet ved 4 × 105 celler / stillads har det mest signifikante aktive spredningsvindue mellem dag 7 og 14. Disse logfasevækstdata giver mulighed for pålidelig fortolkning af forskellige cellecytotoksicitetseksperimenter. Det eliminerer spekulationer om ethvert fald i vækst eller celledød som følge af undertrykt vækst på den 3D-porøse platform snarere end fra lægemiddeltoksicitet. Cellelevedygtighed er også en meget anvendt vurdering af 3D-platformes egnethed til at understøtte væksten af forskellige celletyper33,34. Mens der er mange analyser til måling af cellelevedygtighed, herunder levende / død farvning, ATP-måling, proliferationsassays, fandt vi, at brugen af Alamar Blue kolorimetriske cellelevedygtighedsanalyser var en enkel og effektiv teknik til understøttelse af DNA-kvantificeringsdata.
Den kombinerede anvendelse af DNA-kvantificering og cellelevedygtighed gav supplerende bevis for, at den optimale tæthed til frøceller på stilladset for at opnå fortsat vækst over en 14-dages periode i gennemsnit er 2-4 × 105 celler / stillads. Denne protokol kan dog let tilpasses til at tilfredsstille forskellige eksperimentelle tidsrammer, analysetidspunkter og downstream-applikationer. Selvom denne protokol beskriver evalueringen af monokulturcellevækst af neuroblastomceller på stilladser, kan stilladserne let ændres til brug som en platform for samkultur, beskrevet af do Amaral et al., der udnyttede kollagen-GAG-stilladser til co-kultur keratinocytter og fibroblaster i en undersøgelse af sårheling35.
Den beskrevne 3D-model muliggør visualisering af cellevækst og infiltration ved hjælp af forskellige velkendte teknikker, såsom immunofluorescens og standard H&E. Det er vigtigt at visualisere cellerne sammen med karakteriseringen af vækst ved hjælp af biokemiske assays på grund af mangfoldigheden af cellemorfologi og vækstmønstre på stilladser. Forståelse af vækstmønsteret kan give indsigt i vækstadfærd og fremtidig reaktion på kræftmedicin. For eksempel giver IMR32-vækst ved hjælp af DNA-kvantificering lignende mønstre som Kelly, selvom IMR32 ved visualisering ved hjælp af H&E vokser i større klynger end Kelly, som viste mere spredt vækst (figur 9). Disse varierede vækstmønstre af cellelinjer i stilladser afspejler det kliniske scenario for tumorheterogenitet. Undersøgelse af lægemiddelrespons mod kræft ved hjælp af et panel af cellelinjer med forskellige morfologier i 3D-stilladser vil øge den prædiktive værdi for patientens respons på de samme lægemidler.
Påvisning af gen- eller proteinekspression kan også udføres ved hjælp af andre tilgange såsom RT-qPCR eller ELISA, hvis proteinet af interesse udskilles. En surrogatmarkør for neuroblastomprogression, chromogranin A (CgA)36, blev brugt til yderligere at karakterisere neuroblastomcellevækst i 3D. Som beskrevet i tidligere arbejde17 steg CgA-sekretionen, efterhånden som cellerne spredte sig (figur 10). Mens enkeltlagscellekultur ikke kunne fange denne stigning, da spredning betød, at celler nåede fuld sammenløb i kulturskålene, tillod brugen af 3D-kollagenstilladserne langvarig vurdering af CgA-sekretion.
Denne 3D in vitro-model er muligvis ikke egnet til alle forskningsspørgsmål til undersøgelse af neuroblastombiologi og respons på terapi. En af begrænsningerne er ujævn celleindtrængning i stilladser og dannelse af celleklynger af varierende størrelse, som afhænger af en given cellelinje og kan føre til ukontrollabel diffusion af næringsstoffer og testlægemidler. Denne funktion påvirker robustheden i terapeutisk screening. På trods af denne begrænsning er det imidlertid vigtigt at overveje, at indfødte tumorer også er heterogene i størrelse og kræftcellefordeling og indeholder mange andre celletyper i tumorvævet. For at overvinde denne begrænsning foreslår vi brugen af hvert cellebefolket stillads som et enkelt mikrovæv, for hvilket følgende parametre vil blive optimeret: (a) inkubationstider for cellelevedygtighedsreagenset for at nå cellerne og celleklyngerne og (b) lysering af cellerne i Triton X-100-buffer ved forbehandling af celler på stilladser med en vævslyser for at frigive DNA’et fra cellerne indeholdt dybt i stilladset.
En anden teknisk begrænsning af denne protokol er manglen på mekanisk test af hvert parti nyfremstillede stilladser til denne model. Ved hjælp af stilladsets robuste fremstillingsproces, som i vid udstrækning er blevet karakteriseret i forhold til stilladsets fysiske og kemiske egenskaber, såsom tryk- og trækmodul, porøsitet og visuel porestruktur og homogenitet, sikres det imidlertid, at stilladskvaliteter opretholdes gennem batches 21,24,27,30,37.
Sammenfattende præsenterer dette papir en række enkle metoder til analyse af cellulær vækst på kollagenbaserede stilladser. Både den eksperimentelle tidslinje og analysepunkter kan udskiftes afhængigt af de specifikke forskningsspørgsmål. Denne protokol kan også tilpasses andre celletyper. Resultaterne vist ovenfor giver bevis for, hvordan denne samling af metoder gav indsigt i den optimale såtæthed for forskellige neuroblastomcellelinjer for at skabe kontinuerlig vækst over 14 dage. Sammenlægningen af resultater opnået fra alle metoderne i denne protokol giver en overlegen forståelse af cellevækst inden for 3D-kollagenmatrixen. Fremtidig anvendelse af denne model vil sandsynligvis involvere samkultursystemer, der er specifikke for neuroblastoma TME og testning af forskellige nye kræftlægemidler.
Declarações
The authors have nothing to disclose.
Acknowledgements
Dette arbejde blev støttet af National Children’s Research Centre (NCRC), Irish Research Council (IRC) og Neuroblastoma UK. Illustrationerne blev skabt ved hjælp af BioRender.
Materials
| Cells | |||
| IMR-32 | ATCC | CCL-127 | |
| Kelly | ECACC | 82110411 | |
| KellyCis83 | Made in lab – derived from Kelly (Piskareva et al., 2015) | – | Increasing exposure to cisplatin. Cross resistance acquired |
| SH-SY5Y | ATCC | CRL-2266 | |
| Disposable | |||
| 0.22 µm syringe filter | Millex | SLHP033RS | |
| 1.5 mL Eppendorf tube | Eppendorf | 0030 120.086 | |
| 100 mL sterile Pot | Starstedt | – | |
| 10 mL plastic pipette | Cellstar | 607 180 | |
| 15 mL Falcon tube | Starstedt | 62.554.502 | |
| 25 mL plastic pipette | Cellstar | 760 180 | |
| 50 mL Falcon tube | Starstedt | 62.547.254 | |
| 5 mL plastic pipette | Cellstar | 606 180 | |
| 6 mm Biopsy punches | Kai Medical | BP-60F | |
| Aluminium foil | – | – | |
| Cover Slip | Menzel-Glaser | – | |
| HYPERflask | Corning | CLS10030 | |
| Microscope slides | Thermo Scientific | J1840AMNT | |
| Opaque black 96-well plate | Costar | 3915 | |
| Sterile P10 tips | Starlab | S1121-3810 | |
| Sterile P1000 tips | Starlab | S1122-1830 | |
| Sterile P20 tips | Starlab | S1123-1810 | |
| Sterile P200 tips | Starlab | S1120-8810 | |
| T-175 (175 cm2 flask) | Sarstedt | 83.3912 | |
| T-75 (75 cm2 flask) | Sarstedt | 83.3911.302 | |
| Translucent clear 96 well plate | Cellstar | 655180 | |
| Translucent non-adherent 24 well plates | Cellstar | 83.3922.500 | |
| Equipment | |||
| Autoclave | Astell | – | |
| Automatic tissue processor | Leica | TP1020 | |
| Centrifuge 5804 | Eppendorf | – | |
| Hemocytometer | Hausser Scientific | – | |
| Incubator | ThermoScientific | – | |
| Microtome | Leica | RM2255 | |
| Oven | Memmert | Calibrated by: Cruinn diagnostics Ltd | |
| P10 pipette | Gilson | ||
| P100 pipette | Gilson | ||
| P1000 pipette | Gilson | ||
| P20 pipette | Gilson | Calibrated by: Cruinn diagnostics Ltd | |
| P200 pipette | Gilson | Calibrated by: Cruinn diagnostics Ltd | |
| Paraffin section flotation bath | Electrothermal | MH8517 | Calibrated by: Cruinn diagnostics Ltd |
| Pipette electronic dispenser | Corning | StripipetterUltra | Calibrated by: Cruinn diagnostics Ltd |
| Plate cooler | Leica | EG1140C | Calibrated by: Cruinn diagnostics Ltd |
| Refrigerator -20 °C | Liebherr | – | |
| Refrigerator -80 °C | Liebherr | – | |
| Refrigerator 4 °C | Liebherr | – | |
| Seesaw Rocker | DLAb | SK-D1807-E | |
| Spectrophotometer – Victor3V Platereader | PerkinElmer | 1420 | |
| Tissue culture hood/Laminar flow hood | GMI | 8038-30-1044 | |
| Tissue Lyser | Qiagen | TissueLyser LT | |
| Tweezers | – | – | |
| Water bath | Grant | – | |
| Wax embedder | Leica | EG1140H | |
| Materials | |||
| 1 L Water | Adrona – Biosciences | 568 | |
| 1% Triton-X | Sigma Aldrich | 9002-93-1 | |
| 10x PBS tablets | Sigma Aldrich | P4417-100TAB | |
| 37% paraformaldehyde | Sigma-Aldrich | F8775 | |
| Alamar Blue Cell Viability Reagent | Invitrogen | DAL1100 | |
| Collagen- glycosaminoglycan scaffold | Tissue engineering research group (TERG) | ||
| Collagen-nanohydroxyapatite scaffold | Tissue engineering research group (TERG) | ||
| dH20 | Adrona – Biosciences | 568 | |
| Eosin | Sigma-Aldrich | E4009 | Made as per: (Cunniffe et al., 2010, Fitzgerald et al., 2015; O’Brien et al., 2005) |
| EtOH | Sigma-Aldrich | 1.00983.2500 | Made as per: (Cunniffe et al., 2010, Fitzgerald et al., 2015; O’Brien et al., 2005) |
| F12 | Gibco | 21765-029 | |
| FBS | Gibco | 10270-106 | |
| Hemaytoxylin | Sigma-Aldrich | HHS32-1L | |
| L-Glutamine | Gibco | 25030-024 | |
| MEM | Gibco | 21090-022 | |
| miRNA easy Kit | Qiagen | 217004 | |
| MNEAA’s | Gibco | 11140-035 | |
| Penicillin/streptomycin | Gibco | 015140-122 | |
| Qiazol | Qiagen | 79306 | |
| Quant-iT PicoGreen dsDNA Assay Kit | Invitrogen | P11496 | |
| RPMI | Gibco | 21875-034 | |
| Sodium bicarbonate | Sigma Aldrich | S7795-500G | |
| Tissue embedding Medium | Sigma | A6330-4LB | |
| Trypsin-EDTA | Gibco | 25300-054 | |
| Software | |||
| Excel | – | Excel 2016 | |
| ImageJ | – | – | |
| Prism | – | Version 9 | |
Referências
- Davidoff, A. M. Neuroblastoma. Seminars in Pediatric Surgery. 21 (1), 2-14 (2012).
- Matthay, K. K., et al. Neuroblastoma. Nature Reviews Disease Primers. 2, 16078 (2016).
- Costard, L. S., Hosn, R. R., Ramanayake, H., O’Brien, F. J., Curtin, C. M. Influences of the 3D microenvironment on cancer cell behaviour and treatment responsiveness: a recent update on lung, breast and prostate cancer models. Acta Biomaterialia. , (2021).
- Borriello, L., Seeger, R. C., Asgharzadeh, S., Declerck, Y. A. More than the genes, the tumor microenvironment in neuroblastoma. Cancer Letters. 380 (1), 304-318 (2016).
- Walker, C., Mojares, E., Del Río Hernández, A. Role of extracellular matrix in development and cancer progression. International Journal of Molecular Sciences. 19 (10), 3028 (2018).
- Bissell, M. J., Hall, H. G., Parry, G. How does the extracellular matrix direct gene expression. Journal of Theoretical Biology. 99 (1), 31-68 (1982).
- Schultz, G. S., Davidson, J. M., Kirsner, R. S., Bornstein, P., Herman, I. M. Dynamic reciprocity in the wound microenvironment. Wound Repair and Regeneration. 19 (2), 134-148 (2011).
- Brancato, V., Oliveira, J. M., Correlo, V. M., Reis, R. L., Kundu, S. C. Could 3D models of cancer enhance drug screening. Biomaterials. 232, 119744 (2020).
- Provenzano, P. P., et al. Collagen density promotes mammary tumor initiation and progression. BMC Medicine. 6, 11 (2008).
- Provenzano, P. P., et al. Collagen reorganization at the tumor-stromal interface facilitates local invasion. BMC Medicine. 4, 38 (2006).
- Ouellette, J. N., et al. Navigating the collagen jungle: The biomedical potential of fiber organization in cancer. Bioengenharia. 8 (2), 1-19 (2021).
- Kreger, S. T., Voytik-Harbin, S. L. Hyaluronan concentration within a 3D collagen matrix modulates matrix viscoelasticity, but not fibroblast response. Matrix Biology. 28 (6), 336-346 (2009).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. Journal of Cell Science. 123 (24), 4195-4200 (2010).
- Hume, R. D., et al. Tumour cell invasiveness and response to chemotherapeutics in adipocyte invested 3D engineered anisotropic collagen scaffolds. Scientific Reports. 8 (1), 12658 (2018).
- Fitzgerald, K. A., et al. The use of collagen-based scaffolds to simulate prostate cancer bone metastases with potential for evaluating delivery of nanoparticulate gene therapeutics. Biomaterials. 66, 53-66 (2015).
- Sapudom, J., Pompe, T. Biomimetic tumor microenvironments based on collagen matrices. Biomaterials Science. 6 (8), 2009-2024 (2018).
- Curtin, C., et al. A physiologically relevant 3D collagen-based scaffold-neuroblastoma cell system exhibits chemosensitivity similar to orthotopic xenograft models. Acta Biomaterialia. 70, 84-97 (2018).
- Gavin, C., et al. Neuroblastoma invasion strategies are regulated by the extracellular matrix. Cancers. 13 (4), 1-23 (2021).
- Ridky, T. W., Chow, J. M., Wong, D. J., Khavari, P. A. Invasive three-dimensional organotypic neoplasia from multiple normal human epithelia. Nature Medicine. 16 (12), 1450-1456 (2010).
- Casal, e. J., Crane, J. S. . Biochemistry, Glycosaminoglycans. , (2019).
- O’Brien, F. J., Harley, B. A., Yannas, I. V., Gibson, L. J. The effect of pore size on cell adhesion in collagen-GAG scaffolds. Biomaterials. 26 (4), 433-441 (2005).
- O’Brien, F. J., Harley, B. A., Yannas, I. V., Gibson, L. Influence of freezing rate on pore structure in freeze-dried collagen-GAG scaffolds. Biomaterials. 25 (6), 1077-1086 (2004).
- Haugh, M. G., Murphy, C. M., McKiernan, R. C., Altenbuchner, C., O’Brien, F. J. Crosslinking and mechanical properties significantly influence cell attachment, proliferation, and migration within collagen glycosaminoglycan scaffolds. Tissue Engineering. Part A. 17 (9-10), 1201-1208 (2011).
- Murphy, C. M., Haugh, M. G., O’Brien, F. J. The effect of mean pore size on cell attachment, proliferation and migration in collagen-glycosaminoglycan scaffolds for bone tissue engineering. Biomaterials. 31 (3), 461-466 (2010).
- Haugh, M. G., Jaasma, M. J., O’Brien, F. J. The effect of dehydrothermal treatment on the mechanical and structural properties of collagen-GAG scaffolds. Journal of Biomedical Materials Research – Part A. 89 (2), 363-369 (2009).
- Lowe, B., Hardy, J. G., Walsh, L. J. Optimizing nanohydroxyapatite nanocomposites for bone tissue engineering. ACS Omega. 5 (1), 1-9 (2020).
- Cunniffe, G. M., Dickson, G. R., Partap, S., Stanton, K. T., O’Brien, F. J. Development and characterisation of a collagen nano-hydroxyapatite composite scaffold for bone tissue engineering. Journal of Materials Science. Materials in Medicine. 21 (8), 2293-2298 (2010).
- DuBois, S. G., et al. Metastatic sites in stage IV and IVS neuroblastoma correlate with age, tumor biology, and survival. Journal of Pediatric Hematology/Oncology. 21 (3), 181-189 (1999).
- Ryan, A. J., Gleeson, J. P., Matsiko, A., Thompson, E. M., O’Brien, F. J. Effect of different hydroxyapatite incorporation methods on the structural and biological properties of porous collagen scaffolds for bone repair. Journal of Anatomy. 227 (6), 732-745 (2015).
- Tierney, C. M., et al. The effects of collagen concentration and crosslink density on the biological, structural and mechanical properties of collagen-GAG scaffolds for bone tissue engineering. Journal of the Mechanical Behavior of Biomedical Materials. 2 (2), 202-209 (2009).
- Cox, R. F., Jenkinson, A., Pohl, K., O’Brien, F. J., Morgan, M. P. Osteomimicry of mammary adenocarcinoma cells in vitro; increased expression of bone matrix proteins and proliferation within a 3D collagen environment. PLoS One. 7 (7), 41679 (2012).
- Nolan, J. C., et al. Preclinical models for neuroblastoma: advances and challenges. Cancer Letters. 474, 53-62 (2020).
- Sirivisoot, S., Pareta, R., Harrison, B. S. Protocol and cell responses in threedimensional conductive collagen gel scaffolds with conductive polymer nanofibres for tissue regeneration. Interface Focus. 4 (1), 20130050 (2014).
- Thevenot, P., Nair, A., Dey, J., Yang, J., Tang, L. Method to analyze three-dimensional cell distribution and infiltration in degradable scaffolds. Tissue Engineering. Part C-Methods. 14 (4), 319-331 (2008).
- do Amaral, R. J. F. C., et al. Functionalising collagen-based scaffolds with platelet-rich plasma for enhanced skin wound healing potential. Frontiers in Bioengineering and Biotechnology. 7, 371 (2019).
- Gkolfinopoulos, S., Tsapakidis, K., Papadimitriou, K., Papamichael, D., Kountourakis, P. Chromogranin A as a valid marker in oncology: Clinical application or false hopes. World Journal of Methodology. 7 (1), 9-15 (2017).
- O’Brien, F. J., et al. The effect of pore size on permeability and cell attachment in collagen scaffolds for tissue engineering. Technology and Health Care. 15 (1), 3-17 (2007).

