Global identifikation af co-translationelle interaktionsnetværk ved selektiv ribosomprofilering
Summary
Co-translationelle interaktioner spiller en afgørende rolle i spirende kædemodifikationer, målretning, foldning og samlingsveje. Her beskriver vi selektiv ribosomprofilering, en metode til in vivo, direkte analyse af disse interaktioner i modellen eukaryot Saccharomyces cerevisiae.
Abstract
I de senere år er det blevet tydeligt, at ribosomer ikke kun afkoder vores mRNA, men også styrer fremkomsten af polypeptidkæden ind i det overfyldte cellulære miljø. Ribosomer giver platformen for rumligt og kinetisk kontrolleret binding af membranmålretningsfaktorer, modificerende enzymer og foldning af chaperoner. Selv samlingen i højordens oligomere komplekser samt protein-protein netværksdannelsestrin blev for nylig opdaget at være koordineret med syntese.
Her beskriver vi Selektiv Ribosome Profilering, en metode udviklet til at fange co-translationelle interaktioner in vivo. Vi vil detaljere de forskellige affinitetsrensningstrin, der kræves til indfangning af ribosom-spirende kædekomplekser sammen med co-translationelle interaktionorer, samt mRNA-ekstraktion, størrelsesudelukkelse, omvendt transkription, dyb sekventering og big-data-analysetrin, der kræves for at dechiffrere co-translationelle interaktioner i næsten-codonopløsning.
Introduction
Selective Ribosome Profiling (SeRP) er den eneste metode til dato, der fanger og karakteriserer co-translationelle interaktioner, in vivo, på en direkte måde 1,2,3,4,5,6. SeRP muliggør global profilering af interaktioner af enhver faktor med oversættelse af ribosomer i nærkodonopløsning 2,7.
Metoden er afhængig af flashfrysning af voksende celler og bevarelse af aktiv translation. Cellelysater behandles derefter med RNase I for at fordøje alt mRNA i cellen undtagen ribosombeskyttede mRNA-fragmenter kaldet “ribosomfodspor”. Prøven opdeles derefter i to dele; en del bruges direkte til isolering af alle de cellulære ribosomale fodspor, der repræsenterer al løbende translation i cellen. Den anden del anvendes til affinitetsrensning af den specifikke delmængde af ribosomer forbundet med en faktor af interesse, for eksempel: modificerende enzymer, translokationsfaktorer, foldning af chaperoner og komplekse samlingsinteraktioner. De affinitetsrensede ribosomale fodspor kaldes samlet interactomet. Derefter ekstraheres de ribosombeskyttede mRNA’er og bruges til cDNA-biblioteksgenerering efterfulgt af dyb sekventering.
Sammenlignende analyse af de samlede translatom- og interactomprøver muliggør identifikation af alle orfs, der er forbundet med interessefaktoren, samt karakterisering af hver orf-interaktionsprofil. Denne profil rapporterer de præcise engagementsstart- og afslutningssekvenser, hvorfra man kan udlede de afkodede kodoner og de respektive rester af den nye polypeptidkæde samt på ribosomhastighedsvariationerne under interaktionen 7,8. Figur 1 viser protokollen som en skematisk.
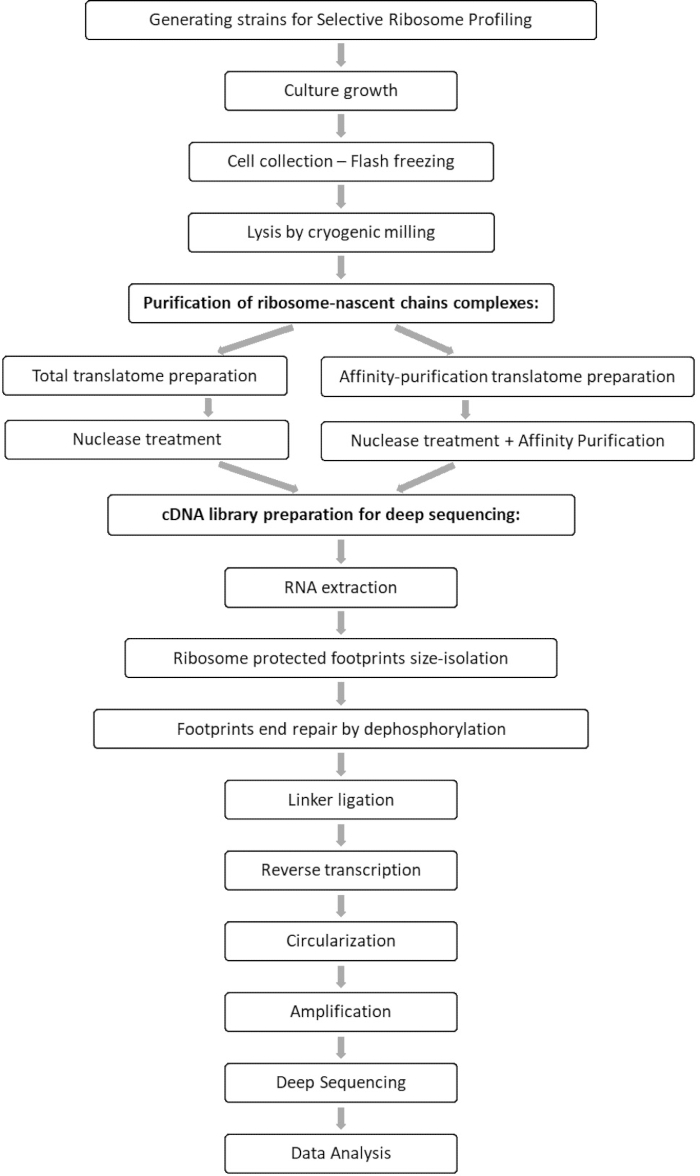
Figur 1: En oversigt over SeRP-protokollen. Denne protokol kan udføres i sin helhed inden for 7-10 dage. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Her beskriver protokollen selective ribosome profileringsmetoden til indfangning af co-translationelle interaktioner i nær codonopløsning. Da ribosomet stiger som et knudepunkt for koordinering af den spirende kæde fremkomst i den overfyldte cytoplasma, er dette en afgørende metode til at identificere og karakterisere de forskellige co-translationelle interaktioner, der kræves for at sikre et funktionelt proteom samt til at studere forskellige sygdomme. Til dato er SeRP den eneste metode, der kan fange og karakteri…
Declarações
The authors have nothing to disclose.
Acknowledgements
Vi vil gerne takke alle laboratoriemedlemmerne for frugtbare diskussioner og Muhammad Makhzumy for den kritiske læsning af manuskriptet. Dette arbejde blev finansieret af ISF (Israeli Science Foundation) bevilling 2106/20.
Materials
| 3'-Phosphorylated 28 nt RNA control oligonucleotide | IDT | custom order | RNase free HPLC purification; 5'-AUGUAGUCGGAGUCGAGGCGC GACGCGA/3Phos/-3' |
| Absolute ethanol | VWR | 20821 | |
| Acid phenol–chloroform | Ambion | AM9722 | |
| Antibody: mouse monclonal anti-HA | Merck | 11583816001 | 12CA5 |
| Aprotinin | Roth | A162.3 | |
| ATP* | NEB | P0756S | 10 mM |
| Bacto agar | BD | 214030 | |
| Bacto peptone | BD | 211820 | |
| Bacto tryptone | BD | 211699 | |
| Bacto yeast extract | BD | 212720 | |
| Bestatin hydrochloride | Roth | 2937.2 | |
| Chloroform | Merck | 102445 | |
| CircLigase II ssDNA Ligase* | Epicentre | CL9025K | 100 U/μL |
| Colloidal Coomassie staining solution | Roth | 4829 | |
| cOmplete, EDTA-free protease inhibitor cocktail tablets | Roche Diagnostics | 29384100 | |
| Cycloheximide | Biological Industries | A0879 | |
| DEPC treated and sterile filtered water* | Sigma | 95284 | |
| D-Glucose anhydrous | Merck | G5767-500G | |
| Diethylpyrocarbonate | Roth | K028 | |
| Dimethylsulfoxide* | Sigma-Aldrich | 276855 | |
| DNA ladder, 10 bp O'RangeRuler* | Thermo Fisher Scientific | SM1313 | |
| DNA loading dye* | Thermo Fisher Scientific | R0631 | 6× |
| DNase I, recombinant | Roche | 4716728001 | RNAse free |
| dNTP solution set* | NEB | N0446S | |
| EDTA* | Roth | 8043 | |
| Glycerol | VWR | 24388.260. | |
| Glycine solution | Sigma-Aldrich | 67419-1ML-F | 1 M |
| GlycoBlue | Ambion | AM9516 | 15 mg/mL |
| HEPES | Roth | HN78.3 | |
| HF Phusion polymerase* | NEB | M0530L | |
| HK from S. cerevisiae | Sigma-Aldrich | H6380-1.5KU | |
| Hydrochloric acid | AppliChem | A1305 | |
| Isopropanol | Sigma-Aldrich | 33539 | |
| Isopropyl β-D-1-thiogalactopyranoside | Roth | CN08 | |
| Kanamycin | Roth | T832.4 | |
| KCl | Roth | 6781.1 | |
| KH2PO4 | Roth | 3904.1 | |
| Leupeptin | Roth | CN33.4 | |
| Linker L(rt) | IDT | custom order | |
| Liquid nitrogen | |||
| MgCl2 | Roth | KK36.3 | |
| Na2HPO4 | Roth | P030.2 | |
| Na2HPO4·2H2O | Roth | T879.3 | |
| NaCl* | Invitrogen | AM97606 | 5 M |
| NaH2PO4·H2O | Roth | K300.2 | |
| NHS-activated Sepharose 4 fast-flow beads | GE Life Sciences | 17090601 | |
| Nonidet P 40 substitute | Sigma | 74385 | |
| Pepstatin A | Roth | 2936.2 | |
| Phenylmethyl sulfonyl fluoride | Roth | 6367 | |
| Precast gels | Bio-Rad | 5671034 | 10% and 12% |
| RNase I | Ambion | AM2294 | |
| SDS, 20% | Ambion | AM9820 | RNase free |
| Sodium acetate* | Ambion | AM9740 | 3 M, pH 5.5 |
| Sodium azide | Merck | S8032-100G | |
| Sodium chloride | Roth | 9265 | |
| Sodium hydroxide* | Sigma | S2770 | 1 N |
| Sucrose | Sigma-Aldrich | 16104 | |
| SUPERase-In RNase Inhibitor | Ambion | AM2694 | |
| Superscript III Reverse Transciptase* | Invitrogen | 18080-044 | |
| SYBR Gold* | Invitrogen | S11494 | |
| T4 polynucleotide kinase* | NEB | M0201L | |
| T4 RNA ligase 2* | NEB | M0242L | |
| TBE polyacrylamide gel* | Novex | EC6215BOX | 8% |
| TBE–urea polyacrylamide gel* | Novex | EC68752BOX | 10% |
| TBE–urea polyacrylamide gel* | Novex | EC6885BOX | 15% |
| TBE–urea sample buffer* | Novex | LC6876 | 2× |
| Tris | Roth | 4855 | |
| Tris* | Ambion | AM9851 | 1 M, pH 7.0 |
| Tris* | Ambion | AM9856 | 1 M, pH 8.0 |
| UltraPure 10× TBE buffer* | Invitrogen | 15581-044 | |
| * – for library preparation | |||
| gasket and spring clamp , 90 mm, | Millipore | XX1009020 | |
| ground joint flask 1 L , | Millipore | XX1504705 |
Referências
- Oh, E., et al. Selective ribosome profiling reveals the cotranslational chaperone action of trigger factor in vivo. Cell. 147 (6), 1295-1308 (2011).
- Shiber, A., et al. Cotranslational assembly of protein complexes in eukaryotes revealed by ribosome profiling. Nature. 561 (7722), 268-272 (2018).
- Becker, A. H., Oh, E., Weissman, J. S., Kramer, G., Bukau, B. Selective ribosome profiling as a tool for studying the interaction of chaperones and targeting factors with nascent polypeptide chains and ribosomes. Nature Protocols. 8 (11), 2212-2239 (2013).
- Galmozzi, C. V., Merker, D., Friedrich, U. A., Döring, K., Kramer, G. Selective ribosome profiling to study interactions of translating ribosomes in yeast. Nature Protocols. , (2019).
- Knorr, A. G., et al. Ribosome-NatA architecture reveals that rRNA expansion segments coordinate N-terminal acetylation. Nature Structural and Molecular Biology. 26 (1), 35-39 (2019).
- Matsuo, Y., Inada, T. The ribosome collision sensor Hel2 functions as preventive quality control in the secretory pathway. Cell Reports. 34 (12), (2021).
- Döring, K., et al. Profiling Ssb-Nascent chain interactions reveals principles of Hsp70-assisted folding. Cell. , (2017).
- Chartron, J. W., Hunt, K. C. L., Frydman, J. Cotranslational signal-independent SRP preloading during membrane targeting. Nature. 536 (7615), 224-228 (2016).
- Janke, C., et al. A versatile toolbox for PCR-based tagging of yeast genes: New fluorescent proteins, more markers and promoter substitution cassettes. Yeast. 21 (11), 947-962 (2004).
- Levi, O., Arava, Y. Expanding the CRISPR/Cas9 Toolbox for Gene Engineering in S. cerevisiae. Current Microbiology. 77 (3), 468-478 (2020).
- Giannoukos, G., et al. Efficient and robust RNA-seq process for cultured bacteria and complex community transcriptomes. Genome Biology. 13 (3), 23 (2012).
- . Illumina Index Adapters – Pooling Guide Available from: https://support.illumina.com/content/dam/illumina-support/documents/documentation/chemistry_documentation/experiment-design/index-adapters-pooling-guide-1000000041074-05.pdf (2019)
- Kanagawa, T. Bias and artifacts in multitemplate polymerase chain reactions (PCR). Journal of Bioscience and Bioengineering. 96 (4), 317-323 (2003).
- Bertolini, M., et al. Interactions between nascent proteins translated by adjacent ribosomes drive homomer assembly. Science. 371 (6524), (2021).
- Kramer, G., Shiber, A., Bukau, B. Mechanisms of cotranslational maturation of newly synthesized proteins. Annual Review of Biochemistry. 88, 337-364 (2019).
- Joazeiro, C. A. P. Mechanisms and functions of ribosome-associated protein quality control. Nature Reviews Molecular Cell Biology. 20 (6), 368-383 (2019).
- Beaupere, C., Chen, R. B., Pelosi, W., Labunskyy, V. M. Genome-wide quantification of translation in budding yeast by ribosome profiling. Journal of Visualized Experiments: JoVE. (130), e56820 (2017).

