Langsgående intravital mikroskopi ved hjelp av et mammary imaging vindu med utskiftbart lokk
Summary
Denne protokollen beskriver et nytt pattedyr bildevindu med et utskiftbart lokk (R.MIW). Intravital mikroskopi etter implantasjon av R.MIW gir mulighet for langsgående og flerdagers avbildning av den sunne og syke brystkjertelen med cellulær oppløsning i de forskjellige utviklingsstadiene.
Abstract
Brystkjertelens forgrenede struktur er svært dynamisk og gjennomgår flere faser av vekst og ombygging etter fødselen. Intravital mikroskopi i kombinasjon med hudklaffkirurgi eller implantasjon av bildevinduer har blitt brukt til å studere dynamikken i den sunne brystkjertelen på forskjellige utviklingsstadier. De fleste pattedyravbildningsteknologier er begrenset til en tidsramme på timer til dager, mens de fleste brystkjerteloppussingsprosesser forekommer i tidsrammer på dager til uker. For å studere ombygging av brystkjertelen, er det nødvendig med metoder som tillater optisk tilgang til vev av interesse for lengre tidsrammer. Her beskrives en forbedret versjon av titanpattedyravbildningsvinduet med et utskiftbart lokk (R.MIW) som tillater høyoppløselig bildebehandling av brystkjertelen med cellulær oppløsning i opptil flere uker. Det er viktig at R.MIW gir vevstilgang gjennom hele varigheten av det intravitale bildebehandlingseksperimentet og kan derfor brukes til lokal vevsmanipulering, merking, legemiddeladministrasjon eller bildestyrt mikrodeseksjon. Samlet sett muliggjør R.MIW høyoppløselig karakterisering av cellulær dynamikk under utvikling av brystkjertelen, homeostase og sykdom.
Introduction
Pattedyrepitelet er et unikt sekretorisk organ tilstede hos pattedyr, som produserer og utskiller melk for å nære avkom. Gjennom livet gjennomgår brystkjertelen flere runder med utvikling og vekst, som er ledsaget av strukturelle og funksjonelle endringer i vevet1. Avhengig av utviklingsstadiet er celletypene som bidrar til vevsoppussing forskjellige, samt plasseringen i kanaltreet.
Multiphoton intravital mikroskopi (IVM) tillater studiet av mammarycelledynamikk in vivo i den innfødte og minimalt perturberte innstillingen 2,3,4. For å få visuell tilgang til brystkjertelen har flere midlertidige ex vivo– eller hudklaffavbildningsteknikker blitt publisert i ulike stadier av brystkjertelutvikling, inkludert pubertet 4,5,6,7, voksen alder 2,8, amming 9,10,11,12 og tumordynamikk 13,14 ,15. Selv om disse teknikkene resulterer i høy romlig og tidsmessig løst avbildning av pattedyrcelledynamikk, er tidsrammen begrenset til timer, mens de fleste brystkjerteloppussingsprosesser tar dager til uker. Derfor er det nødvendig med metoder som tillater optisk tilgang til vev av interesse for lengre tidsrammer. Gjennom årene har flere permanente bildevinduer blitt utviklet for mammary tumor imaging 15,16,17,18, inkludert en titan pattedyr bildevindu (MIW)2,3,19. Selv om det var veldig nyttig å studere brystsvulstvekst, forble visualisering av den sunne brystkjertelstrukturen begrenset til noen dager. Nylig ble det utviklet et fleksibelt silisiumavbildningsvindu, som tillater visualisering av pubertal brystkjertelen over flere uker20. Brystkjertelen er imidlertid innebygd i en adipocyttrik fettpute, noe som fører til omfattende lysspredning og som et resultat begrenset synlighet av brystkanalstrukturene. Derfor er det nødvendig med overlegne bildeforhold til enhver tid for å visualisere vevsdynamikk over lengre perioder i brystkjertelen. Verken den klassiske MIW, eller det fleksible silisiumvinduet tillater vevsmanipulering eller optimalisering av fysisk vevsplassering før avbildning, da vinduet danner et lukket system etter kirurgi og implantasjon. Som et resultat vil optimal optisk tilgang til det underliggende pattedyrvevet sannsynligvis bli utelukket over lengre tidsperioder. I motsetning tillater hudklaffteknikken optimalisering og omplassering av vevet under bildebehandlingsøkten, og en hudklaff kan gjentas flere ganger2. Gjentatte bildebehandlingsøkter gjennom en hudklaff er imidlertid bare mulig når tilstrekkelig tid (minst 7 dager) tildeles mellom operasjoner for å tillate gjenoppretting av huden og derfor hovedsakelig er egnet til å studere prosesser på lengre tidsskalaer. Videre er det tilrådelig å ikke utføre denne prosedyren mange ganger på grunn av sin invasive natur og stor risiko for infeksjoner og arrdannelse ved sårlukking.
For å overvinne disse begrensningene, det vil si for å sikre optimale bildeforhold i en lengre periode med høy frekvens og samtidig tillate vevsmanipulering, ble en forbedret titanversjon av MIW med et utskiftbart lokk (R.MIW) designet for å visualisere den sunne og syke brystkjertelen over flere dager til uke2 (figur 1A, B). R.MIW ble spesialdesignet for å gi optimal vevstilgang, noe som muliggjør direkte vevsmanipulering over hele IVM-eksperimentets varighet, og tillater dermed visualisering av brystkjertelen til rett tid og sted over lengre perioder. Når R.MIW er lukket, danner den et lufttett system som kan sammenlignes med den klassiske MIW (figur 1C). Når det åpnes under aseptiske forhold, tillater R.MIW lokal vevsmanipulering for å forbedre optisk tilgang og muliggjør også lokal administrering av stoffer, for eksempel veihemmere eller agonister, injeksjon av forskjellige celletyper av interesse, for eksempel kreftcelle- eller immuncellepopulasjoner, eller tilsetning av vevsmerkingsfarger. Lokket kan åpnes når som helst mellom bildebehandlingsøkter uten å forårsake skade på det underliggende vevet.
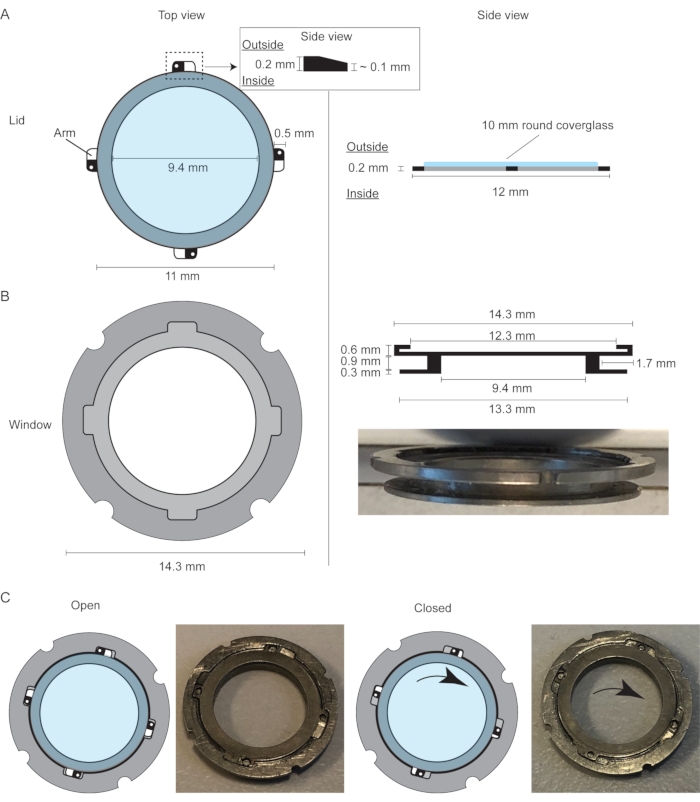
Figur 1: Utformingen av pattedyravbildningsvinduet med et utskiftbart lokk. (A) Ovenfra og sidevisning av det utskiftbare lokket på mammary imaging-vinduet med et 10 mm dekselglass limt til ringen. (B) Toppvisning og sidevisning av pattedyrets bildevindu, som består av en ytre ring og indre ring med et spor i mellom for å sikre vinduet i musens hud ved hjelp av en veskestreng sutur. Den ytre ringen har et lite spor som passer til de fire fremspringene (armene) på lokket. (C) Tegneserie og bilder som demonstrerer åpningen og lukkemekanismene på lokket. Skråkantene sørger for at lokket er festet inne i vindusrammen. Denne figuren er endret fra Messal et al. 2. Klikk her for å se en større versjon av denne figuren.
Denne protokollen beskriver design- og implantasjonsprosedyren til R.MIW, samt en langsgående IVM-strategi for å besøke de samme brystkanalene og deres visualisering med cellulær oppløsning. R.MIW tillater følgende celledelinger og morfologiske endringer i ulike utviklingsfaser av brystkjertelen i forskjellige fluorescerende reportermusmodeller. Samlet sett letter R.MIW høyoppløselig karakterisering av cellulær dynamikk under brystkjertelutvikling, homeostase og sykdom.
Protocol
Representative Results
Discussion
R.MIW tillater langsgående avbildning av den sunne og syke brystkjertelen i sitt opprinnelige og minimalt forstyrrede miljø og tillater gjentatt visualisering av brystkjertelen på ulike utviklingsstadier. R.MIW-designen gjør at vinduet kan åpnes når som helst under eksperimentet. Langsiktig visuell tilgang til vev av interesse kan hindres, for eksempel ved opphopning av celleavfall på dekslene. I slike tilfeller kan R.MIW åpnes før eller umiddelbart etter en bildeøkt for å tillate rengjøring av hele det synlige vevsområdet og lokket. Det avtakbare lokket tillater også manipulasjoner av vevet, samt lokal påføring av stoffer, for eksempel spesifikke hemmere og terapier, merking av fargestoffer eller spesifikke celletyper av interesse.
Denne metoden overvinner begrensningen av de tidligere beskrevne mammary hudklaffprosedyrene 4,7,8,13, som er begrenset til en bildeøkt, og kan visualisere prosesser som forgrening av morfogenese (figur 5), homeostatisk vevsomsetning (figur 6) eller tumorvekst på cellenivå (figur 3B ). Likevel tillater R.MIW samtidig lokal manipulering av vevet mellom bildebehandlingsøkter, som utgjør en stor ressurs for R.MIW sammenlignet med den tidligere publiserte MIW 3,18 og alle andre bildevinduer 20,22. Når du åpner R.MIW, er det viktig å opprettholde aseptiske forhold til enhver tid for å forhindre infeksjonskilde. Muligheten til å åpne R.MIW i et aseptisk miljø gjør det mulig å optimalisere bildeforholdene før hver bildeøkt, noe som i stor grad forbedrer langsiktig visuell tilgang til interessevevet. Spesielt i brystkjertelen, som er innebygd i en adipocyttrik stroma, er dette av stor verdi. Videre kan det utskiftbare lokket unikt muliggjøre lokal administrering av terapeutiske behandlinger, forskjellige celletyper, merking av fargestoffer, bildestyrt mikrodeseksjon eller annen lokal manipulering av vevet uten å måtte avslutte IVM-eksperimentet. For eksempel, for å studere tumorinitiering, kan spesifikke kreftcellepopulasjoner injiseres direkte i kanaltreet eller stroma på et bestemt IVM-tidspunkt og presist brystkjertelplassering, så lenge denne avkastningen er tilgjengelig gjennom R.MIW-ringen. For å studere tumorprogresjon kan spesifikke kreftcellepopulasjoner (på et bestemt sted, i et bestemt mikromiljø eller med en bestemt oppførsel) bli fotomerket under IVM-økten og deretter mikrodissert ved hjelp av et fluorescerende disseksjonsmikroskop etter åpningen av R.MIW. Isolerte celler kan viderebehandles for nedstrømsanalyser, for eksempel (encellet) mRNA-sekvensering. Ved å bruke denne tilnærmingen kan man koble in vivo-celleatferd til molekylære uttrykksprofiler. Fordelen med lokal legemiddeladministrasjon aktivert av R.MIW gjør at vevet kan avbildes før og direkte etter behandling. Intervallet som trengs for å fjerne musen fra bildeboksen og deretter utføre lokal legemiddeladministrasjon etter åpning av R.MIW-lokket, kan utføres på få minutter, noe som gjør det mulig å fange opp hurtigvirkende legemidler umiddelbart.
Vi viser at IVM av brystkjertelen gjennom R.MIW er kompatibel med mange forskjellige fluorescerende reportermusmodeller. Det fettrike miljøet er utfordrende å avbilde, og derfor anbefales bruk av lyse fluoroforer. Som vist her, kan imidlertid enda mindre lyse fluoroforer som mCFP visualiseres gjennom R.MIW under optimale bildeforhold. Uunngåelig vil fettputen utelukke avbildningen av de dypere kanalstrukturene, og begrense avbildningen til de mer overfladiske kanalene. Et oversiktsbilde med lav oppløsning ved starten av hvert IVM-eksperiment vil bidra til å identifisere de ductale strukturene av interesse som er tilstrekkelig overfladiske for høyoppløselig avbildning. Lokal vevsmanipulering, fjerning av bindevev eller reposisjonering av fettvevet etter åpning av R.MIW kan optimalisere IVM for spesifikke ROIer som er overlagt av fettvev. Dette er en viktig fordel i forhold til alle tidligere vindusdesign, som ikke tillater å utføre disse manipulasjonene og vil kreve fullstendig fjerning av selve vinduet. Spesielt for visualisering av den inguinale lymfeknuten, anbefales det å forsiktig fjerne det overdrevne fettvevet, noe som reduserer lysspredning og muliggjør høyoppløselig avbildning. Når du manipulerer vevet, må du alltid holde aseptiske forhold og forhindre blødning eller alvorlig skade på vevet, da de kan påvirke prosessene som studeres under IVM-eksperimentet.
R.MIW er laget av titan, et materiale som vanligvis brukes i klinisk praksis for å erstatte harde vev som ledd eller benplater. Titan har flere fordeler i forhold til stålvinduer, inkludert den lette og inerte karakteren21. Nylig ble flere andre materialer brukt til å generere nye bildevindustyper, inkludert det fleksible silisiumvinduet20. I motsetning til R.MIW krever det fleksible vinduet ingen suturer for implantasjon og er egnet for nesten enhver anatomisk posisjon, spesielt når det gjelder mykt og skjøre vev. Silisiumvinduer har minimal innvirkning på dyremotiliteten på grunn av deres lette og deformerbare natur og kanskje mer egnet i eksperimenter som studerer rask vevsutvidelse og vekst20. En annen fordel i forhold til titanversjonen er at silisiumvinduer er kompatible med andre bildemodaliteter, inkludert magnetisk resonansavbildning20,27. Det vil imidlertid være viktig å huske på at målene er optimalisert for 0,17 mm glassdeksler. Videre er pattedyrvev utsatt for pustebevegelser, som er vanskelig å begrense ved hjelp av det fleksible vinduet, spesielt når du bruker et invertert mikroskop. Pusteartefakter minimeres av R.MIW-designen og fikseringen av R.MIW i avbildningsboksens innlegg. Som et resultat er bilder som er anskaffet ved hjelp av det foreslåtte R.MIW-oppsettet, ikke forvrengt på grunn av pusteartefakter. Imidlertid kan mindre operasjoner i vev lokalisering oppstå, som vanligvis er gradvise og kan korrigeres ved hjelp av post-oppkjøp bevegelseskorrigering programvare28. Med den økende verktøykassen til IVM-teknologier 2,20, vil de spesifikke kravene for hvert eksperiment til slutt bestemme den beste måten å in vivo visualisering av vevet av interesse. Ulike vindusdesign har forskjellige fordeler og ulemper, og avhengig av forskningsspørsmålet, det tilgjengelige mikroskopioppsettet, den nødvendige romlige og tidsmessige oppløsningen, og den totale tidsperioden for den studerte prosessen, må den optimale tilnærmingen bestemmes.
Oppsummert letter R.MIW høyoppløselig karakterisering av cellulær dynamikk under brystkjertelutvikling, homeostase og sykdom over flere dager til uker.
Declarações
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av Forskningsstiftelsen Flandern (PhD grant fundamental research 11L7222N to M.C.), Boehringer Ingelheim Foundation (PhD Fellowship to C.L.G.J.S), et EMBO postdoktorstipend (stipend ALTF 1035-2020 til C.L.G.J.S.), og Doctor Josef Steiner Award (til J.v.R.).
Materials
| 0.9% NaCl | BD | 306573 | Other brands available |
| 10 mm round coverglass | Fisher scientific | 10696365 | Other brands available |
| 5-0 braided silk suturs | Ethicon | W580 | |
| 80% Ethanol | homemade | NA | |
| Anesthesia induction box | Kentscientific | VetFlo-MSEKIT | |
| Buprenorphine (Vetergesic®) | Ecuphar | NA | |
| Cotton tips (sterile) | Fisher scientific | 13113743 | Other brands available |
| Cyanoacrylate adhesive | Loctite | NA | Other brands available |
| Eye ointment | Duratears | NA | |
| Flexible butterfly needle | Greiner Bio-One | 450120 | Other brands available |
| Graefe forceps (blunt) | Fine Science Tools | 11051-10 | |
| Heating pad | Kentscientific | RightTemp Jr. | Other brands available |
| Imaging box | Custom made | NA | |
| Infuse nutrient mixture | Braun | Nutriflex special 70/240 | |
| Insulin syringes | BD | 324911 | Other brands available |
| Inverted multi-photon microscope with automated stage | Leica Microsystems | NA | |
| Isoflurane vaporizer | Kentscientific | VetFlo-1231K | |
| Needle holder | Fine Science Tools | 12510-14 | |
| Parafilm | Sigma-Aldrich | P7793 | semi-transparent tape |
| Paper tape tesa | Tesa | NA | |
| Petroleum Jelly | Vaseline | NA | |
| Razor blades | Fisher scientific | 11904325 | Other brands available |
| Silicon tubing | Solutions Elastomeres | NA | Any houseware |
| Spring scissors (small) | Fine Science Tools | 15018-10 | |
| Sterile PBS | ThermoFisher Scientific | 10010023 | |
| Syringe (10 ml) | BD | 305482 | Other brands available |
| Thin forceps | Fine Science Tools | 11413-11 | |
| Titanium lid for mammary imaging window | Custom made | NA | |
| Titanium mammary imaging window | Custom made | NA | |
| Wooden sticks toothpicks | Fisher scientific | NC1678836 | Other brands available |
Referências
- Watson, C. J., Khaled, W. T. Mammary development in the embryo and adult: new insights into the journey of morphogenesis and commitment. Development. 147 (22), (2020).
- Messal, H. A., van Rheenen, J., Scheele, C. L. G. J. An Intravital Microscopy Toolbox to Study Mammary Gland Dynamics from Cellular Level to Organ Scale. Journal of Mammary Gland Biology and Neoplasia. 26 (1), 9-27 (2021).
- Kedrin, D., et al. Intravital imaging of metastatic behavior through a mammary imaging window. Nature Methods. 5 (12), 1019-1021 (2008).
- Dawson, C. A., Mueller, S. N., Lindeman, G. J., Rios, A. C., Visvader, J. E. Intravital microscopy of dynamic single-cell behavior in mouse mammary tissue. Nature Protocols. 16 (4), 1907-1935 (2021).
- Scheele, C. L., et al. Identity and dynamics of mammary stem cells during branching morphogenesis. Nature. 542 (7641), 313-317 (2017).
- Kotsuma, M., et al. Nondestructive, serial in vivo imaging of a tissue-flap using a tissue adhesion barrier. IntraVital. 1 (1), 69-76 (2012).
- Ingman, W. V., Wyckoff, J., Gouon-Evans, V., Condeelis, J., Pollard, J. W. Macrophages promote collagen fibrillogenesis around terminal end buds of the developing mammary gland. Developmental Dynamics: an official publication of the American Association of Anatomists. 235 (12), 3222-3229 (2006).
- Entenberg, D., et al. large-volume, high-resolution intravital imaging for tissue-wide analysis of single cell dynamics. Methods (San Diego, Calif). 128, 65-77 (2017).
- Masedunskas, A., Weigert, R., Mather, I. H. Intravital Imaging of the Lactating Mammary Gland in Transgenic Mice Expressing Fluorescent Proteins. Advances in Intravital Microscopy. , 187-204 (2014).
- Masedunskas, A., Chen, Y., Stussman, R., Weigert, R., Mather, I. H. Kinetics of milk lipid droplet transport, growth, and secretion revealed by intravital imaging: lipid droplet release is intermittently stimulated by oxytocin. Molecular Biology of the Cell. 28 (7), 935-946 (2017).
- Mather, I. H., Masedunskas, A., Chen, Y., Weigert, R. Symposium review: Intravital imaging of the lactating mammary gland in live mice reveals novel aspects of milk-lipid secretion. Journal of Dairy Science. 102 (3), 2760-2782 (2019).
- Stevenson, A. J., et al. Multiscale imaging of basal cell dynamics in the functionally mature mammary gland. Proceedings of the National Academy of Sciences. 117 (43), 26822-26832 (2020).
- Ewald, A. J., Werb, Z., Egeblad, M. Preparation of Mice for Long-Term Intravital Imaging of the Mammary Gland. Cold Spring Harbor Protocols. 2011 (2), 5562 (2011).
- Ewald, A. J., Werb, Z., Egeblad, M. Monitoring of Vital Signs for Long-Term Survival of Mice under Anesthesia. Cold Spring Harbor Protocols. 2011 (2), 5563 (2011).
- Harney, A. S., Wang, Y., Condeelis, J. S., Entenberg, D. Extended Time-lapse Intravital Imaging of Real-time Multicellular Dynamics in the Tumor Microenvironment. Journal of Visualized Experiments: JoVE. (112), e54042 (2016).
- Harper, K. L., et al. Mechanism of early dissemination and metastasis in Her2+ mammary cancer. Nature. 540 (7634), 588-592 (2016).
- Sobolik, T., et al. Development of novel murine mammary imaging windows to examine wound healing effects on leukocyte trafficking in mammary tumors with intravital imaging. IntraVital. 5 (1), 1125562 (2016).
- Shan, S., Sorg, B., Dewhirst, M. W. A novel rodent mammary window of orthotopic breast cancer for intravital microscopy. Microvascular Research. 65 (2), 109-117 (2003).
- Zomer, A., et al. Intravital imaging of cancer stem cell plasticity in mammary tumors. Stem Cells. 31 (3), 602-606 (2013).
- Jacquemin, G., et al. Longitudinal high-resolution imaging through a flexible intravital imaging window. Science Advances. 7 (25), (2021).
- Niinomi, M. Recent research and development in titanium alloys for biomedical applications and healthcare goods. Science and Technology of Advanced Materials. 4 (5), 445-454 (2003).
- Ritsma, L., et al. Surgical implantation of an abdominal imaging window for intravital microscopy. Nature Protocols. 8 (3), 583-594 (2013).
- Muzumdar, M. D., Tasic, B., Miyamichi, K., Li, N., Luo, L. A global double-fluorescent cre reporter mouse. Genesis. 45 (9), 593-605 (2007).
- Snippert, H. J., et al. Intestinal Crypt Homeostasis Results from Neutral Competition between Symmetrically Dividing Lgr5 Stem Cells. Cell. 143 (1), 134-144 (2010).
- Nowotschin, S., Hadjantonakis, A. K. Use of KikGR a photoconvertible green-to-red fluorescent protein for cell labeling and lineage analysis in ES cells and mouse embryos. BMC Developmental Biology. 9, 49 (2009).
- Kurotaki, Y., Hatta, K., Nakao, K., Nabeshima, Y. I., Fujimori, T. Blastocyst Axis Is Specified Independently of Early Cell Lineage But Aligns with the ZP Shape. Science. 316 (5825), 719-723 (2007).
- Heo, C., et al. A soft, transparent, freely accessible cranial window for chronic imaging and electrophysiology. Scientific Reports. 6, 27818 (2016).
- Warren, S. C., et al. Removing physiological motion from Intravital and clinical functional imaging data. eLife. 7, 35800 (2018).

