Microtensiometer voor confocale microscopie visualisatie van dynamische interfaces
Summary
Dit manuscript beschrijft het ontwerp en de werking van een microtensiometer / confocale microscoop om gelijktijdige metingen van interfaciale spanning en oppervlaktedilatationale reologie uit te voeren terwijl de interfaciale morfologie wordt gevisualiseerd. Dit biedt de real-time constructie van structuur-eigenschap relaties van interfaces die belangrijk zijn in technologie en fysiologie.
Abstract
Adsorptie van oppervlakte-actieve moleculen aan vloeistof-vloeistof interfaces is alomtegenwoordig in de natuur. Het karakteriseren van deze interfaces vereist het meten van adsorptiesnelheden van oppervlakteactieve stoffen, het evalueren van evenwichtsoppervlakspanningen als een functie van de bulkoppervlakteactieve stofconcentratie en het relateren van hoe oppervlaktespanning verandert met veranderingen in het interfaciale gebied na equilibratie. Gelijktijdige visualisatie van de interface met behulp van fluorescentiebeeldvorming met een snelle confocale microscoop maakt de directe evaluatie van structuur-functierelaties mogelijk. In de capillaire drukmicrotensiometer (CPM) wordt een hemisferische luchtbel aan het einde van het capillair vastgepind in een vloeistofreservoir met een volume van 1 ml. De capillaire druk over de belleninterface wordt geregeld via een commerciële microfluïdische stroomregelaar die modelgebaseerde druk, bubbelkromming of bubbelgebiedregeling mogelijk maakt op basis van de Laplace-vergelijking. In vergelijking met eerdere technieken zoals de Langmuir trog en hanger drop, zijn de meet- en regelprecisie en responstijd sterk verbeterd; capillaire drukvariaties kunnen in milliseconden worden toegepast en geregeld. De dynamische respons van de bubbelinterface wordt gevisualiseerd via een tweede optische lens terwijl de bel uitzet en samentrekt. De bubbelcontour is geschikt voor een cirkelvormig profiel om de krommingsradius van de bel, R, te bepalen, evenals eventuele afwijkingen van circulariteit die de resultaten ongeldig zouden maken. De Laplace-vergelijking wordt gebruikt om de dynamische oppervlaktespanning van de interface te bepalen. Na equilibratie kunnen kleine drukoscillaties worden opgelegd door de computergestuurde microfluïdische pomp om de bubbelradius (frequenties van 0,001-100 cycli / min) te oscilleren om de dilatatiemodulus te bepalen De totale afmetingen van het systeem zijn zo klein dat de microtensiometer onder de lens van een snelle confocale microscoop past, waardoor fluorescerend gelabelde chemische soorten kwantitatief kunnen worden gevolgd met submicron laterale resolutie.
Introduction
Lucht-water interfaces bedekt met oppervlakteactieve films zijn alomtegenwoordig in het dagelijks leven. Oppervlakteactieve waterinjecties worden gebruikt om de oliewinning uit uitgeputte velden te verbeteren en worden gebruikt als hydraulische breukoplossingen voor schaliegas en -olie. Gas-vloeistof schuimen en vloeistof-vloeistof emulsies zijn gebruikelijk voor veel industriële en wetenschappelijke processen als smeermiddelen en reinigingsmiddelen en komen veel voor in voedsel. Oppervlakteactieve stoffen en eiwitten op interfaces stabiliseren antilichaamconformaties tijdens verpakking, opslag en toediening 1,2,3,4,5, scheurfilmstabiliteit in het oog 6,7,8 en longmechanica 9,10,11,12,13,14, 15.
De studie van oppervlakteactieve stoffen of oppervlakteactieve stoffen die adsorberen aan interfaces en hun eigenschappen heeft een lange geschiedenis met veel verschillende experimentele technieken 16,17,18,19,20,21,22,23,24,25,26,27 . Een recente ontwikkeling is de capillaire drukmicrotensiometer (CPM), die het onderzoek van interfaciale eigenschappen op sterk gekromde interfaces mogelijk maakt, op veel kleinere lengteschalen, terwijl aanzienlijk minder materialen worden gebruikt dan andere gangbare methoden 9,23,24,25. Confocale fluorescentiemicroscopie (CFM) kan worden gebruikt om de morfologie van lipiden en eiwitten te bestuderen op de lucht-waterinterfaces in de CPM22 of op Langmuir-troggen 20,26,27,28,29. Hier zijn een CPM en CFM gecombineerd om morfologische verschijnselen te verbinden met dynamische en evenwichtsinterfaciale eigenschappen om structuur-functierelaties te ontwikkelen voor biologische en technologische interfaces.
Er zijn tal van parameters van belang in interfaciale oppervlakteactieve systemen die toegankelijk zijn voor de CPM-CFM. In de CPM wordt een luchtbel met een diameter van 30-200 μm vastgepind aan de punt van een glazen capillaire buis. In eerdere versies van de CPM werd het capillaire drukverschil tussen de binnen- en buitenkant van de bel geregeld via een waterkolom en een oscillerende spuitpomp 9,30 ; de hier beschreven nieuwe versie vervangt deze door een hogere precisie, computergestuurde microfluïdische pomp. De oppervlaktespanning (γ) wordt bepaald via de Laplace-vergelijking, ΔP = 2γ/R, uit de drukval over het door de pomp ingestelde interface, ΔP, en optische analyse van de kromtestraal van de bel, R. De dynamische oppervlaktespanning van de interface kan worden bepaald met een tijdresolutie van 10 ms na het genereren van een nieuwe bel in contact met een bulkvloeistof die een oplosbare oppervlakteactieve stof bevat. De adsorptiedynamiek van oppervlakteactieve stoffen kan worden beschreven met de klassieke Ward-Tordai-vergelijking10,31 om essentiële eigenschappen van de oppervlakteactieve stof te bepalen, waaronder de diffusiviteit, oppervlaktedekking en de relatie tussen bulkconcentratie en evenwichtsoppervlaktespanning. Zodra een evenwichtsoppervlaktespanning is bereikt, kan het interfaciale gebied worden geoscilleerd om de dilatatiemodulus te meten, 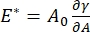 door de veranderingen in oppervlaktespanning te registreren, geïnduceerd door kleine veranderingen in het beloppervlak, A32. Voor complexere interfaces die hun eigen interne structuren ontwikkelen, zoals verstrengelde polymeren of eiwitten, wordt de oppervlaktespanning, , vervangen door een meer algemene oppervlaktespanning 4,33,
door de veranderingen in oppervlaktespanning te registreren, geïnduceerd door kleine veranderingen in het beloppervlak, A32. Voor complexere interfaces die hun eigen interne structuren ontwikkelen, zoals verstrengelde polymeren of eiwitten, wordt de oppervlaktespanning, , vervangen door een meer algemene oppervlaktespanning 4,33, 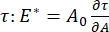 .
.
Longstabiliteit tijdens de ademhaling kan direct worden gekoppeld aan het handhaven van zowel een lage oppervlaktespanning als een hoge dilatatiemodulus op de alveolaire lucht-vloeistofinterface 9,10. Alle interne longoppervlakken zijn bekleed met een continue, micron dikke film van epitheliale voeringvloeistof om weefselhydratatie te behouden34. Deze epitheliale voeringvloeistof is voornamelijk water, met zouten en verschillende andere eiwitten, enzymen, suikers en longsurfactant. Zoals het geval is voor elke gebogen vloeistof-dampinterface, wordt een capillaire druk geïnduceerd met de druk hoger aan de binnenkant van de alveolus (of bel). Als de oppervlaktespanning echter overal in de longen constant was, laat de Laplace-vergelijking, ΔP = 2γ / R, zien dat kleinere longblaasjes een hogere interne druk zouden hebben ten opzichte van grotere longblaasjes, waardoor het gasgehalte van de kleinere longblaasjes naar grotere longblaasjes met lagere druk zou stromen. Dit staat bekend als “Laplace Instability”9,35. Het nettoresultaat is dat de kleinste longblaasjes zouden instorten en gevuld zouden worden met vloeistof en moeilijk opnieuw op te blazen, waardoor een deel van de long zou instorten, en andere delen zouden over-inflateren, die beide typische symptomen zijn van acute respiratory distress syndrome (ARDS). In een goed functionerende long verandert de oppervlaktespanning echter dynamisch als de lucht-epitheliale vloeistofinterface in het interfaciale gebied van alveolus uitzet en samentrekt tijdens het ademen. Als 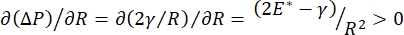 , of
, of 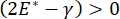 , neemt de Laplace-druk af met afnemende radius en neemt toe met toenemende radius om de Laplace-instabiliteit te elimineren, waardoor de long wordt gestabiliseerd9.
, neemt de Laplace-druk af met afnemende radius en neemt toe met toenemende radius om de Laplace-instabiliteit te elimineren, waardoor de long wordt gestabiliseerd9. 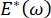 Vandaar, en hoe het afhangt van frequentie, monolaag morfologie en samenstelling, en alveolaire vloeistofsamenstelling kan essentieel zijn voor de longstabiliteit. De CPM-CFM heeft ook de eerste demonstraties gegeven van de effecten van interfaciale kromming op oppervlakteactieve adsorptie25, monolaagmorfologie22 en dilatatiemodulus9. Het kleine volume (~ 1 ml) van het reservoir in de CPM maakt de snelle introductie, verwijdering of uitwisseling van de vloeibare fase mogelijk en minimaliseert de vereiste hoeveelheid dure eiwitten of oppervlakteactieve stoffen10.
Vandaar, en hoe het afhangt van frequentie, monolaag morfologie en samenstelling, en alveolaire vloeistofsamenstelling kan essentieel zijn voor de longstabiliteit. De CPM-CFM heeft ook de eerste demonstraties gegeven van de effecten van interfaciale kromming op oppervlakteactieve adsorptie25, monolaagmorfologie22 en dilatatiemodulus9. Het kleine volume (~ 1 ml) van het reservoir in de CPM maakt de snelle introductie, verwijdering of uitwisseling van de vloeibare fase mogelijk en minimaliseert de vereiste hoeveelheid dure eiwitten of oppervlakteactieve stoffen10.
Contrast in een CPM-CFM-afbeelding is te wijten aan de verdeling van kleine fracties fluorescerend gelabelde lipiden of eiwitten op de interface16,27. Tweedimensionale oppervlakteactieve monolagen vertonen vaak laterale fasescheiding als functie van oppervlaktespanning of oppervlaktedruk, 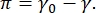 π is het verschil tussen de oppervlaktespanning van een schone vloeistof-vloeistofinterface, γ0, en een met oppervlakteactieve stof bedekte interface, γ. π kan worden beschouwd als de 2D “druk” veroorzaakt door de interacties van oppervlakteactieve moleculen op het grensvlak dat fungeert om de zuivere vloeistofoppervlakspanning te verlagen. Bij lage oppervlaktedrukken bevinden lipide monolagen zich in een vloeistofachtige ongeorganiseerde toestand; dit staat bekend als de vloeistof geëxpandeerde (LE) fase. Naarmate de oppervlaktedruk toeneemt en het gebied per lipidemolecuul afneemt, oriënteren de lipiden zich met elkaar en kunnen ze een eerste orde fase overgang ondergaan naar de lange afstand bestelde vloeistof gecondenseerde (LC) fase 16,20,27. De LE- en LC-fasen kunnen naast elkaar bestaan bij verschillende oppervlaktedrukken en kunnen worden gevisualiseerd als fluorescerend gelabelde lipiden worden uitgesloten van de LC-fase en worden gescheiden naar de LE-fase. De LE-fase is dus helder en de LC-fase is donker wanneer deze wordt afgebeeld met CFM16.
π is het verschil tussen de oppervlaktespanning van een schone vloeistof-vloeistofinterface, γ0, en een met oppervlakteactieve stof bedekte interface, γ. π kan worden beschouwd als de 2D “druk” veroorzaakt door de interacties van oppervlakteactieve moleculen op het grensvlak dat fungeert om de zuivere vloeistofoppervlakspanning te verlagen. Bij lage oppervlaktedrukken bevinden lipide monolagen zich in een vloeistofachtige ongeorganiseerde toestand; dit staat bekend als de vloeistof geëxpandeerde (LE) fase. Naarmate de oppervlaktedruk toeneemt en het gebied per lipidemolecuul afneemt, oriënteren de lipiden zich met elkaar en kunnen ze een eerste orde fase overgang ondergaan naar de lange afstand bestelde vloeistof gecondenseerde (LC) fase 16,20,27. De LE- en LC-fasen kunnen naast elkaar bestaan bij verschillende oppervlaktedrukken en kunnen worden gevisualiseerd als fluorescerend gelabelde lipiden worden uitgesloten van de LC-fase en worden gescheiden naar de LE-fase. De LE-fase is dus helder en de LC-fase is donker wanneer deze wordt afgebeeld met CFM16.
Het doel van dit manuscript is om de stappen te beschrijven die nodig zijn om de gecombineerde confocale micro microtensiometer te bouwen en te bedienen. Dit stelt de lezer in staat om adsorptiestudies uit te voeren, oppervlaktespanning, reologisch gedrag te meten en interfaciale morfologie tegelijkertijd te onderzoeken op een lucht / water- of olie / water-interface op micronschaal. Dit omvat een bespreking van het trekken, snijden en hydrofobiëren van de vereiste haarvaten, instructies voor het gebruik van druk-, krommings- en oppervlakteregelingsmodi en interfaciale overdracht van onoplosbare oppervlakteactieve stof naar de microtensiometer gebogen interface.
Protocol
Representative Results
Discussion
De gecombineerde CPM/CFM is een krachtig hulpmiddel voor het onderzoeken van interfaciale dynamica, evenwichten en morfologie. Dit protocol beschrijft de stappen die nodig zijn voor het verkrijgen van gegevens met CPM/CFM.
Figuur 2 toont het celontwerp met kanalen voor het capillair, oplosmiddel en warmte-uitwisseling aangegeven. De inlaat voor oplosmiddeluitwisseling moet zich aan de onderkant van de cel bevinden, terwijl de uitlaat zich aan de bovenkant moet bev…
Declarações
The authors have nothing to disclose.
Acknowledgements
Alle confocale microscopiebeelden zijn verkregen met behulp van de Nikon A1RHD Multiphoton rechtopstaande confocale microscoop. We erkennen de begeleiding en hulp van het ondersteunend personeel, met name Guillermo Marques, in het University Imaging Center aan de Universiteit van Minnesota. Dit werk werd ondersteund door NIH Grant HL51177. SI werd ondersteund door een Ruth L. Kirschstein NRSA Institutional Research Training Grant F32 HL151128.
Materials
| 1.5 O.D. Tygon tubing | Fischer Scientific | Tubing | |
| A1RHD Multiphoton upright confocal microscope | Nikon | Confocal Microscope | |
| Acid Cleaning Solution | Sulfuric acid and Alnochromix diluted with water 50% by volume, wait until clear befor diluting | ||
| Alnochromix | Alconox | 2510 | Mixed with sulfuric acid to package instructionand diluted to make acid cleaning solution |
| Ceramic glass cutter | Sutter Instruments | ||
| Chloroform | Sigma-Aldrich | 650471 | HPLC Plus |
| Curosurf | Chiesi | Lung Surfactant | |
| Di Water | 18.5 MΩ – cm | ||
| Ethanol | any | 200 proof used for hydrophobization, denatured used for cleaning | |
| Fiber-Lite Model 190 fiber optic illuminator | Dolan-Jenner Industries Inc. | 281900100 | Light source; other light sources should work as well |
| Flow EZ F69 mbar w/Link Module | Fluigent | LU-FEZ-0069 | Microfluidic Pump |
| Fluigent SDK VIs | Fluigent | Required for CPM virtual Interface | |
| Fluoroelastomer gaskets | Machined from 1 mm thick Viton sheet, See figure 3 | ||
| Gas filter | Norgren | F07-100-A3TG | Put between microfluidic pump and pressure regulator |
| Gas regulator | Norgren | 10R0400R | Steps down pressure from sorce to range of pump, connected to gas filter range 2-120 psi |
| Glass Capilary | Sutter Instruments | B150-86-10 | Borosilicate glass O.D. 1.5 mm I.D. 0.86 mm |
| Glass Slide | any | 75 mm x 25 mm | |
| Glass Syringe | Hamilton | 84878 | 25 μL glass syringe |
| Hydrophobizing Agent | Sigma-Aldrich | 667420 | 1H,1H,2H,2H-Perfluoro-octyltriethoxysilane 98%, other hydrophobic triethoxysilane can be substituted |
| Insoluble surfactant | Avanti | 850355C-200mg | 16:0 DPPC in chloroform |
| LabVIEW Software | National Instruments | 2017 | |
| Longpass Filter | ThorLabs | FEL0650 | 650 nm Longpass filter, wavelength must remove excitation lazer frequence |
| Lyso-PC | Avanti | 855675P | 16:0 Lyso PC 1-palmitoyl-2-hydroxy-sn-glycero-3-phosphocholine |
| Masterflex L/S variable speed analog consol pump system w/ Easy-Load II pump head | Masterflex | HV-77916-20 | Peristaltic Pump |
| MATLAB | Mathworks | R2019 | |
| Micropipette Puller P-1000 | Sutter Instruments | Capillary Puller | |
| Microtensiometer Cell and Holder | Cell machined from PEEK, holder machined from aluminum, See Figure 3 and 4 | ||
| Microtensiometer Objective | Nikon | Fluor 20x/0.50W DIC M/N2 ∞/0 WD 2.0 mm | |
| NI Vision Development Module | National Instruments | Required for CPM virtual Interface | |
| PEEK finger tight fittings | IDEX | F-120x | 10-32 Coned Ports |
| PEEK plug | IDEX | P-551 | 10-31 Coned Ports |
| pippette tips | Eppendorf | 22492225 | 100 μL – 1000 μL, Autoclaved |
| Plastic Forceps | Thermo Scientific | 6320-0010 | |
| Plastic Syringe | Fischer Scientific | 14-955-459 | 10 mL |
| Plumbing parts | Fischer Scientific | 3-way valves and other plumbing parts to connect tubing. | |
| Research Plus 1-channel 100 μL–1000 μL | Eppendorf | 3123000063 | Micro pipetter |
| Sulfuric Acid | any | Used for acid cleaning solution | |
| T Plan SLWD 20x/0.30 OFN25 WD 30 mm | Nikon | Confocal Microscope Objective | |
| Texas Red DHPE triethylammonim salt | Thermo Fischer Scientific | 1395MP | Fluorophore |
| Vaccum Pump | Gast | DOA-P704-AA |
Referências
- Freer, E. M., Yim, K. S., Fuller, G. G., Radke, C. J. Interfacial rheology of globular and flexible proteins at the hexadecane/water interface: Comparison of shear and dilatation deformation. Journal of Physical Chemistry B. 108 (12), 3835-3844 (2004).
- Freer, E. M., Yim, K. S., Fuller, G. G., Radke, C. J. Shear and dilatational relaxation mechanisms of globular and flexible proteins at the hexadecane/water interface. Langmuir. 20 (23), 10159-10167 (2004).
- Kannan, A., Shieh, I. C., Fuller, G. G. Linking aggregation and interfacial properties in monoclonal antibody-surfactant formulations. Journal of Colloid and Interface Science. 550, 128-138 (2019).
- Kannan, A., Shieh, I. C., Leiske, D. L., Fuller, G. G. Monoclonal antibody interfaces: Dilatation mechanics and bubble coalescence. Langmuir. 34 (2), 630-638 (2018).
- Li, J. J., et al. Interfacial stress in the development of biologics: Fundamental understanding, current practice, and future perspective. The AAPS Journal. 21 (3), 44 (2019).
- Bhamla, M. S., Giacomin, C. E., Balemans, C., Fuller, G. G. Influence of interfacial rheology on drainage from curved surfaces. Soft Matter. 10 (36), 6917-6925 (2014).
- Fuller, G. G., Vermant, J. Complex fluid-fluid interfaces: Rheology and structure. Annual Review of Chemical and Biomolecular Engineering. 3, 519-543 (2012).
- Rosenfeld, L., et al. Structural and rheological properties of meibomian lipid. Investigative Ophthalmology & Visual Science. 54 (4), 2720-2732 (2013).
- Barman, S., Davidson, M. L., Walker, L. M., Anna, S. L., Zasadzinski, J. A. Inflammation product effects on dilatational mechanics can trigger the Laplace instability and acute respiratory distress syndrome. Soft Matter. 16 (29), 6890-6901 (2020).
- Barman, S., et al., Ramachadran, A., et al. . Recent Advances in Rheology: Theory, Biorheology, Suspension and Interfacial Rheology. , (2022).
- Alonso, C., Zasadzinski, J. A. A brief review of the relationship between monolayer viscosity, phase behavior, surface pressure and temperature using a simple monolayer viscometer. The Journal of Physical Chemistry B. 110 (44), 22185-22191 (2006).
- Alonso, C., et al. More than a monolayer: Relating lung surfactant structure and mechanics to composition. Biophysical Journal. 87 (6), 4188-4202 (2004).
- Alonso, C., Bringezu, F., Brezesinski, G., Waring, A. J., Zasadzinski, J. A. Modifying calf lung surfactant by hexadecanol. Langmuir. 21 (3), 1028-1035 (2005).
- Alonso, C., Waring, A. J., Zasadzinski, J. A. Keeping lung surfactant where it belongs: Protein regulation of two-dimensional viscosity. Biophysical Journal. 89 (1), 266-273 (2005).
- Zasadzinski, J. A., et al. Inhibition of pulmonary surfactant adsorption by serum and the mechanisms of reversal by hydrophilic polymers: Theory. Biophysical Journal. 89 (3), 1621-1629 (2005).
- McConnell, H. M. Structures and transitions in lipid monolayers at the air-water-interface. Annual Reviews of Physical Chemistry. 42, 171-195 (1991).
- McConnell, H. M., Moy, V. T. Shapes of finite two-dimensional lipid domains. Journal of Physical Chemistry. 92 (15), 4520-4525 (1988).
- Zasadzinski, J. A., Stenger, P., Shieh, I., Dhar, P. Overcoming rapid inactivation of lung surfactant: analogies between competitive adsorption and colloid stability. Biochemica et Biophysica Acta. 1798 (4), 801-828 (2010).
- Zasadzinski, J. A., Nag, K., et al. . Surfactant Progress. , (2008).
- Valtierrez-Gaytan, C., et al. Spontaneous evolution of equilibrium morphology in phospholipid-cholesterol monolayers. Science Advances. 8 (14), (2022).
- Williams, I., Zasadzinski, J. A., Squires, T. M. Interfacial rheology and direct imaging reveal domain-templated network formation in phospholipid monolayers penetrated by fibrinogen. Soft Matter. 15 (44), 9076-9084 (2019).
- Sachan, A. K., Zasadzinski, J. A. Interfacial curvature effects on the monolayer morphology and dynamics of a clinical lung surfactant. Proceedings of the National Academy of Sciences of the United States of America. 115 (2), 134-143 (2018).
- Alvarez, N. J., Anna, S. L., Saigal, T., Tilton, R. D., Walker, L. M. Intefacial dynamics and rheology of polymer grafter nanoparticles at air-water and xylene-water interfaces. Langmuir. 28 (21), 8052-8063 (2012).
- Alvarez, N. J., Vogus, D. R., Walker, L. M., Anna, S. L. Using bulk convection in a microtensiometer to approach kinetic-limited surfactant dynamics at fluid-fluid interfaces. Journal of Colloid and Interface Science. 372 (1), 183-191 (2012).
- Alvarez, N. J., Walker, L. M., Anna, S. L. Diffusion-limited adsorption to a spherical geometry: The impact of curvature and competitive time scales. Physical Review. E, Statistical, Nonlinear, and Soft Matter Physics. 82, 011604 (2010).
- Shieh, I., Waring, A. J., Zasadzinski, J. A. Visualizing the analogy between competitive adsorption and colloid stability to restore lung surfactant function. Biophysical Journal. 102 (4), 777-786 (2012).
- Shieh, I., Zasadzinski, J. A. Visualizing monolayers with a water-soluble fluorophore to quantify adsorption, desorption and the double-layer. Proceedings of the National Academy of Sciences of the United States of America. 112 (8), 826-835 (2015).
- Lipp, M. M., Lee, K. Y. C., Takamoto, D. Y., Zasadzinski, J. A., Waring, A. J. Coexistence of buckled and flat monolayers. Physical Review Letters. 81, 1650-1653 (1998).
- Lipp, M. M., Lee, K. Y. C., Waring, A., Zasadzinski, J. A. Fluorescence, polarized fluorescence, and Brewster angle microscopy of palmitic acid and lung surfactant protein B monolayers. Biophysical Journal. 72 (6), 2783-2804 (1997).
- Alvarez, N. J., Walker, L. M., Anna, S. L. A microtensiometer to probe the effect of radius of curvature on surfactant transport to a spherical interface. Langmuir. 26 (16), 13310-13319 (2010).
- Ward, A. F. H., Tordai, L. Time dependents of boundary tensions of solutions. 1. The role of diffusion in time-effects. Journal of Chemical Physics. 14, 453-461 (1946).
- Lucassen, J., Vanden Tempel, M. Dynamic measurements of dilatational properties of a liquid interface. Chemical Engineering Science. 27 (6), 1283-1291 (1972).
- Lin, G. L., et al. Interfacial dilatational deformation accelerates particle formation in monoclonal antibody solutions. Soft Matter. 12 (14), 3293-3302 (2016).
- Bastacky, J., et al. Alveolar lining layer is thin and continuous: low temperature scanning electron microscopy of rat lung. Journal of Applied Physiology. 79 (5), 1615-1628 (1995).
- Adamson, A. W., Gast, A. P. . Physical Chemistry of Surfaces, Sixth ed. , 784 (1997).
- del Rio, O. I., Kwok, D. Y., Wu, R., Alvarez, J. M., Neumann, A. W. Contact angle measurements by axisymmetric drop shape analysis and an automated polynomial fit program. Colloids and Surfaces A Physicochemical and Engineering Aspects. 143 (2-3), 197-210 (1998).
- Kanthe, A., et al. No ordinary proteins: Adsorption and molecular orientation of monoclonal antibodies. Science Advances. 7 (5), 14 (2021).
- Manikantan, H., Squires, T. M. Surfactant dynamics: hidden variables controlling fluid flows. Journal of Fluid Mechanics. 892, 115 (2020).
- Narayan, S., et al. Dilatational rheology of water-in-diesel fuel interfaces: effect of surfactant concentration and bulk-to-interface exchange. Soft Matter. 17 (18), 4751-4765 (2021).
- Meng, G. N., Paulose, J., Nelson, D. R., Manoharan, V. N. Elastic instability of a crystal growing on a curved surface. Science. 343 (6171), 634-637 (2014).
- Kotula, A. P., Anna, S. L. Insoluble layer deposition and dilatational rheology at a microscale spherical cap interface. Soft Matter. 12 (33), 7038-7055 (2016).
- Lipp, M. M., Lee, K. Y. C., Zasadzinski, J. A., Waring, A. J. Phase and morphology changes in lipid monolayers induced by SP-B protein and its amino-terminal peptide. Science. 273 (5279), 1196-1199 (1996).
- Pocivavsek, L., et al. Stress and fold localization in thin elastic membranes. Science. 320 (5878), 912-916 (2008).
- Pocivavsek, L., et al. Lateral stress relaxation and collapse in lipid monolayers. Soft Matter. 4 (10), 2019-2029 (2008).
- Kim, K., Choi, S. Q., Squires, T. M., Zasadzinski, J. A. Cholesterol nanodomains: their effect on monolayer morphology and dynamics. Proceedings of the National Academy of Sciences of the United States of America. 110 (33), 3054-3060 (2013).
- Kim, K., Choi, S. Q., Zasadzinski, J. A., Squires, T. M. Interfacial microrheology of DPPC monolayers at the air-water interface. Soft Matter. 7 (17), 7782-7789 (2011).
- Kim, K., Choi, S. Q., Zasadzinski, J. A., Squires, T. M. Nonlinear chiral rheology of phospholipid monolayers. Soft Matter. 14 (13), 2476-2483 (2018).
- Kotula, A. P., Anna, S. L. Regular perturbation analysis of small amplitude oscillatory dilatation of an interface in a capillary pressure tensiometer. Journal of Rheology. 59, 85-117 (2015).

