गतिशील इंटरफेस के कन्फोकल माइक्रोस्कोपी विज़ुअलाइज़ेशन के लिए माइक्रोटेंसियोमीटर
Summary
यह पांडुलिपि इंटरफेशियल आकृति विज्ञान की कल्पना करते हुए इंटरफेशियल तनाव और सतह फैलाव रियोलॉजी के एक साथ माप करने के लिए एक माइक्रोटेंसियोमीटर / कॉन्फोकल माइक्रोस्कोप के डिजाइन और संचालन का वर्णन करती है। यह प्रौद्योगिकी और शरीर विज्ञान में महत्वपूर्ण इंटरफेस के संरचना-संपत्ति संबंधों का वास्तविक समय निर्माण प्रदान करता है।
Abstract
द्रव-द्रव इंटरफेस के लिए सतह-सक्रिय अणुओं का सोखना प्रकृति में सर्वव्यापी है। इन इंटरफेस की विशेषता के लिए सर्फेक्टेंट सोखना दरों को मापने, थोक सर्फैक्टेंट एकाग्रता के एक समारोह के रूप में संतुलन सतह तनाव का मूल्यांकन करने और संतुलन के बाद इंटरफेशियल क्षेत्र में परिवर्तन के साथ सतह तनाव कैसे बदलता है, इससे संबंधित है। एक उच्च गति कॉन्फोकल माइक्रोस्कोप के साथ प्रतिदीप्ति इमेजिंग का उपयोग करके इंटरफ़ेस का एक साथ दृश्य संरचना-कार्य संबंधों के प्रत्यक्ष मूल्यांकन की अनुमति देता है। केशिका दबाव माइक्रोटेंसियोमीटर (सीपीएम) में, 1 एमएल वॉल्यूम तरल जलाशय में केशिका के अंत में एक अर्धगोलाकार हवा का बुलबुला पिन किया जाता है। बुलबुला इंटरफ़ेस में केशिका दबाव को एक वाणिज्यिक माइक्रोफ्लुइडिक प्रवाह नियंत्रक के माध्यम से नियंत्रित किया जाता है जो लाप्लास समीकरण के आधार पर मॉडल-आधारित दबाव, बुलबुला वक्रता या बुलबुला क्षेत्र नियंत्रण की अनुमति देता है। लैंगमुइर गर्त और लटकन ड्रॉप जैसी पिछली तकनीकों की तुलना में, माप और नियंत्रण परिशुद्धता और प्रतिक्रिया समय बहुत बढ़ाया जाता है; केशिका दबाव विविधताओं को मिलीसेकंड में लागू और नियंत्रित किया जा सकता है। बुलबुला इंटरफ़ेस की गतिशील प्रतिक्रिया को दूसरे ऑप्टिकल लेंस के माध्यम से कल्पना की जाती है क्योंकि बुलबुला फैलता है और अनुबंध करता है। बुलबुला समोच्च बुलबुला वक्रता त्रिज्या, आर, साथ ही परिपत्रता से किसी भी विचलन को निर्धारित करने के लिए एक परिपत्र प्रोफ़ाइल के लिए फिट है जो परिणामों को अमान्य कर देगा। लाप्लास समीकरण का उपयोग इंटरफ़ेस की गतिशील सतह तनाव को निर्धारित करने के लिए किया जाता है। संतुलन के बाद, छोटे दबाव दोलनों को कंप्यूटर-नियंत्रित माइक्रोफ्लुइडिक पंप द्वारा बुलबुला त्रिज्या (0.001-100 चक्र / मिनट की आवृत्तियों) को दोलन करने के लिए लगाया जा सकता है ताकि फैलाव मापांक निर्धारित किया जा सके सिस्टम के समग्र आयाम पर्याप्त रूप से छोटे होते हैं कि माइक्रोटेंसियोमीटर एक उच्च गति वाले कॉन्फोकल माइक्रोस्कोप के लेंस के नीचे फिट बैठता है जिससे फ्लोरोसेंटली टैग की गई रासायनिक प्रजातियों को मात्रात्मक रूप से ट्रैक किया जा सके।
Introduction
सर्फेक्टेंट फिल्मों द्वारा कवर किए गए एयर-वॉटर इंटरफेस दैनिक जीवन में सर्वव्यापी हैं। सर्फेक्टेंट-वॉटर इंजेक्शन का उपयोग समाप्त क्षेत्रों से तेल की वसूली को बढ़ाने के लिए किया जाता है और शेल गैस और तेल के लिए हाइड्रोलिक फ्रैक्चरिंग समाधान के रूप में उपयोग किया जाता है। गैस-तरल फोम और तरल-तरल पायस स्नेहक और सफाई एजेंटों के रूप में कई औद्योगिक और वैज्ञानिक प्रक्रियाओं के लिए आम हैं और भोजन में आम हैं। इंटरफेस पर सर्फेक्टेंट और प्रोटीन पैकेजिंग, भंडारण और प्रशासन 1,2,3,4,5, आंखों में आंसू फिल्म स्थिरता 6,7,8, और फुफ्फुसीय यांत्रिकी 9,10,11,12,13,14 के दौरान एंटीबॉडी विरूपण को स्थिर करते हैं, 15.
इंटरफेस और उनके गुणों के लिए सोखने वाले सतह-सक्रिय एजेंटों या सर्फेक्टेंट्स के अध्ययन का कई अलग-अलग प्रयोगात्मक तकनीकों के साथ एक लंबा इतिहास है 16,17,18,19,20,21,22,23,24,25,26,27 . एक हालिया विकास केशिका दबाव माइक्रोटेंसियोमीटर (सीपीएम) है, जो अन्य सामान्य तरीकों 9,23,24,25 की तुलना में काफी कम सामग्रियों का उपयोग करते हुए, बहुत कम लंबाई के तराजू पर अत्यधिक घुमावदार इंटरफेस पर इंटरफेशियल गुणों की परीक्षा की अनुमति देता है। कॉन्फोकल फ्लोरेसेंस माइक्रोस्कोपी (सीएफएम) का उपयोग सीपीएम22 में हवा-पानी के इंटरफेस पर लिपिड और प्रोटीन की आकृति विज्ञान का अध्ययन करने के लिए किया जा सकता है या लैंगमुइर गर्तों 20,26,27,28,29 पर किया जा सकता है। यहां जैविक और तकनीकी इंटरफेस के लिए संरचना-कार्य संबंधों को विकसित करने के लिए रूपात्मक घटनाओं को गतिशील और संतुलन इंटरफेशियल गुणों से जोड़ने के लिए एक सीपीएम और सीएफएम को जोड़ा गया है।
सीपीएम-सीएफएम के लिए सुलभ इंटरफेशियल सर्फेक्टेंट सिस्टम में महत्व के कई पैरामीटर हैं। सीपीएम में, एक 30-200 μm व्यास हवा का बुलबुला एक ग्लास केशिका ट्यूब की नोक पर पिन किया जाता है। सीपीएम के पहले के संस्करणों में, बुलबुले के अंदर और बाहर के बीच केशिका दबाव अंतर को पानी के स्तंभ और दोलन सिरिंज पंप 9,30 के माध्यम से नियंत्रित किया गया था; यहां वर्णित नया संस्करण इन्हें उच्च परिशुद्धता, कंप्यूटर-नियंत्रित माइक्रोफ्लुइडिक पंप के साथ बदल देता है। सतह तनाव (γ) लाप्लास समीकरण के माध्यम से निर्धारित किया जाता है, ΔP = 2γ/R, पंप, ΔP द्वारा निर्धारित इंटरफ़ेस में दबाव ड्रॉप से, और बुलबुले, R के वक्रता की त्रिज्या के ऑप्टिकल विश्लेषण से। इंटरफ़ेस की गतिशील सतह तनाव को घुलनशील सर्फेक्टेंट युक्त थोक तरल के संपर्क में एक नए बुलबुले की पीढ़ी के बाद 10 एमएस समय संकल्प के साथ निर्धारित किया जा सकता है। सर्फेक्टेंट सोखना गतिशीलता को क्लासिक वार्ड-टोरडाई समीकरण10,31 द्वारा सर्फैक्टेंट के आवश्यक गुणों को निर्धारित करने के लिए वर्णित किया जा सकता है, जिसमें फैलाव, सतह कवरेज और थोक एकाग्रता और संतुलन सतह तनाव के बीच संबंध शामिल हैं। एक बार एक संतुलन सतह तनाव प्राप्त हो जाने के बाद, इंटरफेशियल क्षेत्र को फैलाव मापांक को मापने के लिए दोलन किया जा सकता है, 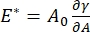 सतह तनाव में परिवर्तन को रिकॉर्ड करके, बुलबुला सतह क्षेत्र में छोटे परिवर्तनों से प्रेरित, ए32। अधिक जटिल इंटरफेस के लिए जो अपनी आंतरिक संरचनाओं जैसे उलझे हुए पॉलिमर या प्रोटीन को विकसित करते हैं, सतह तनाव, को अधिक सामान्य सतह तनाव 4,33 द्वारा प्रतिस्थापित किया जाता है।
सतह तनाव में परिवर्तन को रिकॉर्ड करके, बुलबुला सतह क्षेत्र में छोटे परिवर्तनों से प्रेरित, ए32। अधिक जटिल इंटरफेस के लिए जो अपनी आंतरिक संरचनाओं जैसे उलझे हुए पॉलिमर या प्रोटीन को विकसित करते हैं, सतह तनाव, को अधिक सामान्य सतह तनाव 4,33 द्वारा प्रतिस्थापित किया जाता है। 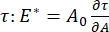
श्वास के दौरान फेफड़ों की स्थिरता सीधे वायुकोशीय वायु-तरल इंटरफ़ेस 9,10 पर कम सतह तनाव और एक उच्च फैलाव मापांक दोनों को बनाए रखने के लिए बंधी हो सकती है। सभी आंतरिक फेफड़ों की सतहों को ऊतक जलयोजन34 को बनाए रखने के लिए उपकला अस्तर तरल पदार्थ की एक निरंतर, माइक्रोन-मोटी फिल्म के साथ पंक्तिबद्ध किया जाता है। यह उपकला अस्तर तरल पदार्थ मुख्य रूप से पानी है, जिसमें लवण और विभिन्न अन्य प्रोटीन, एंजाइम, शर्करा और फेफड़े के सर्फेक्टेंट होते हैं। जैसा कि किसी भी घुमावदार तरल-वाष्प इंटरफ़ेस के मामले में होता है, एक केशिका दबाव एल्वियोलस (या बुलबुला) के अंदर अधिक दबाव के साथ प्रेरित होता है। हालांकि, यदि फेफड़ों के भीतर सतह का तनाव हर जगह स्थिर था, तो लाप्लास समीकरण, ΔP = 2γ/R, से पता चलता है कि छोटे एल्वियोली में बड़े एल्वियोली के सापेक्ष उच्च आंतरिक दबाव होगा, जिससे छोटे एल्वियोली की गैस सामग्री बड़े, कम दबाव एल्वियोली में प्रवाहित होती है। इसे “लाप्लास अस्थिरता” 9,35 के रूप में जाना जाता है। शुद्ध परिणाम यह है कि सबसे छोटा एल्वियोली ढह जाएगा और तरल से भर जाएगा और फेफड़ों के हिस्से को ढहने के कारण फिर से फुलाना मुश्किल हो जाएगा, और अन्य भाग ओवर-फुलाए जाएंगे, जिनमें से दोनों तीव्र श्वसन संकट सिंड्रोम (एआरडीएस) के विशिष्ट लक्षण हैं। हालांकि, ठीक से काम करने वाले फेफड़ों में, सतह तनाव गतिशील रूप से बदलता है क्योंकि एल्वियोलस इंटरफेशियल क्षेत्र में वायु-उपकला द्रव इंटरफ़ेस सांस लेने के दौरान फैलता है और सिकुड़ता है। यदि 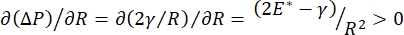 , या
, या 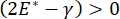 , लाप्लास दबाव घटती त्रिज्या के साथ कम हो जाता है और बढ़ती त्रिज्या के साथ बढ़ता है ताकि लाप्लास अस्थिरता को खत्म किया जा सके, जिससे फेफड़े 9 स्थिर होजाएं। इसलिए,
, लाप्लास दबाव घटती त्रिज्या के साथ कम हो जाता है और बढ़ती त्रिज्या के साथ बढ़ता है ताकि लाप्लास अस्थिरता को खत्म किया जा सके, जिससे फेफड़े 9 स्थिर होजाएं। इसलिए, 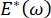 और यह आवृत्ति, मोनोलेयर आकृति विज्ञान और संरचना पर कैसे निर्भर करता है, और वायुकोशीय द्रव संरचना फेफड़ों की स्थिरता के लिए आवश्यक हो सकती है। सीपीएम-सीएफएम ने सर्फेक्टेंट सोखना 25, मोनोलेयरआकृति विज्ञान 22 और फैलाव मापांक9 पर इंटरफेशियल वक्रता के प्रभावों का पहला प्रदर्शन भी प्रदान किया है। सीपीएम में जलाशय की छोटी मात्रा (~ 1 एमएल) तरल चरण के त्वरित परिचय, हटाने या विनिमय की अनुमति देती है और महंगे प्रोटीन यासर्फैक्टेंट्स 10 की आवश्यक मात्रा को कम करती है।
और यह आवृत्ति, मोनोलेयर आकृति विज्ञान और संरचना पर कैसे निर्भर करता है, और वायुकोशीय द्रव संरचना फेफड़ों की स्थिरता के लिए आवश्यक हो सकती है। सीपीएम-सीएफएम ने सर्फेक्टेंट सोखना 25, मोनोलेयरआकृति विज्ञान 22 और फैलाव मापांक9 पर इंटरफेशियल वक्रता के प्रभावों का पहला प्रदर्शन भी प्रदान किया है। सीपीएम में जलाशय की छोटी मात्रा (~ 1 एमएल) तरल चरण के त्वरित परिचय, हटाने या विनिमय की अनुमति देती है और महंगे प्रोटीन यासर्फैक्टेंट्स 10 की आवश्यक मात्रा को कम करती है।
सीपीएम-सीएफएम छवि में कंट्रास्ट इंटरफ़ेस16,27 पर फ्लोरोसेंटली टैग किए गए लिपिड या प्रोटीन के छोटे अंशों के वितरण के कारण होता है। द्वि-आयामी सर्फेक्टेंट मोनोलेयर अक्सर सतह तनाव या सतह के दबाव के एक समारोह के रूप में पार्श्व चरण पृथक्करण प्रदर्शित करते हैं, 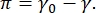 π एक साफ द्रव-द्रव इंटरफ़ेस की सतह तनाव के बीच का अंतर है, γ0, और एक सर्फैक्टेंट-कवर इंटरफ़ेस, γ π इंटरफ़ेस पर सर्फैक्टेंट अणुओं की बातचीत के कारण 2-डी “दबाव” के रूप में सोचा जा सकता है जो शुद्ध द्रव सतह तनाव को कम करने के लिए कार्य करता है। कम सतह के दबाव में, लिपिड मोनोलेयर तरल जैसी अव्यवस्थित अवस्था में होते हैं; इसे तरल विस्तारित (एलई) चरण के रूप में जाना जाता है। जैसे-जैसे सतह का दबाव बढ़ता है और प्रति लिपिड अणु का क्षेत्र कम हो जाता है, लिपिड एक दूसरे के साथ उन्मुख होते हैं और लंबी दूरी के तरल संघनित (एलसी) चरण 16,20,27 में पहले क्रम चरण संक्रमण से गुजर सकते हैं। एलई और एलसी चरण विभिन्न सतह दबावों पर सह-अस्तित्व में रह सकते हैं और फ्लोरोसेंटली टैग किए गए लिपिड को एलसी चरण से बाहर रखा जाता है और एलई चरण में अलग किया जा सकता है। इस प्रकार, एलई चरण उज्ज्वल है और सीएफएम16 के साथ चित्रित होने पर एलसी चरण अंधेरा है।
π एक साफ द्रव-द्रव इंटरफ़ेस की सतह तनाव के बीच का अंतर है, γ0, और एक सर्फैक्टेंट-कवर इंटरफ़ेस, γ π इंटरफ़ेस पर सर्फैक्टेंट अणुओं की बातचीत के कारण 2-डी “दबाव” के रूप में सोचा जा सकता है जो शुद्ध द्रव सतह तनाव को कम करने के लिए कार्य करता है। कम सतह के दबाव में, लिपिड मोनोलेयर तरल जैसी अव्यवस्थित अवस्था में होते हैं; इसे तरल विस्तारित (एलई) चरण के रूप में जाना जाता है। जैसे-जैसे सतह का दबाव बढ़ता है और प्रति लिपिड अणु का क्षेत्र कम हो जाता है, लिपिड एक दूसरे के साथ उन्मुख होते हैं और लंबी दूरी के तरल संघनित (एलसी) चरण 16,20,27 में पहले क्रम चरण संक्रमण से गुजर सकते हैं। एलई और एलसी चरण विभिन्न सतह दबावों पर सह-अस्तित्व में रह सकते हैं और फ्लोरोसेंटली टैग किए गए लिपिड को एलसी चरण से बाहर रखा जाता है और एलई चरण में अलग किया जा सकता है। इस प्रकार, एलई चरण उज्ज्वल है और सीएफएम16 के साथ चित्रित होने पर एलसी चरण अंधेरा है।
इस पांडुलिपि का लक्ष्य संयुक्त कॉन्फोकल माइक्रोस्कोप माइक्रोटेंसियोमीटर के निर्माण और संचालन के लिए आवश्यक चरणों का वर्णन करना है। यह पाठक को सोखना अध्ययन करने, सतह तनाव, रियोलॉजिकल व्यवहार को मापने और माइक्रोन-स्केल एयर / पानी या तेल / पानी इंटरफ़ेस पर एक साथ इंटरफेशियल आकृति विज्ञान की जांच करने की अनुमति देगा। इसमें आवश्यक केशिकाओं को खींचने, काटने और हाइड्रोफोबाइज़ करने के तरीके, दबाव, वक्रता और सतह क्षेत्र नियंत्रण मोड का उपयोग करने के निर्देश, और माइक्रोटेंसियोमीटर घुमावदार इंटरफ़ेस में अघुलनशील सर्फैक्टेंट के इंटरफेशियल ट्रांसफर की चर्चा शामिल है।
Protocol
Representative Results
Discussion
सीएफएम इंटरफेशियल गतिशीलता, संतुलन और आकृति विज्ञान की जांच के लिए एक शक्तिशाली उपकरण है। यह प्रोटोकॉल सीपीएम/सीएफएम के साथ डेटा प्राप्त करने के लिए आवश्यक चरणों का वर्णन करता है।
च…
Declarações
The authors have nothing to disclose.
Acknowledgements
सभी कॉन्फोकल माइक्रोस्कोपी छवियों को निकॉन ए 1 आरएचडी मल्टीफोटॉन ईमानदार कॉन्फोकल माइक्रोस्कोप का उपयोग करके प्राप्त किया गया था। हम मिनेसोटा विश्वविद्यालय में यूनिवर्सिटी इमेजिंग सेंटर में सहायक कर्मचारियों, विशेष रूप से गिलर्मो मार्केस के मार्गदर्शन और सहायता को स्वीकार करते हैं। इस काम को एनआईएच ग्रांट एचएल 51177 द्वारा समर्थित किया गया था। एसआई को रूथ एल किर्शस्टीन एनआरएसए संस्थागत अनुसंधान प्रशिक्षण अनुदान एफ 32 एचएल 151128 द्वारा समर्थित किया गया था।
Materials
| 1.5 O.D. Tygon tubing | Fischer Scientific | Tubing | |
| A1RHD Multiphoton upright confocal microscope | Nikon | Confocal Microscope | |
| Acid Cleaning Solution | Sulfuric acid and Alnochromix diluted with water 50% by volume, wait until clear befor diluting | ||
| Alnochromix | Alconox | 2510 | Mixed with sulfuric acid to package instructionand diluted to make acid cleaning solution |
| Ceramic glass cutter | Sutter Instruments | ||
| Chloroform | Sigma-Aldrich | 650471 | HPLC Plus |
| Curosurf | Chiesi | Lung Surfactant | |
| Di Water | 18.5 MΩ – cm | ||
| Ethanol | any | 200 proof used for hydrophobization, denatured used for cleaning | |
| Fiber-Lite Model 190 fiber optic illuminator | Dolan-Jenner Industries Inc. | 281900100 | Light source; other light sources should work as well |
| Flow EZ F69 mbar w/Link Module | Fluigent | LU-FEZ-0069 | Microfluidic Pump |
| Fluigent SDK VIs | Fluigent | Required for CPM virtual Interface | |
| Fluoroelastomer gaskets | Machined from 1 mm thick Viton sheet, See figure 3 | ||
| Gas filter | Norgren | F07-100-A3TG | Put between microfluidic pump and pressure regulator |
| Gas regulator | Norgren | 10R0400R | Steps down pressure from sorce to range of pump, connected to gas filter range 2-120 psi |
| Glass Capilary | Sutter Instruments | B150-86-10 | Borosilicate glass O.D. 1.5 mm I.D. 0.86 mm |
| Glass Slide | any | 75 mm x 25 mm | |
| Glass Syringe | Hamilton | 84878 | 25 μL glass syringe |
| Hydrophobizing Agent | Sigma-Aldrich | 667420 | 1H,1H,2H,2H-Perfluoro-octyltriethoxysilane 98%, other hydrophobic triethoxysilane can be substituted |
| Insoluble surfactant | Avanti | 850355C-200mg | 16:0 DPPC in chloroform |
| LabVIEW Software | National Instruments | 2017 | |
| Longpass Filter | ThorLabs | FEL0650 | 650 nm Longpass filter, wavelength must remove excitation lazer frequence |
| Lyso-PC | Avanti | 855675P | 16:0 Lyso PC 1-palmitoyl-2-hydroxy-sn-glycero-3-phosphocholine |
| Masterflex L/S variable speed analog consol pump system w/ Easy-Load II pump head | Masterflex | HV-77916-20 | Peristaltic Pump |
| MATLAB | Mathworks | R2019 | |
| Micropipette Puller P-1000 | Sutter Instruments | Capillary Puller | |
| Microtensiometer Cell and Holder | Cell machined from PEEK, holder machined from aluminum, See Figure 3 and 4 | ||
| Microtensiometer Objective | Nikon | Fluor 20x/0.50W DIC M/N2 ∞/0 WD 2.0 mm | |
| NI Vision Development Module | National Instruments | Required for CPM virtual Interface | |
| PEEK finger tight fittings | IDEX | F-120x | 10-32 Coned Ports |
| PEEK plug | IDEX | P-551 | 10-31 Coned Ports |
| pippette tips | Eppendorf | 22492225 | 100 μL – 1000 μL, Autoclaved |
| Plastic Forceps | Thermo Scientific | 6320-0010 | |
| Plastic Syringe | Fischer Scientific | 14-955-459 | 10 mL |
| Plumbing parts | Fischer Scientific | 3-way valves and other plumbing parts to connect tubing. | |
| Research Plus 1-channel 100 μL–1000 μL | Eppendorf | 3123000063 | Micro pipetter |
| Sulfuric Acid | any | Used for acid cleaning solution | |
| T Plan SLWD 20x/0.30 OFN25 WD 30 mm | Nikon | Confocal Microscope Objective | |
| Texas Red DHPE triethylammonim salt | Thermo Fischer Scientific | 1395MP | Fluorophore |
| Vaccum Pump | Gast | DOA-P704-AA |
Referências
- Freer, E. M., Yim, K. S., Fuller, G. G., Radke, C. J. Interfacial rheology of globular and flexible proteins at the hexadecane/water interface: Comparison of shear and dilatation deformation. Journal of Physical Chemistry B. 108 (12), 3835-3844 (2004).
- Freer, E. M., Yim, K. S., Fuller, G. G., Radke, C. J. Shear and dilatational relaxation mechanisms of globular and flexible proteins at the hexadecane/water interface. Langmuir. 20 (23), 10159-10167 (2004).
- Kannan, A., Shieh, I. C., Fuller, G. G. Linking aggregation and interfacial properties in monoclonal antibody-surfactant formulations. Journal of Colloid and Interface Science. 550, 128-138 (2019).
- Kannan, A., Shieh, I. C., Leiske, D. L., Fuller, G. G. Monoclonal antibody interfaces: Dilatation mechanics and bubble coalescence. Langmuir. 34 (2), 630-638 (2018).
- Li, J. J., et al. Interfacial stress in the development of biologics: Fundamental understanding, current practice, and future perspective. The AAPS Journal. 21 (3), 44 (2019).
- Bhamla, M. S., Giacomin, C. E., Balemans, C., Fuller, G. G. Influence of interfacial rheology on drainage from curved surfaces. Soft Matter. 10 (36), 6917-6925 (2014).
- Fuller, G. G., Vermant, J. Complex fluid-fluid interfaces: Rheology and structure. Annual Review of Chemical and Biomolecular Engineering. 3, 519-543 (2012).
- Rosenfeld, L., et al. Structural and rheological properties of meibomian lipid. Investigative Ophthalmology & Visual Science. 54 (4), 2720-2732 (2013).
- Barman, S., Davidson, M. L., Walker, L. M., Anna, S. L., Zasadzinski, J. A. Inflammation product effects on dilatational mechanics can trigger the Laplace instability and acute respiratory distress syndrome. Soft Matter. 16 (29), 6890-6901 (2020).
- Barman, S., et al., Ramachadran, A., et al. . Recent Advances in Rheology: Theory, Biorheology, Suspension and Interfacial Rheology. , (2022).
- Alonso, C., Zasadzinski, J. A. A brief review of the relationship between monolayer viscosity, phase behavior, surface pressure and temperature using a simple monolayer viscometer. The Journal of Physical Chemistry B. 110 (44), 22185-22191 (2006).
- Alonso, C., et al. More than a monolayer: Relating lung surfactant structure and mechanics to composition. Biophysical Journal. 87 (6), 4188-4202 (2004).
- Alonso, C., Bringezu, F., Brezesinski, G., Waring, A. J., Zasadzinski, J. A. Modifying calf lung surfactant by hexadecanol. Langmuir. 21 (3), 1028-1035 (2005).
- Alonso, C., Waring, A. J., Zasadzinski, J. A. Keeping lung surfactant where it belongs: Protein regulation of two-dimensional viscosity. Biophysical Journal. 89 (1), 266-273 (2005).
- Zasadzinski, J. A., et al. Inhibition of pulmonary surfactant adsorption by serum and the mechanisms of reversal by hydrophilic polymers: Theory. Biophysical Journal. 89 (3), 1621-1629 (2005).
- McConnell, H. M. Structures and transitions in lipid monolayers at the air-water-interface. Annual Reviews of Physical Chemistry. 42, 171-195 (1991).
- McConnell, H. M., Moy, V. T. Shapes of finite two-dimensional lipid domains. Journal of Physical Chemistry. 92 (15), 4520-4525 (1988).
- Zasadzinski, J. A., Stenger, P., Shieh, I., Dhar, P. Overcoming rapid inactivation of lung surfactant: analogies between competitive adsorption and colloid stability. Biochemica et Biophysica Acta. 1798 (4), 801-828 (2010).
- Zasadzinski, J. A., Nag, K., et al. . Surfactant Progress. , (2008).
- Valtierrez-Gaytan, C., et al. Spontaneous evolution of equilibrium morphology in phospholipid-cholesterol monolayers. Science Advances. 8 (14), (2022).
- Williams, I., Zasadzinski, J. A., Squires, T. M. Interfacial rheology and direct imaging reveal domain-templated network formation in phospholipid monolayers penetrated by fibrinogen. Soft Matter. 15 (44), 9076-9084 (2019).
- Sachan, A. K., Zasadzinski, J. A. Interfacial curvature effects on the monolayer morphology and dynamics of a clinical lung surfactant. Proceedings of the National Academy of Sciences of the United States of America. 115 (2), 134-143 (2018).
- Alvarez, N. J., Anna, S. L., Saigal, T., Tilton, R. D., Walker, L. M. Intefacial dynamics and rheology of polymer grafter nanoparticles at air-water and xylene-water interfaces. Langmuir. 28 (21), 8052-8063 (2012).
- Alvarez, N. J., Vogus, D. R., Walker, L. M., Anna, S. L. Using bulk convection in a microtensiometer to approach kinetic-limited surfactant dynamics at fluid-fluid interfaces. Journal of Colloid and Interface Science. 372 (1), 183-191 (2012).
- Alvarez, N. J., Walker, L. M., Anna, S. L. Diffusion-limited adsorption to a spherical geometry: The impact of curvature and competitive time scales. Physical Review. E, Statistical, Nonlinear, and Soft Matter Physics. 82, 011604 (2010).
- Shieh, I., Waring, A. J., Zasadzinski, J. A. Visualizing the analogy between competitive adsorption and colloid stability to restore lung surfactant function. Biophysical Journal. 102 (4), 777-786 (2012).
- Shieh, I., Zasadzinski, J. A. Visualizing monolayers with a water-soluble fluorophore to quantify adsorption, desorption and the double-layer. Proceedings of the National Academy of Sciences of the United States of America. 112 (8), 826-835 (2015).
- Lipp, M. M., Lee, K. Y. C., Takamoto, D. Y., Zasadzinski, J. A., Waring, A. J. Coexistence of buckled and flat monolayers. Physical Review Letters. 81, 1650-1653 (1998).
- Lipp, M. M., Lee, K. Y. C., Waring, A., Zasadzinski, J. A. Fluorescence, polarized fluorescence, and Brewster angle microscopy of palmitic acid and lung surfactant protein B monolayers. Biophysical Journal. 72 (6), 2783-2804 (1997).
- Alvarez, N. J., Walker, L. M., Anna, S. L. A microtensiometer to probe the effect of radius of curvature on surfactant transport to a spherical interface. Langmuir. 26 (16), 13310-13319 (2010).
- Ward, A. F. H., Tordai, L. Time dependents of boundary tensions of solutions. 1. The role of diffusion in time-effects. Journal of Chemical Physics. 14, 453-461 (1946).
- Lucassen, J., Vanden Tempel, M. Dynamic measurements of dilatational properties of a liquid interface. Chemical Engineering Science. 27 (6), 1283-1291 (1972).
- Lin, G. L., et al. Interfacial dilatational deformation accelerates particle formation in monoclonal antibody solutions. Soft Matter. 12 (14), 3293-3302 (2016).
- Bastacky, J., et al. Alveolar lining layer is thin and continuous: low temperature scanning electron microscopy of rat lung. Journal of Applied Physiology. 79 (5), 1615-1628 (1995).
- Adamson, A. W., Gast, A. P. . Physical Chemistry of Surfaces, Sixth ed. , 784 (1997).
- del Rio, O. I., Kwok, D. Y., Wu, R., Alvarez, J. M., Neumann, A. W. Contact angle measurements by axisymmetric drop shape analysis and an automated polynomial fit program. Colloids and Surfaces A Physicochemical and Engineering Aspects. 143 (2-3), 197-210 (1998).
- Kanthe, A., et al. No ordinary proteins: Adsorption and molecular orientation of monoclonal antibodies. Science Advances. 7 (5), 14 (2021).
- Manikantan, H., Squires, T. M. Surfactant dynamics: hidden variables controlling fluid flows. Journal of Fluid Mechanics. 892, 115 (2020).
- Narayan, S., et al. Dilatational rheology of water-in-diesel fuel interfaces: effect of surfactant concentration and bulk-to-interface exchange. Soft Matter. 17 (18), 4751-4765 (2021).
- Meng, G. N., Paulose, J., Nelson, D. R., Manoharan, V. N. Elastic instability of a crystal growing on a curved surface. Science. 343 (6171), 634-637 (2014).
- Kotula, A. P., Anna, S. L. Insoluble layer deposition and dilatational rheology at a microscale spherical cap interface. Soft Matter. 12 (33), 7038-7055 (2016).
- Lipp, M. M., Lee, K. Y. C., Zasadzinski, J. A., Waring, A. J. Phase and morphology changes in lipid monolayers induced by SP-B protein and its amino-terminal peptide. Science. 273 (5279), 1196-1199 (1996).
- Pocivavsek, L., et al. Stress and fold localization in thin elastic membranes. Science. 320 (5878), 912-916 (2008).
- Pocivavsek, L., et al. Lateral stress relaxation and collapse in lipid monolayers. Soft Matter. 4 (10), 2019-2029 (2008).
- Kim, K., Choi, S. Q., Squires, T. M., Zasadzinski, J. A. Cholesterol nanodomains: their effect on monolayer morphology and dynamics. Proceedings of the National Academy of Sciences of the United States of America. 110 (33), 3054-3060 (2013).
- Kim, K., Choi, S. Q., Zasadzinski, J. A., Squires, T. M. Interfacial microrheology of DPPC monolayers at the air-water interface. Soft Matter. 7 (17), 7782-7789 (2011).
- Kim, K., Choi, S. Q., Zasadzinski, J. A., Squires, T. M. Nonlinear chiral rheology of phospholipid monolayers. Soft Matter. 14 (13), 2476-2483 (2018).
- Kotula, A. P., Anna, S. L. Regular perturbation analysis of small amplitude oscillatory dilatation of an interface in a capillary pressure tensiometer. Journal of Rheology. 59, 85-117 (2015).

