Analyse de la forme des lignes des spectres RMN dynamiques pour caractériser les réarrangements de sphère de coordination dans un complexe chiral de polyhydrure de rhénium
Summary
L’analyse de la forme des lignes des spectres RMN recueillis sur une plage de températures sert de guide pour le réarrangement des atomes de la sphère de coordination interne à un complexe chiral de polyhydrure de rhénium(V) à huit coordonnées, ReH5(PPh3)2 (sec-butylamine). L’analyse de la forme des lignes est également utilisée pour déterminer les paramètres d’activation ΔH‡, ΔS‡ et ΔG‡ pour ces réarrangements d’atomes.
Abstract
La spectroscopie par résonance magnétique nucléaire (RMN) en solution dynamique est la méthode typique de caractérisation des réarrangements dynamiques des atomes dans la sphère de coordination pour les complexes de polyhydrure de métaux de transition. L’ajustement de la forme des lignes des spectres RMN dynamiques peut conduire à des estimations des paramètres d’activation des processus de réarrangement dynamique. Une combinaison de la spectroscopie RMN dynamique 31 P-{1 H} d’atomes de phosphore liés aux métaux avec la spectroscopie RMN dynamique 1H-{31P} des ligands hydrures peut identifier les réarrangements de ligands hydrures qui se produisent en conjonction avec un réarrangement d’atomes de phosphore. Pour les molécules qui présentent une telle paire couplée de réarrangements, la spectroscopie RMN dynamique peut être utilisée pour tester des modèles théoriques pour les réarrangements de ligands. La spectroscopie RMN dynamique 1H-{31P} et l’ajustement de la forme de ligne peuvent également identifier la présence d’un processus d’échange qui déplace un ligand hydrure spécifique au-delà de la sphère de coordination interne du métal par un échange de protons avec une molécule de solvant telle que l’eau adventice. La préparation d’un nouveau composé, ReH5(PPh3)2(sec-butylamine), qui illustre de multiples processus de réarrangement dynamique, est présentée ainsi que l’ajustement de la forme des lignes des spectres RMN dynamiques du complexe. Les résultats de l’ajustement de la forme de la ligne peuvent être analysés par l’équation d’Eyring pour estimer les paramètres d’activation des processus dynamiques identifiés.
Introduction
La spectroscopie RMN est couramment utilisée pour caractériser les processus dynamiques qui se produisent à l’intérieur ou entre les molécules. Pour de nombreux réarrangements intramoléculaires simples, l’estimation de ΔG‡ est aussi simple que la mesure de la différence de fréquence, Δν, entre deux résonances à la limite d’échange lent et la détermination de la température de coalescence pour ces mêmes résonances (Figure 1)1. La relation,
ΔG‡ = 4,575 x 10-3 kcal/mol x T c [9,972 + log (Tc/Δν)]
où Tc est la température de coalescence pour une paire de résonances qui représentent la forme d’échange lent d’un échantillon dynamique, peut être utilisé pour résoudre l’énergie libre d’activation pour un tel réarrangement dynamique. Les systèmes dynamiques plus complexes nécessitent l’ajustement de la forme des lignes des spectres RMN dynamiques ou une autre technique de RMN telle que la spectroscopie d’échange bidimensionnel (2D-EXSY) ou la spectroscopie d’effet Overhauser à cadre rotatif bidimensionnel (2D-ROESY) pour estimer les paramètres d’activation.
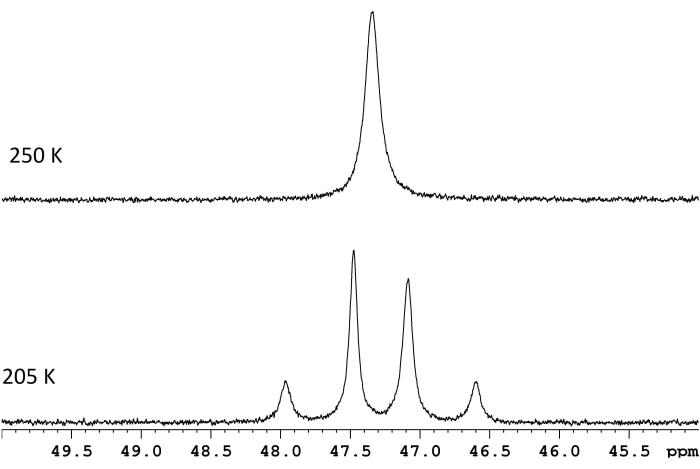
Figure 1 : Spectres RMN pour une solution d 8-toluène de ReH5(PPh3)2(sec-butylamine) à deux températures. La différence de fréquence entre les deux doublets à échange lent (trace inférieure, 117,8 Hz) et une température de coalescence de 250 K (trace supérieure) correspondent à une barrière d’énergie (ΔG‡) de 11,8 kcal/mol. Veuillez cliquer ici pour voir une version agrandie de cette figure.
L’ajustement de la forme des lignes des spectres RMN dynamiques est une technique courante utilisée depuis longtemps pour l’estimation des paramètres d’activation qui décrivent les réarrangements dynamiques pour les substances ayant une énergie d’activation d’environ 5 à 25 kcal/mol 2,3,4,5. La détermination des barrières énergétiques à l’échange de protons entre l’eau et les molécules d’amine6, la barrière énergétique à la rotation autour de la liaison C-N dans le diméthylformamide7, ou la taille générale des fractions organiques8 ne sont que quelques exemples des nombreuses propriétés qui ont été évaluées par ajustement de la forme des raies des spectres RMN dynamiques. Ce manuscrit démontre l’utilisation de l’ajustement de la forme des lignes pour caractériser les processus dynamiques intermoléculaires et intramoléculaires qui se produisent pour le complexe ReH5 (PPh3) 2 (sec-butyl amine). Les objectifs de cette expérience et d’expériences similaires d’ajustement de la RMN en forme de ligne sont les suivants: 1) caractériser tous les processus d’échange d’atomes dynamiques intramoléculaires observables RMN s’ils sont présents, 2) identifier et caractériser les processus d’échange d’atomes dynamiques intramoléculaires observables RMN s’ils sont présents, 3) identifier les échanges d’atomes intramoléculaires corrélés qui se produisent pour, dans cet exemple, les atomes d’hydrogène et de phosphore, et 4) pour l’exemple présenté ici, comparer deux modèles publiés pour les processus dynamiques qui se produisent dans le complexe ReH5(PPh3)2 (sec-butylamine).
Les systèmes de polyhydrure de rhénium(V) à huit coordonnées sont des systèmes dynamiques complexes dans lesquels les ligands participent à de multiples processus dynamiques et les atomes de phosphore peuvent participer à un processus dynamique unique qui est un deuxième aspect d’un processus d’échange de ligands hydrures 9,10,11,12,13,14,15,16,17,18 ,19,20,21,22,23,24,25,26,
27,28,29. Les complexes de polyhydrure de rhénium(V) pseudododécaédriques à huit coordonnées adoptent une géométrie moléculaire (Figure 2), qui peut être décrite comme une paire de trapèzes orthogonaux de ligands17,26. Les sommets sur les longs bords des trapèzes sont communément étiquetés comme des sites B et, dans les complexes de polyhydrure de rhénium, sont généralement les sites occupés par des ligands donneurs neutres à deux électrons tels que les phosphines tertiaires ou les ligands amine. Les sommets sur les bords courts des trapèzes sont communément étiquetés comme des sites A et sont généralement occupés par des ligands anioniques à deux électrons, hydrures. Les spectres RMN à température ambiante des complexes polyhydrure de rhénium(V) sont, généralement, trompeusement simples en raison des nombreux processus dynamiques qui se produisent dans les solutions à température ambiante.
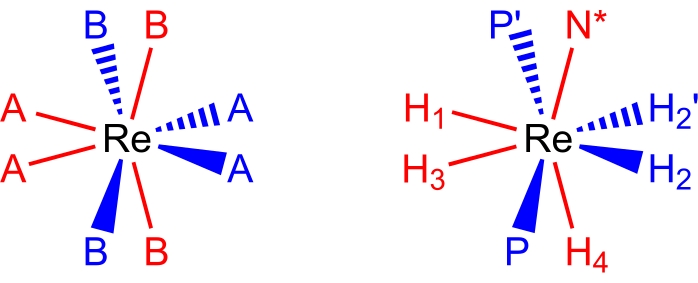
Figure 2 : Un ensemble de coordination dodécaédrique (à gauche) et le complexeReH5(PPh3)2(sec-butylamine) dans la même perspective (à droite). Les sites de couleur rouge représentent les sites de coordination qui forment un trapèze vertical, et les sites de couleur bleue représentent les sites de coordination qui forment un trapèze horizontal. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Les complexes de la forme ReH5(PPh3)2(amine) sont la classe de complexes polyhydrure de rhénium la plus étudiée en ce qui concerne les processus dynamiques 9,10,12,13,16,30,31. Trois processus dynamiques (Figure 3) ont été identifiés pour les complexes ReH5(PPh3)2(amine) : 1) un échange de protons entre le seul ligand hydrure du site B et un proton d’une molécule d’eau (fortuit ou intentionnel)9,13, 2) un échange tourniquet d’une paire de ligands hydrure de site A avec unligand 9 hydrure de site B adjacent, 11,13,30,31, et 3) une inversion stérique (ou pseudorotation) qui se manifeste par un échange par paires des ligands hydrures du site A et un mouvement par paires des atomes du site B vers le côté opposé du centre du rhénium (comme illustré sur la figure 4)4,5,6,8,26,27 . Le mouvement des atomes du site B vers le côté opposé du rhénium est observable par spectroscopie RMN dynamique comme: 1) un processus qui rend les 3 et 5 protons inéquivalents de N = pyridine équivalents à température ambiante10,30,31, 2) un processus qui provoque un échange rapide des isomères E et Z de N = ligands amines aromatiques substitués de manière asymétrique à température ambiante9, 10,13,30,31, ou 3) un processus qui provoque un échange rapide des perspectives stériques d’une paire diastéréotopique d’atomes de phosphore par rapport à un centre chiral situé sur le ligand amine9,30,31. Le complexe chiral ReH5(PPh3)2(sec-butylamine) qui n’a pas encore été signalé auparavant offre l’occasion de décrire de façon générale les méthodes qui peuvent être utilisées pour identifier et caractériser les réarrangements dynamiques des complexes de polyhydrure de rhénium.
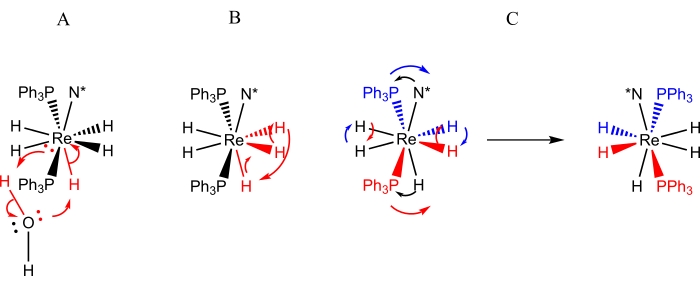
Figure 3 : Représentations des processus dynamiques observés par spectroscopie RMN pour les solutions deReH5(PPh3)2(sec-butylamine). La représentation A représente l’échange d’un seul proton d’eau adventive contre le ligand hydrure unique du site B. La représentation B représente l’échange de tourniquets de trois ligands hydrures adjacents, dont deux résident dans le site A tandis que le troisième est le ligand hydrure unique du site B. La représentation C représente à la fois l’échange par paires de ligands hydrures du site A ainsi que l’inversion stérique des atomes de phosphore par rapport au ligand amine chiral (N*). Il convient de noter que l’échange par paires du ligand de l’hydrure du site A ne nécessite pas de déplacement des ligands hydrure du site A vers le côté opposé du centre du rhénium. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Pour les systèmes chimiques tels que les complexes de polyhydrure de rhénium, qui présentent un ensemble complexe de processus dynamiques, l’ajustement de la forme des lignes des spectres RMN dynamiques est la technique RMN la plus utilisée pour caractériser les processus 9,11,13,16,21,29. Les technologies bidimensionnelles EXSY 9,32 ou 2D-ROESY11 sont des techniques alternatives de RMN dynamique qui peuvent également être utilisées pour caractériser quantitativement les processus dynamiques. Les spectres EXSY bidimensionnels sont généralement mesurés dans le domaine de la température d’échange lent; les spectres ROESY bidimensionnels sont généralement mesurés dans le domaine de la température d’échange rapide. Les deux techniques bidimensionnelles peuvent nécessiter beaucoup de temps dans le spectromètre pour l’acquisition de données, en ce sens que chacune des techniques acquiert un ensemble de données beaucoup plus grand, à une température donnée, que les ensembles de données unidimensionnels nécessaires pour l’analyse de l’ajustement de la forme de la ligne. Des processus dynamiques simples qui sont bien compris, tels que l’échange dynamique des deux groupes méthyle du diméthylformamide, peuvent être facilement caractérisés par l’une des trois techniques de RMN. Des systèmes plus complexes, tels que ReH5 (PPh3) 2 (sec-butyl amine), dans lesquels des ligands d’hydrures individuels participent à de multiples processus dynamiques, ou des systèmes qui ne sont pas nécessairement bien compris, tels qu’un nouveau complexe polyhydrure de métal de transition qui peut ou non échanger des protons entre un ligand hydrure hydrure et de l’eau adventive, sont plus facilement caractérisés quantitativement par la méthode RMN ajustée en forme de ligne que par les méthodes de RMN bidimensionnelle. Contrairement aux méthodes de RMN bidimensionnelle, la méthode d’ajustement de la forme de ligne fournit une visualisation facilement interprétable de la correspondance entre un modèle testé et les données expérimentales ainsi que la preuve visuelle d’un échange qui déplace un ligand hydrure au-delà de la sphère de coordination interne du rhénium. Sur la base des hauteurs et des formes des pics dans les spectres d’échange lent, même un système dynamique complexe tel que ReH5 (PPh3) 2 (sec-butylamine) peut conduire à un ensemble initial de modèles d’échange facilement testés. De plus, lorsque plusieurs modèles théoriques ont été rapportés pour une transformation moléculaire, l’ajustement de la forme des lignes des spectres RMN dynamiques peut permettre une comparaison visuelle de chaque modèle par rapport aux spectres observés.
Au-delà des trois techniques de RMN mentionnées ci-dessus, des expériences de RMN de substitution isotopique impliquantD2Oou HD ont été utilisées pour démontrer qualitativement l’échange intermoléculaire d’atomes pour des systèmes complexes de polyhydrure de rhénium, mais n’ont pas été utilisées pour les caractérisations quantitatives 9,33,34,35. Les calculs théoriques présentent une méthode supplémentaire pour caractériser les processus dynamiques des systèmes dynamiques complexes30,31,36. Les calculs théoriques ont l’avantage sur l’ajustement de forme de ligne en ce sens qu’ils peuvent être utilisés pour différencier les possibilités qui ne peuvent pas être distinguées par l’analyse de l’ajustement de forme de ligne. Par exemple, des calculs théoriques ont été utilisés pour décrire un échange qui implique trois ligands hydrures adjacents sur certains complexes rhénium(V) comme un échange tourniquet des trois ligands hydrures, plutôt qu’une paire alternée d’échanges par paires avec chaque échange par paires, y compris un ligand hydrure unique et l’un des deux ligands hydrures chimiquement équivalents30, 31. Les résultats des calculs théoriques sont généralement comparés aux caractérisations quantitatives observées expérimentalement à partir de l’une des trois techniques de RMN mentionnées ci-dessus pour vérifier la validité des résultats calculés.
L’ajustement de la forme des lignes des spectres RMN dynamiques tire parti du changement d’apparence des spectres RMN qui se produit lorsque les noyaux actifs RMN se déplacent entre différents environnements chimiques lors d’une mesure RMN. Les spectres RMN à échange lent (spectres avec des résonances lorentziennes indépendantes pour chaque ensemble de noyaux échangeurs) se produisent à des températures où la différence de fréquence entre les résonances pour les noyaux qui s’échangent est grande par rapport à la vitesse d’échange des noyaux37. Les spectres RMN à échange rapide (spectres avec une seule résonance lorentzienne pour l’échange de noyaux) se produisent à des températures où la vitesse d’échange des noyaux est beaucoup plus grande que la différence de fréquence entre les résonances d’échange lent37. Les taux de change intermédiaires se produisent pour les températures comprises entre le domaine de température d’échange lent et le domaine de température d’échange rapide37. Si les paramètres fondamentaux de la fréquence de Larmor, du décalage chimique des noyaux échangeurs, des constantes de couplage (le cas échéant) pour les noyaux échangeurs et des populations relatives de chaque type de noyau sont connus, les constantes de vitesse pour les échanges putatifs entre noyaux peuvent être déterminées en comparant les spectres simulés aux spectres observés à plusieurs températures intermédiaires. De bons ajustements pour les simulations à plusieurs températures donnent des données de constante de température et de vitesse qui peuvent être utilisées avec l’équation d’Eyring pour estimer les paramètres d’activation pour le ou les échanges putatifs. Les résultats de la méthode se sont avérés à la fois exacts et reproductibles.
Protocol
Representative Results
Discussion
Il y a quatre éléments dans la préparation de ReH7(PPh3)2 qui peuvent avoir une incidence sur la quantité et la pureté du matériau produit. Tout d’abord, l’utilisation d’un bain de glace pendant les 15 premières minutes de la réaction est importante pour éliminer la chaleur de la réaction qui se produit entre le borohydrure de sodium et l’eau. Des températures initiales plus élevées entraînent une diminution du rendement du produit ReH7(PPh 3)2 en raison d…
Declarações
The authors have nothing to disclose.
Acknowledgements
Les auteurs remercient le Département de chimie et de physique et le Programme de subventions pour la créativité et la recherche (Naik, Moehring) de l’Université Monmouth pour leur soutien financier à ce travail.
Materials
| Bruker Avance II 400 MHz NMR spectrometer | Bruker Biospin | The instrument includes a two channel probe (1H and X) with the X channel tunable from 162 MHz to 10 Mhz. The instrument is also VT capable with a dewar and heat exchanger for VT work. | |
| d8-toluene | MilliporeSigma | 434388 | |
| Powerstat variable transformer | Powerstat | ||
| sec-butyl amine | MilliporeSigma | B89000 | |
| Sodium borohydride | MilliporeSigma | 452882 | |
| Tetrahydrofuran | MilliporeSigma | 186562 | |
| Thermowell C3AM 100 mL | Thermowell | ||
| Topspin 3.0 or 4.1.4 with dNMR | Bruker Biospin | Data was acquired with Topspin version 3.0 and data handling was performed on a second computer that was running Topspin version 4.1.4.. | |
| Trichlorooxobis(triphenylphosphine) rhenium(V) | MilliporeSigma | 370193 | |
| Vacuubrand PC3000 vacuum pump with a CVC 3000 controller | Vacuubrand |
Referências
- Zimmer, K. D., Shoemaker, R., Ruminski, R. R. Synthesis and characterization of a fluxional Re(I) carbonyl complex fac-[Re(CO)3(dpop’)Cl] with the nominally tri-dentate ligand dipyrido(2,3-α:3′,2′-j)phenazine (dpop). Inorganica Chimica Acta. 359 (5), 1478-1484 (2006).
- McGlinchey, M. J. Symmetry breaking in NMR spectroscopy: the elucidation of hidden molecular rearrangement processes. Symmetry. 6 (3), 622-654 (2014).
- Casarini, D., Luazzi, L., Mazzanti, A. Recent advances in stereodynamics and conformational analysis by dynamic NMR and theoretical calculations. European Journal of Organic Chemistry. 2010 (11), 2035 (2010).
- Palmer, A. G., Williams, J., McDermott, A. Nuclear magnetic resonance studies of biopolymer dynamics. Journal of Physical Chemistry. 100 (31), 13293-13310 (1996).
- Kern, D., Kern, G., Scherer, G., Fischer, G., Drakenberg, T. Kinetic analysis of cyclophilin-catalyzed prolyl cis/trans isomerization by dynamic NMR spectroscopy. Bioquímica. 34 (41), 13594-13602 (1995).
- Menger, F. M., Lynn, J. L. Fast proton transfer at a micelle surface. Journal of the American Chemical Society. 97 (4), 948-949 (1975).
- Pines, A., Rabinovitz, M. A nuclear magnetic resonance total line-shape treatment of internal rotation in dimethylformamide. Tetrahedron Letters. 9 (31), 3529-3532 (1968).
- Mancinelli, M., Bencivenni, G., Pecorari, D., Mazzanti, A. Stereochemistry and recent applications of axially chiral organic molecules. European Journal of Organic Chemistry. 2020 (27), 4070-4086 (2020).
- Streisel, D. J., et al. Fluxionality, substitution, and hydrogen exchange at eight-coordinate rhenium(V) polyhydride centers. Inorganica Chimica Acta. 496 (1), 119028 (2019).
- Jimenez, Y., Strepka, A. M., Borgohain, M. D., Hinojosa, P. A., Moehring, G. A. Ortho-metalation, rotational isomerization, and hydride-hydride coupling at rhenium(V) polyhydride complexes stabilized by aromatic amine ligands. Inorganica Chimica Acta. 362 (9), 3259-3266 (2009).
- Lee, J. C., Yao, W., Crabtree, R. H., Ruegger, H. Fluxionality in [ReH5(PPh3)2(pyridine)]. Inorganic Chemistry. 35 (3), 695-699 (1996).
- Patel, B. P., Kavallieratos, K., Crabtree, R. H. Effects of dihydrogen bonding on fluxionality in ReH5(PPh3)2L. Journal of Organometallic Chemistry. 528 (1), 205-207 (1997).
- Geetha, B., et al. Chiral amine ligands at rhenium(V) pentahydride complexes allow for characterization of an energetically accessible and reversible steric inversion of diastereotopic phosphorus atoms. Inorganica Chimica Acta. 531 (1), 120741 (2022).
- Paulo, A., Ascenso, J., Domingos, A., Galvao, A., Santos, I. Rhenium-(III) and -(V) hydride complexes with modified poly(pyrazolyl)borates. Journal of the Chemical Society, Dalton Transactions. 1999 (8), 1293-1300 (1999).
- Bianchini, C., et al. Synthesis and characterization of rhenium polyhydrides stabilized by the tripodal ligand MeC(CH2PPh2)3. Journal of Organometallic Chemistry. 451 (1), 97-106 (1993).
- Scorzelli, A. G., Macalush, B. E., Naik, D. V., Moehring, G. A. Comparative study of fluxional processes at two different classes of eight-coordinate rhenium(V) polyhydride complexes. Inorganica Chimica Acta. 516 (1), 120120 (2021).
- Luo, X. -. L., Crabtree, R. H. Synthesis and spectroscopic characterization of rhenium complexes ReH5(triphos)] and [ReH6(triphos)]+ [triphos = PPh(CH2CH2PPh2)2]. Journal of the Chemical Society. 1991 (5), 587-590 (1991).
- Kim, Y., Deng, H., Gallucci, J. C., Wojcicki, A. Rhenium polyhydride complexes containing PhP(CH2CH2CH2PCy2)2 (Cyttp): protonation, insertion, and ligand substitution reactions of ReH5(Cyttp) and structural characterization of ReH5(Cyttp) and [ReH4(η2-H2)(Cyttp)]SbF6. Inorganic Chemistry. 35 (24), 7166-7173 (1996).
- Bolano, S., et al. Synthesis, characterization, protonation studies and X-ray crystal structure of ReH5(PPh3)2(PTA) (PTA = 1,3,5-triaza-7-phosphaadamantane). Journal of Organometallic Chemistry. 691 (4), 629-637 (2006).
- Ginsberg, A. P., Abrahams, S. C., Jamieson, P. B. Nonrigid stereochemistry in eight-coordinate pentahydridorhenium complexes. Journal of the American Chemical Society. 95 (14), 4751-4752 (1973).
- Bolano, S., Bravo, J., Garcia-Fontan, S. Mono- and dinuclear rhenium polyhydride complexes bearing the chelating ligand 1,2-bis(dicyclohexylphosphinanyloxy)ethane. European Journal of Inorganic Chemistry. 2004 (24), 4812-4819 (2004).
- Leeaphon, M., Rohl, K., Thomas, R. J., Fanwick, P. E., Walton, R. A. Reactions of the polyhydride complex ReH7(PPh3)2 with quinoline, 2-hydroxyquinoline, and 2-mercaptoquinoline. The preparation and characterization of hydrido complexes of rhenium(V) and chloro complexes of rhenium(III). Inorganic Chemistry. 32 (24), 5562-5568 (1993).
- Mejia, E., Togni, A. Rhenium complexes containing the chiral tridentate ferrocenyl ligand pigiphos. Organometallics. 30 (17), 4765-4770 (2011).
- Moehring, G. A., Walton, R. A. Reactions of heptahydrobis(triphenylphosphine)rhenium with bidentate aromatic heterocycles. Inorganic Chemistry. 26 (17), 2910-2912 (1987).
- Kosanovich, A. J., Reibenspies, J. H., Ozerov, A. V. Complexes of high-valent rhenium supported by the PCP pincer. Organometallics. 35 (4), 513-519 (2016).
- Emge, T. J., Koetzle, T. F., Bruno, J. W., Caulton, K. G. Pentahydridorhenium: crystal and molecular structure of ReH5(PMePh2)3. Inorganic Chemistry. 23 (24), 4012-4017 (1984).
- Costello, M. T., Fanwick, P. E., Green, M. A., Walton, R. A. Reactions of Heptahydridobis(triphenylphosphine)rhenium with 1-(diphenylphosphino)-2-(diphenylarsino)ethane (arphos) and 1,2-bis(diphenylarsino)ethane (dpae). Structural characterization of ReH5(PPh3)2(arphos-As) and ReH5(PPh3)2(dpae-As). Inorganic Chemistry. 30 (4), 861-864 (1991).
- Alvarez, D., Lundquist, E. G., Ziller, J. W., Evans, W. J., Caulton, K. G. Synthesis, structure and applications of transition-metal polyhydride anions. Journal of the American Chemical Society. 111 (22), 8392-8398 (1989).
- Albinati, A., et al. Synthesis, characterization, and interconversion of the rhenium polyhydrides ReH3(η4-NP3)] and [ReH4(η4-NP3)]+ {NP3 = tris[2-(diphenylphosphanyl)ethyl]amine}. European Journal of Inorganic Chemistry. 2002 (6), 1530-1539 (2002).
- Bosque, R., et al. Site preference energetics, fluxionality, and intramolecular M−H···H−N hydrogen bonding in a dodecahedral transition metal polyhydride. Inorganic Chemistry. 36 (24), 5505-5511 (1997).
- Tao, Y., Sou, W., Luo, G. -. G., Kraka, E. Describing polytopal rearrangement processes of octacoordinate structures. I. renewed insights into fluxionality of the rhenium polyhydride complex ReH5(PPh3)2(Pyridine). Inorganic Chemistry. 60 (4), 2492-2502 (2021).
- Beringhelli, T., D’Alfonso, G., Minoja, A. P. Rhenium-platinum mixed metal clusters. Characterization in solution and dynamic behavior of the isomers of [Re3Pt(µ-H3)(CO)14]. An example of a labile metal fragment that undergoes intermolecular exchange. Organometallics. 13 (2), 663-668 (1994).
- Grieco, G., Blacque, O. Solution and solid-state structure of the first NHC-substituted rhenium heptahydrides. European Journal of Inorganic Chemistry. 2019 (34), 3810-3819 (2019).
- Wazio, J. A., Jimenez, V., Soparawalla, S., John, S., Moehring, G. A. Hydrogen exchange of rhenium(VII) heptahydridobis(triphenylphosphine) with water, aniline, methanol, and itself. Inorganica Chimica Acta. 362 (1), 159-165 (2009).
- Chatt, J., Coffey, R. S. Hydrido-complexes of rhenium-containing tertiary phosphines. Journal of the Chemical Society, A. 1969, 1963-1972 (1969).
- Tao, Y., Wang, X., Zou, W., Luo, G. -. G., Kraka, E. Unusual intramolecular motion of ReH92- in K2ReH9 crystal: circle dance and three-arm turnstile mechanisms revealed by computational study. Inorganic Chemistry. 61 (2), 1041-1050 (2022).
- Berger, X., Braun, S. . 200 and More NMR Experiments a Practical Course. , (2004).
- He, G., Chen, J., Sung, H. H. -. Y., Williams, I. D., Jia, G. Substituent effect on reactions of ReH5(PMe2Ph)3 with propargyl alcohols. Inorganica Chimica Acta. 518 (1), 120239 (2021).
- Donnelly, L. J., Parsons, S., Morrison, C. A., Thomas, S. P., Love, J. B. Synthesis and structures of anionic rhenium polyhydride complexes of boron-hydride ligands and their application in catalysis. Chemical Science. 11 (9), 9994-9999 (2020).
- Donnelly, L. J., et al. C-H borylation catalysis of heteroaromatics by a rhenium boryl polyhydride. ACS Catalysis. 11 (12), 7394-7400 (2021).
- Jin, H., et al. CO-enabled rhenium hydride catalyst for directed C(sp2)-H bond alkylation with olefins. Organic Chemistry Frontiers. 2 (4), 378-382 (2015).
- Takaya, H., Ito, M., Murahashi, S. -. I. Rhenium-catalyzed addition of carbonyl compounds to the carbon−nitrogen triple bonds of nitriles: α-C−H activation of carbonyl compounds. Journal of the American Chemical Society. 131 (31), 10824-10825 (2009).
- Carr, S. W., Fowles, E. H., Fontaine, X. L. R., Shaw, B. L. Multihydride complexes of rhenium, osmium or iridium containing monodentate ditertiary phosphine ligands: selective hydrogen-deuterium exchanges of the rhenium multihydrides. Journal of the Chemical Society, Dalton Transactions. 1990 (2), 573-579 (1990).
- Jin, H., et al. Rhenium-catalyzed acceptorless dehydrogenative coupling via dual activation of alcohols and carbonyl compounds. ACS Catalysis. 3 (10), 2195-2198 (2013).
- Loza, M. L., de Gala, S., Crabtree, R. H. Steric crowding in a rhenium polyhydride induced by a chelating disilyl ligand: synthesis, characterization, and reactivity of ReH5(disil)(PPh3)2 (disil = 1,2-Bis(dimethylsilyl)benzene and 1,2-Bis(dimethylsilyl)ethane). Inorganic Chemistry. 33 (22), 5073-5078 (1994).
- Lin, Y., Zhu, X., Xiang, M. Transition metal polyhydrides-catalyzed addition of activated nitriles to aldehydes and ketones via Knoevenagel condensation. Journal of Organometallic Chemistry. 448 (1-2), 215-218 (1993).
- Abdukader, A., Jin, H., Cheng, Y., Zhu, C. Rhenium-catalyzed amination of alcohols by hydrogen transfer process. Tetrahedron Letters. 55 (30), 4172-4174 (2014).
- Lin, Y., Zhou, Y. Selective transfer hydrogenation catalyzed by transition metal polyhydrides. Fenzi Cuihua. 5 (2), 119-124 (1991).
- Green, M. A., Huffman, J. C., Caulton, K. G., Rybak, W. K., Ziolkowski, J. J. Ligand scavenging and catalytic utilization of the phototransient ReH5(PMe2Ph)2. Journal of Organometallic Chemistry. 218 (2), 39-43 (1981).
- Komiya, S., Chigira, T., Suzuki, T., Hirano, M. Polymerization of alkyl methacrylate catalyzed by hydridorhenium complexes. Chemistry Letters. 4 (4), 347-348 (1999).
- Michos, D., Luo, X. L., Faller, J. W., Crabtree, R. H. Tungsten(VI) hexahydride complexes supported by chelating triphosphine ligands: protonation to give η2-dihydrogen complexes and catalytic dehydrogenation of cyclooctane to cyclooctene. Inorganic Chemistry. 32 (8), 1370-1375 (1993).

