関節疾患のモデリングと薬剤検査のための膝関節チップの作成
Summary
ヒト間葉系幹細胞から4種類の組織を作製し、ヒト膝関節の軟骨、骨、脂肪パッド、滑膜を再現するための詳細な方法を提供します。これらの4つの組織は、カスタマイズされたバイオリアクターに統合され、マイクロ流体工学を介して接続されるため、膝関節オンチップが生成されます。
Abstract
変形性関節症(OA)のような衰弱性関節疾患の高い有病率は、高い社会経済的負担をもたらします。現在、関節障害を標的とする利用可能な薬はほとんどが緩和的です。効果的な疾患修飾OA薬(DMOAD)の満たされていないニーズは、主に疾患メカニズムを研究し、潜在的なDMOADをテストするための適切なモデルがないことによって引き起こされてきました。ここでは、ヒト間葉系幹細胞(MSC)に由来する脂肪、線維、および骨軟骨組織成分を含むミニチュア滑膜関節模倣微生物生理学的システム(miniJoint)の確立について説明します。三次元(3D)微小組織を得るために、MSCを、分化前または分化後に光架橋可能なメタクリレートゼラチンに封入した。次に、細胞を含む組織構築物を3Dプリントされたバイオリアクターに統合し、miniJointを形成しました。骨形成性、線維形成性、および脂肪生成性媒体の別々の流れを導入して、それぞれの組織表現型を維持した。一般的に共有される流れは、軟骨、滑膜、および脂肪組織を介して灌流され、組織のクロストークを可能にしました。このフローパターンにより、機構研究のための1つまたは複数の組織成分における摂動の誘導が可能になります。さらに、潜在的なDMOADは、すべての媒体ストリームを介した「全身投与」、または共有された「滑液」シミュレーションフローのみに薬物を添加することによる「関節内投与」のいずれか を介して テストできます。したがって、miniJointは、個別化医療における疾患メカニズムを効率的に研究し、薬物をテストするための汎用性の高い in vitro プラットフォームとして機能します。
Introduction
変形性関節症(OA)のような関節疾患は非常に蔓延しており、衰弱させ、世界中の障害の主な原因となっています1。米国だけでも、OAは2,700万人の患者に影響を及ぼし、60歳以上の成人の12.1%に発生していると推定されています2。残念ながら、現在関節疾患の管理に使用されているほとんどの薬は緩和薬であり、効果的な疾患修飾OA薬(DMOAD)は入手できません3。この満たされていない医療ニーズは、主に、疾患メカニズムを研究し、潜在的なDMOADを開発するための効果的なモデルがないことに起因しています。従来の2次元(2D)細胞培養は、関節組織の3D特性を反映しておらず、組織外植片の培養は、著しい細胞死によって妨げられることが多く、通常、動的な組織相互接続を再現できません4。さらに、遺伝的および解剖学的差異は、動物モデルの生理学的関連性を有意に低下させる4。
臓器チップ(OoC)、または微小生理学的システムは、工学、生物学、および医学のインターフェースにおける有望な研究分野です。これらのインビトロプラットフォームは、それらのインビボ対応物の定義された健康的または病理学的特徴を複製する最小の機能単位である5。さらに、これらの小型化されたシステムは、多様な細胞およびマトリックスをホストし、異なる組織間の生物物理学的および生化学的相互作用をシミュレートすることができる。したがって、天然の滑膜関節を忠実に再現できる微生物生理学的システムは、関節疾患をモデル化し、潜在的なDMOADを開発するための効果的なプラットフォームを提供することを約束します。
ヒト間葉系幹細胞(MSC)は、全身の多くの組織から単離され、骨形成性、軟骨形成性、および脂肪生成性系統に分化することができます6。MSCは、骨、軟骨、脂肪組織を含むさまざまな組織のエンジニアリングに成功しており6、膝関節の組織コンポーネントを設計するための有望な細胞源であることを意味します。私たちは最近、MSC由来の骨、軟骨、線維、脂肪組織で構成されるminiJointという名前のミニチュア関節模倣微生物生理学的システムを開発しました7。特に、この斬新な設計により、マイクロ流体の流れや透過による組織クロストークが可能になります(図1)。ここでは、チップコンポーネントの製造、組織コンポーネントのエンジニアリング、チップ内の操作された組織の培養、および下流の分析のための組織の収集のためのプロトコルを示します。
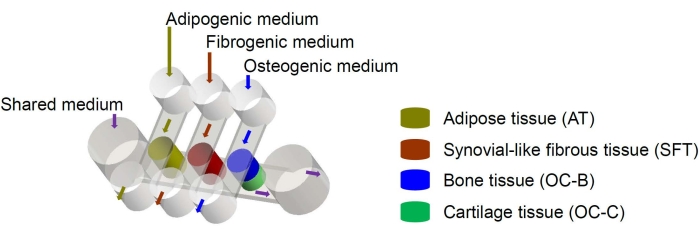
図1:さまざまな組織コンポーネントと媒体の流れの配置を示すminiJointチップの概略図。OC =骨軟骨組織。この図の拡大版を表示するには、ここをクリックしてください。
Protocol
Representative Results
Discussion
本稿では、骨、軟骨、脂肪組織、滑膜様組織を間葉系幹細胞から形成し、カスタマイズされたバイオリアクター内で共培養する膝関節オンチップシステムを作成するためのプロトコルを紹介します。プラグアンドプレイ機能を備えたこの多成分ヒト細胞由来システムは、関節疾患の病因を研究し、医薬品を開発するための新しいツールです。
異なる組織が特定の培地を?…
Declarações
The authors have nothing to disclose.
Acknowledgements
この研究は主に国立衛生研究所(UG3/UH3TR002136、UG3/UH3TR003090)からの資金提供を受けて行われた。さらに、ヒト組織サンプルを提供してくれたPaul Manner博士(ワシントン大学)と、MSCの単離と細胞プールの作成に協力してくれたJian Tan博士に感謝します。
Materials
| 3-isobutyl-1-methylxanthine | Sigma -Aldrich | I17018-1G | |
| 6 well non-tissue culture plate | Corning Falcon® Plates | 351146 | |
| 24 well non-tissue culture plate | Corning Falcon® Plates | 351147 | |
| 30 mL syringes | BD Syringe Luer Lock Cascade Health | 302832 | |
| Alcian blue stain | EK Industries | 1198 | 1% w/v, pH 1.0 |
| Advanced DMEM | Gibco | 12491-015 | |
| αMEM | Gibco | 12571-063 | |
| Antibiotic-antimycotic | Gibco | 15240-062 | |
| Biopsy punch | Integra Miltex | 12-460-407 | |
| BODIPY® fluorophore | Molecular Probes | ||
| Bone morphogenic protein 7 (BMP7) | Peprotech | ||
| Curved forceps | Fisher Brand | 16100110 | |
| DMEM | Gibco | 11995-065 | Dulbecco’s Modified Eagle Medium |
| Dexmethasome | Sigma -Aldrich | 02-05-2002 | |
| E-Shell 450 photopolymer in | EnvisionTec | RES-01-4022 | |
| Fetal Bovine Serum | Gemini-Bio Products | 900-208 | |
| GlutaMAX | Gibco | 3505-061 | |
| gelatin from bovine skin | Hyclone | 1003372809 | |
| Hank’s Balanced Salt Solution | Sigma -Aldrich | SH30588.02 | |
| indomethacin | Sigma -Aldrich | I7378-56 | |
| Insulin-Transferrin-Selenium-Ethanolamine (ITS) | Gibco | 51500-056 | |
| interleukin 1β | Peprotech | 200-01B | |
| Leur-loc connectors | Cole-Parmer Instruments | 45508-50 | |
| L-proline | Sigma -Aldrich | 115388-93-7 | |
| β-glycerophosphate | Sigma -Aldrich | 1003129352 | |
| Medium bags | KiYATEC | FC045 | |
| Methacrylic Anhydride | Sigma -Aldrich | 102378580 | |
| Phosphate buffered Saline | Corning | 21-040-CM | |
| Pointed forceps | Fisher Brand | 12000122 | |
| Silicon mold | McMaster-Carr | RC00114P | |
| Silicon o-rings | McMaster-Carr | ZMCCs1X5 | 1mm x 5mm |
| SolidWorks | Dassault Systèmes SE, Vélizy-Villacoublay, France | ||
| Surgical Blades | Integra Miltex | 4-122 | |
| Syringe pump | Lagato210P, KD Scientific | Z569631 | 10 syringe racks |
| T-182 tissue culture flasks | Fisher Brand | FB012939 | |
| Tissue Culture Dish 150 mm | Fisher Brand | FB012925 | |
| Transforming Growth Factor Beta (TGF-β3) | Peprotech | 100-36E | |
| Trypsin | Gibco | 25200-056 | |
| UV Flashlight | KBS | KB70109 | 395 nm |
| Vida Desktop 3D Printer | EnvisionTec | ||
| Vitamin D3 | Sigma -Aldrich | 32222-06-3 | 1,25-dihydroxyvitamin D3 |
Referências
- Safiri, S., et al. Global, regional and national burden of osteoarthritis 1990-2017: A systematic analysis of the Global Burden of Disease Study 2017. Annals of the Rheumatic Diseases. 79 (6), 819-828 (2020).
- Lawrence, R. C., et al. Estimates of the prevalence of arthritis and other rheumatic conditions in the United States: Part II. Arthritis and Rheumatism. 58 (1), 26-35 (2008).
- Makarczyk, M. J., et al. Current models for development of disease-modifying osteoarthritis drugs. Tissue Engineering. Part C, Methods. 27 (2), 124-138 (2021).
- He, Y., et al. Pathogenesis of osteoarthritis: risk factors, regulatory pathways in chondrocytes, and experimental models. Biologia. 9 (8), 194 (2020).
- Ronaldson-Bouchard, K., Vunjak-Novakovic, G. Organs-on-a-chip: A fast track for engineered human tissues in drug development. Cell Stem Cell. 22 (3), 310-324 (2018).
- Lin, H., Sohn, J., Shen, H., Langhans, M. T., Tuan, R. S. Bone marrow mesenchymal stem cells: aging and tissue engineering applications to enhance bone healing. Biomaterials. 203, 96-110 (2019).
- Li, Z., et al. Human mesenchymal stem cell-derived miniature joint system for disease modeling and drug testing. Advanced Science. 9 (21), 2105909 (2022).
- Lin, H., Cheng, A. W., Alexander, P. G., Beck, A. M., Tuan, R. S. Cartilage tissue engineering application of injectable gelatin hydrogel with in situ visible-light-activated gelation capability in both air and aqueous solution. Tissue Engineering. Part A. 20 (17-18), 2402-2411 (2014).
- Fairbanks, B. D., Schwartz, M. P., Bowman, C. N., Anseth, K. S. Photoinitiated polymerization of PEG-diacrylate with lithium phenyl-2,4,6-trimethylbenzoylphosphinate: polymerization rate and cytocompatibility. Biomaterials. 30 (35), 6702-6707 (2009).
- Lin, H., Lozito, T. P., Alexander, P. G., Gottardi, R., Tuan, R. S. Stem cell-based microphysiological osteochondral system to model tissue response to interleukin-1β. Molecular Pharmaceutics. 11 (7), 2203-2212 (2014).
- Yin, B., et al. Hybrid macro-porous titanium ornamented by degradable 3D gel/nHA micro-scaffolds for bone tissue regeneration. International Journal of Molecular Sciences. 17 (4), 575 (2016).
- Lin, Z., et al. Osteochondral tissue chip derived from iPSCs: Modeling OA pathologies and testing drugs. Frontiers in Bioengineering and Biotechnology. 7, 411 (2019).
- Atukorala, I., et al. Synovitis in knee osteoarthritis: A precursor of disease. Annals of the Rheumatic Diseases. 75 (2), 390-395 (2016).
- Occhetta, P., et al. Hyperphysiological compression of articular cartilage induces an osteoarthritic phenotype in a cartilage-on-a-chip model. Nature Biomedical Engineering. 3 (7), 545-557 (2019).
- He, C., et al. Modeling early changes associated with cartilage trauma using human-cell-laden hydrogel cartilage models. Stem Cell Research and Therapy. 13 (1), 400 (2022).
- Elsissy, J. G., et al. Bacterial septic arthritis of the adult native knee joint: A review. JBJS Reviews. 8 (1), 0059 (2020).
- Romero-Lopez, M., et al. Macrophage effects on mesenchymal stem cell osteogenesis in a three-dimensional in vitro bone model. Tissue Engineering. Part A. 26 (19-20), 1099-1111 (2020).

