Nachweis von abnormalem Prionprotein durch Immunhistochemie
Summary
Die Immunmarkierung abnormaler Prionproteine unter Verwendung immunhistochemischer Protokolle erfordert spezifische Methoden zur Herstellung von Proben- und Anti-PrP-Antikörpern. Das vorliegende Protokoll beschreibt die wichtigsten Schritte bei der Epitop-Demaskierung, um eine korrekte PrP-Immunmarkierung sicherzustellen und die unspezifische Hintergrundfärbung zu minimieren. Dieser Ansatz berücksichtigt auch Biosicherheitsmaßnahmen bei der Durchführung immunhistochemischer Studien mit den Prionen-infizierten Geweben.
Abstract
Abnorme Prionproteine (PrPSc) sind die krankheitsassoziierte Isoform des zellulären Prionproteins und diagnostische Marker für transmissible spongiforme Enzephalopathien (TSE). Diese neurodegenerativen Erkrankungen betreffen Menschen und verschiedene Tierarten und umfassen Scrapie, zoonotische bovine spongiforme Enzephalopathie (BSE), chronische Auszehrungskrankheit von Hirschen (CWD) und die neu identifizierte Kamel-Prionen-Krankheit (CPD). Die Diagnose von TSE beruht auf dem Immunnachweis von PrPSc durch Anwendung sowohl der Immunhistochemie (IHC) als auch der westlichen Immunoblot-Methoden (WB) auf Enzephalongewebe, nämlich den Hirnstamm (Obex-Spiegel). IHC ist eine weit verbreitete Methode, die primäre Antikörper (monoklonal oder polyklonal) gegen Antigene von Interesse in Zellen eines Gewebeschnitts verwendet. Die Antikörper-Antigen-Bindung kann durch eine Farbreaktion sichtbar gemacht werden, die in dem Bereich des Gewebes oder der Zelle, auf den der Antikörper gerichtet wurde, lokalisiert bleibt. Daher werden die immunhistochemischen Techniken bei Prionenerkrankungen, wie auch in anderen Forschungsgebieten, nicht nur zu diagnostischen Zwecken, sondern auch in Pathogenesestudien eingesetzt. Solche Studien beinhalten den Nachweis der PrPSc-Muster und -Typen aus den zuvor beschriebenen, um die neuen Prionenstämme zu identifizieren. Da BSE den Menschen infizieren kann, wird empfohlen, Einrichtungen und/oder Praktiken des Biosicherheitslabors der Stufe 3 (BSL-3) für den Umgang mit Rindern, kleinen Wiederkäuern und Hirschproben zu verwenden, die in die TSE-Überwachung einbezogen werden. Darüber hinaus werden nach Möglichkeit Containment- und Prionengeräte empfohlen, um die Kontamination zu begrenzen. Das PrPSc IHC-Verfahren besteht aus einem Ameisensäure-Epitop-Demaskierungsschritt, der auch als Prioneninaktivierungsmaßnahme fungiert, da formalinfixierte und in Paraffin eingebettete Gewebe, die in dieser Technik verwendet werden, infektiös bleiben. Bei der Interpretation der Ergebnisse muss darauf geachtet werden, die unspezifische Immunmarkierung von der Zielmarkierung zu unterscheiden. Zu diesem Zweck ist es wichtig, Artefakte der Immunmarkierung zu erkennen, die bei bekannten TSE-negativen Kontrolltieren erhalten wurden, um diese von spezifischen PrP Sc-Immunmarkierungstypen zu unterscheiden, die zwischen TSE-Stämmen, Wirtsspezies und prnp-Genotyp variieren können, die hierin näher beschrieben werden.
Introduction
Nach der Prionenhypothese ist die abnorme Isoform (PrPSc) die primäre oder einzige Komponente des Infektionserregers bei transmissiblen spongiformen Enzephalopathien (TSE). Die Bestätigung für die Diagnose von TSE beruht auf dem Immunnachweis von PrPSc durch Anwendung von immunhistochemischen (IHC) Protokollen und/oder westlichen Immunoblot-Methoden (WB) von Enzephalongeweben1.
IHC ist eine Methode, bei der monoklonale oder in einigen Fällen polyklonale Antikörper (als primäre Antikörper) als erster Schritt bei der Immunfärbung von spezifisch zielgerichteten Antigenen von Interesse, die sich in Zellen eines Gewebeschnitts befinden, verwendet werden. Jede effektive primäre Antikörper-Antigen-Bindung wird dann unter Verwendung von Sekundärantikörpern visualisiert, die für die primären Antikörper spezifisch sind. Diese sekundären Antikörper sind an Enzyme wie Meerrettichperoxidase (HRP) oder alkalische Phosphatase (AP) konjugiert. Die Visualisierung wird dann erreicht, indem diesen Enzymen ein Substrat hinzugefügt wird, wodurch unlösliche Farbprodukte entstehen, die in Bereichen lokalisiert sind, in denen die primären Antikörper an die Zielantigene gebunden sind. Eine verbesserte Visualisierung kann durch Gegenfärbung erreicht werden, wobei ein Farbstoff verwendet wird, um einen Kontrast zwischen immunmarkiertem und nicht immunmarkiertem Gewebezu erzeugen 2.
Bei IHC unter Verwendung von formalinfixiertem Paraffingewebe (FFPE) kann die Formalinfixierung die Wirksamkeit von Primärantikörpern aufgrund der Vernetzung durch Formaldehyd und Erwärmung und Dehydratisierung während der Paraffineinbettung zunichte machen. Diese verändern die Konformation von Proteinen, zerstören, denaturieren oder maskieren die Epitope, wodurch ihre Erkennung verringert oder aufgehobenwird 3. Dies erfordert daher eine Antigen-Retrieval (AR). Die AR-Techniken stören die Vernetzung der Formaldehyd-verwandten chemischen Gruppen in den antigenen Molekülen und stellen so die ursprüngliche Antigen-Protein-Konformation wieder her oder entlarven sie. Dies führt zur Wiederherstellung der Antikörper-Antigen-Affinität (Epitop) für die Immunmarkierung. Die letztendliche Wirksamkeit von AR hängt von den Eigenschaften des Zielantigens und/oder des Primärantikörpers2 ab.
Die Hitze-induzierte Antigen (Epitop) Retrieval (HIER) ist ein Verfahren von AR3 und wird routinemäßig für den PrPSc IHC-Nachweis verwendet, wie hierin beschrieben. IHC ist essentiell für die Diagnose und wird in Forschungslabors verwendet, um die Gewebeverteilung eines pathologieassoziierten Antigens zu bestimmen. Es wird unter anderem häufig bei der Diagnose und Erforschung von Krebs, Neurowissenschaften und Infektionskrankheiten4 eingesetzt. Bei TSE spielt IHC eine wichtige Rolle in der Diagnose und Forschung zur Bestätigung und Untersuchung der PrPSc-Verteilung in natürlichen Wirten und experimentellen Modellen. IHC trägt zu Prionen-Pathogenese-Studien und zur Analyse von PrP-Sc-Ablagerungstypen und -mustern bei, insbesondere in neuralen Geweben5, um Abweichungen von routinemäßig beschriebenen Infektionen zu erkennen und mutmaßliche neue Prionenstämme zu identifizieren.
Da Prionen der bovinen spongiformen Enzephalopathie (BSE) den Menschen infizieren können, können bestimmte Laborprotokolle, die an der Arbeit mit BSE beteiligt sind, die Verwendung von BSL-3-Einrichtungen und -Praktiken erfordern6. Dazu gehört die Verwendung eines versiegelten Sekundärbehälters für den Transport potenziell BSE-infizierter Gewebeproben innerhalb des Instituts und des Labors. Dazu gehört auch die Ausweisung von Eindämmungsbereichen und Prionen-Spezialgeräten für die BSE-Forschung und -Analyse, wann immer dies möglich ist. Dies geschieht, um eine Kontamination außerhalb des Arbeitsbereichs zu verhindern und einen begrenzten Raum zu schaffen, da Dekontaminationsverfahren erforderlich werden.
Dementsprechend befolgt das Labor für Pathologie des INIAV die empfohlenen Einrichtungen und Praktiken der Biosicherheitsstufe 3 (BSL-3) 6, um potenziell mit Prionen infizierte Gewebeproben von Rindern, kleinen Wiederkäuern und Hirschen im Zusammenhang mitder TSE-Überwachung zu verwalten.
Formalinfixierte und in Paraffin eingebettete Gewebe, die in TSE-Diagnose- oder Forschungsverfahren enthalten sind, insbesondere im Zentralnervensystem, können potenziell infektiös sein. Daher müssen diese fixierten Gewebe vor der Gewebeverarbeitung mit Ameisensäure behandelt werden, um die Infektiosität von Prionen, falls vorhanden, zu verringern. Dies geschieht durch Einlegen von fixierten, beschnittenen Geweben (ca. 2-4 mm Dicke) in eine Verarbeitungskassette. Die Kassette wird dann in 98% Ameisensäure getaucht (für 1 h). Nach dem Eintauchen werden die Kassetten mit Taschentüchern 30 Minuten lang in fließendem Leitungswasser gewaschen und vor der weiteren Verarbeitung in das Fixiermittel zurückgeführt. Wenn Gewebeschnitte vor der Verarbeitung nicht behandelt werden, müssen postmikrotomische Gewebeschnitte vor der histologischen Färbung mindestens 5 Minuten lang in unverdünnte Ameisensäure getaucht werden7. Das IHC-Protokoll für PrPSc enthält einen routinemäßigen Ameisensäure-Epitop-Demaskierungsschritt, der auch zur Inaktivierung von Prionen7 dient. Nach diesen Prion-Inaktivierungsschritten kann das resultierende fixierte Gewebe dann an BSL-2 unter Verwendung von Standard-BSL-2-Praktiken verarbeitet werden.
Die Mindestanforderung an die Gewebeentnahme für die TSE-Diagnose bei jedem Tier, das in die TSE-Überwachung einbezogen wird, ist die Entnahme des Hirnstamms (auf obex-Ebene). Darüber hinaus wird empfohlen, zum Nachweis von atypischer BSE und Scrapie auch einen Teil des Kleinhirns zu sammeln 1,8. Für die CWD-Diagnose sollten sowohl Hirnstamm (Obex) als auch retropharyngeale Lymphknoten getestet werden, da PrP Sc in lymphatischen Geweben ohne nachweisbares PrPSc in Obex9 nachgewiesen werden konnte, überprüft von Machado et al.10.
Der obex-Teil des Hirnstamms umfasst diagnostische TSE-Zielstellen, nämlich den dorsalen Vaguskern (DVN), den solitären Traktkern (STN) und den spinalen Traktkern des Trigeminusnervs (V). In diesen Bereichen kommt es auch in den frühen Stadien von BSE und klassischer Scrapie durchweg zu einer bilateralen PrP-Sc-Akkumulation. In klinischen Fällen von fortgeschrittener TSE zeigen alle Bereiche der grauen Substanz innerhalb des Hirnstamms eine weit verbreitete PrPSc-Verteilung 11.
Vor dem Schneiden und Verarbeiten werden die Hirnproben ausgewertet (Abbildung 1), um den Grad der Autolyse und das Vorhandensein von Gewebeschäden zu ermitteln, die möglicherweise die Eignung der Probe für eine IHC-basierte Bestätigungsdiagnose beeinträchtigen8. Um die Integrität der präparativen Protokolle und der Analyseergebnisse zu validieren, werden die TSE-positiven und -negativen Gewebeproben als Kontrollen in Verbindung mit der Präparation von Geweben aus Testfällen in jeden Assay einbezogen.
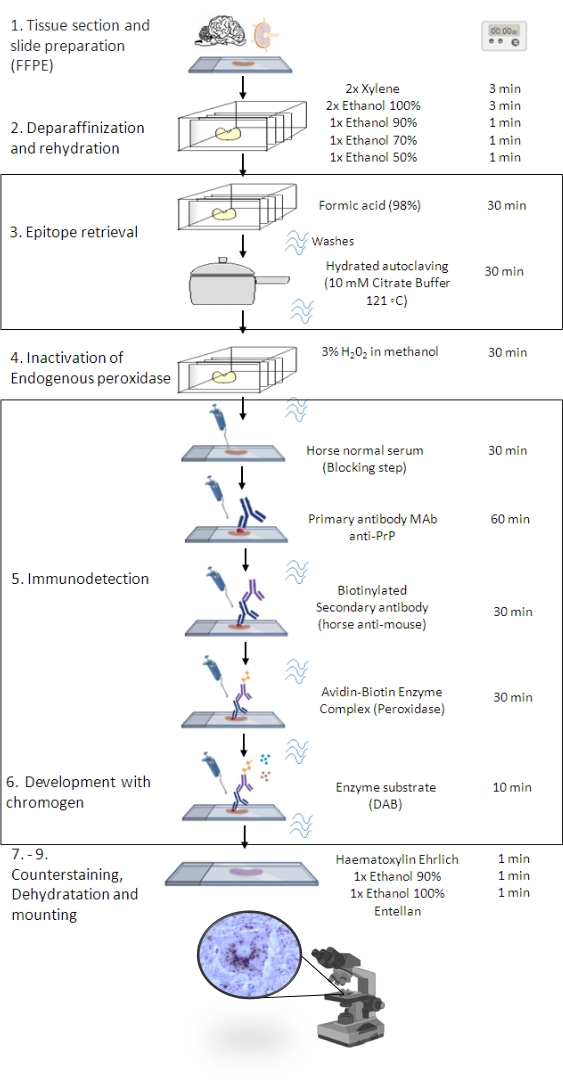
Abbildung 1: Das PrPSc IHC-Verfahren. Darstellung des schrittweisen Ablaufs des PrPSc IHC-Verfahrens von der Entparaffinisierung von Gewebeschnitten bis zur eventuellen Immunfärbung und Detektion (FFPE – Formalin-fixiertes Paraffin-eingebettet; Mab – monoklonaler Antikörper; DAB – 3,3′ Diaminobenzidin). Diese Figur wurde BioRender.com erstellt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Protocol
Representative Results
Discussion
TSE sind potentielle Zoonosen. Nach dem Auftreten von BSE im Vereinigten Königreich im Jahr 1986 wurde Portugal zu einem der Mitgliedstaaten der Europäischen Union mit einer höheren Inzidenz dieser Krankheit14,15. Um diese Krankheit und andere TSE, die aufgetreten sind (klassische und atypische Traberkrankheit, BSE-Varianten und derzeit die Überwachung der chronischen Auszehrung bei Hirschen), zu kontrollieren, wurden von der Generaldirektion für Lebensmitte…
Declarações
The authors have nothing to disclose.
Acknowledgements
Dieser Artikel wurde durch das Projekt POCI-01-0145-FEDER-029947 “Risikobewertung für chronische Auszehrungskrankheiten in Portugal” finanziert, das von FCT (Fundação para a Ciência e a Tecnologia) – FEDER -Balcão2020 unterstützt wird. Außerdem erhielten die Autoren der Forschungseinheit CECAV eine Förderung durch das FCT im Rahmen des Projekts UIDB/CVT/0772/2020.Wir danken Bruce C. Campbell, Forschungsdirektor (im Ruhestand), Western Regional Research Center, USDA, für seine Unterstützung.
Materials
| Absolute ethanol | Labchem | LB0507-9010 | Undituled |
| Diluted 90%, 70% and 50% in distilled water | |||
| Avidin-biotin complex and peroxidase Vectastain Elite ABC kit Peroxidase |
Vector Laboratories | PK-6100 | Prepare and gently mix 30 min before use according to kit instructions. Do not mix after standing. |
| Biotinylated secondary antibody (Horse anti-mouse IgG H+L) | Vector Laboratories | BA-2000-1.5 | Dilute at 1/200 in TBS with 10% horse normal serum. Prepare the volume required depending on the number of sections. |
| Chromogen Diaminobenzidine- DAB, substrate kit, Peroxidase | Vector Laboratories | SK-4100 | Prepare before use according to kit instructions. Use 400 µL of solution per section. |
| DakoCytomation Pascal pressure chamber | DAKO | S2800 | |
| Ehrlich’s Hematoxylin: | |||
| Hematoxylin | Merck | 115938 | Dissolve 2 g of hematoxylin in 100 mL of absolute ethanol. Add 100 mL of distilled water, 10 mL of glacial acetic acid and 15 g of potassium alum with constant stirring. Add 100 mL of glycerin. The natural oxidation process takes 2 months, before use. |
| Absolute ethanol | Labchem | LB0507-9010 | |
| Glacial acetic acid | Merck | 101830 | |
| Potassium alum | Merck | 1.01047.1000 | |
| Glycerin | Merck | 1.04091.1000 | |
| Endogenous Peroxidase Block solution (3% concentration H2O2): | 40 mL Hydrogen peroxide (30% w/w) in 360 mL Methanol. Prepare before use |
||
| Hydrogen peroxide (30% w/w) | Scharlau | HI0136 | |
| Methanol | Sigma Aldrich | 322415-2L | |
| Formic acid 98% | Merck | 1.00264.1000 | Undiluted |
| Microtome | Shandon-AS325 | Microtome | Shandon-AS325 |
| Mounting medium Entellan | Merck | 107960 | Ready- to- use. |
| Normal serum (20% ) block solution in TBS: Horse normal serum |
Gibco |
16050-122 |
Prepare final volume according to the number of sections in the assay (200 µL of solution per section). |
| Primary antibody anti-PrP Mouse MAb 2G11 | BIORAD | MCA2460 | PrP 146-R154R171182 Ovine including atypical scrapie, cervine, feline. Not suitable for bovine. According to the number of sections in the assay (200 µL of solution per section) and antibody dilution, prepare final volume in TBS supplemented with 10% of normal serum from the species the secondary antibody was raised in (horse normal serum) Usual antibody dilution: MAb 2G11 1/100 but working dilution should be established in every new batch to get the concentration to give the strongest labelling with lowest background. For storage, freeze aliquot volumes of a minimum of 10 μL into sterile microtubes. Defrost and use one aliquot at a time. |
| Primary antibody anti-PrP Mouse MAb 12F10 | Cayman Chemical Company | 189710 | PrP142-160 Bovine, not suitable for ovine Usual antibody dilution: 1/200 but working dilution should also be established. Prepare as MAb 2G11 |
| Shandon CoverplateTM chamber | Thermo Scientific | 72110017 | |
| Shandon Sequenza® Immunstaining center | Thermo Scientific | 73300001 | |
| Shandon Sequenza® Immunstaining slide rack | Thermo Scientific | 73310017 | |
| Solution Citrate Buffer (10 mM pH 6.1): | 2.55 g Tri-sodium citrate dihydrate and 0.255 g Citric acid in one litre purified water. Adjust pH of working solution to 6.1 using 10 mM citric acid solution (1.05 g citric acid in 500 mL purified water) Prepare on assay day. |
||
| Tri-sodium citrate dihydrate | Sigma-aldrich | S4641-500G | |
| Citric acid | Sigma Aldrich | C0759 | |
| Staining jar and basket | Deltalab | 19360 | |
| 19361 | |||
| Superfrost Plus microscope slides | VWR | 631-0108 | |
| Tris-Buffered Saline solution (TBS) (50 mM TRIZMA BASE; 0.8% NaCI; pH 7.6): | 10xTBS (stock solution 0.5 M TRIZMA BASE; 8% NaCI; pH 7.6): TRIZMA BASE 60,57 g and NaCl 80 g in 800 mL purified water. Adjust pH of stock solution using Hydrochloric acid 37% and final volume to one litre with purified water (keep 5± 3 °C until 2 months) Dilute TBS stock solution 1/10 on assay day. |
||
| TRIZMA BASE | Sigma Aldrich | T6066-1KG | |
| Sodium Chloride (NaCl) | Merck | 106404 | |
| Xylene | Panreac Applied Chem ITW reagents | 251769 | Undiluted |
Referências
- . WOAH, Manual of Diagnostic Tests and Vaccines for Terrestrial Animals Online Access. Chapter 3.4.5.-Bovine Spongiform Encephalopathy (Version May 2021) and Chapter 3.8.11. – Scrapie (Version May 2022) Available from: https://www.woah.org/en/what-we-do/standards/codes-and-manuals/terrestrial-manual-online-access/ (2022)
- Ramos-Vara, J. A. Principles and methods of immunohistochemistry. Methods in Molecular Biology. 1641, 115-128 (2017).
- Krenacs, L., Krenacs, T., Stelkovics, E., Raffeld, M., Oliver, C., Jamur, M. Heat-Induced antigen retrieval for immunohistochemical reactions in routinely processed paraffin sections. Immunocytochemical Methods and Protocols. Methods in Molecular Biology. 588, 103-119 (2010).
- Duraiyan, J., Govindarajan, R., Kaliyappan, K., Palanisamy, M. Applications of immunohistochemistry). Journal Pharmacy Bioallied Sciences. 4, 307-309 (2012).
- Orge, L., et al. Neuropathology of Animal Prion Diseases. Biomolecules. 11 (3), 466 (2021).
- . Biosafety in Microbiological and Biomedical Laboratories. 6th Edition Revised June 2020 Available from: https://www.cdc.gov/labs/pdf/SF_19_308133-A_BMBL6_00-BOOK-WEB-final-3.pdf (2022)
- APHA. Fixation, tissue processing, histology and immunohistochemistry procedures for diagnosis of animal TSE (BSE, scrapie, atypical scrapie, CWD). Histo & IHC protocols for TSE diagnosis_Rev_Jan2019.pdf. TSEglobalNet – International Reference Laboratory for TSE. , (2022).
- Sample requirements for TSE testing and confirmation. Version 1.0. TSE EURL Available from: https://www.izsplv.it/it/istituto/212-centri-eccellenza/laboratori-internazionali-riferimento/422-eurl_tses.html (2019)
- TSE EU Reference Laboratory Guidelines for the detection of Chronic Wasting Disease in cervids. Version 1.0. TSE EURL Available from: https://www.izsplv.it/it/istituto/212-centri-eccellenza/laboratori-internazionali-riferimento/422-eurl_tses.html (2019)
- Machado, C. N., et al. TSE Monitoring in Wildlife Epidemiology, Transmission, Diagnosis, Genetics and Control. Wildlife Population Monitoring. IntechOpen. , (2019).
- APHA. Neuropathology: Confirmatory diagnosis of transmissible spongiform encephalopathies (TSEs) in cattle and small ruminants. Confirmatory (Histo & IHC) diagnostic criteria Rev_Jan2019.pdf. TSEglobalNet – International Reference Laboratory for TSE. , (2019).
- Ryder, S. J., Spencer, Y. I., Bellerby, P. J., March, S. A. Immunohistochemical detection of PrP in the medulla oblongata of sheep: The spectrum of staining in normal and scrapie-affected sheep. The Veterinary Record. 148 (1), 7-13 (2001).
- Simmons, M. M., et al. Experimental classical bovine spongiform encephalopathy: definition and progression of neural PrP immunolabeling in relation to diagnosis and disease controls. Veterinary Pathology. 48 (5), 948-963 (2011).
- Orge, L., et al. Identification of H-type BSE in Portugal. Prion. 9 (1), 22-28 (2015).
- Orge, L., Simas, J. P., Fernandes, A. C., Ramos, M., Galo, A. Similarity of the lesion profile of BSE in Portuguese cattle to that described in British cattle. Veterinary Record. 147 (17), 486-488 (2000).
- Pires, M. A., Travassos, F. S., Gärtner, F. Atlas of veterinary pathology. Biopathology. Lidel VII. 195 (6), 179-180 (2004).
- Pires, M. A., et al. Immunology protocols, didactic series. Applied Sciences. , 357 (2010).

