Påvisning av unormalt prionprotein ved immunhistokjemi
Summary
Immunmerking av unormalt prionprotein ved bruk av immunhistokjemiske protokoller krever spesifikke prøve- og anti-PrP-antistoffpreparasjonsmetoder. Den nåværende protokollen beskriver de viktigste trinnene i epitopdemasking for å sikre riktig PrP-immunmerking og for å minimere uspesifikk bakgrunnsfarging. Også denne tilnærmingen vurderer biosikkerhetstiltak når man utfører immunhistokjemiske studier med prioninfiserte vev.
Abstract
Unormale prionproteiner (PrPSc) er den sykdomsassosierte isoformen av cellulært prionprotein og diagnostiske markører for overførbare spongiforme encefalopatier (TSE). Disse nevrodegenerative sykdommene påvirker mennesker og flere dyrearter og inkluderer skrapesyke, zoonotisk bovin spongiform encefalopati (BSE), kronisk sløsende sykdom av hjortedyr (CWD) og den nylig identifiserte kamelprionsykdommen (CPD). Diagnostisering av TSE er avhengig av immundeteksjon av PrPSc ved bruk av både immunhistokjemi (IHC) og vestlige immunoblotmetoder (WB) på encefalonvev, nemlig hjernestammen (obex-nivå). IHC er en mye brukt metode som bruker primære antistoffer (monoklonal eller polyklonal) mot antigener av interesse i celler i en vevsseksjon. Antistoff-antigenbindingen kan visualiseres ved en fargereaksjon som forblir lokalisert i området av vevet eller cellen der antistoffet ble målrettet. Som sådan, i prionsykdommer, som i andre forskningsfelt, brukes immunhistokjemiteknikkene ikke bare til diagnostiske formål, men også i patogenesestudier. Slike studier innebærer å oppdage PrPSc-mønstre og -typer fra de som tidligere er beskrevet for å identifisere de nye prionstammene. Siden BSE kan infisere mennesker, anbefales det at biosikkerhetslaboratoriet nivå-3 (BSL-3) fasiliteter og / eller praksis brukes til å håndtere storfe, små drøvtyggere og hjortedyrprøver som inngår i TSE-overvåkingen. I tillegg anbefales oppsamlingsutstyr og prion-dedikert utstyr, når det er mulig, for å begrense forurensning. PrPSc IHC-prosedyren består av et maursyre-epitop-demasking trinn som også fungerer som et prioninaktiveringsmål, da formalinfiksert og parafininnebygd vev som brukes i denne teknikken forblir smittsomt. Ved tolkning av resultatene må det utvises forsiktighet for å skille uspesifikk immunmerking fra målmerking. For dette formålet er det viktig å gjenkjenne artefakter av immunmerking oppnådd i kjente TSE-negative kontrolldyr for å skille de fra spesifikke PrP Sc-immunmerkingstyper, som kan variere mellom TSE-stammer, vertsarter og prnp-genotype, nærmere beskrevet her.
Introduction
Ifølge prionhypotesen er den unormale isoformen (PrPSc) den primære eller eneste komponenten av det smittsomme stoffet i overførbare spongiforme encefalopatier (TSE). Bekreftelse for diagnostisering av TSE er avhengig av immundeteksjon av PrPSc ved bruk av immunhistokjemi (IHC) protokoller og / eller vestlige immunoblotmetoder (WB) av encephalon vev1.
IHC er en metode som benytter monoklonale eller, i noen tilfeller, polyklonale antistoffer (som primære antistoffer) som et første skritt i immunfarging av spesifikt målrettede antigener av interesse lokalisert i celler i en vevsseksjon. Enhver effektiv primær antistoff-antigenbinding visualiseres deretter ved bruk av sekundære antistoffer som er spesifikke for de primære antistoffene. Disse sekundære antistoffene konjugeres til enzymer, slik som pepperrotperoksidase (HRP) eller alkalisk fosfatase (AP). Visualisering oppnås deretter ved å legge til et substrat til disse enzymene, og produsere uoppløselige fargeprodukter lokalisert i områder der de primære antistoffene er bundet til de målrettede antigenene. Forbedret visualisering kan oppnås ved motfarging, hvor et fargestoff brukes til å skape en kontrast mellom immunmerket og ikke-immunmerket vev2.
Med IHC ved bruk av formalinfast parafininnebygd vev (FFPE), kan formalinfiksering oppheve effektiviteten av primære antistoffer på grunn av kryssbinding ved formaldehyd og oppvarming og dehydrering under parafininnbygging. Disse endrer konformasjonen av proteiner, ødelegger, denaturerer eller maskerer epitopene, og reduserer eller opphever dermed deres deteksjon3. Som sådan krever dette antigengjenfinning (AR). AR-teknikkene forstyrrer formaldehydrelatert kjemisk gruppe-kryssbinding i de antigene molekylene, og gjenoppretter eller avdekker dermed den opprinnelige antigen-proteinkonformasjonen. Dette resulterer i gjenoppretting av antistoff-antigen (epitop) affinitet for immunmerking. Den endelige effekten av AR avhenger av egenskapene til det målrettede antigenet og / eller det primære antistoffet2.
Heat-induced antigen (epitope) retrieval (HIER) er en prosedyre for AR3 og brukes rutinemessig for PrPSc IHC-deteksjon, som beskrevet her. IHC er avgjørende for diagnose og brukes i forskningslaboratorier for å bestemme vevsfordelingen av et patologiassosiert antigen. Det er mye brukt i diagnostisering og forskning på kreft, nevrovitenskap og smittsomme sykdommer4, blant andre. For TSE spiller IHC en viktig rolle i diagnostisering og forskning for å bekrefte og undersøke PrPSc-distribusjon i naturlige verter og eksperimentelle modeller. IHC bidrar til prionpatogenesestudier og analyse av PrP Sc-avsetningstyper og mønstre, nemlig i nevrale vev5, for å oppdage avvik fra rutinemessig beskrevne infeksjoner og identifisere antatte nye prionstammer.
Fordi prioner av bovin spongiform encefalopati (BSE) kan infisere mennesker, kan visse laboratorieprotokoller involvert i arbeidet med BSE kreve bruk av BSL-3-fasiliteter og praksis6. Disse inkluderer bruk av en forseglet sekundær beholder for å transportere potensielle BSE-infiserte vevsprøver i instituttet og laboratoriet. Det inkluderer også utpeking av inneslutningsområder og prion-dedikert utstyr for BSE-forskning og analyse når det er mulig. Dette gjøres for å forhindre forurensning utenfor arbeidsområdet og gi et begrenset rom siden dekontamineringsprosedyrer blir nødvendige.
Følgelig følger laboratoriet for patologi av INIAV anbefalte biosikkerhetsnivå-3 (BSL-3) fasiliteter og praksis6 for å håndtere potensielle prioninfiserte prøver av vev fra storfe, små drøvtyggere og hjortedyr forbundet med TSE-overvåkingen.
Formalinfiksert og parafininnebygd vev som inngår i TSE-diagnostiske eller forskningsprosedyrer, spesielt i sentralnervesystemet, kan være potensielt smittsomt. Derfor må disse faste vevene behandles med maursyre for å redusere smittsomheten til prioner, hvis tilstede, før vevsbehandling. Dette utføres ved å plassere faste, trimmede vev (ca. 2-4 mm tykkelse) i en prosesseringskassett. Kassetten senkes deretter ned i 98% maursyre (i 1 time). Etter nedsenking vaskes kassettene med vev i rennende vann fra springen i 30 minutter, og returneres til fikseringsmiddelet før videre behandling. Dersom vevssnitt ikke behandles før behandling, må postmikrotomiske vevssnitt senkes ned i ufortynnet maursyre i minst 5 minutter før histologisk farging7. IHC-protokollen for PrPSc inkluderer et rutinemessig maursyre-epitop-demasking trinn, som også tjener til å inaktivere prioner7. Etter disse prioninaktiveringstrinnene kan de resulterende faste vevene deretter behandles ved BSL-2 ved hjelp av standard BSL-2-praksis.
Minimumskravet til vevsprøvetaking for TSE-diagnose hos dyr som inngår i TSE-overvåking, er innsamling av hjernestammen (på obexnivå). For å påvise atypisk BSE og skrapesyke anbefales det i tillegg at en del av lillehjernen også samles 1,8. For CWD-diagnose bør både hjernestamme (obex) og retropharyngeale lymfeknuter testes, da PrP Sc kan påvises i lymfoid vev uten påviselig PrPSc i obex9, gjennomgått av Machado et al.10.
Obex-delen av hjernestammen inkluderer diagnostiske TSE-målsteder, nemlig den dorsale vagalkjernen (DVN), ensomhetskjernen (STN) og spinalkanalkjernen i trigeminusnerven (V). Disse områdene presenterer konsekvent bilateral PrPSc-akkumulering , selv i de tidlige stadiene av BSE og klassisk skrapesyke. I kliniske tilfeller av avansert TSE viser alle gråsubstansområdene i hjernestammen utbredt PrPSc-distribusjon 11.
Før snitting og prosessering evalueres hjerneprøvene (figur 1) for å fastslå grad av autolyse og tilstedeværelse av eventuelle vevsskader som potensielt kan svekke prøvens egnethet for IHC-basert bekreftende diagnose8. For å validere integriteten til de forberedende protokollene og analyseresultatene, er TSE-positive og negative vevsprøver inkludert som kontroller i forbindelse med fremstilling av vev fra testtilfeller i hver analyse.
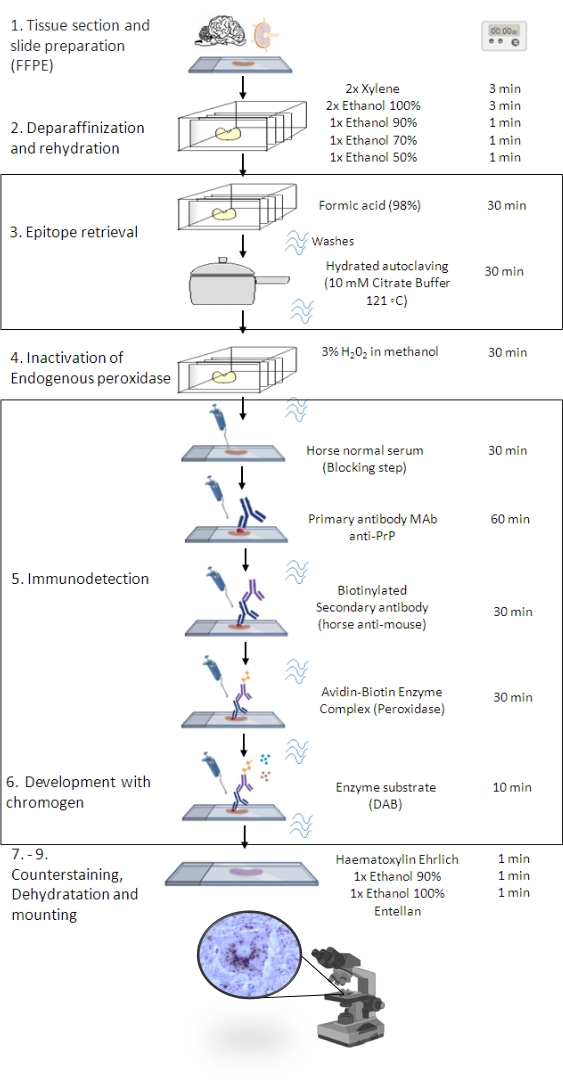
Figur 1: PrPSc IHC-prosedyren. Representasjon som viser trinnvis sekvens av PrPSc IHC-prosedyre fra deparaffinisering av vevsseksjoner til eventuell immunfarging og deteksjon (FFPE – Formalin-fixed paraffin-embedded; Mab – monoklonalt antistoff; DAB – 3,3′ diaminobenzidin). Denne figuren ble opprettet i BioRender.com. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
TSE er potensielle zoonotiske sykdommer. Etter fremveksten av BSE i 1986 i Storbritannia, ble Portugal en av EUs medlemsstater med en høyere forekomst av denne sykdommen14,15. For å kontrollere denne sykdommen, andre TSE som har dukket opp (klassisk og atypisk skrapesyke, BSE-varianter, og for tiden overvåking av skrantesyke hos hjortedyr), ble overvåkingsmekanismer utviklet av Generaldirektoratet for mat og veterinær (DGAV) og Nasjonalt institutt for landbr…
Declarações
The authors have nothing to disclose.
Acknowledgements
Denne artikkelen ble finansiert av prosjektet POCI-01-0145-FEDER-029947 “Risikovurdering av kronisk sløsende sykdom i Portugal” støttet av FCT (Fundação para a Ciência e a Tecnologia) – FEDER -Balcão2020. Også forfatterne av forskningsenheten CECAV mottok finansiering fra FCT, under prosjektet UIDB / CVT / 0772/2020.Vi takker Bruce C. Campbell, forskningsdirektør (pensjonert), Western Regional Research Center, USDA, for hans hjelp.
Materials
| Absolute ethanol | Labchem | LB0507-9010 | Undituled |
| Diluted 90%, 70% and 50% in distilled water | |||
| Avidin-biotin complex and peroxidase Vectastain Elite ABC kit Peroxidase |
Vector Laboratories | PK-6100 | Prepare and gently mix 30 min before use according to kit instructions. Do not mix after standing. |
| Biotinylated secondary antibody (Horse anti-mouse IgG H+L) | Vector Laboratories | BA-2000-1.5 | Dilute at 1/200 in TBS with 10% horse normal serum. Prepare the volume required depending on the number of sections. |
| Chromogen Diaminobenzidine- DAB, substrate kit, Peroxidase | Vector Laboratories | SK-4100 | Prepare before use according to kit instructions. Use 400 µL of solution per section. |
| DakoCytomation Pascal pressure chamber | DAKO | S2800 | |
| Ehrlich’s Hematoxylin: | |||
| Hematoxylin | Merck | 115938 | Dissolve 2 g of hematoxylin in 100 mL of absolute ethanol. Add 100 mL of distilled water, 10 mL of glacial acetic acid and 15 g of potassium alum with constant stirring. Add 100 mL of glycerin. The natural oxidation process takes 2 months, before use. |
| Absolute ethanol | Labchem | LB0507-9010 | |
| Glacial acetic acid | Merck | 101830 | |
| Potassium alum | Merck | 1.01047.1000 | |
| Glycerin | Merck | 1.04091.1000 | |
| Endogenous Peroxidase Block solution (3% concentration H2O2): | 40 mL Hydrogen peroxide (30% w/w) in 360 mL Methanol. Prepare before use |
||
| Hydrogen peroxide (30% w/w) | Scharlau | HI0136 | |
| Methanol | Sigma Aldrich | 322415-2L | |
| Formic acid 98% | Merck | 1.00264.1000 | Undiluted |
| Microtome | Shandon-AS325 | Microtome | Shandon-AS325 |
| Mounting medium Entellan | Merck | 107960 | Ready- to- use. |
| Normal serum (20% ) block solution in TBS: Horse normal serum |
Gibco |
16050-122 |
Prepare final volume according to the number of sections in the assay (200 µL of solution per section). |
| Primary antibody anti-PrP Mouse MAb 2G11 | BIORAD | MCA2460 | PrP 146-R154R171182 Ovine including atypical scrapie, cervine, feline. Not suitable for bovine. According to the number of sections in the assay (200 µL of solution per section) and antibody dilution, prepare final volume in TBS supplemented with 10% of normal serum from the species the secondary antibody was raised in (horse normal serum) Usual antibody dilution: MAb 2G11 1/100 but working dilution should be established in every new batch to get the concentration to give the strongest labelling with lowest background. For storage, freeze aliquot volumes of a minimum of 10 μL into sterile microtubes. Defrost and use one aliquot at a time. |
| Primary antibody anti-PrP Mouse MAb 12F10 | Cayman Chemical Company | 189710 | PrP142-160 Bovine, not suitable for ovine Usual antibody dilution: 1/200 but working dilution should also be established. Prepare as MAb 2G11 |
| Shandon CoverplateTM chamber | Thermo Scientific | 72110017 | |
| Shandon Sequenza® Immunstaining center | Thermo Scientific | 73300001 | |
| Shandon Sequenza® Immunstaining slide rack | Thermo Scientific | 73310017 | |
| Solution Citrate Buffer (10 mM pH 6.1): | 2.55 g Tri-sodium citrate dihydrate and 0.255 g Citric acid in one litre purified water. Adjust pH of working solution to 6.1 using 10 mM citric acid solution (1.05 g citric acid in 500 mL purified water) Prepare on assay day. |
||
| Tri-sodium citrate dihydrate | Sigma-aldrich | S4641-500G | |
| Citric acid | Sigma Aldrich | C0759 | |
| Staining jar and basket | Deltalab | 19360 | |
| 19361 | |||
| Superfrost Plus microscope slides | VWR | 631-0108 | |
| Tris-Buffered Saline solution (TBS) (50 mM TRIZMA BASE; 0.8% NaCI; pH 7.6): | 10xTBS (stock solution 0.5 M TRIZMA BASE; 8% NaCI; pH 7.6): TRIZMA BASE 60,57 g and NaCl 80 g in 800 mL purified water. Adjust pH of stock solution using Hydrochloric acid 37% and final volume to one litre with purified water (keep 5± 3 °C until 2 months) Dilute TBS stock solution 1/10 on assay day. |
||
| TRIZMA BASE | Sigma Aldrich | T6066-1KG | |
| Sodium Chloride (NaCl) | Merck | 106404 | |
| Xylene | Panreac Applied Chem ITW reagents | 251769 | Undiluted |
Referências
- . WOAH, Manual of Diagnostic Tests and Vaccines for Terrestrial Animals Online Access. Chapter 3.4.5.-Bovine Spongiform Encephalopathy (Version May 2021) and Chapter 3.8.11. – Scrapie (Version May 2022) Available from: https://www.woah.org/en/what-we-do/standards/codes-and-manuals/terrestrial-manual-online-access/ (2022)
- Ramos-Vara, J. A. Principles and methods of immunohistochemistry. Methods in Molecular Biology. 1641, 115-128 (2017).
- Krenacs, L., Krenacs, T., Stelkovics, E., Raffeld, M., Oliver, C., Jamur, M. Heat-Induced antigen retrieval for immunohistochemical reactions in routinely processed paraffin sections. Immunocytochemical Methods and Protocols. Methods in Molecular Biology. 588, 103-119 (2010).
- Duraiyan, J., Govindarajan, R., Kaliyappan, K., Palanisamy, M. Applications of immunohistochemistry). Journal Pharmacy Bioallied Sciences. 4, 307-309 (2012).
- Orge, L., et al. Neuropathology of Animal Prion Diseases. Biomolecules. 11 (3), 466 (2021).
- . Biosafety in Microbiological and Biomedical Laboratories. 6th Edition Revised June 2020 Available from: https://www.cdc.gov/labs/pdf/SF_19_308133-A_BMBL6_00-BOOK-WEB-final-3.pdf (2022)
- APHA. Fixation, tissue processing, histology and immunohistochemistry procedures for diagnosis of animal TSE (BSE, scrapie, atypical scrapie, CWD). Histo & IHC protocols for TSE diagnosis_Rev_Jan2019.pdf. TSEglobalNet – International Reference Laboratory for TSE. , (2022).
- Sample requirements for TSE testing and confirmation. Version 1.0. TSE EURL Available from: https://www.izsplv.it/it/istituto/212-centri-eccellenza/laboratori-internazionali-riferimento/422-eurl_tses.html (2019)
- TSE EU Reference Laboratory Guidelines for the detection of Chronic Wasting Disease in cervids. Version 1.0. TSE EURL Available from: https://www.izsplv.it/it/istituto/212-centri-eccellenza/laboratori-internazionali-riferimento/422-eurl_tses.html (2019)
- Machado, C. N., et al. TSE Monitoring in Wildlife Epidemiology, Transmission, Diagnosis, Genetics and Control. Wildlife Population Monitoring. IntechOpen. , (2019).
- APHA. Neuropathology: Confirmatory diagnosis of transmissible spongiform encephalopathies (TSEs) in cattle and small ruminants. Confirmatory (Histo & IHC) diagnostic criteria Rev_Jan2019.pdf. TSEglobalNet – International Reference Laboratory for TSE. , (2019).
- Ryder, S. J., Spencer, Y. I., Bellerby, P. J., March, S. A. Immunohistochemical detection of PrP in the medulla oblongata of sheep: The spectrum of staining in normal and scrapie-affected sheep. The Veterinary Record. 148 (1), 7-13 (2001).
- Simmons, M. M., et al. Experimental classical bovine spongiform encephalopathy: definition and progression of neural PrP immunolabeling in relation to diagnosis and disease controls. Veterinary Pathology. 48 (5), 948-963 (2011).
- Orge, L., et al. Identification of H-type BSE in Portugal. Prion. 9 (1), 22-28 (2015).
- Orge, L., Simas, J. P., Fernandes, A. C., Ramos, M., Galo, A. Similarity of the lesion profile of BSE in Portuguese cattle to that described in British cattle. Veterinary Record. 147 (17), 486-488 (2000).
- Pires, M. A., Travassos, F. S., Gärtner, F. Atlas of veterinary pathology. Biopathology. Lidel VII. 195 (6), 179-180 (2004).
- Pires, M. A., et al. Immunology protocols, didactic series. Applied Sciences. , 357 (2010).

