Aplicação do AlDeSense na Estratificação de Células de Câncer de Ovário com Base na Atividade da Aldeído Desidrogenase 1A1
Summary
Métodos para medir a atividade de ALDH1A1 em células vivas são críticos na pesquisa do câncer devido ao seu status como um biomarcador de tronco. Neste estudo, empregamos uma sonda fluorogênica isoforme-seletiva para determinar os níveis relativos de atividade de ALDH1A1 em um painel de cinco linhagens de células de câncer de ovário.
Abstract
A recidiva após o tratamento do câncer é frequentemente atribuída à persistência de uma subpopulação de células tumorais conhecidas como células-tronco cancerosas (CSCs), que são caracterizadas por sua notável capacidade de iniciação tumoral e auto-renovação. Dependendo da origem do tumor (por exemplo, ovários), o perfil de biomarcadores de superfície da CSC pode variar drasticamente, tornando a identificação de tais células por meio de coloração imuno-histoquímica um esforço desafiador. Ao contrário, a aldeído desidrogenase 1A1 (ALDH1A1) tem emergido como um excelente marcador para identificar CSCs, devido ao seu perfil de expressão conservado em quase todas as células progenitoras, incluindo CSCs. A isoforma ALDH1A1 pertence a uma superfamília de 19 enzimas que são responsáveis pela oxidação de vários aldeídos endógenos e xenobióticos aos produtos correspondentes do ácido carboxílico. desenvolveram recentemente o AlDeSense, uma sonda “turn-on” isoform-seletiva para a detecção da atividade de ALDH1A1, bem como um reagente de controle de correspondência não reativo (Ctrl-AlDeSense) para explicar a coloração fora do alvo. Esta ferramenta isoform-seletiva já demonstrou ser uma ferramenta química versátil através da detecção da atividade de ALDH1A1 em células de leucemia mielóide K562, mamosferas e xenoenxertos CSC derivados de melanoma. Neste artigo, a utilidade da sonda foi mostrada através de experimentos adicionais de fluorimetria, microscopia confocal e citometria de fluxo, onde a atividade relativa de ALDH1A1 foi determinada em um painel de cinco linhagens de células de câncer de ovário.
Introduction
As células-tronco cancerosas (CSCs) são uma subpopulação de células tumorais que exibem propriedades semelhantes às células-tronco1. Semelhante aos seus homólogos não cancerosos, os CSCs possuem a extraordinária capacidade de se auto-renovar e proliferar. Juntamente com outros mecanismos incorporados, como a regulação positiva dos transportadores de de ligação de ATP, as CSCs são frequentemente poupadas dos esforços iniciais de remoção cirúrgica, bem como da terapia adjuvante subsequente2. Devido ao seu papel crítico na resistência ao tratamento3, recidiva4 e metástase5, as CSCs tornaram-se uma prioridade na pesquisa do câncer. Embora haja uma variedade de antígenos de superfície celular (por exemplo, CD133) que podem ser usados para identificar CSCs6, alavancar a atividade enzimática de aldeídos desidrogenases (ALDHs) encontradas no citoplasma tem emergido como uma alternativa atraente7. ALDHs são uma superfamília de 19 enzimas responsáveis por catalisar a oxidação de aldeídos endógenos e xenobióticos reativos aos produtos correspondentes do ácido carboxílico8.
Em geral, a desintoxicação de aldeídos é crucial na proteção das células contra eventos indesejáveis de ligações cruzadas e estresse oxidativo que podem danificar a integridade das células-tronco9. Além disso, a isoforma 1A1 controla o metabolismo do ácido retinóico, que por sua vez influencia a haste via sinalização retinaldeído10. O AlDeSense 11,12, uma sonda de detecção baseada em atividade de pequenas moléculas (ABS) para detectar seletivamente a atividade de ALDH1A1, foi recentemente desenvolvido. Os projetos em ABS alcançam a detecção do analito através de uma mudança química em vez de um evento de ligação, permitindo alta seletividade e diminuição das respostas fora do alvo13,14,15,16. O princípio de projeto da sonda fluorogênica seletiva de isoformas baseia-se em um mecanismo de têmpera de transferência de elétrons (d-PeT) doador-fotoinduzido17, originário do grupo funcional aldeído, que serve para suprimir a assinatura fluorescente da sonda18. Após a conversão mediada por ALDH1A1 para o ácido carboxílico, o relaxamento radiativo é desbloqueado para produzir um produto altamente fluorescente. Como a têmpera d-PeT nunca é 100% eficiente, a fluorescência residual que pode levar a possíveis resultados falso-positivos foi considerada ao estabelecer este ensaio através do desenvolvimento de Ctrl-AlDeSense, um reagente não responsivo com características fotofísicas correspondentes (por exemplo, rendimento quântico) e um padrão de coloração citoplasmático idêntico nas células. Quando usado em conjunto, este emparelhamento único pode distinguir de forma confiável células com alta atividade de ALDH1A1 daquelas que exibem baixos níveis via fluorimetria, imagem molecular e citometria de fluxo. Várias vantagens importantes estão associadas ao uso de corantes ativados por isoforma seletiva em relação aos métodos tradicionais de imuno-histoquímica. Por exemplo, as CSCs são hipotetizadas para serem enterradas profundamente dentro de um tumor e, portanto, são mais acessíveis a uma molécula pequena em relação a anticorpos grandes19. Além disso, o produto fluorescente transformado não modifica covalentemente nenhum componente celular, o que significa que pode ser prontamente removido através de ciclos de lavagem para deixar um CSC em um estado não modificado. Por fim, a resposta ativada identifica apenas células e funções viáveis, assim como o ensaio MTT, devido à sua dependência do cofator NAD+.
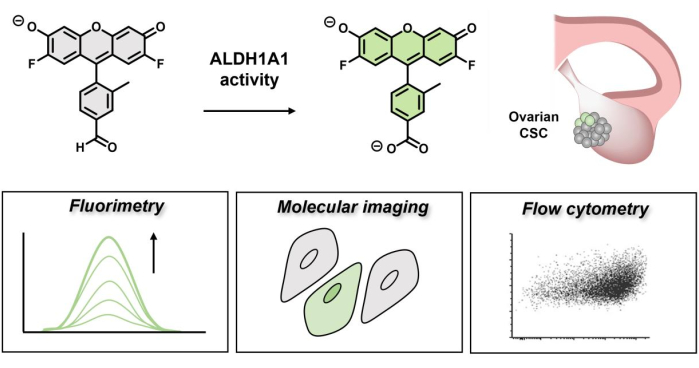
Figura 1: Esquema demonstrando o acionamento fluorescente do AlDeSense. O corante isoform-seletivo é ativado pela ALDH1A1 e pode ser usado para identificar a atividade elevada da ALDH1A1 em células cancerosas do ovário via fluorimetria, imagem molecular e citometria de fluxo. Clique aqui para ver uma versão maior desta figura.
Em trabalhos anteriores, o ensaio de sonda fluorogênica isoform-seletiva estratificada com sucesso em células ALDH altas (ALDH+) de células ALDH baixas (ALDH-) em células K562 de leucemia crônica humana, células de câncer de mama humano MDA-MB-231 e células de melanoma murino B16F0. Isso é importante porque, para muitos tipos de câncer, a alta expressão da proteína ALDH1A1 significa pior prognóstico clínico20. Isso pressupõe que níveis elevados de ALDH1A1 são indicativos de CSCs que podem escapar do tratamento, desenvolver resistência e disseminar-se por todo o corpo. No entanto, no caso do câncer de ovário, há estudos relatando o achado oposto (alta expressão de ALDH1A1 está ligada à melhora da sobrevida das pacientes)21,22,23,24. Embora isso possa parecer contraditório à primeira vista, a expressão não necessariamente se correlaciona com a atividade enzimática, que pode ser influenciada por mudanças no microambiente tumoral (por exemplo, fluxo de pH, gradientes de oxigênio), disponibilidade do cofator NAD+ ou substratos de aldeídos, níveis de ácidos carboxílicos (inibição do produto) e modificações pós-traducionais que podem alterar a atividade enzimática25 . Além disso, o câncer de ovário é dividido em cinco tipos histológicos principais (seroso de alto grau, seroso de baixo grau, endometrioide, de células claras e mucinoso), os quais hipotetizamos que apresentarão níveis variáveis de atividade da ALDH1A126. Com o objetivo de investigar a atividade de ALDH1A1 em tumores ovarianos, um ensaio de sonda fluorogênica isoforme-seletiva foi empregado para identificar populações de ALDH1A1+ em um painel de cinco linhagens de células de câncer de ovário pertencentes aos diferentes tipos histológicos mencionados acima. As linhagens celulares testadas neste estudo incluem células BG-1, Caov-3, IGROV-1, OVCAR-3 e PEO4, cobrindo histotipos de células claras e serosas. Neste trabalho, destacou-se a versatilidade e a generalizabilidade da sonda para identificar CSCs para os pesquisadores que buscam realizar estudos semelhantes em outras linhagens de células cancerosas imortalizadas, bem como em amostras de pacientes. O uso do AlDeSense lançará luz sobre as vias bioquímicas envolvidas na manutenção da CSC em microambientes teciduais complexos e potencialmente servirá como uma ferramenta clínica para determinar o prognóstico e medir a agressividade do câncer.
Protocol
Representative Results
Discussion
A pan-seletividade é uma limitação importante de muitas sondas ALDH; no entanto, vários exemplos de isoformas seletivas foram recentemente relatados 32,33,34,35,36,37,38,39,40,41. A s…
Declarações
The authors have nothing to disclose.
Acknowledgements
Este trabalho foi apoiado pelo National Institutes of Health (R35GM133581 para JC) e pelo Cancer Center at Illinois Graduate Scholarship (concedido à SG). JC agradece à Fundação Camille e Henry Dreyfus pelo apoio. Os autores agradecem ao Dr. Thomas E. Bearrood por sua contribuição inicial para preparar estoques de AlDeSense e AlDeSense AM. Agradecemos ao Sr. Oliver D. Pichardo Peguero e ao Sr. Joseph A. Forzano por sua assistência na preparação de vários precursores sintéticos. Agradecemos ao Prof. Erik Nelson (Departamento de Fisiologia Molecular e Integrativa, UIUC) pelas células Caov-3, IGROV-1 e PEO4. Agradecemos ao Prof. Paul Hergenrother (Departamento de Química, UIUC) pelas células BG-1. Agradecemos às instalações centrais do Carl R. Woese Institute for Genomic Biology pelo acesso ao microscópio confocal Zeiss LSM 700 e ao software correspondente. Agradecemos ao Flow Cytometry Facility pelo acesso ao BD LSR II CMtO Analyzer. Agradecemos à Dra. Sandra McMasters e ao Cell Media Facility pela assistência na preparação de meios de cultura celular.
Materials
| 0.25% Trypsin, 0.1% EDTA in HBSS w/o Calcium, Magnesium and Sodium Bicarbonate | Corning | 25-050-CI | |
| 1x Phosphate Buffer Saline | Corning | 21-040-CMX12 | |
| AccuSpin Micro 17R | Fisher Scientific | 13-100-675 | |
| AlDeSense | Synthesized in-house | ||
| BG-1 | A gift provided by the Prof. Paul Hergenrother Lab, University of Illinois Urbana-Champaign | ||
| BioLite 25cm2 Flask | Thermo Fisher Scientific | 130189 | |
| Biosafety Cabinet 1300 series A2 | Thermo Fisher Scientific | ||
| Caov-3 | A gift provided by the Prof. Erik Nelson Lab, University of Illinois Urbana-Champaign | ||
| Cell homogenizer | Fisher Scientific | ||
| Centrifuge 5180R | Eppendorf | 22627040 | |
| Contrl-AlDeSense | Synthesized in-house | ||
| DMEM, 10% FBS, 1% P/S | Prepared by UIUC cell media facility | ||
| Falcon Round-Bottom Polystyrene Test Tubes with Cell Strainer Snap Cap, 5mL | Corning | 352003 | |
| FCS Express 6 | Provided by UIUC CMtO | ||
| FL microscope | EVOS | ||
| Fluorometer | Photon Technology International | ||
| Forma Series II Water-Jacketed CO2 Incubator | Fisher Scientific | 3110 | |
| IGROV-1 | A gift provided by the Prof. Erik Nelson Lab, University of Illinois Urbana-Champaign | ||
| ImageJ | NIH | ||
| Innova 42R Incubated Shaker | |||
| LSM 700 | Zeiss | ||
| LSR II | BD | ||
| Nunc Lab-Tek Chambered #1.0 Borosicilate Coverglass System | Thermo Fisher Scientific | 155383 | |
| OVCAR-3 | ATCC | HTB-161 | |
| PEO4 | A gift provided by the Prof. Erik Nelson Lab, University of Illinois Urbana-Champaign | ||
| Pierce Protease Inhibitor Tablets | Thermo Scientific | A32963 | |
| Poly-L-Lysine | Cultrex | 3438-100-01 | |
| Rocker | VWR | ||
| RPMI, 10% FBS, 1% P/S | Prepared by UIUC cell media facility | ||
| RPMI, 20% FBS, 1% P/S, 0.01 mg/mL Insulin | Prepared by UIUC cell media facility |
Referências
- Bonnet, D., Dick, J. E. Human acute myeloid leukaemia is organised as a heirarchy that originates from a primitive haematopoetic cell. Nature Medicine. 3 (7), 730-737 (1997).
- Begicevic, R. R., Falasca, M. ABC transporters in cancer stem cells: Beyond chemoresistance. International Journal of Molecular Sciences. 18 (11), 2362 (2017).
- Cojoc, M., Mäbert, K., Muders, M. H., Dubrovska, A. A role for cancer stem cells in therapy resistance: Cellular and molecular mechanisms. Seminars in Cancer Biology. 31, 16-27 (2015).
- Islam, F., Gopalan, V., Smith, R. A., Lam, A. K. Y. Translational potential of cancer stem cells: A review of the detection of cancer stem cells and their roles in cancer recurrence and cancer treatment. Experimental Cell Research. 335 (1), 135-147 (2015).
- Li, F., Tiede, B., Massagué, J., Kang, Y. Beyond tumorigenesis: Cancer stem cells in metastasis. Cell Research. 17 (1), 3-14 (2007).
- Kim, W. T., Ryu, C. J. Cancer stem cell surface markers on normal stem cells. BMB Reports. 50 (6), 285-298 (2017).
- Pors, K., Moreb, J. S. Aldehyde dehydrogenases in cancer: An opportunity for biomarker and drug development. Drug Discovery Today. 19 (12), 1953-1963 (2014).
- Jackson, B., et al. Update on the aldehyde dehydrogenase gene (ALDH) superfamily. Human Genomics. 5 (4), 283-303 (2011).
- Vasiliou, V., Pappa, A., Petersen, D. R. Role of aldehyde dehydrogenases in endogenous and xenobiotic metabolism. Chemico-Biological Interactions. 129 (1-2), 1-19 (2000).
- Tomita, H., Tanaka, K., Tanaka, T., Hara, A. Aldehyde dehydrogenase 1A1 in stem cells and cancer. Oncotarget. 7 (10), 11018-11032 (2016).
- Anorma, C., et al. Surveillance of cancer stem cell plasticity using an isoform-selective fluorescent probe for aldehyde dehydrogenase 1A1. ACS Central Science. 4 (8), 1045-1055 (2018).
- Bearrood, T. E., Aguirre-Figueroa, G., Chan, J. Rational design of a red fluorescent sensor for ALDH1A1 displaying enhanced cellular uptake and reactivity. Bioconjugate Chemistry. 31 (2), 224-228 (2020).
- Chan, J., Dodani, S. C., Chang, C. J. Reaction-based small-molecule fluorescent probes for chemoselective bioimaging. Nature Chemistry. 4 (12), 973-984 (2012).
- East, A. K., Lucero, M. Y., Chan, J. New directions of activity-based sensing for in vivo NIR imaging. Chemical Science. 12 (10), 3393-3405 (2021).
- Yadav, A. K., et al. Activity-based NIR bioluminescence probe enables discovery of diet-induced modulation of the tumor microenvironment via nitric oxide. ACS Central Science. 8 (4), 461-472 (2022).
- Yadav, A. K., et al. An activity-based sensing approach for the detection of cyclooxygenase-2 in Live Cells. Angewandte Chemie. 59 (8), 3307-3314 (2020).
- Ueno, T., et al. Rational principles for modulating fluorescence properties of fluorescein. Journal of the American Chemical Society. 126 (43), 14079-14085 (2004).
- Tanaka, F., Mase, N., Barbas 3rd, C. F. Design and use of fluorogenic aldehydes for monitoring the progress of aldehyde transformations. Journal of the American Chemical Society. 126 (12), 3692-3693 (2004).
- Thurber, G. M., Schmidt, M. M., Wittrup, K. D. Antibody tumor penetration: transport opposed by systemic and antigen-mediated clearance. Advanced Drug Delivery Reviews. 60 (12), 1421-1434 (2008).
- Marcato, P., Dean, C. A., Giacomantonio, C. A., Lee, P. W. K. Aldehyde dehydrogenase its role as a cancer stem cell marker comes down to the specific isoform. Cell Cycle. 10 (9), 1378-1384 (2011).
- Meng, E., et al. ALDH1A1 maintains ovarian cancer stem cell-like properties by altered regulation of cell cycle checkpoint and DNA repair network signaling. PLoS One. 9 (9), e107142 (2014).
- Kaipio, K., et al. ALDH1A1-related stemness in high-grade serous ovarian cancer is a negative prognostic indicator but potentially targetable by EGFR/mTOR-PI3K/aurora kinase inhibitors. The Journal of Pathology. 250 (2), 159-169 (2020).
- Deng, S., et al. Distinct expression levels and patterns of stem cell marker, aldehyde dehydrogenase isoform 1 (ALDH1), in human epithelial cancers. PLoS One. 5 (4), e10277 (2010).
- Chang, B., et al. ALDH1 expression correlates with favorable prognosis in ovarian cancers. Modern Pathology. 22 (6), 817-823 (2009).
- Gardner, S. H., Reinhardt, C. J., Chan, J. Advances in activity-based sensing probes for isoform-selective imaging of enzymatic activity. Angewandte Chemie. 60 (10), 5000-5009 (2021).
- Reid, B. M., Permuth, J. B., Sellers, T. A. Epidemiology of ovarian cancer: a review. Cancer Biology and Medicine. 14 (1), 9-32 (2017).
- Tulake, W., et al. Upregulation of stem cell markers ALDH1A1 and OCT4 as potential biomarkers for the early detection of cervical carcinoma. Oncology Letters. 16 (5), 5525-5534 (2018).
- Nwani, N. G., et al. A novel ALDH1A1 inhibitor targets cells with stem cell characteristics in ovarian cancer. Cancers. 11 (4), 502 (2019).
- Roy, M., Connor, J., Al-Niaimi, A., Rose, S. L., Mahajan, A. Aldehyde dehydrogenase 1A1 (ALDH1A1) expression by immunohistochemistry is associated with chemo-refractoriness in patients with high-grade ovarian serous carcinoma. Human Pathology. 73, 1-6 (2018).
- Landen Jr, C. N., et al. Targeting aldehyde dehydrogenase cancer stem cells in ovarian cancer. Molecular Cancer Therapeutics. 9 (12), 3186-3199 (2010).
- Condello, S., et al. β-catenin-regulated ALDH1A1 is a target in ovarian cancer spheroids. Oncogene. 34 (18), 2297-2308 (2015).
- Storms, R. W., et al. Isolation of primitive human hematopoietic progenitors on the basis of aldehyde dehydrogenase activity. Proceedings of the National Academy of Sciences. 96 (16), 9118-9123 (1999).
- Duellman, S. J., et al. A bioluminescence assay for aldehyde dehydrogenase activity. Analytical Biochemistry. 434 (2), 226-232 (2013).
- Minn, I., et al. A red-shifted fluorescent substrate for aldehyde dehydrogenase. Nature Communications. 5, 3662 (2014).
- Dollé, L., Boulter, L., Leclercq, I. A., van Grunsven, L. A. Next generation of ALDH substrates and their potential to study maturational lineage biology in stem and progenitor cells. American Journal of Physiology. Gastrointestinal and Liver Physiology. 308 (7), 573-578 (2015).
- Yagishita, A., et al. Development of highly selective fluorescent probe enabling flow-cytometric isolation of ALDH3A1-positive viable cells. Bioconjugate Chemistry. 28 (2), 302-306 (2017).
- Maity, S., et al. Thiophene bridged aldehydes (TBAs) image ALDH activity in cells: Via modulation of intramolecular charge transfer. Chemical Science. 8 (10), 7143-7151 (2017).
- Koenders, S. T. A., et al. Development of a retinal-based probe for the profiling of retinaldehyde dehydrogenases in cancer cells. ACS Central Science. 5 (12), 1965-1974 (2019).
- Oe, M., et al. Deep-red/near-infrared turn-on fluorescence probes for aldehyde dehydrogenase 1A1 in cancer stem cells. ACS Sensors. 6 (9), 3320-3329 (2021).
- Yagishita, A., Ueno, T., Tsuchihara, K., Urano, Y. Amino BODIPY-based blue fluorescent probes for aldehyde dehydrogenase 1-expressing cells. Bioconjugate Chemistry. 32 (2), 234-238 (2021).
- Okamoto, A., et al. Identification of breast cancer stem cells using a newly developed long-acting fluorescence probe, C5S-A, targeting ALDH1A1. Anticancer Research. 42 (3), 1199-1205 (2022).

