हेमटोपोइएटिक स्टेम और पूर्वज कोशिकाओं के लिए फ्लो साइटोमेट्री के माध्यम से रिश्तेदारी, विभाजन संख्या और फेनोटाइप का एक साथ मूल्यांकन
Summary
यहां प्रस्तुत एक फ्लो साइटोमेट्री-आधारित तकनीक है जो एक साथ सेल डिवीजनों, सतह सेल फेनोटाइप और सेलुलर रिश्तेदारी की संख्या को मापने की अनुमति देती है। उन गुणों को क्रमपरिवर्तन-आधारित ढांचे का उपयोग करके सांख्यिकीय रूप से परीक्षण किया जा सकता है।
Abstract
कुछ तकनीकें एक ही सेल के लिए फेनोटाइप और भाग्य का एक साथ आकलन कर सकती हैं। फेनोटाइप को चिह्नित करने के लिए उपयोग किए जाने वाले अधिकांश वर्तमान प्रोटोकॉल, हालांकि बड़े डेटासेट उत्पन्न करने में सक्षम हैं, रुचि के सेल के विनाश की आवश्यकता होती है, जिससे इसके कार्यात्मक भाग्य का आकलन करना असंभव हो जाता है। हेमटोपोइजिस जैसी विषम जैविक विभेदक प्रणालियों का वर्णन करना इसलिए मुश्किल है। सेल डिवीजन ट्रैकिंग रंगों पर निर्माण करते हुए, हमने कई एकल हेमटोपोइएटिक पूर्वजों के लिए रिश्तेदारी, विभाजन संख्या और भेदभाव की स्थिति को एक साथ निर्धारित करने के लिए एक प्रोटोकॉल विकसित किया। यह प्रोटोकॉल विभिन्न जैविक स्रोतों से अलग मुराइन और मानव हेमटोपोइएटिक पूर्वजों की पूर्व विवो भेदभाव क्षमता के आकलन की अनुमति देता है। इसके अलावा, जैसा कि यह फ्लो साइटोमेट्री और सीमित संख्या में अभिकर्मकों पर आधारित है, यह अपेक्षाकृत सस्ती तरीके से एकल-सेल स्तर पर बड़ी मात्रा में डेटा उत्पन्न कर सकता है। हम एक मजबूत सांख्यिकीय ढांचे के साथ संयुक्त एकल-सेल विश्लेषण के लिए विश्लेषणात्मक पाइपलाइन भी प्रदान करते हैं। जैसा कि यह प्रोटोकॉल एकल-कोशिका स्तर पर कोशिका विभाजन और भेदभाव को जोड़ने की अनुमति देता है, इसका उपयोग मात्रात्मक रूप से सममित और असममित भाग्य प्रतिबद्धता, आत्म-नवीकरण और भेदभाव के बीच संतुलन और किसी दिए गए प्रतिबद्धता भाग्य के लिए विभाजन की संख्या का आकलन करने के लिए किया जा सकता है। कुल मिलाकर, इस प्रोटोकॉल का उपयोग प्रयोगात्मक डिजाइनों में किया जा सकता है जिसका उद्देश्य एकल-कोशिका परिप्रेक्ष्य से हेमटोपोइएटिक पूर्वजों के बीच जैविक अंतर को उजागर करना है।
Introduction
पिछले दशक को सेलुलर और आणविक जीव विज्ञान के लिए एकल-कोशिका दृष्टिकोण के विश्वव्यापी प्रसार द्वारा चिह्नित किया गया था। एकल-कोशिका जीनोमिक्स1,2 के चरणों का पालन करते हुए, आजकल एक एकल कोशिका (जैसे, डीएनए, आरएनए, प्रोटीन) के कई घटकों का अध्ययन करना संभव है, जिसमें हर साल नई एकल कोशिका-ओमिक्स तकनीक ें बढ़ रही हैं। इन तकनीकों ने इम्यूनोलॉजी, न्यूरोबायोलॉजी, ऑन्कोलॉजी और अन्य के क्षेत्रों के लिए पुराने और नए प्रश्नों पर प्रकाश डाला है, दोनों मानव और मॉडल जीव कोशिकाओंका उपयोग करते हैं। व्यक्तिगत कोशिकाओं के बीच अंतर को उजागर करके, एकल सेल-ओमिक्स ने हेमटोपोइजिस के एक नए मॉडल की परिभाषा को प्रेरित किया, जो हेमटोपोइएटिक स्टेम और पूर्वज कोशिकाओं (एचएसपीसी) की विविधता पर केंद्रित है और असतत सजातीय आबादी 4,5 के शास्त्रीय मॉडल से दूर जा रहा है।
सभी -ओमिक्स तकनीकों की कुछ कमियों में से एक रुचि के सेल का विनाश है, जो इसकी कार्यक्षमता का आकलन करने की संभावना को दर्शाता है। इसके विपरीत, अन्य एकल-कोशिका विधियां, जैसे एकल-कोशिका प्रत्यारोपण परख और वंश अनुरेखण प्रौद्योगिकियां, विवो 6,7 में व्यक्तिगत कोशिकाओं के भाग्य का आकलन करके पूर्वज कोशिका की कार्यक्षमता का रीडआउट प्रदान करती हैं। वंशावली अनुरेखण प्रौद्योगिकियों में एक आनुवंशिकआनुवंशिक 7 या फ्लोरोसेंट लेबल 8,9 के साथ रुचि के सेल को लेबल करना शामिल है, जिससे एक ही समय में कई एकल कोशिकाओं के भाग्य का पालन किया जा सकता है। हालांकि, शुरुआती कोशिकाओं का लक्षण वर्णन आमतौर पर मापदंडों की एक सीमित संख्या तक सीमित होता है, जैसे कि फ्लो साइटोमेट्री10 द्वारा मूल्यांकन किए गए कुछ सतह प्रोटीन की अभिव्यक्ति। इसके अलावा, एकल-कोशिका वंश अनुरेखण प्रौद्योगिकियों को सेलुलर लेबल का श्रमसाध्य पता लगाने की आवश्यकता होती है, आमतौर पर डीएनए / आरएनए अनुक्रमण या इमेजिंग के माध्यम से। यह अंतिम बिंदु विशेष रूप से उन स्थितियों की संख्या को सीमित करता है जिन्हें एक ही प्रयोग में परीक्षण किया जा सकता है।
एकल कोशिकाओं की कार्यक्षमता का अध्ययन करने के लिए उपयोग की जाने वाली विधियों का एक अन्य वर्ग एकल एचएसपीसी की पूर्व विवो सेल संवर्धन प्रणाली है। प्रदर्शन करने में आसान, इन स्वर्ण मानक परखों में व्यक्तिगत कोशिकाओं को 96-वेल्स सेल कल्चर वाहिकाओं में क्रमबद्ध करना शामिल है, और संस्कृति के बाद, सेल संतति फेनोटाइप को चिह्नित करना, आमतौर पर फ्लो साइटोमेट्री या रूपात्मक विश्लेषण द्वारा। इन परखों का उपयोग ज्यादातर परिपक्व कोशिकाओं में एचएसपीसी के दीर्घकालिक भेदभाव को चिह्नित करने के लिए किया गया है, आमतौर पर संस्कृति11,12 के 2-3 सप्ताह के बाद। वैकल्पिक रूप से, उनका उपयोग मानव स्टेम सेल प्रत्यारोपण19 के लिए चिकित्सा लाभ के वादे के साथ पूर्व विवो एचएसपीसी 13,14,15,16,17,18 को बनाए रखने और विस्तारित करने की कोशिश करने के लिए किया गया है। अंत में, उनका उपयोग अल्पकालिक संस्कृति20 का उपयोग करके एचएसपीसी की प्रारंभिक प्रतिबद्धता का अध्ययन करने के लिए किया गया है, इस संस्कृति में उत्पन्न कोशिकाओं की कम संख्या मुख्य सीमित कारक है। इन विभिन्न प्रकार के पूर्व विवो परखों का एक दोष यह है कि वे केवल आंशिक रूप से विवो जटिलता को दर्शाते हैं; फिर भी, वे मानव एचएसपीसी भेदभाव का अध्ययन करने के दुर्लभ तरीकों में से एक हैं।
मौजूदा एकल-कोशिका विधियों (एकल सेल-ओमिक्स, वंश अनुरेखण और पूर्व विवो संस्कृति) से जानकारी का एक लापता टुकड़ा सेल डिवीजनों का सटीक पता लगाना है, एचएसपीसी डायनामिक्स21 का अध्ययन करते समय विचार करने के लिए एक आवश्यक पैरामीटर। फ्लो साइटोमेट्री के माध्यम से विभाजन की संख्या का आकलन करने का एक सरल तरीका घुलनशील “प्रोटीन रंजक” का उपयोग है, जैसे 5-(और 6)-कार्बोक्सीफ्लोरेसिन डायसेटेट सक्सिनिमिडिल एस्टर (सीएफएसई)22। ये विभाजन रंजक दाग वाली कोशिकाओं के साइटोप्लाज्म के अंदर फैलते हैं, और आधे से पतला होते हैं और हर कोशिका विभाजन में दो बेटी कोशिकाओं में पारित होते हैं, जिससे 10 डिवीजनों तक की गणना करने की अनुमति मिलती है। कई विभाजन रंगों के संयोजन से, एक ही कुएं में कई अलग-अलग पूर्वजों को बीज देना संभव है, क्योंकि प्रत्येक व्यक्तिगत डाई विभिन्न वंशजों को अलग करने की अनुमति देता है। यह मल्टीप्लेक्स क्लोनल और डिवीजन-ट्रैकिंग के लिए सेल रंगों के उपयोग के पीछे का सिद्धांत है जिसे पहली बार मुराइन लिम्फोसाइट्स23,24 के लिए पेश किया गया था।
यहां, हम म्यूरिन और मानव एचएसपीसी के साथ उपयोग के लिए मल्टीजेन परख के विकास को प्रस्तुत करते हैं। यह विभेदन, विभाजन और रिश्तेदारी के गुणों के लिए एक साथ कई एकल कोशिकाओं के परीक्षण की अनुमति देता है। यह उच्च-थ्रूपुट, प्रदर्शन करने में आसान, और सस्ती परख सेलुलर फेनोटाइप, प्रदर्शन किए गए विभाजनों की संख्या, और सेल रिश्तेदारी और कुएं में अन्य कोशिकाओं के साथ क्लोनल संबंध को मापने की अनुमति देती है, सभी एक ही समय में। इसका उपयोग मात्रात्मक रूप से सममित और असममित भाग्य प्रतिबद्धता, आत्म-नवीकरण और भेदभाव के बीच संतुलन और किसी दिए गए प्रतिबद्धता भाग्य के लिए आवश्यक विभाजनों की संख्या का आकलन करने के लिए किया जा सकता है। प्रोटोकॉल के लिए एक प्रतिदीप्ति सक्रिय सेल सॉर्टर (एफएसीएस) और एक प्लेट रीडर के साथ एक फ्लो साइटोमीटर की आवश्यकता होती है, साथ ही सेल कल्चर करने के लिए आवश्यक उपकरण भी। मानव एचएसपीसी पर परख के निष्पादन के लिए तकनीकी प्रोटोकॉल के अलावा, हम विस्तृत विश्लेषण ढांचा भी प्रदान करते हैं, जिसमें सेल परिवार25 की अवधारणा से संबंधित सेलुलर गुणों का आकलन करने के लिए आवश्यक सांख्यिकीय परीक्षण शामिल है। इस प्रोटोकॉल का उपयोग पहले से ही मुराइन एचएसपीसी डिब्बे26,27 का वर्णन करने के लिए सफलतापूर्वक किया गया है।
निम्नलिखित प्रोटोकॉल प्रारंभिक सामग्री28 के रूप में चुंबकीय रूप से समृद्ध सीडी 34 + कोशिकाओं का उपयोग करता है। इस तरह, विभिन्न रक्त स्रोतों (जैसे, गर्भनाल रक्त, अस्थि मज्जा, परिधीय रक्त) से मानव एचएसपीसी को कुशलतापूर्वक दाग और अलग करना संभव है। सीडी 34– अंश को त्यागना महत्वपूर्ण नहीं है, क्योंकि इसका उपयोग विभिन्न प्रकार के प्रयोगात्मक नियंत्रणों को सेट करने के लिए प्रोटोकॉल के हिस्से के रूप में किया जाएगा। प्रयोगात्मक वर्कफ़्लो और आवश्यकताओं के अनुसार, उल्लिखित सेल मात्रा और वॉल्यूम को ऊपर या नीचे बढ़ाया जा सकता है। इसी तरह, प्रोटोकॉल को विभिन्न प्रकार के पूर्वजों के अध्ययन के लिए अनुकूलित किया जा सकता है, बस सेल सॉर्टिंग और फ्लो साइटोमेट्री चरणों के लिए उपयोग किए जाने वाले एंटीबॉडी को संशोधित करके।
Protocol
Representative Results
Discussion
मल्टीजेन परख एक उच्च-थ्रूपुट, प्रदर्शन करने में आसान और सस्ती परख है, जो लिम्फोसाइट 23,24,35 और मुराइन हेमटोपोइएटिक कोशिकाओं 26,27 का अध्ययन करने में सहायक रही है। यहां, हम दृष्टिकोण का एक नया विकास प्रस्तुत करते हैं जो अल्पकालिक संस्कृति (चित्रा 6) का उपयोग करके एकल-कोशिका स्तर पर मानव एचएसपीसी प्रतिबद्धता के शुरुआती चरण को समझने की अनुमति देता है। एकल-सेल एक्स विवो कल्चर सिस्टम का उपयोग आमतौर पर परिपक्व कोशिकाओं में एचएसपीसी के दीर्घकालिक भाग्य का आकलन करने के लिए किया जाता है, लेकिन कुछभाग्य दूसरों की तुलना में पहले होते हैं, संभावित रूप से कम भाग्य की ओर विश्लेषण को पूर्वाग्रहित करते हैं। इसके अलावा, ये संस्कृति प्रणालियां आमतौर पर भाग्य प्रतिबद्धता के दौरान विभाजन के बारे में जानकारी से चूक जाती हैं। पहले प्रतिबद्धता के कदम संस्कृति की शुरुआत में ही होते हैं, कभी-कभी विभाजन26,37 के बिना, प्रारंभिक भाग्य प्रतिबद्धता का अध्ययन करने के लिए अल्पकालिक संस्कृति और ट्रैकिंग डिवीजन आवश्यक हो जाता है। भाग्य, विभाजन और रिश्तेदारी का एक साथ पालन करके, यह परख मानव एचएसपीसी में पहले विभाजन और भाग्य निर्णय की भूमिका को समझने की अनुमति देती है। परख का उपयोग करके, यह अनुमान लगाना संभव है कि प्रतिबद्धता प्रक्रिया कितने विभाजनों के बाद होती है, उन शुरुआती पूर्वजों के लिए आत्म-नवीकरण और भेदभाव के बीच संतुलन, और उन गुणों को पीढ़ियों में कैसे विरासत में मिला है। हमारे ज्ञान के लिए, यह एकमात्र परख है जो एकल-सेल रिज़ॉल्यूशन पर मानव एचएसपीसी के लिए इस प्रकार के माप की अनुमति देता है। इसके अलावा, सेल डिवीजन रंगों के विभिन्न संयोजनों का उपयोग करके, हमने विश्लेषण के थ्रूपुट में वृद्धि की, जिससे यह परख बड़े डेटासेट को जल्दी से उत्पन्न करने के लिए एक मूल्यवान उपकरण बन गया। डाई संयोजन एक ही कुएं में कई परिवारों का पालन करने की अनुमति देते हैं, जिससे अल्पकालिक संस्कृति में विश्लेषण के लिए उपलब्ध कोशिकाओं की संख्या बढ़ जाती है। संयोजनों की संख्या को संभावित रूप से अन्य रंगों (जैसे, पीली डाई) को जोड़ने या सीएफएसई और सीटीवी के अनुपात को संशोधित करने के माध्यम से और भी बढ़ाया जा सकता है। हालांकि, यह विश्लेषण किए जा सकने वाले अन्य मापदंडों की संख्या को कम करता है।
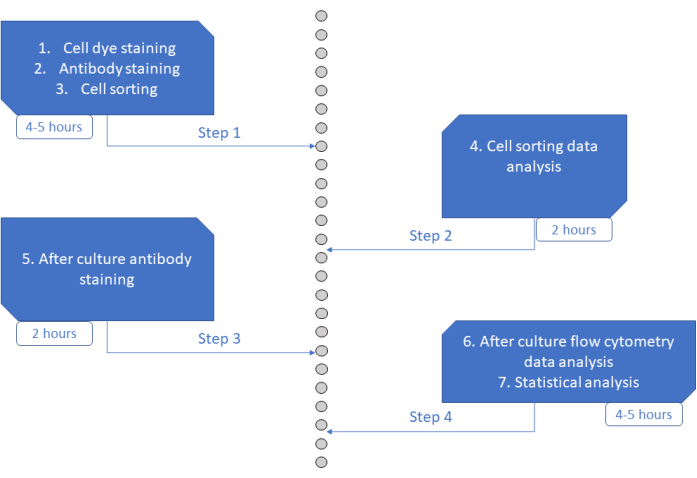
चित्रा 6: प्रोटोकॉल का योजनाबद्ध प्रतिनिधित्व। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
विश्लेषण को सफलतापूर्वक करने के लिए, कुओं की बड़ी संख्या और विश्लेषण करने के लिए कोशिकाओं की कम संख्या के कारण, प्लेट रीडर से लैस विश्लेषक पर फ्लो साइटोमेट्री विश्लेषण चलाना आवश्यक है। बेंच एनालाइज़र की नई पीढ़ी विशेष रूप से इस परख के लिए अनुकूलित है, क्योंकि उनमें से अधिकांश में सेल हानि के प्रतिशत को कम करने के लिए एक छोटी मृत मात्रा है। यह बदले में प्रत्येक कुएं की संपूर्णता को पुनर्प्राप्त करने में उच्च दक्षता की गारंटी देता है, जिससे 70% रेंज26 में अनुमानित दक्षता का संकेत मिलता है। फ्लो साइटोमेट्री अधिग्रहण के दौरान सेल हानि का अनुमान लगाना प्रत्येक व्यक्तिगत परिवार के विश्लेषण के लिए महत्वपूर्ण है। उदाहरण के लिए, कोई कोशिका मृत्यु नहीं मानते हुए और डिवीजनों की संख्या की गणना करते हुए, प्रत्येक परिवार में कोशिकाओं की संख्या का अनुमान लगाना संभव है। फिर भी, कुछ पुष्टित्मक प्रयोगों को चलाना वांछनीय है, विशेष रूप से परीक्षण की गई संस्कृति स्थितियों में कोशिका मृत्यु के अनुमान में और कोशिकाओं की परिभाषित संख्या का उपयोग करके प्रयोगात्मक रूप से वसूली दर को मापना।
इस प्रोटोकॉल के महत्वपूर्ण चरणों में से एक पीक असाइनमेंट है। जैसा कि पहले ही उल्लेख किया गया है, एक अच्छी गुणवत्ता वाला पीक वितरण सेल सॉर्टिंग में बहुत संकीर्ण चोटियों के अलगाव से दृढ़ता से निर्भर है। फिर भी, वितरण के आधार पर विशिष्ट रूप से डिवीजनों की सही संख्या असाइन करना अभी भी मुश्किल है। चूंकि सेल सॉर्टिंग और फ्लो साइटोमेट्री विश्लेषण दो अलग-अलग मशीनों पर किया जाता है, इसलिए प्रत्येक सिग्नल की तीव्रता की सीधे तुलना करना संभव नहीं है, इसलिए यह जानना मुश्किल हो सकता है कि हिस्टोग्राम के दाहिने छोर पर देखा गया पहला शिखर पीक 0 या पीक 1 है या नहीं। इस संबंध में, कुछ समाधान संभव हैं; एक तरीका इन कोशिकाओं (जैसे, लाइव-सेल इमेजिंग) द्वारा किए गए विभाजनों की संख्या को सटीक रूप से मापने के लिए एक ऑर्थोगोनल प्रयोग करना है। एक और संभावना प्रवाह साइटोमेट्री विश्लेषण चलाने से पहले, उल्टे ब्राइटफील्ड माइक्रोस्कोप के तहत कुएं में कोशिकाओं की संख्या की गणना करना है। यह विभाजन ों की औसत संख्या का अनुमान लगाएगा (यह मानते हुए कि कोई कोशिका मृत्यु नहीं है)। अंत में, चरम असाइनमेंट के लिए एक पोस्ट-हॉक समाधान “असंभव परिवारों” की असामान्य संख्या का पता लगाना है; ये परिवार प्रति पीढ़ी कोशिकाओं की संभावित संख्या से अधिक से बने होते हैं (उदाहरण के लिए, पीढ़ी 2 में पांच कोशिकाएं, या पीढ़ी 1 में दो कोशिकाएं और पीढ़ी 2 में एक कोशिका)। असंभव परिवारों को बाहर करने की संभावना को सांख्यिकीय विश्लेषण चरण में कोडित किया गया है, और असंभव परिवार को ध्वजांकित किया गया है। यदि इन त्रुटियों की घटना बहुत अधिक है, तो यह मानना उचित है कि शिखर असाइनमेंट को संशोधित करने की आवश्यकता है।
इस प्रोटोकॉल में, हमने परख के लिए डेटा प्रतिनिधित्व और विश्लेषण के कुछ उदाहरण शामिल किए, क्योंकि यह बड़े डेटासेट38 की पीढ़ी और व्याख्या में एक आवश्यक कदम बन गया है। पहला उदाहरण हीटमैप है जो प्रति परिवार आयोजित सभी विश्लेषण कोशिकाओं की समग्रता को दर्शाता है। यह डेटा के सामान्य गुणों और संभावित निष्कर्षों का पता लगाने के लिए एक कुशल उपकरण है: क्या परिवार कई सेल प्रकारों से बने होते हैं या क्या वे संरचना में सजातीय होते हैं? क्या परिवार कई पीढ़ियों में फैले हुए हैं, या वे ज्यादातर एक ही संख्या में विभाजित हैं? इस खोजपूर्ण विश्लेषण को तब अधिक विशिष्ट भूखंडों और सांख्यिकीय परीक्षण के साथ पूरक करने की आवश्यकता है। इसका उपयोग मात्रात्मक रूप से सममित और असममित भाग्य प्रतिबद्धता, विभाजन के बिना भेदभाव, आत्म-नवीकरण और भेदभाव के बीच संतुलन और किसी दिए गए प्रतिबद्धता भाग्य के लिए विभाजन की संख्या का आकलन करने के लिए किया जा सकता है। प्रयोगात्मक योजना के दौरान, पूछे गए प्रश्न के प्रकार के अनुसार सेल संस्कृति की लंबाई निर्धारित करना मौलिक है; उदाहरण के लिए, पहले दो प्रश्नों (सममित / असममित संतुलन और विभाजन के बिना भेदभाव) के लिए, बहुत छोटे संस्कृतियों के चरणों की योजना बनाने से बड़ी संख्या में परिवारों के अलगाव की अनुमति मिलती है जिन्होंने सभी26 में केवल एक या कोई विभाजन नहीं किया है। इसके विपरीत, लंबे प्रयोग एक विशिष्ट सेल प्रतिबद्धता के लिए आवश्यक डिवीजनों की संख्या की खोज की अनुमति देते हैं, क्योंकि वे भेदभाव के विभिन्न चरणों में परिवारों का नमूना लेते हैं। फिर भी, यह विधि दीर्घकालिक संस्कृतियों (2-3 सप्ताह) के लिए डिज़ाइन नहीं की गई है, क्योंकि सेल डाई कमजोर पड़ने से सात या आठ डिवीजनों से अधिक को सटीक रूप से ट्रैककरने में सक्षम नहीं है। नतीजतन, यह उपकरण ज्यादातर हेमटोपोइएटिक पूर्वजों की प्रारंभिक प्रतिबद्धता का अध्ययन करने के लिए अनुकूलित है, और इन कोशिकाओं के दीर्घकालिक भेदभाव गुणों पर मजबूत निष्कर्ष निकालने के लिए डिज़ाइन नहीं किया गया है।
सांख्यिकीय ढांचा विशेष रूप से इस प्रकार के डेटा के विश्लेषण के लिए विकसित किया गया था और क्रमपरिवर्तन26 की अवधारणा पर आधारित था। सेल प्रकार के वितरण और किए गए विभाजनों की संख्या पर पारिवारिक निर्भरता के अवलोकन के कारण यह आवश्यक था। दूसरे शब्दों में, कोशिकाएं जो एक ही परिवार का हिस्सा हैं, वे समान फेनोटाइप प्रदर्शित करने और समान संख्या में विभाजित करने की अधिक संभावना रखते हैं। जबकि एक गहन विश्लेषण इस काम के दायरे से परे है, विभिन्न स्थितियों का आकलन करते समय सांख्यिकीय परीक्षणों का प्रदान किया गया सेट पर्याप्त होना चाहिए।
अंत में, यह प्रोटोकॉल हेमटोपोइएटिक स्टेम और पूर्वज कोशिकाओं की सेलुलर गतिशीलता का आकलन करने के लिए एक मूल्यवान उपकरण का गठन करता है, एक तेजी से और सस्ती तरीके से। समय बिंदु, संस्कृति की स्थिति और विश्लेषण किए गए एचएसपीसी के प्रकार के बारे में इसकी लचीलापन और बहुमुखी प्रतिभा के कारण, यह विभिन्न प्रयोगात्मक स्थितियों का परीक्षण करने की अनुमति देता है। फ्लो साइटोमेट्री-आधारित परख के रूप में, इसे अधिकांश प्रयोगशालाओं में लागू किया जा सकता है, और इसे व्यापक पूर्व ज्ञान की आवश्यकता नहीं होती है, जिससे यह स्क्रीनिंग और पायलट प्रयोगों के लिए एक अच्छा उम्मीदवार बन जाता है।
Declarações
The authors have nothing to disclose.
Acknowledgements
हम फ्लो साइटोमेट्री प्रयोगों को स्थापित करने में उनकी मदद के लिए इंस्टीट्यूट क्यूरी फ्लो फैसिलिटी के सदस्यों को धन्यवाद देना चाहते हैं। हम कई चर्चाओं के दौरान टीम पेरी के अन्य सदस्यों के योगदान को भी स्वीकार करना चाहते हैं। फिल हॉजकिन (वाल्टर एंड एलिजा हॉल इंस्टीट्यूट ऑफ मेडिकल रिसर्च) को लिम्फोसाइटों पर सेल डिवीजन रंगों के मल्टीप्लेक्सिंग के अपने प्रोटोकॉल को साझा करने के लिए धन्यवाद देते हैं। हम इस प्रोटोकॉल के विकास के लिए आवश्यक जैविक संसाधन प्रदान करने के लिए सेंट लुइस अस्पताल कॉर्ड ब्लड बायोबैंक को धन्यवाद देते हैं। अध्ययन को सीएनआरएस और बेटनकोर्ट-शुलर फाउंडेशन (एलपी को) से एटीआईपी-एवेनिर अनुदान, लैबेक्स सेलटिसफाइबायो (एएनआर-10-एलबीएक्स-0038) (एलपी और एडी को), इडेक्स पेरिस-साइंस-लेट्रेस प्रोग्राम (एएनआर -10-आईडीईएक्स-0001-02 पीएसएल) से अनुदान द्वारा समर्थित किया गया था। साथ ही यूरोपीय संघ के क्षितिज 2020 अनुसंधान और नवाचार कार्यक्रम ईआरसी एसटीजी 758170-माइक्रोबार (एलपी के लिए), एडी के तहत यूरोपीय अनुसंधान परिषद (ईआरसी) से वित्त पोषण को फोंडेशन डी फ्रांस से फैलोशिप द्वारा समर्थित किया गया था।
Materials
| 1.5 mL polypropylene microcentrifuge tubes | vWR | 87003-294 | |
| 15-mL polypropylene tubes | vWR | 734-0451 | |
| 50-mL polypropylene tubes | vWR | 734-0448 | |
| 96-well U-bottom culture plate | Falcon | 353077 | |
| Anti-human Lin APC | Thermo Fisher | 22-7776-72 | Dilution 1/40 |
| ARIA III | BD | Can be replaced with any FACS sorter able to sort individual cells in 96-wells plate | |
| Carboxyfluorescein succinimidyl ester (CFSE) | Life Technologies | C34570 | |
| Cell Trace Violet (CTV) | Life Technologies | C34571 | |
| Compensation beads | BD | 552843 | |
| Dulbecco’s modified Eagle medium (DMEM) | Life Technologies | 11320033 | |
| Ethylenediaminetetraacetic acid (EDTA) | Thermo Scientific | J62948-36 | Prepare a solution 0.5 M, in sterilised water |
| FC block Fc1.3216 | BD | 564220 | Dilution 1/50 |
| Fetal Bovine Serum (FBS) | Dutscher | S1900-500C | Batch S00CH |
| FlowJo v10.8.1 | BD | ||
| Mouse anti-human CD10 PerCP-5.5, clone HI10a | Biolegend | 312216 | Dilution 1/20 |
| Mouse anti-human CD123 BUV395, clone 7G3 | BD | 564195 | Dilution 1/15 |
| Mouse anti-human CD34 APC-Cy7, clone 581 | Biolegend | 343513 | Dilution 1/40 |
| Mouse anti-human CD38 BV650, clone HB7 | Biolegend | 356620 | Dilution 1/40 |
| Mouse anti-human CD45RA AF700, clone HI100 | BD | 560673 | Dilution 1/20 |
| Mouse anti-human CD45RA PE-Cy7, clone HI100 | BD | 560675 | Dilution 1/20 |
| Mouse anti-human CD90 PE, clone 5E10 | Biolegend | 328110 | Dilution 1/20 |
| Phosphate Buffered Saline (PBS) 1X | Life Technologies | 10010001 | |
| Python | |||
| R | |||
| Sterile 12×75 mm conical polypropylene tubes | Falcon | ||
| ZE5 | Biorad | Can be replaced with any flow cytometry analyzer equipped with a plate reader | |
| Laboratory prepared | |||
| Cell culture media | Depends from the specific experiment. Prepare fresh daily and store at +4 °C until use | ||
| DMEM + 10% FBS | Can be stored in sterile conditions, at +4 °C up to 1 year. To prepare 500 mL, add 50 mL of FBS to 450 mL DMEM | ||
| PBS 1X + EDTA 0.1% | Can be stored in sterile conditions, at room temperature, up to 1 year. To prepare 500 mL, add 3.42 mL of EDTA 0.5 M to 500 mL PBS 1X | ||
| Staining buffer | Can be stored in sterile conditions, at +4 °C up to 1 year. To prepare 500 mL, add 2 mL of EDTA 0.5 M and 1 mL FBS to 500 mL PBS 1X |
Referências
- Ginhoux, F., Yalin, A., Dutertre, C. A., Amit, I. Single-cell immunology: Past, present, and future. Immunity. 55 (3), 393-404 (2022).
- Ke, M., Elshenawy, B., Sheldon, H., Arora, A., Buffa, F. M. Single cell RNA-sequencing: A powerful yet still challenging technology to study cellular heterogeneity. Bioessays. 44 (11), 2200084 (2022).
- Regev, A., et al. The human cell atlas. Elife. 6, 27041 (2017).
- Laurenti, E., Göttgens, B. From haematopoietic stem cells to complex differentiation landscapes. Nature. 553 (7689), 418-426 (2018).
- Haas, S., Trumpp, A., Milsom, M. D. Causes and consequences of hematopoietic stem cell heterogeneity. Cell Stem Cell. 22 (5), 627-638 (2018).
- Loughran, S. J., Haas, S., Wilkinson, A. C., Klein, A. M., Brand, M. Lineage commitment of hematopoietic stem cells and progenitors: insights from recent single cell and lineage tracing technologies. Experimental Hematology. 88, 1-6 (2020).
- Perié, L., Duffy, K. R. Retracing the in vivo haematopoietic tree using single-cell methods. FEBS Letters. 590 (22), 4068-4083 (2016).
- Yu, V. W. C., et al. Epigenetic memory underlies cell-autonomous heterogeneous behavior of hematopoietic stem cells. Cell. 167 (5), 1310-1322 (2016).
- Ganuza, M., et al. Lifelong haematopoiesis is established by hundreds of precursors throughout mammalian ontogeny. Nature Cell Biology. 19 (10), 1153-1163 (2017).
- Naik, S. H., Schumacher, T. N., Perié, L. Cellular barcoding: A technical appraisal. Experimental Hematology. 42 (8), 598-608 (2014).
- Quek, L., et al. Genetically distinct leukemic stem cells in human CD34 − acute myeloid leukemia are arrested at a hemopoietic precursor-like stage. The Journal of Experimental Medicine. 213 (8), 1513-1535 (2016).
- Karamitros, D., et al. Single-cell analysis reveals the continuum of human lympho-myeloid progenitor cells. Nature Immunology. 19 (1), 85-97 (2018).
- Boitano, A. E., et al. Aryl hydrocarbon receptor antagonists promote the expansion of human hematopoietic stem cells. Science. 329 (5997), 1345-1348 (2010).
- Delaney, C., et al. Notch-mediated expansion of human cord blood progenitor cells capable of rapid myeloid reconstitution. Nature Medicine. 16 (2), 232-236 (2010).
- Fares, I., et al. Cord blood expansion. Pyrimidoindole derivatives are agonists of human hematopoietic stem cell self-renewal. Science. 345 (6203), 1509-1512 (2014).
- Guo, B., Huang, X., Lee, M. R., Lee, S. A., Broxmeyer, H. E. Antagonism of PPAR-γ 3 signaling expands human hematopoietic stem and progenitor cells by enhancing glycolysis. Nature Medicine. 24 (3), 360-367 (2018).
- Vannini, N., et al. The NAD-booster nicotinamide riboside potently stimulates hematopoiesis through increased mitochondrial clearance. Cell Stem Cell. 24 (3), 405-418 (2019).
- Gupta, R., et al. Nov/CCN3 enhances cord blood engraftment by rapidly recruiting latent human stem cell activity. Cell Stem Cell. 26 (4), 527-541 (2020).
- Horwitz, M. E., et al. Omidubicel vs standard myeloablative umbilical cord blood transplantation: results of a phase 3 randomized study. Blood. 138 (16), 1429-1440 (2021).
- Weinreb, C., Rodriguez-Fraticelli, A., Camargo, F. D., Klein, A. M. Lineage tracing on transcriptional landscapes links state to fate during differentiation. Science. 367 (6479), 3381 (2020).
- Loeffler, D., Schroeder, T. Understanding cell fate control by continuous single-cell quantification. Blood. 133 (13), 1406-1414 (2019).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. Journal of Visualized Experiments. (70), e4287 (2012).
- Marchingo, J. M., et al. T-cell stimuli independently sum to regulate an inherited clonal division fate. Nature Communications. 7, 13540 (2016).
- Horton, M. B., et al. Multiplexed division tracking dyes for proliferation-based clonal lineage tracing. Journal of Immunology. 201 (3), 1097-1103 (2018).
- Lehmann, E. L., Romano, J. P., Casella, G. . Testing statistical hypotheses. , 784 (2005).
- Tak, T., et al. HSPCs display within-family homogeneity in differentiation and proliferation despite population heterogeneity. Elife. 10, 360624 (2021).
- Sommerkamp, P., et al. Mouse multipotent progenitor 5 cells are located at the interphase between hematopoietic stem and progenitor cells. Blood. 137 (23), 3218-3224 (2021).
- Kato, K., Radbruch, A. Isolation and characterization of CD34+ hematopoietic stem cells from human peripheral blood by high-gradient magnetic cell sorting. Cytometry. 14 (4), 384-392 (1993).
- Miltenyi, S., Müller, W., Weichel, W., Radbruch, A. High gradient magnetic cell separation with MACS. Cytometry. 11 (2), 231-238 (1990).
- Doulatov, S., et al. Revised map of the human progenitor hierarchy shows the origin of macrophages and dendritic cells in early lymphoid development. Nature Immunology. 11 (7), 585-593 (2010).
- Goardon, N., et al. Coexistence of LMPP-like and GMP-like leukemia stem cells in acute myeloid leukemia. Cancer Cell. 19 (1), 138-152 (2011).
- Laurenti, E., et al. CDK6 levels regulate quiescence exit in human hematopoietic stem cells. Cell Stem Cell. 16 (3), 302-313 (2015).
- Aiuti, A., et al. Lentiviral hematopoietic stem cell gene therapy in patients with Wiskott-Aldrich syndrome. Science. 341 (6148), 1233151 (2013).
- Davison, A. C., Hinkley, D. V. . Bootstrap Methods and their Application. , (1997).
- Horton, M. B., et al. Lineage tracing reveals B cell antibody class switching is stochastic, cell-autonomous, and tuneable. Immunity. 55 (10), 1843-1855 (2022).
- Notta, F., et al. Distinct routes of lineage development reshape the human blood hierarchy across ontogeny. Science. 351 (6269), 2116 (2016).
- Grinenko, T., et al. Hematopoietic stem cells can differentiate into restricted myeloid progenitors before cell division in mice. Nature Communications. 9 (1), 1898 (2018).
- Saeys, Y., Van Gassen, S., Lambrecht, B. N. Computational flow cytometry: Helping to make sense of high-dimensional immunology data. Nature Reviews Immunology. 16 (7), 449-462 (2016).

