Samtidig bedömning av släktskap, divisionsnummer och fenotyp via flödescytometri för hematopoetiska stam- och stamceller
Summary
Här presenteras en flödescytometribaserad teknik som möjliggör samtidig mätning av antalet celldelningar, ytcellsfenotyp och cellulärt släktskap. Dessa egenskaper kan testas statistiskt med hjälp av ett permutationsbaserat ramverk.
Abstract
Få tekniker kan bedöma fenotyp och öde för samma cell samtidigt. De flesta av de nuvarande protokollen som används för att karakterisera fenotyp, även om de kan generera stora dataset, kräver förstörelse av cellen av intresse, vilket gör det omöjligt att bedöma dess funktionella öde. Heterogena biologiska differentieringssystem som hematopoes är därför svåra att beskriva. Baserat på celldelningsspårningsfärgämnen utvecklade vi vidare ett protokoll för att samtidigt bestämma släktskap, divisionsnummer och differentieringsstatus för många enskilda hematopoetiska förfäder. Detta protokoll möjliggör bedömning av ex vivo-differentieringspotentialen hos murina och humana hematopoetiska stamfäder, isolerade från olika biologiska källor. Dessutom, eftersom det är baserat på flödescytometri och ett begränsat antal reagens, kan det snabbt generera en stor mängd data, på encellsnivå, på ett relativt billigt sätt. Vi tillhandahåller också den analytiska pipelinen för encellsanalys, kombinerat med ett robust statistiskt ramverk. Eftersom detta protokoll tillåter länkning av celldelning och differentiering på encellsnivå kan det användas för att kvantitativt bedöma symmetriskt och asymmetriskt ödesåtagande, balansen mellan självförnyelse och differentiering och antalet divisioner för ett givet engagemangsöde. Sammantaget kan detta protokoll användas i experimentella mönster som syftar till att avslöja de biologiska skillnaderna mellan hematopoetiska förfäder, ur ett encellsperspektiv.
Introduction
Det senaste decenniet präglades av den globala spridningen av encelliga metoder för cell- och molekylärbiologi. I stegen med encellsgenomik1,2 är det numera möjligt att studera många komponenter i en enda cell (t.ex. DNA, RNA, proteiner), med nya encells-omics-tekniker som växer fram varje år. Dessa tekniker har belyst gamla och nya frågor för områdena immunologi, neurobiologi, onkologi och andra, både med hjälp av mänskliga och modellorganismceller3. Genom att belysa skillnaderna mellan enskilda celler ledde single cell -omics till definitionen av en ny modell av hematopoies, centrerad på heterogeniteten hos hematopoetiska stam- och stamceller (HSPC) och rörde sig bort från den klassiska modellen av diskreta homogena populationer 4,5.
En av de få nackdelarna med alla -omics-tekniker är förstörelsen av cellen av intresse, vilket utesluter möjligheten att bedöma dess funktionalitet. Omvänt ger andra encellsmetoder, såsom encellstransplantationsanalys och härstamningsspårningsteknik, en avläsning av förfadercellens funktionalitet genom att bedöma ödet för enskilda celler in vivo 6,7. Släktspårningsteknik innebär att märka cellen av intresse med en ärftlig genetisk7 eller en fluorescerande etikett8,9, vilket gör att ödet för flera enskilda celler kan följas samtidigt. Karakteriseringen av utgångscellerna är emellertid typiskt begränsad till ett begränsat antal parametrar, såsom uttrycket av några ytproteiner bedömda med flödescytometri10. Dessutom kräver spårningsteknik för encellslinjer mödosam detektion av den cellulära etiketten, vanligtvis via DNA / RNA-sekvensering eller avbildning. Denna sista punkt begränsar särskilt antalet förhållanden som kan testas i ett enda experiment.
En annan klass av metoder som används för att studera funktionaliteten hos enskilda celler är ex vivo-cellodlingssystem för enskilda HSPC. Lätt att utföra, dessa guldstandardanalyser involverar sortering av enskilda celler i 96-brunnar cellodlingskärl och efter odling karakteriserar cellprogens fenotyp, vanligtvis genom flödescytometri eller morfologisk analys. Dessa analyser har mestadels använts för att karakterisera den långsiktiga differentieringen av HSPC i mogna celler, vanligtvis efter 2-3 veckors odling11,12. Alternativt har de använts för att försöka upprätthålla och expandera ex vivo HSPC 13,14,15,16,17,18, med löfte om medicinsk nytta för mänsklig stamcellstransplantation 19. Slutligen har de använts för att studera HSPC: s tidiga engagemang med korttidskultur20, med det låga antalet celler som genereras i denna kultur som den viktigaste begränsande faktorn. En nackdel med dessa olika typer av ex vivo-analyser är att de endast delvis återspeglar in vivo-komplexiteten; ändå är de ett av de sällsynta sätten att studera mänsklig HSPC-differentiering.
En saknad information från befintliga encellsmetoder (single cell-omics, härstamningsspårning och ex vivo-kultur) är noggrann detektion av celldelningar, en viktig parameter att tänka på när man studerar HSPC-dynamik21. Ett enkelt sätt att bedöma antalet divisioner via flödescytometri är användningen av lösliga “proteinfärgämnen”, som 5-(och 6)-karboxifluoresceindiacetatsuccinimidylester (CFSE)22. Dessa delningsfärgämnen diffunderar inuti cytoplasman hos de färgade cellerna och späds med hälften och överförs till de två dottercellerna vid varje celldelning, vilket möjliggör uppräkning upp till 10 divisioner. Genom att kombinera flera delningsfärgämnen är det möjligt att fröa flera enskilda föregångare i samma brunn, eftersom varje enskilt färgämne möjliggör separation av de olika efterkommande. Detta är principen bakom användningen av cellfärgämnen för multiplex klonal och delningsspårning som först introducerades för murina lymfocyter23,24.
Här presenterar vi utvecklingen av MultiGen-analysen för användning med murina och humana HSPC. Det möjliggör testning av många enskilda celler samtidigt för deras egenskaper differentiering, delning och släktskap ex vivo. Denna höga genomströmning, lätt att utföra och billig analys gör det möjligt att mäta den cellulära fenotypen, antalet utförda divisioner och cellkinskapet och klonalförhållandet med de andra cellerna i brunnen, allt samtidigt. Den kan användas för att kvantitativt bedöma symmetriskt och asymmetriskt ödesåtagande, balansen mellan självförnyelse och differentiering och antalet uppdelningar som är nödvändiga för ett givet åtagandeöde. Protokollet kräver en fluorescensaktiverad cellsorterare (FACS) och en flödescytometer med en plattläsare, plus den utrustning som krävs för att utföra cellodling. Förutom det tekniska protokollet för utförande av analysen på humana HSPC, tillhandahåller vi också den detaljerade analysramen, inklusive den statistiska testning som krävs för att bedöma cellulära egenskaper relaterade till begreppet cellfamilj25. Detta protokoll har redan använts framgångsrikt för att beskriva murina HSPC-fack26,27.
Följande protokoll använder magnetiskt anrikade CD34 + -celler som utgångsmaterial28. På detta sätt är det möjligt att effektivt färga och isolera de mänskliga HSPC: erna från olika blodkällor (t.ex. navelsträngsblod, benmärg, perifert blod). Det är viktigt att inte kassera CD34-fraktionen, eftersom den kommer att användas som en del av protokollet för att ställa in olika typer av experimentella kontroller. De nämnda cellmängderna och volymerna kan skalas upp eller ner, beroende på experimentellt arbetsflöde och nödvändigheter. På samma sätt kan protokollet anpassas till studier av olika typer av förfäder, helt enkelt genom att modifiera antikropparna som används för cellsorterings- och flödescytometristegen.
Protocol
Representative Results
Discussion
MultiGen-analysen är en high-throughput, lätt att utföra och odyr analys, som har varit avgörande för att studera lymfocyt 23,24,35 och murina hematopoetiska celler 26,27. Här presenterar vi en ny utveckling av tillvägagångssättet som gör det möjligt att dechiffrera ex vivo den tidiga fasen av humant HSPC-engagemang, på encellsnivå med hjälp av kortvarig kultur (figur 6). Encelliga ex vivo-odlingssystem används vanligtvis för att bedöma HSPC: s långsiktiga öde i mogna celler, men vissa öden inträffar tidigare än andra36, vilket potentiellt fördjupar analysen mot färre öden. Dessutom saknar dessa kultursystem vanligtvis information om uppdelningar under ödesåtagandet. De första engagemangsstegen har visat sig inträffa så tidigt som i början av kulturen, ibland utan division26,37, vilket gör kortsiktig kultur och spårning av division avgörande för att studera tidigt ödesengagemang. Genom att samtidigt följa ödet, uppdelningen och släktskapet tillåter denna analys att förstå rollen för den första divisionen och ödesbeslutet i mänskliga HSPC. Med hjälp av analysen är det möjligt att dra slutsatsen efter hur många divisioner engagemangsprocessen sker, balansen mellan självförnyelse och differentiering för de tidiga förfäderna och hur dessa egenskaper ärvs över generationer. Såvitt vi vet är detta den enda analysen som tillåter dessa typer av mätningar för humana HSPC, med encellsupplösning. Dessutom, med hjälp av olika kombinationer av celldelningsfärgämnen, ökade vi genomströmningen av analysen, vilket gjorde denna analys till ett värdefullt verktyg för att snabbt generera stora dataset. Färgkombinationerna gör det möjligt att följa flera familjer i samma brunnar, vilket ökar antalet celler som är tillgängliga för analys i korttidsodling. Antalet kombinationer kan potentiellt ökas ännu mer, genom tillsats av andra färgämnen (t.ex. gult färgämne) eller modifiering av förhållandet mellan CFSE och CTV. Detta minskar dock antalet andra parametrar som kan analyseras.
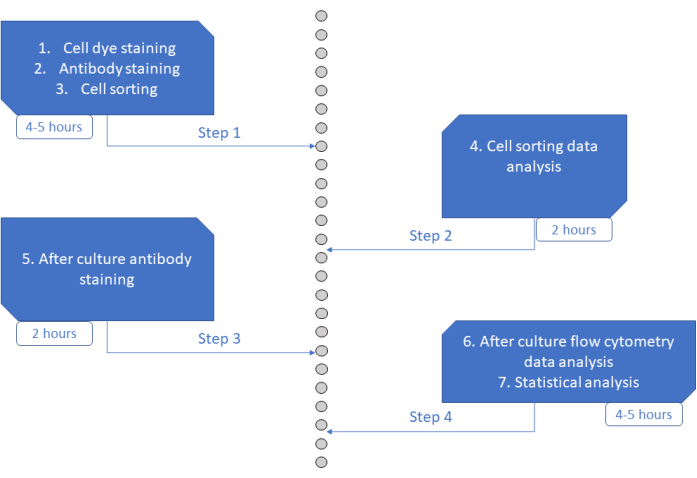
Figur 6: Schematisk representation av protokollet. Klicka här för att se en större version av denna figur.
För att utföra analysen framgångsrikt, på grund av det stora antalet brunnar och det reducerade antalet celler som ska analyseras, är det nödvändigt att köra flödescytometrianalysen på en analysator utrustad med en plattläsare. Den nya generationen bänkanalysatorer är särskilt anpassade för denna analys, eftersom de flesta av dem har en mindre dödvolym för att minska andelen cellförlust. Detta garanterar i sin tur en högre effektivitet vid återvinning av hela varje brunn, vilket leder till en effektivitet som uppskattas i intervallet70% 26. Att uppskatta cellförlusten under flödescytometriförvärvet är avgörande för analysen av varje enskild familj. Till exempel, förutsatt ingen celldöd och räknar antalet divisioner, är det möjligt att uppskatta antalet celler per varje familj. Det är dock önskvärt att utföra några bekräftande experiment, särskilt vid uppskattning av celldöd under de testade odlingsbetingelserna och mätning av återhämtningshastigheten experimentellt med användning av ett definierat antal celler.
Ett av de avgörande stegen i detta protokoll är topptilldelningen. Som redan nämnts är en toppfördelning av god kvalitet starkt beroende av isolering av mycket smala toppar vid cellsortering. Ändå är det fortfarande svårt att tilldela rätt antal divisioner baserat unikt på fördelningen. Eftersom cellsortering och flödescytometrianalys utförs på två olika maskiner är det inte möjligt att direkt jämföra intensiteten hos varje signal, så det kan vara svårt att veta om den första toppen som observeras i histogrammets högra ände är topp 0 eller topp 1. I detta avseende är få lösningar möjliga; Ett sätt är att utföra ett ortogonalt experiment för att noggrant mäta antalet divisioner som utförs av dessa celler (t.ex. levande cellavbildning). En annan möjlighet är att helt enkelt räkna antalet celler i brunnen under ett inverterat ljusfältmikroskop innan flödescytometrianalysen körs. Detta kommer att härleda ett genomsnittligt antal divisioner (förutsatt ingen celldöd). Slutligen är en post-hoc-lösning för topptilldelning detektering av ett ovanligt antal “omöjliga familjer”; Dessa familjer består av ett större antal celler per generation än möjligt (t.ex. fem celler i generation 2, eller två celler i generation 1 och en cell i generation 2). Möjligheten att exkludera omöjliga familjer kodas i det statistiska analyssteget, och flaggar för den omöjliga familjen. Om förekomsten av dessa fel är för hög är det rimligt att anta att topptilldelningen behöver revideras.
I detta protokoll inkluderade vi några exempel på datarepresentation och analys för analysen, eftersom detta har blivit ett viktigt steg i genereringen och tolkningen av stora dataset38. Det första exemplet är värmekartan som visar totaliteten av alla analyserade celler, organiserade per familj. Detta är ett effektivt verktyg för att utforska de allmänna egenskaperna hos data och potentiella slutsatser: är familjer sammansatta av flera celltyper eller tenderar de att vara homogena i sammansättning? Är familjer spridda över flera generationer, eller delar de oftast lika många gånger? Denna explorativa analys måste sedan kompletteras med mer specifika diagram och statistiska tester. Den kan användas för att kvantitativt bedöma symmetriskt och asymmetriskt ödesengagemang, differentiering utan uppdelning, balansen mellan självförnyelse och differentiering och antalet divisioner för ett givet åtagandeöde. Det är grundläggande, under experimentplaneringen, att ställa in cellodlingslängden i enlighet med den typ av fråga som ställs; Till exempel, för de två första frågorna (symmetrisk/asymmetrisk balans och differentiering utan uppdelning), möjliggör planering av mycket korta kultursteg isolering av ett stort antal familjer som bara har utfört en eller ingen uppdelning alls26. Omvänt tillåter längre experiment utforskning av antalet divisioner som krävs för ett specifikt cellåtagande, eftersom de samplar familjer i olika stadier av differentiering. Ändå är denna metod inte utformad för långsiktiga kulturer (2-3 veckor), eftersom cellfärgutspädning inte kan spåra mer än sju eller åtta divisioner22. Som en konsekvens är detta verktyg mestadels anpassat för att studera det tidiga engagemanget hos hematopoetiska förfäder och är inte utformat för att göra robusta slutsatser om dessa cellers långsiktiga differentieringsegenskaper.
Den statistiska ramen utvecklades specifikt för analys av denna typ av data och baserades på begreppet permutationer26. Detta var nödvändigt på grund av observationen av ett familjärt beroende av celltypfördelningen och antalet utförda divisioner. Med andra ord är celler som ingår i samma familj också mer benägna att visa liknande fenotyper och dela samma antal gånger. Även om en djupgående analys ligger utanför ramen för detta arbete, bör den tillhandahållna uppsättningen statistiska tester vara tillräckliga för att bedöma olika förhållanden.
Sammanfattningsvis utgör detta protokoll ett värdefullt verktyg för att bedöma den cellulära dynamiken hos hematopoetiska stam- och stamceller ex vivo, på ett snabbt och billigt sätt. På grund av dess flexibilitet och mångsidighet när det gäller tidpunkt, odlingsförhållanden och typ av HSPC analyseras, gör det möjligt att testa en mängd olika experimentella förhållanden. Som en flödescytometribaserad analys kan den implementeras i de flesta laboratorier, och den kräver inte omfattande förkunskaper, vilket gör den till en bra kandidat för screenings och pilotexperiment.
Declarações
The authors have nothing to disclose.
Acknowledgements
Vi vill tacka medlemmarna i Institut Curie Flow Facility för deras hjälp med att sätta upp flödescytometriexperimenten. Vi vill också uppmärksamma bidragen från de andra medlemmarna i Team Perié, under flera diskussioner. Vi tackar Dr. Julia Marchingo och Prof. Phil Hodgkin (Walter end Eliza Hall Institute of Medical Research) för att dela sitt protokoll för multiplexering av celldelningsfärgämnen på lymfocyter. Vi tackar biobanken för navelsträngsblod på Saint Louis sjukhus för att ha tillhandahållit de biologiska resurser som är nödvändiga för utvecklingen av detta protokoll. Studien stöddes av ett ATIP-Avenir-bidrag från CNRS och Bettencourt-Schueller Foundation (till LP), bidrag från Labex CelTisPhyBio (ANR-10-LBX-0038) (till LP och AD), Idex Paris-Science-Lettres Program (ANR-10-IDEX-0001-02 PSL) (till LP), Canceropole INCA Emergence (2021-1-EMERG-54b-ICR-1, till LP) och ITMO MIIC-bidraget (21CM044, till L.P.). Förutom finansiering från Europeiska forskningsrådet (ERC) under Europeiska unionens forsknings- och innovationsprogram Horizon 2020 ERC StG 758170-Microbar (till LP), stöddes A.D. av ett stipendium från Fondation de France.
Materials
| 1.5 mL polypropylene microcentrifuge tubes | vWR | 87003-294 | |
| 15-mL polypropylene tubes | vWR | 734-0451 | |
| 50-mL polypropylene tubes | vWR | 734-0448 | |
| 96-well U-bottom culture plate | Falcon | 353077 | |
| Anti-human Lin APC | Thermo Fisher | 22-7776-72 | Dilution 1/40 |
| ARIA III | BD | Can be replaced with any FACS sorter able to sort individual cells in 96-wells plate | |
| Carboxyfluorescein succinimidyl ester (CFSE) | Life Technologies | C34570 | |
| Cell Trace Violet (CTV) | Life Technologies | C34571 | |
| Compensation beads | BD | 552843 | |
| Dulbecco’s modified Eagle medium (DMEM) | Life Technologies | 11320033 | |
| Ethylenediaminetetraacetic acid (EDTA) | Thermo Scientific | J62948-36 | Prepare a solution 0.5 M, in sterilised water |
| FC block Fc1.3216 | BD | 564220 | Dilution 1/50 |
| Fetal Bovine Serum (FBS) | Dutscher | S1900-500C | Batch S00CH |
| FlowJo v10.8.1 | BD | ||
| Mouse anti-human CD10 PerCP-5.5, clone HI10a | Biolegend | 312216 | Dilution 1/20 |
| Mouse anti-human CD123 BUV395, clone 7G3 | BD | 564195 | Dilution 1/15 |
| Mouse anti-human CD34 APC-Cy7, clone 581 | Biolegend | 343513 | Dilution 1/40 |
| Mouse anti-human CD38 BV650, clone HB7 | Biolegend | 356620 | Dilution 1/40 |
| Mouse anti-human CD45RA AF700, clone HI100 | BD | 560673 | Dilution 1/20 |
| Mouse anti-human CD45RA PE-Cy7, clone HI100 | BD | 560675 | Dilution 1/20 |
| Mouse anti-human CD90 PE, clone 5E10 | Biolegend | 328110 | Dilution 1/20 |
| Phosphate Buffered Saline (PBS) 1X | Life Technologies | 10010001 | |
| Python | |||
| R | |||
| Sterile 12×75 mm conical polypropylene tubes | Falcon | ||
| ZE5 | Biorad | Can be replaced with any flow cytometry analyzer equipped with a plate reader | |
| Laboratory prepared | |||
| Cell culture media | Depends from the specific experiment. Prepare fresh daily and store at +4 °C until use | ||
| DMEM + 10% FBS | Can be stored in sterile conditions, at +4 °C up to 1 year. To prepare 500 mL, add 50 mL of FBS to 450 mL DMEM | ||
| PBS 1X + EDTA 0.1% | Can be stored in sterile conditions, at room temperature, up to 1 year. To prepare 500 mL, add 3.42 mL of EDTA 0.5 M to 500 mL PBS 1X | ||
| Staining buffer | Can be stored in sterile conditions, at +4 °C up to 1 year. To prepare 500 mL, add 2 mL of EDTA 0.5 M and 1 mL FBS to 500 mL PBS 1X |
Referências
- Ginhoux, F., Yalin, A., Dutertre, C. A., Amit, I. Single-cell immunology: Past, present, and future. Immunity. 55 (3), 393-404 (2022).
- Ke, M., Elshenawy, B., Sheldon, H., Arora, A., Buffa, F. M. Single cell RNA-sequencing: A powerful yet still challenging technology to study cellular heterogeneity. Bioessays. 44 (11), 2200084 (2022).
- Regev, A., et al. The human cell atlas. Elife. 6, 27041 (2017).
- Laurenti, E., Göttgens, B. From haematopoietic stem cells to complex differentiation landscapes. Nature. 553 (7689), 418-426 (2018).
- Haas, S., Trumpp, A., Milsom, M. D. Causes and consequences of hematopoietic stem cell heterogeneity. Cell Stem Cell. 22 (5), 627-638 (2018).
- Loughran, S. J., Haas, S., Wilkinson, A. C., Klein, A. M., Brand, M. Lineage commitment of hematopoietic stem cells and progenitors: insights from recent single cell and lineage tracing technologies. Experimental Hematology. 88, 1-6 (2020).
- Perié, L., Duffy, K. R. Retracing the in vivo haematopoietic tree using single-cell methods. FEBS Letters. 590 (22), 4068-4083 (2016).
- Yu, V. W. C., et al. Epigenetic memory underlies cell-autonomous heterogeneous behavior of hematopoietic stem cells. Cell. 167 (5), 1310-1322 (2016).
- Ganuza, M., et al. Lifelong haematopoiesis is established by hundreds of precursors throughout mammalian ontogeny. Nature Cell Biology. 19 (10), 1153-1163 (2017).
- Naik, S. H., Schumacher, T. N., Perié, L. Cellular barcoding: A technical appraisal. Experimental Hematology. 42 (8), 598-608 (2014).
- Quek, L., et al. Genetically distinct leukemic stem cells in human CD34 − acute myeloid leukemia are arrested at a hemopoietic precursor-like stage. The Journal of Experimental Medicine. 213 (8), 1513-1535 (2016).
- Karamitros, D., et al. Single-cell analysis reveals the continuum of human lympho-myeloid progenitor cells. Nature Immunology. 19 (1), 85-97 (2018).
- Boitano, A. E., et al. Aryl hydrocarbon receptor antagonists promote the expansion of human hematopoietic stem cells. Science. 329 (5997), 1345-1348 (2010).
- Delaney, C., et al. Notch-mediated expansion of human cord blood progenitor cells capable of rapid myeloid reconstitution. Nature Medicine. 16 (2), 232-236 (2010).
- Fares, I., et al. Cord blood expansion. Pyrimidoindole derivatives are agonists of human hematopoietic stem cell self-renewal. Science. 345 (6203), 1509-1512 (2014).
- Guo, B., Huang, X., Lee, M. R., Lee, S. A., Broxmeyer, H. E. Antagonism of PPAR-γ 3 signaling expands human hematopoietic stem and progenitor cells by enhancing glycolysis. Nature Medicine. 24 (3), 360-367 (2018).
- Vannini, N., et al. The NAD-booster nicotinamide riboside potently stimulates hematopoiesis through increased mitochondrial clearance. Cell Stem Cell. 24 (3), 405-418 (2019).
- Gupta, R., et al. Nov/CCN3 enhances cord blood engraftment by rapidly recruiting latent human stem cell activity. Cell Stem Cell. 26 (4), 527-541 (2020).
- Horwitz, M. E., et al. Omidubicel vs standard myeloablative umbilical cord blood transplantation: results of a phase 3 randomized study. Blood. 138 (16), 1429-1440 (2021).
- Weinreb, C., Rodriguez-Fraticelli, A., Camargo, F. D., Klein, A. M. Lineage tracing on transcriptional landscapes links state to fate during differentiation. Science. 367 (6479), 3381 (2020).
- Loeffler, D., Schroeder, T. Understanding cell fate control by continuous single-cell quantification. Blood. 133 (13), 1406-1414 (2019).
- Tario, J. D., et al. Optimized staining and proliferation modeling methods for cell division monitoring using cell tracking dyes. Journal of Visualized Experiments. (70), e4287 (2012).
- Marchingo, J. M., et al. T-cell stimuli independently sum to regulate an inherited clonal division fate. Nature Communications. 7, 13540 (2016).
- Horton, M. B., et al. Multiplexed division tracking dyes for proliferation-based clonal lineage tracing. Journal of Immunology. 201 (3), 1097-1103 (2018).
- Lehmann, E. L., Romano, J. P., Casella, G. . Testing statistical hypotheses. , 784 (2005).
- Tak, T., et al. HSPCs display within-family homogeneity in differentiation and proliferation despite population heterogeneity. Elife. 10, 360624 (2021).
- Sommerkamp, P., et al. Mouse multipotent progenitor 5 cells are located at the interphase between hematopoietic stem and progenitor cells. Blood. 137 (23), 3218-3224 (2021).
- Kato, K., Radbruch, A. Isolation and characterization of CD34+ hematopoietic stem cells from human peripheral blood by high-gradient magnetic cell sorting. Cytometry. 14 (4), 384-392 (1993).
- Miltenyi, S., Müller, W., Weichel, W., Radbruch, A. High gradient magnetic cell separation with MACS. Cytometry. 11 (2), 231-238 (1990).
- Doulatov, S., et al. Revised map of the human progenitor hierarchy shows the origin of macrophages and dendritic cells in early lymphoid development. Nature Immunology. 11 (7), 585-593 (2010).
- Goardon, N., et al. Coexistence of LMPP-like and GMP-like leukemia stem cells in acute myeloid leukemia. Cancer Cell. 19 (1), 138-152 (2011).
- Laurenti, E., et al. CDK6 levels regulate quiescence exit in human hematopoietic stem cells. Cell Stem Cell. 16 (3), 302-313 (2015).
- Aiuti, A., et al. Lentiviral hematopoietic stem cell gene therapy in patients with Wiskott-Aldrich syndrome. Science. 341 (6148), 1233151 (2013).
- Davison, A. C., Hinkley, D. V. . Bootstrap Methods and their Application. , (1997).
- Horton, M. B., et al. Lineage tracing reveals B cell antibody class switching is stochastic, cell-autonomous, and tuneable. Immunity. 55 (10), 1843-1855 (2022).
- Notta, F., et al. Distinct routes of lineage development reshape the human blood hierarchy across ontogeny. Science. 351 (6269), 2116 (2016).
- Grinenko, T., et al. Hematopoietic stem cells can differentiate into restricted myeloid progenitors before cell division in mice. Nature Communications. 9 (1), 1898 (2018).
- Saeys, Y., Van Gassen, S., Lambrecht, B. N. Computational flow cytometry: Helping to make sense of high-dimensional immunology data. Nature Reviews Immunology. 16 (7), 449-462 (2016).

