En højopløsning, enkeltkornet, in vivo pollenhydrering bioassay for Arabidopsis thaliana
Summary
En forbedret metode til måling af pollenhydreringsprofiler i Arabidopsis thaliana er beskrevet her. Den nye metode tilbyder højere opløsning, er ikke-invasiv og er meget reproducerbar. Protokollen repræsenterer et nyt værktøj til en finere dissektion af de processer, der regulerer de tidlige stadier af bestøvning.
Abstract
Seksuel reproduktion i blomstrende planter kræver indledende interaktion mellem pollenkornet og den stigmatiske overflade, hvor der etableres en molekylær dialog mellem de interaktive partnere. Undersøgelser på tværs af en række arter har afsløret, at en række molekylære kontrolpunkter regulerer pollen-stigma-interaktionen for at sikre, at kun kompatibel, generelt intraspecifik pollen har succes med at påvirke befrugtning. I arter, der har et ‘tørt stigma’, såsom modelplanten Arabidopsis thaliana, er det første kontrolpunkt efter bestøvning, præzygotisk kompatibilitet, etablering af pollenhydrering.
Denne bestøvningsfase er stramt reguleret, hvorved signaler fra pollenkornet fremkalder frigivelse af vand fra stigmatiseringen, hvilket tillader pollenhydrering. Evnen til nøjagtigt at måle og spore pollenhydrering over tid er nøglen til design af eksperimenter rettet mod at forstå reguleringen af dette kritiske trin i reproduktion. Offentliggjorte protokoller bruger ofte blomster, der er blevet udskåret fra moderplanten, vedligeholdt på flydende eller faste medier og bulkbestøvet.
Dette papir beskriver et ikke-invasivt, in vivo bestøvningsbioassay, der tillader minut-for-minut hydreringssporing af individuelle A. thaliana pollenkorn i høj opløsning. Assayet er meget reproducerbart, i stand til at detektere meget subtile variationer af pollenhydratiseringsprofiler og er således velegnet til analyse af mutanter, der påvirker veje, der regulerer bestøvning. Selvom protokollen er længere end dem, der er beskrevet for bulkbestøvninger, gør den præcision og reproducerbarhed, den giver, sammen med dens in vivo-natur , den ideel til detaljeret dissektion af bestøvningsfænotyper.
Introduction
Vellykket seksuel reproduktion i angiospermer er typisk afhængig af overførsel af intraspecifikke pollenkorn fra anther til stigma, enten inden for eller mellem individer (dvs. bestøvning). Denne overførsel af pollenkorn til en modtagelig blomst medieres normalt af bestøvere eller abiotiske faktorer; Som sådan resulterer dette også ofte i aflejring af heterospecifik pollen under naturlige forhold. Med nogle få undtagelser er progressionen af bestøvning med heterospecifik pollen evolutionært ufordelagtig, hvilket reducerer reproduktionsegnetheden gennem tabte parringsmuligheder, hvor de fleste resulterende hybridafkom enten ikke udvikler sig hensigtsmæssigt eller er sterile1. Således har der udviklet sig mekanismer til at blokere bestøvning af ‘inkompatibel’ heterospecifik pollen2. Hurtig genkendelse af kompatibel pollen er derfor uden tvivl den vigtigste proces i de tidlige stadier af seksuel reproduktion i mange blomstrende planter.
I familien Brassicaceae, hvor stigmatiseringer er af den ‘tørre’ type, virker en række molekylære kontrolpunkter på flere stadier i reproduktionsprocessen, der regulerer bestøvning, således at kun kompatibel pollen er vellykket. Pollenhydrering er et af de vigtigste kontrolpunkter (figur 1), da pollen, der ikke hydrerer, ikke kan udvikle sig til at producere et pollenrør og derefter levere sæd til den kvindelige gametofyt. Ofte undlader uforenelige korn at passere dette første bestøvningskontrolpunkt og får derfor ikke adgang til stigmatisk vand3. Blandt medlemmer af familien Brassicaceae sker genkendelsen af pollen hurtigt, idet kompatibiliteten etableres inden for få minutter efter pollenkornets fastgørelse til støvlen 4,5. I de senere år er der gjort store fremskridt, og vi begynder nu at forstå de molekylære mekanismer, der regulerer vigtige bestøvningskontrolpunkter.
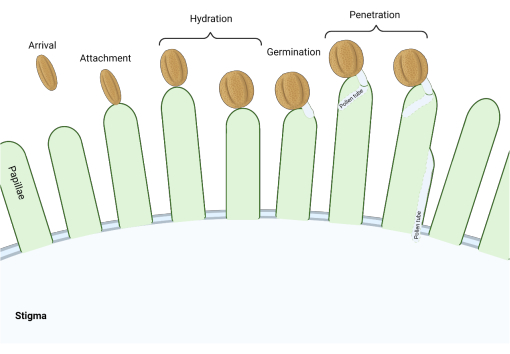
Figur 1: Oversigt over vigtige hændelser under kompatibel bestøvning. Disse stadier, såsom pollenhydrering og pollenrørspiring, er også bestøvningskontrolpunkter, der skal navigeres med succes for at opnå kompatibel bestøvning. Diagrammet repræsenterer en ‘tør’ type stigma, som er typisk for arter fra Brassicaceae-familien 2,20. Klik her for at se en større version af denne figur.
Banebrydende forskning i Brassica selvinkompatibilitet (SI) system, hvor ‘selv’ pollen anerkendes og afvises, etablerede paradigmet for pollen-stigma anerkendelse i Brassicaceae 6,7,8,9,10. SI i Brassica og dets slægtninge medieres af ‘genkendelsesproteiner’, der befinder sig på overfladen af pollen og ved den stigmatiske plasmamembran, der ved interaktion fører til pollenafstødning. SI-pollenafvisning fungerer ved forstyrrelse af det basale pollen-stigma-kompatibilitetssystem, som, når det aktiveres fuldt ud af opfattelsen af kompatibelt pollen, fører til målrettet sekretion af stigmatiseringen og dermed driver pollenhydrering (for anmeldelser af pollenkompatibilitetsmekanismen, se11,12). I eksemplet med SI er den pollenbårne ligand et lille cysteinrigt protein, S-locus cystein rig (SCR / SP11), og den stigmatiske receptor er S-locus receptorkinase (SRK).
For nylig, i Arabidopsis thaliana, en anden gruppe af små cystein-rige pollen-bårne proteiner, pollen coat protein klasse Bs (VedPCP-Bs), har vist sig at være vigtige regulatorer af pollen accept gennem aktivering af pollen hydrering13. Stigmatiske receptorer af AtPCP-Bs og aspekter af nedstrøms reguleringsvejen er også for nylig blevet beskrevet14,15. Interessant nok har mutationsundersøgelser af gener, der koder for potentielle pollenbårne og stigmatiske signalmediatorer af pollenhydrering (herunder vedPCP-Bs) undladt at generere planter, der har en komplet blok til pollenhydreringskontrolpunktet. Dette tyder stærkt på, at flere andre, men uopdagede, faktorer spiller en rolle i reguleringen af pollenhydrering. Med udgangspunkt i den metode, der først blev beskrevet af Wang et al.13, beskriver vi her et forbedret in vivo-bioassay med høj opløsning, der er egnet til identifikation af subtile pollenhydratiseringsdefekter i kandidatmutante A. thaliana-linjer.
Protocol
Representative Results
Discussion
For blomstrende planter er de meget tidlige stadier af seksuel reproduktion uden tvivl de vigtigste. På niveau med pollen-stigma-interaktionen træffes molekylære beslutninger, der bestemmer de interaktive partneres ‘kompatibilitet’. Sådanne beslutninger skal, hvis de træffes korrekt, undgå spild af ressourcer, der kan påvirke reproduktionsevnen21. At tillade kun kompatibel pollen at udføre befrugtning er således en vigtig komponent i opretholdelsen af veltilpassede genotyper og dermed arternes evolutionære succes. Forskning udført med modelplanten A. thaliana har været yderst værdifuld for at uddybe vores forståelse af denne proces. En række undersøgelser i løbet af de sidste par årtier har afsløret tilstedeværelsen af faktorer i pollenpelsen, der virker ved det første kompatibilitetskontrolpunkt, hvor pollen får adgang til stigmatisk vand for at tillade pollenhydrering13. På trods af disse første indsigter i de mekanismer, der regulerer pollen-stigma-kompatibilitet, er der stadig mange huller i vores forståelse af denne proces. Til dato kan ingen mutanter af pollenbårne ligander eller stigmatiske receptorer, der vides at påvirke pollenhydrering, fuldstændigt blokere kompatibel bestøvning, hvilket tyder på tilstedeværelsen af andre uopdagede pollenhydreringsdeterminanter. Ved let at kunne observere fænotypen af interesse er pollenhydreringsbioassayet, der er beskrevet her, en af de mest ligetil teknikker til at studere potentielle mutanter, der regulerer bestøvning.
Eksisterende metoder til måling af pollenhydrering bruger almindeligvis bulkbestøvninger og rapporterer færre tidspunkter 14,22,23 og kan således gå glip af vigtige subtile hydreringsprofilfænotyper. For eksempel har undersøgelsen af Wang et al.13 sammen med arbejde med andre pollencoatproteinmutanter i vores laboratorium (upublicerede observationer) afsløret spændende forskelle i hydreringsprofiler mellem mutanter. Sådanne subtile forskelle kan indeholde vigtige fingerpeg om de reguleringsmekanismer, der ligger til grund for kompatibel bestøvning.
Metoden beskrevet her fokuserer på erhvervelse af relativt små antal målinger mellem mutant- og WT-plantelinjer med vægt på metodologisk præcision for at reducere variationen inden for datasættene. Selvom denne metode er meget reproducerbar (som vist i figur 7), forudsat at temperatur og fugtighed kontrolleres tilstrækkeligt, er det vigtigt at indsamle hydreringsdata for næsten lige mange WT og mutant pollen på samme dag for yderligere at reducere potentialet for variation. Data kan derefter samles på tværs af forskellige dage, hvis det er nødvendigt. Derudover er valg af passende WT-kontrolanlæg afgørende for korrekt fortolkning af hydreringsresultaterne. For pollenmodtageren skal den samme plantelinje bruges til at modtage både WT-kontrol og mutante pollenkorn.
For eksempel bruger vi pA9-barnase mandlige sterile plantelinje, som også er omtalt i videoprotokollen, som pollenmodtager for både WT (kontrol) og mutant (eksperimentel) pollen, når vi undersøger T-DNA pollenmutantlinjer (såsom ‘KD’ mutanten beskrevet i figur 8). Blanding af data fra en sådan mandlig steril linje, som ikke behøver at blive emaskuleret, med data indsamlet fra en manuelt emaskuleret kontrollinje bør undgås, da disse stigmas sandsynligvis vil opføre sig anderledes. Ligeledes bør emaskulerede mutantlinjer anvendes sammen med en emaskuleret WT (kontrol) linje, når det er muligt. Den samme forsigtighed bør også anvendes, når man overvejer den genetiske baggrund for de undersøgte planter. Mens de mest populære T-DNA-mutantsamlinger blev genereret i Col-0-baggrunden, er andre, såsom FLAG-samlingen fra Institut national de la Recherche Agronomique (INRA), tilgængelige i Wassilewskija (WS) genetiske baggrund24,25. I sådanne tilfælde anbefales det at anvende den respektive økotypes WT-anlægslinjer som kontrol.
Selvom vi her har fokuseret på pollenhydrering i løbet af de første 10 minutter af pollen-stigma-interaktionen, kan denne metode også tilpasses til at omfatte hydreringsprofiler, der dækker en længere periode. Et centralt træk ved protokollen er, at blomster forbliver knyttet til moderplantestrømmen, offentliggjorte protokoller kræver typisk udskæring af støvlen og placering i medier for at opretholde vævet i løbet af eksperimentet14,18,26. Selvom der ikke er noget direkte bevis for, at en sådan semi in vivo-tilgang påvirker pollenhydrering eller faktisk ændrer in vivo-reguleringen af denne proces, er det tænkeligt, at udskæring af blomsterne fra moderplanten kan påvirke bestøvningen. Således opnår denne protokol et ægte in vivo-miljø til undersøgelse af pollen-stigma-interaktionen, hvor plantens strukturelle integritet bevares.
Overførslen af enkelte pollenkorn til ‘jomfruelige’ stigmatiske papiller er uden tvivl en af de mest udfordrende operationer, der er beskrevet i denne protokol. Det er ikke ualmindeligt at overføre klynger af pollenkorn ved en fejl. Imidlertid kan chancen for, at dette sker, reduceres kraftigt ved at sikre, at kun et monolag pollen er til stede på tangen (figur 3A) (eller endda bare et enkelt pollenkorn; Figur 5), og/eller ved at udnytte pollenkorn, der allerede er orienteret, således at de ‘stikker ud’ fra andre på spidsen af tangen. Vi har fundet ud af, at en erfaren operatør med succes kan gennemføre overførslen af en enkelt pollen til en stigmatisk papillacelle på cirka 3 minutter og registrere data for op til fem pollenkorn over en periode på 1 time. Således kan der over en periode på 2-4 dage akkumuleres tilstrækkelige data til meningsfuld statistisk analyse af de undersøgte plantelinjer.
Menneskelige fejl er potentielt den største kilde til variation i analysen af datasæt afledt af undersøgelser, der anvender denne protokol. For eksempel kommer definitionen af ‘pollengrænsen’ under billedanalyse ned til den enkelte forskers vurdering. Der er således potentiale for, at målinger foretaget af forskellige forskere, selv på det samme datasæt, kan generere variation. Hvor det er muligt, bør en enkelt forsker udføre målingerne for at minimere prøveudtagningsfejl. Desuden ophæver koblingen af analysen af WT og mutante datasæt foretaget af den samme operatør den potentielt subjektive definition af »pollengrænsen« og variationen mellem operatørerne.
Afslutningsvis beskrives en sofistikeret, men præcis metode til måling af pollenhydratiseringsprofiler i modelorganismen A. thaliana. Vi har vist, at ved at udnytte denne protokol, meget konsistente pollen hydrering data for A. thaliana let kan erhverves. Tre uafhængige batcher af data for WT-bestøvninger indsamlet på forskellige dage viste konsistente små afvigelser på <3% på tværs af alle tidspunkter (figur 7 og supplerende tabel S1). Selvom bioassayet, der præsenteres her, er lidt mere komplekst end de fleste eksisterende protokoller, er opløsningen af de genererede data overlegen og egnet til identifikation og karakterisering af nye mutanter, der påvirker veje, der regulerer kompatibel bestøvning.
Declarações
The authors have nothing to disclose.
Acknowledgements
Denne forskning blev støttet af University of Bath (University of Bath, Bath, UK, BA2 7AY) postgraduate stipendier til Y.-L.L. og L.W. Figur 1 blev oprettet med BioRender.com (https://biorender.com/).
Materials
| A9-barnase line | University of Bath | Courtsey of Prof. Rod Scott | Male sterile Arabidopsis thaliana wildtype equivalent line of the ecotype Columbia-0 |
| Dumont Tweezer, Dumont #5 Inox 11cm | Fisher | Dumont 500342 | Tweezer uses for transfer of pollen grain |
| GraphPad Prsim (version 8.0.2) | Dotmatics | Prism | Comprehensive data analysis, graphing and statistics software |
| JMP (version 17) | JMP Statistical Discovery LLC | JMP 17 | Statistical analysis software |
| Levington F2S seed & modular compost (with sand) | Levington | LEV75F2SMS | General-purpose compost for plant growth |
| Micromanipulator | Singer instrument Co. LTD. | Singer Micromanipulator | Micromanipulator to aid transfer of pollen grain |
| Nikon Digit sight DS-U1 | Nikon | DS-U1 | Microscope camera (coupletd to SMZ1500) |
| Nikon Eclipse TE2000-S Inverted Microscope | Nikon | TE2000-S | Inverted microscope |
| Nikon SMZ1500 Stereomicroscope | Nikon | SMZ1500 | Stereomicroscope |
| Nikon DS-Fi3 microscope camera | Nikon | DS-Fi3 | Microscope camera (coupletd to TE2000-S) |
| Nikon NIS-Elements Basic Research | Nikon | NIS-Elements BR | Image accquisition and analysis software (for DS-Fi3) |
| Nikon NIS-Elements F | Nikon | NIS-Elements F | Image accquisition and analysis software (for DS-U1) |
| WT Col-0 plant line | NASC | N700000 | Wildtype Arabidopsis thaliana, ecotype Columbia-0 |
Referências
- Rieseberg, L. H., Willis, J. H. Plant speciation. Science. 317 (5840), 910-914 (2007).
- Hiscock, S. J., Allen, A. M. Diverse cell signalling pathways regulate pollen-stigma interactions: the search for consensus. New Phytologist. 179 (2), 286-317 (2008).
- Kandasamy, M. K., Nasrallah, J. B., Nasrallah, M. E. Pollen pistil interactions and developmental regulation of pollen-tube growth in Arabidopsis. Development. 120 (12), 3405-3418 (1994).
- Bosch, M., Wang, L. Pollen-stigma interactions in Brassicaceae: complex communication events regulating pollen hydration. Journal of Experimental Botany. 71 (9), 2465-2468 (2020).
- Rozier, F., et al. Live-cell imaging of early events following pollen perception in self-incompatible Arabidopsis thaliana. Journal of Experimental Botany. 71 (9), 2513-2526 (2020).
- Dickinson, H. Dry stigmas, water and self-incompatibility in Brassica. Sexual Plant Reproduction. 8, 1-10 (1995).
- Takasaki, T., et al. The S receptor kinase determines self-incompatibility in Brassica stigma. Nature. 403 (6772), 913-916 (2000).
- Schopfer, C. R., Nasrallah, M. E., Nasrallah, J. B. The male determinant of self-incompatibility in Brassica. Science. 286 (5445), 1697-1700 (1999).
- Takayama, S., et al. Direct ligand-receptor complex interaction controls Brassica self-incompatibility. Nature. 413 (6855), 534-538 (2001).
- Shiba, H., et al. A pollen coat protein, SP11/SCR, determines the pollen S-specificity in the self-incompatibility of Brassica species. Plant Physiology. 125 (4), 2095-2103 (2001).
- Broz, A. K., Bedinger, P. A. Pollen-pistil interactions as reproductive barriers. Annual Review of Plant Biology. 72 (1), 615-639 (2021).
- Cheung, A. Y., Duan, Q., Li, C., James Liu, M. -. C., Wu, H. -. M. Pollen-pistil interactions: It takes two to tangle but a molecular cast of many to deliver. Current Opinion in Plant Biology. 69, 102279 (2022).
- Wang, L. D., et al. PCP-B class pollen coat proteins are key regulators of the hydration checkpoint in Arabidopsis thaliana pollen-stigma interactions. New Phytologist. 213 (2), 764-777 (2017).
- Liu, C., et al. Pollen PCP-B peptides unlock a stigma peptide-receptor kinase gating mechanism for pollination. Science. 372 (6538), 171-175 (2021).
- Bordeleau, S. J., Sanchez, L. E. C., Goring, D. R. Finding new Arabidopsis receptor kinases that regulate compatible pollen-pistil interactions. Frontiers in Plant Science. 13, 1022684 (2022).
- Suwabe, K., et al. Double-locking mechanism of self-compatibility in Arabidopsis thaliana: the synergistic effect of transcriptional depression and disruption of coding region in the male specificity gene. Frontiers in Plant Science. 11, 576140 (2020).
- Smyth, D. R., Bowman, J. L., Meyerowitz, E. M. Early flower development in Arabidopsis. Plant Cell. 2 (8), 755-767 (1990).
- Lee, H. K., Macgregor, S., Goring, D. R. A toolkit for teasing apart the early stages of pollen-stigma interactions in Arabidopsis thaliana. Pollen and Pollen Tube Biology. 2160, 13-28 (2020).
- Dilkes, B. P., et al. The maternally expressed WRKY transcription factor TTG2 controls lethality in interploidy crosses of Arabidopsis. PLoS Biology. 6 (12), 2707-2720 (2008).
- Riglet, L., et al. KATANIN-dependent mechanical properties of the stigmatic cell wall mediate the pollen tube path in Arabidopsis. eLife. 9, e57282 (2020).
- Zhou, L. Z., Dresselhaus, T. Friend or foe: Signaling mechanisms during double fertilization in flowering seed plants. Plant Development and Evolution. 131, 453-496 (2019).
- Gao, X. -. Q., et al. The Arabidopsis KINβγ subunit of the SnRK1 complex regulates pollen hydration on the stigma by mediating the level of reactive oxygen species in pollen. PLoS Genetics. 12 (7), e1006228 (2016).
- Lee, H. K., Goring, D. R. Two subgroups of receptor-like kinases promote early compatible pollen responses in the Arabidopsis thaliana pistil. Journal of Experimental Botany. 72 (4), 1198-1211 (2021).
- O’Malley, R. C., Barragan, C. C., Ecker, J. R. A user’s guide to the Arabidopsis T-DNA insertion mutant collections. Pollen and Pollen Tube Biology. 1284, 323-342 (2015).
- Samson, F., et al. FLAGdb++: a database for the functional analysis of the Arabidopsis genome. Nucleic Acids Research. 32, D347-D350 (2004).
- Doucet, J., et al. Investigations into a putative role for the novel BRASSIKIN pseudokinases in compatible pollen-stigma interactions in Arabidopsis thaliana. BMC Plant Biology. 19 (1), 549 (2019).

