Högkvalitativ hjärn- och benmärgskärnförberedelse för Single Nuclei Multiome-analyser
Summary
Framgången för transkriptomik med en cell/en kärna och multi-omik beror till stor del på kvaliteten på celler/kärnor. Därför måste isolering av celler/kärnor från vävnad och rening av dem vara mycket standardiserad. Detta protokoll beskriver beredningen av kärnor från hjärnan och benmärgen för nedströms single-nuclei multiome-analys.
Abstract
Encellsanalys har blivit det bästa tillvägagångssättet för att reda ut komplexiteten i biologiska processer som kräver att man bedömer variabiliteten hos individuella cellulära svar på behandling eller infektion med encellsupplösning.
Många tekniker för molekylär profilering av enskilda celler har utvecklats under de senaste 10 åren, och flera dedikerade tekniker har kommersialiserats. 10X Genomics droppbaserad encellsprofilering är en utbredd teknik som erbjuder färdiga reagenser för transkriptomisk och multi-omisk encellsprofilering. Tekniken inkluderar arbetsflöden för encells- och enkelkärns-RNA-sekvensering (scRNA-Seq respektive snRNA-Seq), scATAC-Seq, encellsimmunprofilering (BCR/TCR-sekvensering) och multiome. Den senare kombinerar transkriptionell (scRNA-Seq) och epigenetisk information (scATAC-Seq) som kommer från samma cell.
Kvaliteten (viabilitet, integritet, renhet) hos encells- eller enkärnssuspensioner som isolerats från vävnader och analyserats med någon av dessa metoder är avgörande för att generera data av hög kvalitet. Protokollen för provberedning bör därför anpassas till varje biologisk vävnads särdrag och säkerställa att cell- och kärnsuspensioner av hög kvalitet genereras.
I den här artikeln beskrivs två protokoll för att förbereda hjärn- och benmärgsprover för den underordnade multiome 10X Genomics-pipelinen. Protokollen utförs stegvis och omfattar vävnadsdissociation, cellsortering, cellkärnisolering och kvalitetskontroll av preparerad cellkärnesuspension som används som utgångsmaterial för cellpartitionering och streckkodning, biblioteksberedning och sekvensering. Dessa standardiserade protokoll producerar högkvalitativa kärnbibliotek och robusta och tillförlitliga data.
Introduction
Under många år har encellstekniker varit guldstandarden för analys av biologiska processer. De var till en början begränsade till fenotypning av enskilda celler genom mikroskopi, flödescytometri och liknande analyser. Ett genombrott inom encellsanalys kom med utvecklingen av metoder för molekylär profilering av enskilda celler, i synnerhet encells-RNA-sekvensering (scRNA-Seq) som möjliggjorde karakterisering av hela transkriptomet hos enskilda celler. ScRNA-Seq är mycket kraftfull och genererar information om transkriptionsstatusen för en cell i ett specifikt tillstånd och vid en viss tidpunkt. Det ger dock ingen insyn i den genreglering som driver transkriptionen, eller i de molekylära modifieringar som sker över tid. För att övervinna denna begränsning har många ansträngningar investerats i utvecklingen av encells-multi-omics-analyser som möjliggör analys av flera faktorer och processer från samma cell 1,2,3,4. Den första framgångsrika mätningen av två modaliteter inom enskilda celler kom genom att länka multiplexa ytproteinuttrycksmönster med det fullständiga transkriptomet av enskilda celler i CITE-Seq-metoden5. Nyare evolutioner kombinerar genuttryck med kromatintillgänglighet (Assay for Transposase-Accessible Chromatin using sequencing, ATAC-Seq), och fångar därmed samtidigt transkriptomiska och epigenomiska modaliteter i samma celler (t.ex. sci-CAR)6. De första kommersiella lösningarna som gjorde det möjligt att associera transkriptomik med cellfenotyp eller med epigenetiska förändringar i samma cell kom från 10X Genomics.
Experiment för molekylär profilering av enskilda celler omfattar följande steg: 1) dissociation av vävnad eller beredning av encellssuspensioner, 2. Cellrening och/eller isolering av kärnor. (3) partitionering och streckkodning; (4) bibliotekskonstruktion och kvalitetskontroll; (5) Nästa generations sekvensering. (6) Analys av data. Även om steg (3)-(6) kan variera avsevärt beroende på vilken teknik som används, är de inledande stegen i allmänhet gemensamma för dem alla. Kvaliteten på den beredda cell/kärnsuspensionen kommer att avgöra det övergripande resultatet av experimentet. Beroende på typ av vävnad kan det vara svårt att få fram högkvalitativa encells-/kärnsuspensioner. Särdragen hos vissa vävnader, såsom hjärta, muskler, hjärna, lungor, tarmar och andra, kräver metoder för vävnadsstörning och isolering av kärnor som är anpassade till varje typ av prov för att garantera produktion av kärnor av hög kvalitet för molekylär analys 7,8,9,10 . Vävnadsstörningsmetoderna och dissociationsprotokollen kan vara mekaniska, enzymatiska (t.ex. en blandning av kollagenaser och DNase), eller en kombination av de två, och kan utföras manuellt eller med instrument (t.ex. Qiagen DSC-400, gentleMACS).
Encellstekniker har blivit ett populärt verktyg för biomedicinsk forskning. Inom neurobiologin kräver celldiversiteten i hjärnan och komplexiteten i deras funktioner högupplöst analys med hög genomströmning för visualisering av sällsynta cellpopulationer och för att bedöma deras heterogenitet 11,12,13,14. Att koppla samman cellulär identitet och genregleringsmekanismer i enskilda celler ger insikter i hjärnans utveckling och fysiologi. Ett annat exempel är studier av immunsvar i samband med infektions-, autoimmuna eller cancersjukdomar, som är starkt beroende av encellsanalyser. Heterogeniteten hos immuncellernas undergrupper och komplexiteten i deras aktivitet och interaktioner med andra celltyper kräver encellsupplösning för att dechiffrera de mekanismer som ligger till grund för immunsvaret. Immuncellerna härstammar från benmärgen, där hematopoetiska stamceller består av gradvis differentierande celler som förvärvar och förlorar cellytemarkörer genom en stegvis process innan de lämnar benmärgen för att ta sig hem i periferin. Encellsanalys möjliggör minutiös karakterisering av cellulära utvecklingsstadier. Det kan uppnås genom fenotypning av en cell, som konventionellt utförs med flödescytometri med flera parametrar. Transkriptomiska signaturer i enskilda celler har dock visat sig avslöja en mer exakt identifiering av subtyper av stamceller eftersom dessa celler är fördelade i kluster som faller in i varandra och därför kan felidentifieras när man använder en grov cellytemarkör15. Ett ökande antal studier avslöjar de epigenetiska modifieringar som hematopoetiska stam- och stamceller (HSPC) kan förvärva från exponering för olika medel, vilket leder till en betydande inverkan på immunsystemets långsiktiga respons 16,17,18,19. De nya multi-omics-teknikerna gör det möjligt att studera dessa processer med encellsupplösning.
Många protokoll för cell- och kärnisolering har beskrivits för hjärna 11,20,21,22 och benmärgsprover23,24. För att minimera bias på grund av experimentell variabilitet är det nödvändigt att validera optimerade protokoll för beredning av enskilda kärnor för gemensam transkriptomisk och epigenomisk sekvensering av enskilda celler, och därigenom säkerställa reproducerbarheten av encellsmultiomiska analyser.
Här beskrivs två robusta protokoll för kärnpreparering från (1) färskfryst hjärnvävnad och (2) färsk benmärg HSPC för nedströms encellig Multiome-analys (Figur 1).
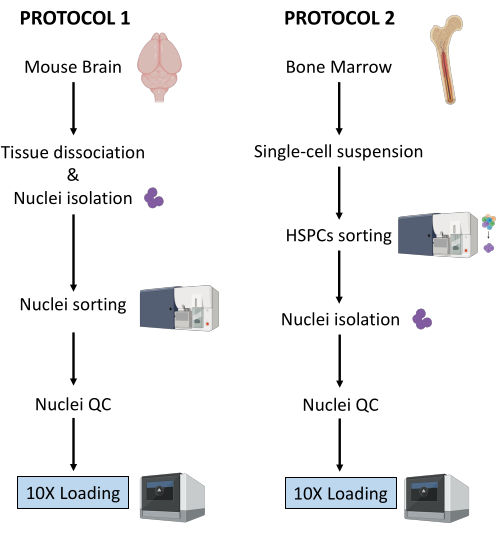
Figur 1: Schematisk representation av protokoll för isolering av kärnor från färskfrysta hjärn- och benmärgsvävnader. Klicka här för att se en större version av denna figur.
Protocol
Representative Results
Discussion
Beredning av högkvalitativ cell- eller kärnsuspension är av avgörande betydelse för framgången för encells- eller enkärns-RNA-Seq- och encellsmulti-omic-analyser 29,30,31. Här har vi beskrivit protokoll för provberedning och cellkärneisolering för multiomanalyser från två typer av vävnad: hjärna och benmärg.
Hjärnprotokollet som beskrivs i detta dokument gör det möjligt att återvinna kärnor av hög kvalitet från färskfryst hjärnvävnad. Den innehåller följande steg: fryst vävnadsstörning, isolering av kärnor, rening av kärnor och kvalitetskontroll av det beredda materialet. Hjärnvävnaden består av många olika celltyper, och proceduren för vävnadsdissociation och isolering av kärnor bör bevara de proportioner av cellpopulationer som finns i den ursprungliga vävnaden. Här optimerades lysbuffertens sammansättning och inkubationstid för att möjliggöra fullständig och skonsam lys av alla cellpopulationer som utgör vävnaden.
Benmärgens HSPC-protokoll är något annorlunda eftersom det krävs ytterligare ett steg i början av experimentet för att isolera den aktuella cellpopulationen från en heterogen cellulär suspension. Efter insamling av färsk vävnad lyseras röda blodkroppar och provet anrikas för den cellundergrupp som är av intresse. Målcellerna lyseras, kärnorna isoleras och kvaliteten på det beredda materialet kontrolleras.
10X Genomics tillhandahåller flera protokoll som validerats för cellkärneisolering i många olika vävnader32,33. Bolaget kommersialiserar också ett kärnisoleringskit med en enkel pipeline för att isolera kärnor från validerade vävnader34. Dessa protokoll behöver dock ytterligare optimering för att skräddarsy särdragen hos vissa prover. Ett exempel är de exempel som kräver att du arbetar med låg cellindata. För dessa prover är de mest utmanande stegen centrifugeringar som måste vara tillräckligt stränga för att rengöra provet och tillräckligt skonsamma för att undvika cell-/kärnförlust. Med det protokoll som beskrivs här har vi anpassat 10X Genomics Shown Protocol – Nuclei Isolation for Single Cell Multiome ATAC + GEX Sequencing (CG000365 – Rev C)27 för att hitta en fin balans mellan dessa två krav. Som visas i exemplet med beredning av kärnor från sorterade HSPC:er har vi förbättrat kärnåtervinningen utan att provets kvalitet påverkas.
En ytterligare utmaning är steget med lys av renade celler för cellkärnisolering. Hårdare lysförhållanden och längre inkubationstider kan skada kärnor och därmed påverka kvaliteten på sekvenseringsdata. Figur 5 visar representativ avbildning av kärnor från benmärgsprover vid olika inkubationstider med lysbuffert och illustrerar hur olika cellkärnornas tillstånd kan vara beroende på celllysen. I exemplet med HSPC:erna har vi identifierat 3 minuters lys som det tillstånd som resulterar i den högsta andelen friska, intakta kärnor och den lägsta andelen skadade kärnor. Inkubationstiderna för lys bör optimeras för varje ny typ av prov.
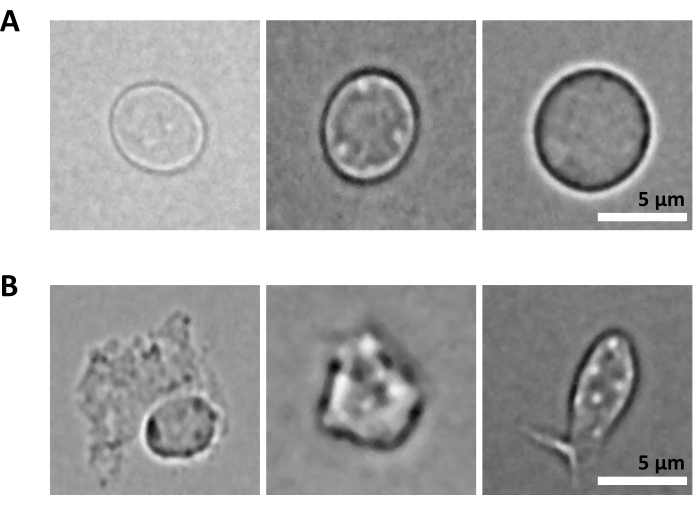
Figur 5: Kvalitetskontroll av kärnor med mikroskopi. Bilden visar representativa ljusfältsbilder av isolerade kärnor från benmärg hos möss med (A) intakta och (B) skadade kärnor. Skalstreck 5 μm. Bilderna togs med ett inverterat mikroskop med ett 40x ELWD NA 0,60 objektiv och 1,5x digital zoom. Klicka här för att se en större version av denna figur.
Båda protokollen som beskrivs i detta arbete bygger på att man renar målceller eller kärnor med hjälp av FACS-instrument med hög kapacitet. Detta steg är av avgörande betydelse för protokoll för framställning av encelliga/kärnor där sällsynta undergrupper av celler ska isoleras från heterogena suspensioner. I dessa, som i exemplet som visas här för HSPC-sortering, kan en högdimensionell flödescytometripanel krävas för att möjliggöra “gating” på den cellpopulation som är av intresse. Sorteringen är extremt snabb och exakt, vilket leder till över 95 % renhet hos de sorterade celldelmängderna. Detta tillvägagångssätt utsätter den cellulära suspensionen för ett tryck på upp till 70 psi och kan därför vara begränsande för sortering av ömtåliga celler (t.ex. dendritiska celler, neutrofiler) eftersom det kan orsaka bristning av deras cellmembran. I dessa fall bör alternativa lösningar väljas för cellulär rening, inklusive magnetisk sortering, tillämpning av den nya generationens instrument (t.ex. CellenOne, Cellenion; MACSQuant Tyto, Miltenyi)35,36, eller droppbaserade system (t.ex. ODIN, Sensific)37. Icke desto mindre är den långsamma sorteringshastigheten hos dessa tekniker, med cellsortering som varar i timmar istället för minuter, en starkt begränsande faktor för tillämpningen av dessa metoder vid framställning av livskraftiga celler för Multiome och andra encellsapplikationer baserade på analys av stora cellantal.
För rening av kärnor isolerade från vävnaden är FACS den bästa metoden på grund av dess genomströmning och renheten hos det isolerade materialet. Kärnor är inte känsliga för tryck, och filtrerade vävnadsisolat kan enkelt renas genom cellsorteraren. Om laboratoriet inte är utrustat med ett FACS-instrument finns andra alternativ, något mindre effektiva men tillräckligt bra. Exempel på detta är ultracentrifugering eller användning av liten utrustning som MARS (Applied Cell) som separerar partiklar baserat på deras skillnad i storlek, med hjälp av akustiska vågor; CURIOX laminär bricka som använder hydrofoba egenskaper hos cell-/kärnsuspensioner; eller LEVITAS bio som förlitar sig på cellernas fysiska egenskaper (levitation) för att separera dem från skräpet.
Här beskriver vi protokoll för att erhålla ett stort antal kärnor och den bästa renheten för nedströms Multiome-protokollet. FACS-sortering och upprepade centrifugeringssteg resulterar i en betydande förlust av det ursprungliga materialet. Av denna anledning kräver protokollet för kärnpreparering från hjärnan som vi beskriver här tillräckligt rikligt med utgångsmaterial för att resultera i insamling av minst 500 000 kärnor efter FACS-sorteringen. Alternativa protokoll bör användas om detta kriterium inte kan uppfyllas. När man arbetar med sällsynta cellpopulationer eller små vävnadssnitt kan den tillgängliga mängden utgångsmaterial vara en begränsande faktor. För att ta itu med detta problem är det möjligt att förbättra kärnåtervinningen genom att (a) minska lysvolymen, (b) minska tvättvolymen, (c) använda en enda tvätt med förlängd centrifugeringstid för att försöka förbättra återhämtningen enligt 10X Genomics-protokoll för isolering av kärnor med låg cellingång. För multiomisk analys av material med lågt innehåll är det värt att överväga plattbaserade applikationer som scNMT, SNARE-seq och Paired-seq38 som kräver mycket färre indataprover.
Sammanfattningsvis har vi beskrivit två robusta protokoll för beredning av kärnor från hjärnan och benmärgens HSPC för nedströms Multiome-analys. Dessa protokoll är tillämpliga i alla vetenskapliga projekt som kräver högkvalitativa suspensioner av enskilda kärnor från dessa två typer av vävnad, oavsett vilken vetenskaplig fråga som ställs. Vår grupp har tillämpat protokollet för isolering av hjärnkärnor i studier av hjärnans utveckling vid inaktivering av olika målgener och i studier av immunsvar i samband med neurologiska sjukdomar. Vi använder protokollet för isolering av benmärgskärnor för att dechiffrera deltagandet av olika hematopoetiska subpopulationer i etableringen av immunsystemet.
Declarações
The authors have nothing to disclose.
Acknowledgements
Ana Jeemin Choi fick stöd av ett stipendium från Pasteur – Paris University (PPU) International Ph.D. Program.
Materials
| 18 G x 1 ½ (1.2 mm x 38 mm) Agani needles | Terumo | AN*1838S1 | |
| 15 mL tubes | Falcon | 352097 | |
| 5 mL round bottom FACS tube with cell strainer cap 35 µm | falcon | 352235 | |
| 50 mL tubes | Falcon | 352070 | |
| 7-AAD | BD pharmagen | 559925 | |
| ACK Lysing Buffer | Gibco | A10492-01 | |
| APC anti-mouse CD117 (c-Kit) | BioLegend | 105812 | Clone: 2B8 |
| APC/Cyanine 7 anti-mouse CD16/32 (FcγR) | BioLegend | 101328 | Clone: 93 |
| BD FACSAria III | BD Biosciences | non-applicable | |
| BD FACSDiva Software v8.0.1 | BD Biosciences | non-applicable | |
| Bovine Serum Albumin stock solution 10% | Miltenyi Biotec | 130-091-376 | |
| Cell staining buffer | Biolegend | 420201 | |
| CFI Suprplan Fluor ELWD 40XC ON 0.6 | Nikon | non-applicable | |
| CMOS camera Prime 95B 25 mm | Photometrix | non-applicable | |
| Countess II FL Automated Cell Counter | Invitrogen | AMQAF1000 | |
| Countess cell counting chamber slide | Invitrogen | C10283 | |
| Coverglass 24 mm x 24 mm 0.13-0.17 mm | Brand | BR470819 | |
| Digitonine 5% | Invitrogen | BN2006 | |
| Disposable Scalpels | Swann-Morton | 0508 | |
| DMEM (1x) + GlutaMAX-I | Gibco | 31966-021 | |
| DPBS (10x) | Gibco | 14200-067 | |
| DTT | Sigma aldrich | 646563 | |
| Epifluorescence inverted microscope Nikon Ti2 -E | Nikon | non-applicable | |
| Eppendorf Safe-Lock Tubes 0.5 mL | Eppendorf | 30123603 | |
| Ethanol 70% | VWR | 83801.290 | |
| FITC anti-mouse CD34 | Invitrogen | 11-0341-85 | Clone: RAM34 |
| Forceps for dissection | FST | 11152-10 | |
| Heat-inactivated Fetal Bovine Serum (FBS) | Gibco | 11533387 | |
| Dounce Homogeniser 2 mL | Bellco glass | 1984-10002 | Pestle “A” Large Clearance: .0030-.0050″ and Pestle “B” Small Clearance: .0005-.0025″ |
| LIVE/DEAD fixable aqua dead cell stain kit | Invitrogen | L34957 | |
| Magnesium chloride solution 1 M | Sigma aldrich | M1028 | |
| Microcentrifuge | Eppendorf | 5424R | |
| Mounting medium Fluoromount-G | invitrogen | 00-4958-02 | |
| Nonidet P40 substitute | Sigma aldrich | 74385 | |
| Nuclease free water | ThermoFischer | AM9932 | |
| Nuclei buffer 20x | 10X Genomics | 2000153/2000207 | |
| Nuclei isolation kit EZ prep | Sigma Aldrich | NUC-101 | |
| OneComp eBeads compensation beads | Invitrogen | 01-1111-41 | |
| Pacific Blue anti-mouse lineage cocktail (including anti-mouse CD3, Ly-6G/Ly-6C, CD11b, CD45R/B220, TER-119) |
BioLegend | 133310 | Clones (in the same order as the antibodies listed): 17A2, RB6-8C5, M1/70, RA3-6B2, Ter-119 |
| PCR Tube Strips 0.2 mL | Eppendorf | 951010022 | |
| PE anti-mouse Ly-6A/E (Sca-1) | BioLegend | 122507 | Clone: E13-161.7 |
| Petri dish 100 mm x 20 mm OPTILUX | Falcon | 353003 | |
| Ply-L-lysine 0.01% sterile-filtered suitable for cell culture | Sigma | P4707 | |
| Printed microscope slides 8 well 6 mm numbered | Epredia | ER-301B-CE24 | |
| Protein LoBind Tubes 1.5 mL | Eppendorf | 30108116 | |
| Recombinant Rnase inhibitor 5000 U | Takara | 2313A | |
| Scissors for dissection | FST | 14090-09 | |
| Sodium chloride solution 5 M | Sigma aldrich | 59222C | |
| Syringe filters, PES, 0.2 µm | Fisher Scientific | 15206869 | |
| Transparent nail polish | any | non-applicable | |
| Trizma Hydrochloride solution pH 7.4 | Sigma aldrich | T2194 | |
| Trypan Blue 0.4% | gibco | 15250061 | |
| Tween 20 | Biorad | 1662404 | |
| UltraPure Distilated Water Dnase/Rnase Free | Invitrogen | 10977-035 |
Referências
- Clark, S. J., et al. scNMT-seq enables joint profiling of chromatin accessibility DNA methylation and transcription in single cells. Nature Communications. 9 (1), 781 (2018).
- Lee, J., Hyeon, D. Y., Hwang, D. Single-cell multiomics: technologies and data analysis methods. Experimental & Molecular Medicine. 52 (9), 1428-1442 (2020).
- Cerrizuela, S., et al. High-throughput scNMT protocol for multiomics profiling of single cells from mouse brain and pancreatic organoids. STAR Protocols. 3 (3), 101555 (2022).
- Dimitriu, M. A., Lazar-Contes, I., Roszkowski, M., Mansuy, I. M. Single-cell multiomics techniques: From conception to applications. Frontiers in Cell and Developmental Biology. 10, 854317 (2022).
- Stoeckius, M., et al. Simultaneous epitope and transcriptome measurement in single cells. Nature Methods. 14 (9), 865-868 (2017).
- Cao, J., et al. . Joint profiling of chromatin accessibility and gene expression in thousands of single cells. 361 (6409), 1380-1385 (2018).
- Narayanan, A., et al. Nuclei Isolation from Fresh Frozen Brain Tumors for Single-Nucleus RNA-seq and ATAC-seq.Journal of Visualized Experiments. JoVE. 162, 61542 (2020).
- Kim, M., et al. Single-nucleus transcriptomics reveals functional compartmentalization in syncytial skeletal muscle cells. Nature Communications. 11 (1), 6375 (2020).
- Santos, M. D., et al. Extraction and sequencing of single nuclei from murine skeletal muscles. STAR Protocols. 2 (3), 100694 (2021).
- Safabakhsh, S., et al. Isolating nuclei from frozen human heart tissue for single-nucleus RNA sequencing. Current Protocols. 2 (7), (2022).
- Lau, S. -. F., Cao, H., Fu, A. K. Y., Ip, N. Y. Single-nucleus transcriptome analysis reveals dysregulation of angiogenic endothelial cells and neuroprotective glia in Alzheimer’s disease. Proceedings of the National Academy of Sciences of the United States of America. 117 (41), 25800-25809 (2020).
- Armand, E. J., Li, J., Xie, F., Luo, C., Mukamel, E. A. Single-cell sequencing of brain cell transcriptomes and epigenomes. Neuron. 109 (1), 11-26 (2021).
- Morabito, S., et al. Single-nucleus chromatin accessibility and transcriptomic characterization of Alzheimer’s disease. Nature Genetics. 53 (8), 1143-1155 (2021).
- Chen, S., et al. Spatially resolved transcriptomics reveals genes associated with the vulnerability of middle temporal gyrus in Alzheimer’s disease. Acta Neuropathologica Communications. 10 (1), (2022).
- Paul, F., et al. Transcriptional heterogeneity and lineage commitment in myeloid progenitors. Cell. 163 (7), 1663-1677 (2015).
- Kaufmann, E., et al. BCG educates hematopoietic stem cells to generate protective innate immunity against tuberculosis. Cell. 172 (1-2), 176-190 (2018).
- Christ, A., et al. diet triggers NLRP3-dependent innate immune reprogramming. Cell. 172 (1-2), 162-175 (2018).
- Moorlag, S. J. C. F. M., et al. β-Glucan Induces protective trained immunity against mycobacterium tuberculosis infection: A key role for IL-1. Cell Reports. 31 (7), 107634 (2020).
- de Laval, B., et al. C/EBPβ-dependent epigenetic memory induces trained immunity in hematopoietic stem cells. Cell Stem Cell. 26 (5), 657-674 (2020).
- Renthal, W., et al. Characterization of human mosaic Rett syndrome brain tissue by single-nucleus RNA sequencing. Nature Neuroscience. 21 (12), 1670-1679 (2018).
- Yang, A. C., et al. A human brain vascular atlas reveals diverse mediators of Alzheimer’s risk. Nature. 603 (7903), 885-892 (2022).
- Lee, D. R., Zhang, Y., Rhodes, C. T., Petros, T. J. Generation of single-cell and single-nuclei suspensions from embryonic and adult mouse brains. STAR Protocols. 4 (1), 101944 (2022).
- Corces, M. R., et al. Lineage-specific and single-cell chromatin accessibility charts human hematopoiesis and leukemia evolution. Nature Genetics. 48 (10), 1193-1203 (2016).
- Ranzoni, A. M., et al. Integrative single-cell RNA-seq and ATAC-seq analysis of human developmental hematopoiesis. Cell Stem Cell. 28 (3), 472-487 (2021).
- . 10X Genomics Chromium Next GEM Single Cell Multiome ATAC + Gene Expression User Guide. Document Number CG000338 Rev F. At. , (2022).
- J, , et al. Microdissection of mouse brain into functionally and anatomically different regions. Journal of Visualized Experiments: JoVE. 168, 61941 (2021).
- . . 10X Genomics 10X Genomics Demonstrated Protocol – Nuclei Isolation for Single Cell Multiome ATAC + GEX sequencing (CG000365 – Rev C). At. , (2022).
- Haag, S., Murthy, A. Murine monocyte and macrophage culture. Bio-Protocol. 11 (6), (2021).
- Haque, A., Engel, J., Teichmann, S. A., Lönnberg, T. A practical guide to single-cell RNA-sequencing for biomedical research and clinical applications. Genome Medicine. 9 (1), (2017).
- Jiang, P. Quality control of single-cell RNA-seq. Methods in Molecular Biology. , 1-9 (1935).
- Regan, C., Preall, J. Practical considerations for single-cell genomics. Current Protocols. 2 (8), (2022).
- . . 10X Genomics 10X Genomics Demonstrated Protocol – Nuclei Isolation for Single Cell ATAC Sequencing (CG000169 – Rev E). At. , (2022).
- . 10X Genomics 10X Genomics Demonstrated Protocol – Nuclei Isolation from Complex Tissues for Single Cell Multiome. ATAC + Gene Expression Sequencing. (CG000375 – Rev C). At. , (2022).
- . . 10X Genomics 10X Genomics – Chromium Nuclei Isolation Kit (CG000505 – Rev A). AT. , (2022).
- Shomroni, O., et al. A novel single-cell RNA-sequencing approach and its applicability connecting genotype to phenotype in ageing disease. Scientific Reports. 12 (1), 4091 (2022).
- Ocañas, S. R., Pham, K. D., Blankenship, H. E., Machalinski, A. H., Chucair-Elliott, A. J., Freeman, W. M. Minimizing the ex vivo confounds of cell-isolation techniques on transcriptomic and translatomic profiles of purified microglia. 9 (2), 0348-0321 (2022).
- Gérard, A., et al. High-throughput single-cell activity-based screening and sequencing of antibodies using droplet microfluidics. Nature Biotechnology. 38 (6), 715-721 (2020).
- Vandereyken, K., Sifrim, A., Thienpont, B., Voet, T. Methods and applications for single-cell and spatial multi-omics. Nature Reviews. Genetics. 24, 494-515 (2023).

