Analys av proteinkomplexbildning vid mikromolära koncentrationer genom att koppla mikrofluidik med massfotometri
Summary
Detta protokoll kombinerar massfotometri med ett nytt mikrofluidiksystem för att undersöka protein-proteininteraktioner med låg affinitet. Detta tillvägagångssätt är baserat på snabb utspädning av högkoncentrerade komplex i lösning, vilket möjliggör mätningar med låg affinitet och breddar användbarheten av massfotometri.
Abstract
Massfotometri är en mångsidig massmätningsteknik som gör det möjligt att studera biomolekylära interaktioner och komplex bildning i lösning utan etiketter. Massfotometri är i allmänhet lämpad för att analysera prover i koncentrationsområdet 100 pM-100 nM. I många biologiska system är det dock nödvändigt att mäta mer koncentrerade prover för att studera lågaffinitet eller transienta interaktioner. Här demonstrerar vi en metod som effektivt utökar intervallet av provkoncentrationer som kan analyseras med massfotometri från nanomolar till tiotals mikromolar.
I detta protokoll kombineras massfotometri med ett nytt mikrofluidiksystem för att undersöka bildandet av proteinkomplex i lösning i det mikromolära koncentrationsområdet. Med mikrofluidiksystemet kan användare hålla ett prov vid en önskad högre koncentration följt av utspädning till det nanomolära området – flera millisekunder före massfotometrimätningen. På grund av utspädningshastigheten erhålls data innan provets jämvikt har förskjutits (dvs. komplexet dissocierar).
Tekniken används för att mäta interaktioner mellan en immunglobulin G (IgG) antikropp och den neonatala Fc-receptorn, vilket visar bildandet av högordningskomplex som inte var kvantifierbara med statiska massfotometrimätningar.
Sammanfattningsvis gör kombinationen av massfotometri och mikrofluidik det möjligt att karakterisera prover i det mikromolära koncentrationsområdet och är skicklig på att mäta biomolekylära interaktioner med svagare affiniteter. Dessa förmågor kan tillämpas i en rad olika sammanhang – inklusive utveckling och design av bioterapier – vilket möjliggör grundlig karakterisering av olika protein-proteininteraktioner.
Introduction
Protein-proteininteraktioner understryker de flesta cellulära funktioner, från immunreglering till DNA-replikation och translation. Som ett resultat av detta finns det ett grundläggande behov inom livsvetenskaperna att undersöka ett brett spektrum av interaktioner mellan olika heterogena komplex som ofta bildas. Deras detektering, karakterisering och kvantifiering är dock ofta utmanande, särskilt för interaktioner med låg affinitet1.
Immunoprecipitationsanalyser används ofta för att detektera interaktioner med hög affinitet, men för interaktioner med låg affinitet och transienta interaktioner är detektion i stort sett ogenomförbar2. Fluorescenstekniker kan också användas men kräver potentiellt störande tillsats av fluorescerande etiketter2. Cryo-EM kan ge en strukturell ögonblicksbild och en ensembleavläsning av de proteinkomplex som bildats med hög rumslig upplösning, men kräver också vanligtvis att man arbetar med koncentrationer som är för låga för avbildning av interaktioner med låg affinitet. Cryo-EM medför också utmaningar relaterade till kostnad, tillgänglighet, provberedning och analystid3.
Dessutom har ytplasmonresonans (SPR) blivit ett populärt sätt att kvantifiera protein-proteininteraktioner, även om det kräver proteinimmobilisering, vilket kan påverka bindningsjämvikten och resultera i variabla on-hastigheter, vilket minskar mätnoggrannheten 4,5. Det involverar också flera analyssteg före datainsamling och analys6.
Massfotometri är en teknik med en enda molekyl som har använts för att analysera protein-proteininteraktioner 5,6,7. Det fungerar genom att mäta massan av enskilda molekyler eller komplex baserat på ljuset de sprider när de landar på ytan av ett glastäcke8. Massfotometrimätningar har använts för att kvantifiera bindningsaffiniteter från den relativa förekomsten av bindningspartners och de komplex de bildar5. I likhet med andra metoder med en enda molekyl bör dock koncentrationen i det prov som ska mätas vanligtvis vara mindre än 100 nM. Om koncentrationen är högre kommer molekylerna som landar på glasytan att överlappa varandra rumsligt, vilket resulterar i dålig datakvalitet7. Följaktligen kan svagare interaktioner (KD ~mikromolarer), som dissocierar vid dessa lägre koncentrationer, inte mätas på ett tillförlitligt sätt eftersom det inte är möjligt att observera den nödvändiga blandningen av obundna och bundna arter5.
Här beskriver vi ett tillvägagångssätt som övervinner denna begränsning baserat på en ny kopplad mikrofluidik-massfotometrienhet. Specifikt används ett mikrofluidiksystem i kombination med massfotometern för att effektivt utöka utbudet av interaktioner som kan kvantifieras med massfotometri. Mikrofluidik har visat sig erbjuda en rad möjligheter för att undersöka protein-proteininteraktioner, inklusive snabb utspädning för att upptäcka svaga interaktioner 1,9. Systemet som beskrivs här fungerar genom att snabbt späda ut provet upp till 10 000 gånger på ett mikrofluidiskt chip och omedelbart flöda det över chipets observationsområde, vilket gör det möjligt för massfotometrimätningen att starta inom 50 ms från det att molekylerna påbörjade utspädningsprocessen10. Utspädningen sker när provet och bufferten kombineras i en omvänd Tesla-ventilblandare på chipet, där de relativa flödeshastigheterna för de två lösningarna bestämmer hur mycket utspädning som sker (se protokollsteg 8). Flödeshastigheten kan styras med programvaran för mikrofluidisk styrning. Att ändra flödeshastigheten kan ändra den relativa populationen av arten eftersom det kan påverka antalet landningshändelser på glasets yta, vilket är det som mäts av massfotometern.
Processens hastighet är tillräckligt snabb för att mätningen ska hinna slutföras innan interaktionens integritet har störts (för mer information, se även diskussionen). Detta kan förstås genom en kort titt på teorin om första ordningens reaktioner, där 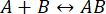 . Den framåtriktade (associations-) hastighetskonstanten är kf, den bakåtriktade (dissociation) hastighetskonstanten är kb och jämviktsdissociationskonstanten (KD) definieras som
. Den framåtriktade (associations-) hastighetskonstanten är kf, den bakåtriktade (dissociation) hastighetskonstanten är kb och jämviktsdissociationskonstanten (KD) definieras som
KD= kb/ kf
För proteinbindning begränsas kfi allmänhet av reaktanternas diffusion11 och är därför begränsad till intervallet 106-10 7 M-1·s-1. Eftersom intervallet för är begränsat kommer en reaktion med låg affinitet (KD~mikromolarer) att ha kb≈ 1 s-1. Det vill säga, kb= kf · KD= (106 M-1·s-1) (10-6 M) = 1 s-1, med komplexets halveringstid runt 0,7 s11,12.
Vårt exempelsystem är bindningen av den monoklonala IgG-antikroppen trastuzumab till den lösliga domänen av den neonatala Fc-receptorn IgG (FcRn), som är kända interagerande partners13. Tidigare publicerade data erhållna med enbart konventionell massfotometri (dvs. med manuell utspädning av prover) visade att proteinerna bildar flera arter. FcRn-monomerer, FcRn-dimerer och obundet IgG var tydligt synliga, medan IgG-FcRn-komplex (vid förhållandena 1:1 och 1:2) också detekterades (vid pH 5,0) men endast med mycket låg förekomst5. Denna observation föranleder frågan om huruvida bildning av IgG-FcRn-komplex kan detekteras tydligare om det mäts vid en högre koncentration. Kombinationen av massfotometri med en kopplad metod för snabb utspädning som beskrivs här gav mer robusta bevis för komplex bildning genom en ökning av deras uppmätta partiklar.
Massfotometri- och mikrofluidikprotokollet som beskrivs här gör det möjligt att karakterisera bildandet av komplex med en KD upp till mikromolområdet. En empirisk bestämning av KD kommer att kräva ytterligare förbättringar av flödessensorns noggrannhet, pumpstabilitet, chip-till-chip-variationer och mätplats inuti observationsfönstret, eftersom alla dessa faktorer skulle påverka tiden från det att provet späds ut till att det mäts.
Samma tillvägagångssätt kan användas för att undersöka bindningen mellan alla lösliga proteiner, förutsatt att de har distinkta molekylvikter (separerade med minst 25 kDa) som faller inom det intervall som är lämpligt för analys med en massfotometer (30 kDa till 6 MDa). De erhållna insikterna kan vara till hjälp för studier i en rad olika sammanhang – från att få en mekanistisk förståelse av cellulära funktioner till design av nya bioterapeutiska läkemedel.
Protocol
Representative Results
Discussion
Protokollet som beskrivs här tillhandahåller en metod för att detektera och kvantifiera protein-proteininteraktioner med låg affinitet. Den använder en massfotometer kopplad till ett mikrofluidiksystem med snabb utspädning. Massfotometri är ett märkningsfritt, bioanalytiskt verktyg som på ett tillförlitligt sätt kan mäta molekylmassa i lösning för biomolekyler16, för dem inom intervallet 30 kDa till 6 MDa. Eftersom massfotometri är en teknik med en enda molekyl som analyserar prover en efter en, är den i allmänhet begränsad till prover i koncentrationsintervallet 100 pM-100 nM. Över detta intervall kommer molekylerna som landar på glasytan att överlappa varandra rumsligt, vilket resulterar i dålig datakvalitet; Under detta intervall erhålls för lite data för att göra en robust analys7. En viktig konsekvens är att det kan begränsa undersökningen av proteininteraktioner till de som bildar en blandning av bundna och obundna arter inom det intervallet.
Här beskrev vi ett steg-för-steg-protokoll för att använda ett mikrofluidiksystem med snabb utspädning för att effektivt utöka intervallet av provkoncentrationer som är mottagliga för massfotometri. Genom att späda ut provet på det mikrofluidiska chipet och sedan flöda det över detektorns observationsfönster inom 50 ms, fångar systemet upp de komplex som finns i det outspädda provet innan interaktionsjämvikten förskjuts. Provet levereras kontinuerligt till detektorn under enskilda mätningar. Under dessa förhållanden kommer 95 % av komplexet att förbli intakt när provet mäts, även för interaktioner med låg affinitet – med en KD i storleksordningen mikromolarer och dissociationshastigheter så snabbt som 1 s-1.
Detta kan beräknas enligt följande: För en reaktion 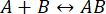 med en framåthastighet kfoch en bakåtriktad hastighet kb,
med en framåthastighet kfoch en bakåtriktad hastighet kb,
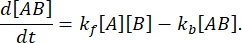
Vid jämvikt förblir koncentrationerna av alla tre arterna (A, B och komplexet AB) konstanta, så 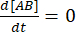 och
och 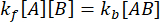 . Under det konservativa antagandet att störningen (utspädningen, i detta fall) kan få komplexet att dissociera, men den framåtriktade (associations) reaktionen inte fortsätter, kan termen kf [A] [B] behandlas som försumbar, och följande förenkling kan göras:
. Under det konservativa antagandet att störningen (utspädningen, i detta fall) kan få komplexet att dissociera, men den framåtriktade (associations) reaktionen inte fortsätter, kan termen kf [A] [B] behandlas som försumbar, och följande förenkling kan göras:
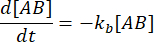
Integrering ger följande uttryck för koncentrationen av komplex vid tidpunkten efter störningen av jämvikten:
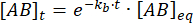
Den del av komplexet som förblir bunden vid tidpunkten t efter störningen av jämvikten är således:
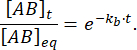
Vid = 50 ms, för en reaktion med kb≈ 1 s-1, är den fraktionsbundna 0,95, eller 95%11,12.
Massfotometri användes här och tidigare5 för att undersöka bindningen av den monoklonala IgG-antikroppen trastuzumab till den lösliga domänen av FcRn. De två bindningspartnerna har rapporterats binda med nanomolär affinitet vid surt pH17. Massfotometri användes för att kvalitativt bedöma förekomsten av de komplex som bildades medan bindningspartnerna hade pH 5,0, och proverna späddes snabbt ut genom ett extra mikrofluidiskt system. Proceduren optimerades för den specifika protein-proteininteraktionen baserat på tidigare rapporterade resultat5. Samma procedur kan användas för att studera andra interaktioner, förutsatt att användarna har förkunskaper eller optimerar de experimentella förhållandena för systemet i fråga, såsom vilka buffertar som ska användas, den initiala proteinkoncentrationen, den förväntade stökiometrin och mängden inkubation som behövs för att interaktionen ska nå en jämvikt.
När IgG-FcRn-blandningen späddes ut manuellt var det svårt att detektera förekomst av IgG-FcRn-komplex, trots att dessa proteiner är kända för att interagera5. Denna uppsats visar att den snabba utspädningsmetoden resulterar i en märkbart ökad mängd av dessa komplex. För samma prov, när snabb utspädning användes, observerades båda 1:1 FcRn-IgG-komplex och 2:1 FcRn-IgG-komplex tydligt. Dessa skillnader i komplex bildning visar vikten av att studera biomolekylära interaktionssystem över ett brett spektrum av koncentrationer.
Dessutom visar dessa resultat också att det är enkelt att använda mikrofluidik med analys av enskilda molekyler för att fånga svaga interaktioner – vilket fyller en betydande lucka i metoden. Kombinationen av snabbutspädande mikrofluidik med massfotometri ger attraktiva fördelar på grund av fördelarna med massfotometri som en analytisk teknik. Det vill säga, massfotometri kräver inga etiketter, innebär minimal provberedning och mätningarna görs i lösning. För detta protokoll är en annan viktig fördel med massfotometri dess förmåga att urskilja och kvantifiera alla bildade arter (förutsatt att de har en distinkt massa på >30 kDa). Detta står i kontrast till till exempel SPR, som kan mäta graden av bindning och avbindning men inte direkt kan tillhandahålla information om stökiometri8.
För detta protokoll, liksom för massfotometriexperiment mer allmänt, är flera överväganden till hjälp. För det första bör den slutliga proteinkoncentrationen ligga inom gränsen för vad massfotometri kan mäta (100 pM-100 nM). Den startande inkubationskoncentrationen bör också ligga inom intervallet för mikrofluidiksystemet (upp till 90 μM) och teoretiseras vara högre än den faktiska KD för interaktionen10. Den rekommenderade utgångspunkten är ett blandningsförhållande på 1:1 koncentration mellan de interagerande arterna vid μM-koncentration. Förhållandet kan sedan varieras till 1:2, 1:5 eller, som i fallet med denna interaktion, 1:10. Om det inte finns någon tidigare information om proteininteraktionerna måste användaren optimera experimentet och börja med en hög koncentration (rekommenderad 20 μM) för varje partner för att avgöra om affiniteten hos komponenterna ligger inom det koncentrationsintervall som upprätthålls av den presenterade metoden (dvs. komplex bildas). Optimering kan också innebära att man väljer andra buffertförhållanden för att främja interaktionerna eller titreringen av en av interaktionskomponenterna för att bestämma rätt blandningsförhållande. När dessa har bestämts är det möjligt att optimera koncentrationer och flöden för att möjliggöra optimala förhållanden för studien och metoden, t.ex. att minska koncentrationerna för att möjliggöra bättre toppupplösning.
För det andra, för att framgångsrikt replikera detta experiment, bör föroreningar minimeras. Vanliga källor till föroreningar som är kända för att negativt påverka massfotometrimätningar inkluderar andra proteiner eller cellulärt skräp som finns kvar efter rening, ofiltrerade buffertar, micellbildande rengöringsmedel (om de finns i för hög koncentration) och buffertar som innehåller höga koncentrationer av salt, glycerol eller andra komponenter. Som diskuterats i protokollet ovan bör bubblor i mikrofluidiksystemet avlägsnas. Bubblor kan bildas i rörsystemet eller om proverna har hög ytspänning och är benägna att skumbildas. Bubblor kan också bildas i nedsänkningsoljan, vilket kan detekteras från fokusringen (Figur 3). Om bubblor inte kan avlägsnas med hjälp av de steg som beskrivs i protokollet är en annan lösning att avgasa provet med hjälp av en exsickator och en vakuumpump, vilket lämnar provet under reducerat tryck i några minuter. Vortexing eller skakning av högkoncentrerade proteinlösningar rekommenderas inte eftersom dessa åtgärder kan främja bubbelbildning.
Medan mätningen av en specifik protein-proteininteraktion demonstreras här, kan samma protokoll tillämpas på andra protein-proteininteraktionssystem utan betydande modifiering. En ytterligare framtida inriktning av detta protokoll skulle vara att använda mätningarna för att beräkna KD-värden för de identifierade komplexen, vilket har beskrivits på andra ställen i samband med massfotometri 5,7. Medan de tidigare studierna använde data från experiment med manuell utspädning och starkare interaktioner, kan analysprincipen lätt tillämpas i detta sammanhang – förutsatt att ytterligare förbättringar i mikrofluidikanordningen implementeras (såsom ökad flödessensornoggrannhet och pumpstabilitet).
Utöver protein-protein-interaktioner kommer det sannolikt att finnas bredare tillämpningar för den kombinerade metoden med massfotometri och mikrofluidik med snabb utspädning. Massfotometri kan användas för att bedöma provets renhet, aggregering och homogenitet18,19; studera proteinoligomerisering20, makromolekylär montering21 eller polymerisation22; och på andra områden. Massfotometrianalys sträcker sig också bortom proteiner; Det har använts för att undersöka interaktioner mellan nukleinsyror och proteiner23, viruspartiklar24 och nanopartiklar25. Detta protokoll beskriver således en viktig tillämpning av ett kombinerat mikrofluidiksystem för massfotometri – det möjliggör direkt mätning av svaga protein-proteininteraktioner på nivån av enskilda molekyler och komplex. Värdet av den aktuella applikationen är högt, eftersom det öppnar möjligheten att direkt karakterisera interaktioner som generellt har varit svåra att studera – med relevans inom kritiska terapeutiska områden. Detta kombinerade tillvägagångssätt skulle också kunna ligga till grund för ett bredare spektrum av undersökningar av prover med koncentrationer upp till tiotals mikromolar.
Declarações
The authors have nothing to disclose.
Acknowledgements
W.S. stöds av ett UKRI Future Leaders Fellowship [MR/V02213X/1]. Manuskripttexten och grafiken utarbetades med stöd från medlemmar av Refeyns team för vetenskaplig kommunikation (Panagiota Paganopoulou, Neus Torres Tamarit och Catherine Lichten). Vi värdesätter också värdefull feedback från Camille Hetez, Sofia Ferreira och Matthias Langhorst.
Materials
| 2-Propanol (Isopropanol) | VWR International LLC | 20880.320 | |
| Data acquisition software | Refeyn | AcquireMP (v2022 R1) | |
| Data analysis software | Refeyn | DiscoverMP (v2022 R1) | |
| FCRN, His-Tag | Sigma | SRP0624 | |
| Herceptin (IgG) | Cambridge Bioscience | HY-P9907-1mg | |
| Mass photometer | Refeyn | TwoMP | |
| Microfluidics box | Refeyn | MassFluidix HC system | |
| Microfluidics chip | Refeyn | MassFluidix HC chip | |
| Microfluidics control software | Fluigent | OxyGEN | |
| Phosphate Buffered Saline (PBS), 1x Ultra Pure | VWR International LLC | K812 | |
| Sodium Hydroxide (NaOH) | Sigma | S2770 | |
| β-Amylase, from sweet potato | Sigma | A8781 |
Referências
- Arter, W. E., Levin, A., Krainer, G., Knowles, T. P. J. Microfluidic approaches for the analysis of protein-protein interactions in solution. Biophysical Reviews. 12 (2), 575-585 (2020).
- Hellenkamp, B., Thurn, J., Stadlmeier, M., Hugel, T. Kinetics of transient protein complexes determined via diffusion-independent microfluidic mixing and fluorescence stoichiometry. The Journal of Physical Chemistry. B. 122 (49), 11554-11560 (2018).
- Li, Z. Editorial: Methods in structural biology: Cryo-electron microscopy. Frontiers in Molecular Biosciences. 9, 1041386 (2022).
- Herling, T. W., et al. A microfluidic platform for real-time detection and quantification of protein-ligand interactions. Biophysical Journal. 110 (9), 1957-1966 (2016).
- Soltermann, F., et al. Quantifying protein-protein interactions by molecular counting with mass photometry. Angewandte Chemie International Edition. 59 (27), 10774-10779 (2020).
- Wu, D., Piszczek, G. Rapid determination of antibody-antigen affinity by mass photometry. Journal of Visualized Experiments: JoVE. 168, 61784 (2021).
- Wu, D., Piszczek, G. Measuring the affinity of protein-protein interactions on a single-molecule level by mass photometry. Analytical Biochemistry. 592, 113575 (2020).
- Young, G., et al. Quantitative mass imaging of single biological macromolecules. Science. 360 (6387), 423-427 (2018).
- Zijlstra, N., et al. Rapid microfluidic dilution for single-molecule spectroscopy of low-affinity biomolecular complexes. Angewandte Chemie International Edition. 56 (25), 7126-7129 (2017).
- MassFluidix® HC system for rapid dilution via microfluidics. Available from: https://www.refeyn.com/massfluidix-hc-system (2023)
- Pollard, T. D. A guide to simple and informative binding assays. Molecular Biology of the Cell. 21 (23), 4061-4067 (2010).
- Jarmoskaite, I., AlSadhan, I., Vaidyanathan, P. P., Herschlag, D. How to measure and evaluate binding affinities. eLife. 9, e57264 (2020).
- Monnet, C., et al. Selection of IgG variants with increased FcRn binding using random and directed mutagenesis: Impact on effector functions. Frontiers in Immunology. 6, 39 (2015).
- . Refeyn TwoMP: Transforming biomolecular characterisation Available from: https://www.refeyn.com/twomp-mass-photometer (2022)
- Lai, S. -. H., Tamara, S., Heck, A. J. R. Single-particle mass analysis of intact ribosomes by mass photometry and Orbitrap-based charge detection mass spectrometry. iScience. 24 (11), 103211 (2021).
- Wu, D., Piszczek, G. Standard protocol for mass photometry experiments. European Biophysics Journal. 50 (3-4), 403-409 (2021).
- Vaughn, D. E., Bjorkman, P. J. Structural basis of pH-dependent antibody binding by the neonatal Fc receptor. Structure. 6 (1), 63-73 (1998).
- Niebling, S., et al. Biophysical screening pipeline for Cryo-EM grid preparation of membrane proteins. Frontiers in Molecular Biosciences. 9, 882288 (2022).
- Paul, S. S., Lyons, A., Kirchner, R., Woodside, M. T. Quantifying oligomer populations in real time during protein aggregation using single-molecule mass photometry. ACS Nano. 16 (10), 16462-16470 (2022).
- Schulz, L., et al. Evolution of increased complexity and specificity at the dawn of form I Rubiscos. Science. 378 (6616), 155-160 (2022).
- Malay, A. D., et al. An ultra-stable gold-coordinated protein cage displaying reversible assembly. Nature. 569 (7756), 438-442 (2019).
- Hundt, N., Cole, D., Hantke, M. F., Miller, J. J., Struwe, W. B., Kukura, P. Direct observation of the molecular mechanism underlying protein polymerization. Science Advances. 8 (35), eabm7935 (2022).
- Acharya, A., et al. Distinct RPA domains promote recruitment and the helicase-nuclease activities of Dna2. Nature Communications. 12, 6521 (2021).
- Ebberink, E. H. T. M., Ruisinger, A., Nuebel, M., Thomann, M., Heck, A. J. R. Assessing production variability in empty and filled adeno-associated viruses by single molecule mass analyses. Molecular Therapy – Methods & Clinical Development. 27, 491-501 (2022).
- Melo, L., et al. Size distributions of gold nanoparticles in solution measured by single-particle mass photometry. The Journal of Physical Chemistry B. 125 (45), 12466-12475 (2021).

