मास फोटोमेट्री के साथ माइक्रोफ्लुइडिक्स को युग्मित करके माइक्रोमोलर सांद्रता में प्रोटीन कॉम्प्लेक्स गठन का विश्लेषण
Summary
यह प्रोटोकॉल कम आत्मीयता प्रोटीन-प्रोटीन इंटरैक्शन की जांच के लिए एक उपन्यास माइक्रोफ्लुइडिक्स सिस्टम के साथ बड़े पैमाने पर फोटोमेट्री को जोड़ती है। यह दृष्टिकोण समाधान में अत्यधिक केंद्रित परिसरों के तेजी से कमजोर पड़ने पर आधारित है, जो कम-आत्मीयता माप को सक्षम बनाता है और बड़े पैमाने पर फोटोमेट्री की प्रयोज्यता को व्यापक बनाता है।
Abstract
मास फोटोमेट्री एक बहुमुखी द्रव्यमान माप तकनीक है जो लेबल के बिना समाधान में बायोमोलेक्यूलर इंटरैक्शन और जटिल गठन के अध्ययन को सक्षम बनाती है। मास फोटोमेट्री आम तौर पर 100 पीएम-100 एनएम एकाग्रता रेंज में नमूनों का विश्लेषण करने के लिए अनुकूल है। हालांकि, कई जैविक प्रणालियों में, कम-आत्मीयता या क्षणिक बातचीत का अध्ययन करने के लिए अधिक केंद्रित नमूनों को मापना आवश्यक है। यहां, हम एक ऐसी विधि का प्रदर्शन करते हैं जो प्रभावी रूप से नमूना सांद्रता की सीमा का विस्तार करती है जिसका विश्लेषण नैनोमोलर से दसियों माइक्रोमोलर तक बड़े पैमाने पर फोटोमेट्री द्वारा किया जा सकता है।
इस प्रोटोकॉल में, बड़े पैमाने पर फोटोमेट्री को माइक्रोमोलर एकाग्रता रेंज में समाधान में प्रोटीन परिसरों के गठन की जांच करने के लिए एक उपन्यास माइक्रोफ्लुइडिक्स प्रणाली के साथ जोड़ा जाता है। माइक्रोफ्लुइडिक्स प्रणाली के साथ, उपयोगकर्ता एक वांछित उच्च सांद्रता पर एक नमूना बनाए रख सकते हैं, जिसके बाद नैनोमोलर रेंज को कमजोर करना – बड़े पैमाने पर फोटोमेट्री माप से पहले कई मिलीसेकंड। कमजोर पड़ने की गति के कारण, नमूने के संतुलन को स्थानांतरित करने से पहले डेटा प्राप्त किया जाता है (यानी, परिसर का पृथक्करण)।
तकनीक को एक इम्युनोग्लोबुलिन जी (आईजीजी) एंटीबॉडी और नवजात एफसी रिसेप्टर के बीच बातचीत को मापने के लिए लागू किया जाता है, जो उच्च-क्रम परिसरों के गठन को दर्शाता है जो स्थिर द्रव्यमान फोटोमेट्री माप के साथ मात्रात्मक नहीं थे।
अंत में, बड़े पैमाने पर फोटोमेट्री और माइक्रोफ्लुइडिक्स का संयोजन माइक्रोमोलर एकाग्रता रेंज में नमूनों को चिह्नित करना संभव बनाता है और कमजोर समानता के साथ बायोमोलेक्यूलर इंटरैक्शन को मापने में कुशल है। इन क्षमताओं को कई संदर्भों में लागू किया जा सकता है – बायोथेरेप्यूटिक्स के विकास और डिजाइन सहित – विविध प्रोटीन-प्रोटीन इंटरैक्शन के गहन लक्षण वर्णन को सक्षम करना।
Introduction
प्रोटीन-प्रोटीन इंटरैक्शन प्रतिरक्षा विनियमन से डीएनए प्रतिकृति और अनुवाद तक अधिकांश सेलुलर कार्यों को रेखांकित करते हैं। नतीजतन, आमतौर पर बनने वाले विविध विषम परिसरों में बातचीत की एक विशाल श्रृंखला की जांच करने के लिए पूरे जीवन विज्ञान में एक मौलिक आवश्यकता है। हालांकि, उनकी पहचान, लक्षण वर्णन, और मात्रा का ठहराव अक्सर चुनौतीपूर्ण होते हैं, विशेष रूप से कम आत्मीयता बातचीत1 के लिए.
इम्यूनोप्रिपिटेशन परख का उपयोग अक्सर उच्च-आत्मीयता इंटरैक्शन का पता लगाने के लिए किया जाता है, लेकिन कम-आत्मीयता और क्षणिक बातचीत के लिए, पता लगाना काफी हद तक अव्यवहार्य है2. प्रतिदीप्ति तकनीक भी इस्तेमाल किया जा सकता है, लेकिन फ्लोरोसेंट लेबल2 के संभावित विघटनकारी जोड़ की आवश्यकता है. क्रायो-ईएम एक संरचनात्मक स्नैपशॉट और उच्च स्थानिक संकल्प के साथ गठित प्रोटीन परिसरों का एक पहनावा रीडआउट प्रदान कर सकता है, लेकिन आमतौर पर कम आत्मीयता बातचीत की इमेजिंग के लिए बहुत कम सांद्रता पर काम करने की आवश्यकता होती है। क्रायो-ईएम लागत, पहुंच, नमूना तैयार करने और विश्लेषण समय से संबंधित चुनौतियां भी लाताहै।
इसके अतिरिक्त, सतह प्लास्मोन अनुनाद (एसपीआर) प्रोटीन-प्रोटीन इंटरैक्शन की मात्रा निर्धारित करने का एक लोकप्रिय तरीका बन गया है, हालांकि इसके लिए प्रोटीन स्थिरीकरण की आवश्यकता होती है, जो बाध्यकारी संतुलन को प्रभावित कर सकता है और परिणामस्वरूप परिवर्तनीय ऑन-दरों में परिणाम हो सकता है, इस प्रकार माप सटीकता 4,5 को कम कर सकता है। यह भी डेटा संग्रह और विश्लेषण 6 से पहले कई परख कदम शामिलहै.
मास फोटोमेट्री एक एकल अणु तकनीक है जिसका उपयोग प्रोटीन-प्रोटीन इंटरैक्शन 5,6,7का विश्लेषण करने के लिए किया गया है। यह एकल अणुओं या परिसरों के द्रव्यमान को मापने के द्वारा काम करता है, जब वे एक ग्लास कवरस्लिप8 की सतह पर उतरते हैं, तो वे बिखरते हैं। मास फोटोमेट्री माप का उपयोग बाध्यकारी भागीदारों के सापेक्ष बहुतायत और उनके द्वारा बनाएगए परिसरों से बाध्यकारी समानता को निर्धारित करने के लिए किया गया है। फिर भी, अन्य एकल-अणु तकनीकों की तरह, मापा जाने वाला नमूना की एकाग्रता आमतौर पर 100 एनएम से कम होनी चाहिए। यदि एकाग्रता अधिक है, तो कांच की सतह पर उतरने वाले अणु स्थानिक रूप से ओवरलैप करेंगे, जिसके परिणामस्वरूप खराब डेटा गुणवत्ता7. नतीजतन, कमजोर बातचीत (केडी ~ माइक्रोमोलर्स), जो इन कम सांद्रता पर अलग हो जाती है, को मज़बूती से मापा नहीं जा सकता है क्योंकि अनबाउंड और बाउंड प्रजातियों के आवश्यक मिश्रण का निरीक्षण करना संभव नहींहै 5.
यहां, हम एक दृष्टिकोण का वर्णन करते हैं जो एक नए युग्मित माइक्रोफ्लुइडिक्स मास फोटोमेट्री डिवाइस के आधार पर इस सीमा पर काबू पाता है। विशेष रूप से, एक माइक्रोफ्लुइडिक्स सिस्टम का उपयोग मास फोटोमीटर के संयोजन में किया जाता है ताकि बड़े पैमाने पर फोटोमेट्री द्वारा निर्धारित की जा सकने वाली बातचीत की सीमा को प्रभावी ढंग से विस्तारित किया जा सके। माइक्रोफ्लुइडिक्स को प्रोटीन-प्रोटीन इंटरैक्शन की जांच के लिए संभावनाओं की एक श्रृंखला की पेशकश करने के लिए दिखाया गया है, जिसमें कमजोर इंटरैक्शन 1,9का पता लगाने के लिए तेजी से कमजोर पड़ने शामिल है। इस के साथ साथ साथ वर्णित प्रणाली तेजी से एक microfluidic चिप पर 10,000 गुना तक नमूना पतला और तुरंत चिप के अवलोकन क्षेत्र भर में यह प्रवाहित करने के लिए अणुओं कमजोर पड़ने की प्रक्रिया10 शुरू कर दिया जब अणुओं से 50 एमएस के भीतर शुरू करने के लिए बड़े पैमाने पर फोटोमेट्री माप को सक्षम करने, संचालित संचालित करता है. कमजोर पड़ने तब होता है जब नमूना और बफर चिप पर एक रिवर्स टेस्ला वाल्व मिक्सर में संयुक्त होते हैं, दो समाधानों के सापेक्ष प्रवाह दर के साथ कमजोर पड़ने की मात्रा निर्धारित होती है (प्रोटोकॉल चरण 8 देखें)। प्रवाह दर microfluidic नियंत्रण सॉफ्टवेयर के साथ नियंत्रणीय है. प्रवाह दर को बदलने से प्रजातियों की सापेक्ष आबादी बदल सकती है क्योंकि यह कांच की सतह पर लैंडिंग घटनाओं की संख्या को प्रभावित कर सकती है, जिसे द्रव्यमान फोटोमीटर द्वारा मापा जाता है।
बातचीत की अखंडता बाधित होने से पहले माप पूरा करने के लिए प्रक्रिया की गति काफी तेज है (अधिक जानकारी के लिए, चर्चा भी देखें)। इसे प्रथम-क्रम प्रतिक्रियाओं के सिद्धांत पर एक संक्षिप्त नज़र के माध्यम से समझा जा सकता है, जहां 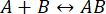 । अग्र (संघ) दर स्थिरांक kf है, पश्चगामी (पृथक्करण) दर स्थिरांक kb है, और संतुलन पृथक्करण स्थिरांक (KD) को किस रूप में परिभाषित किया गया है?
। अग्र (संघ) दर स्थिरांक kf है, पश्चगामी (पृथक्करण) दर स्थिरांक kb है, और संतुलन पृथक्करण स्थिरांक (KD) को किस रूप में परिभाषित किया गया है?
केडी = केबी /
प्रोटीन बाइंडिंग के लिए, kfआम तौर पर अभिकारकों के प्रसार11 द्वारा सीमित होता है और इसलिए 10 6-107 M-1·s-1 की सीमा तक सीमित होता है। क्योंकि की सीमा सीमित है, एक कम-आत्मीयता (KD ~ माइक्रोमोलर्स) प्रतिक्रिया में kb≈ 1 s-1 होगा। अर्थात्, kb = kf · KD= (106 M-1·s-1) (10-6 M) = 1 s-1, कॉम्प्लेक्स का आधा जीवन लगभग 0.7 s11,12 के साथ।
हमारी उदाहरण प्रणाली आईजीजी मोनोक्लोनल एंटीबॉडी ट्रास्टुज़ुमाब को आईजीजी नवजात एफसी रिसेप्टर (एफसीआरएन) के घुलनशील डोमेन के लिए बाध्य करती है, जो इंटरैक्टिंग पार्टनर13 के रूप में जानी जाती हैं। अकेले पारंपरिक द्रव्यमान फोटोमेट्री (यानी, नमूनों के मैनुअल कमजोर पड़ने के साथ) का उपयोग करके प्राप्त पहले प्रकाशित आंकड़ों से पता चला है कि प्रोटीन कई प्रजातियां बनाते हैं। FcRn मोनोमर्स, FcRn डिमर, और अनबाउंड IgG स्पष्ट रूप से दिखाई दे रहे थे, जबकि IgG-FcRn कॉम्प्लेक्स (1:1 और 1:2 अनुपात पर) का भी पता चला (पीएच 5.0 पर) लेकिन केवल बहुत कम बहुतायत5 के साथ। यह अवलोकन इस सवाल का संकेत देता है कि क्या आईजीजी-एफसीआरएन जटिल गठन को अधिक स्पष्ट रूप से पता लगाया जा सकता है यदि उच्च एकाग्रता पर मापा जाता है। दरअसल, यहां वर्णित एक युग्मित तेजी से कमजोर पड़ने वाले दृष्टिकोण के साथ बड़े पैमाने पर फोटोमेट्री के संयोजन ने उनके मापा कणों में वृद्धि से जटिल गठन के अधिक मजबूत सबूत प्रदान किए।
यहां वर्णित मास फोटोमेट्री और माइक्रोफ्लुइडिक्स प्रोटोकॉल माइक्रोमोलर रेंज तक केडी के साथ परिसरों के गठन को चिह्नित करना संभव बनाता है। केडी के एक अनुभवजन्य निर्धारण के लिए प्रवाह संवेदक सटीकता, पंप स्थिरता, चिप-टू-चिप विविधताओं और अवलोकन विंडो के अंदर माप स्थान पर और सुधार की आवश्यकता होगी, क्योंकि ये सभी कारक उस समय को प्रभावित करेंगे जब नमूना पतला हो जाता है मापा जा रहा है।
किसी भी घुलनशील प्रोटीन के बीच बंधन की जांच करने के लिए एक ही दृष्टिकोण लागू किया जा सकता है, बशर्ते उनके पास अलग-अलग आणविक भार (कम से कम 25 केडीए से अलग) हों जो द्रव्यमान फोटोमीटर (30 केडीए से 6 एमडीए) के साथ विश्लेषण के लिए उपयुक्त सीमा में आते हैं। प्राप्त अंतर्दृष्टि कई संदर्भों में अध्ययन के लिए सहायक हो सकती है – सेलुलर कार्यों की यंत्रवत समझ प्राप्त करने से लेकर नई बायोथेरेप्यूटिक दवाओं के डिजाइन तक।
Protocol
Representative Results
Discussion
प्रोटोकॉल यहाँ उल्लिखित का पता लगाने और कम आत्मीयता प्रोटीन प्रोटीन बातचीत यों यों के लिए एक विधि प्रदान करता है. यह एक बड़े पैमाने पर फोटोमीटर का उपयोग करता है जो एक तेजी से कमजोर पड़ने वाले माइक्रोफ्लुइडिक्स सिस्टम से जुड़ा होता है। मास फोटोमेट्री एक लेबल-मुक्त, जैव-विश्लेषणात्मक उपकरण है जो 30 केडीए से 6 एमडीए की सीमा के भीतर उन लोगों के लिए बायोमोलेक्यूल्स16 के समाधान में आणविक द्रव्यमान को मज़बूती से माप सकता है। चूंकि मास फोटोमेट्री एक एकल-अणु तकनीक है जो एक-एक करके नमूनों का विश्लेषण करती है, यह आम तौर पर 100 पीएम-100 एनएम एकाग्रता सीमा में नमूनों तक सीमित होती है। इस सीमा से ऊपर, कांच की सतह पर उतरने वाले अणु स्थानिक रूप से ओवरलैप करेंगे, जिसके परिणामस्वरूप खराब डेटा गुणवत्ता होगी; इस सीमा के नीचे, मजबूत विश्लेषण करने के लिए बहुत कम डेटा प्राप्त किया जाताहै 7. एक महत्वपूर्ण परिणाम यह है कि यह प्रोटीन इंटरैक्शन की जांच को उन लोगों तक सीमित कर सकता है जो उस सीमा के भीतर बाध्य और अनबाउंड प्रजातियों का मिश्रण बनाते हैं।
यहां, हमने बड़े पैमाने पर फोटोमेट्री के लिए उत्तरदायी नमूना सांद्रता की सीमा को प्रभावी ढंग से विस्तारित करने के लिए तेजी से कमजोर पड़ने वाले माइक्रोफ्लुइडिक्स सिस्टम का उपयोग करने के लिए चरण-दर-चरण प्रोटोकॉल विस्तृत किया है। माइक्रोफ्लुइडिक चिप पर नमूना पतला करके और फिर इसे 50 एमएस के भीतर डिटेक्टर अवलोकन खिड़की में प्रवाहित करके, सिस्टम इंटरैक्शन संतुलन शिफ्ट होने से पहले undiluted नमूने में मौजूद परिसरों को पकड़ लेता है। नमूना लगातार व्यक्तिगत माप के दौरान डिटेक्टर को दिया जाता है। इन शर्तों के तहत, नमूना मापा जाता है जब परिसर का 95% बरकरार रहेगा, यहां तक कि कम आत्मीयता बातचीत के लिए – माइक्रोमोलर के आदेश पर एक केडी के साथ और पृथक्करण दर 1 एस -1 के रूप में तेजी से।
इसकी गणना निम्नानुसार की जा सकती है: आगे की दर kfऔर पश्चगामी दर kb के साथ प्रतिक्रिया 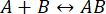 के लिए,
के लिए,
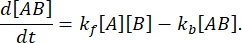
संतुलन पर, सभी तीन प्रजातियों (ए, बी, और जटिल एबी) की सांद्रता स्थिर रहती है, इसलिए 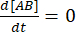 और
और 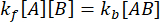 । रूढ़िवादी धारणा के तहत कि गड़बड़ी (कमजोर पड़ने, इस मामले में) जटिल को अलग करने का कारण बन सकती है, लेकिन आगे (एसोसिएशन) प्रतिक्रिया आगे नहीं बढ़ती है, शब्द केएफ [ए] [बी] को नगण्य माना जा सकता है, और निम्नलिखित सरलीकरण किया जा सकता है:
। रूढ़िवादी धारणा के तहत कि गड़बड़ी (कमजोर पड़ने, इस मामले में) जटिल को अलग करने का कारण बन सकती है, लेकिन आगे (एसोसिएशन) प्रतिक्रिया आगे नहीं बढ़ती है, शब्द केएफ [ए] [बी] को नगण्य माना जा सकता है, और निम्नलिखित सरलीकरण किया जा सकता है:
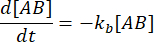
एकीकरण संतुलन के गड़बड़ी के बाद समय पर जटिल की एकाग्रता के लिए निम्नलिखित अभिव्यक्ति देता है:
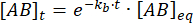
संकुल का वह अंश जो साम्यावस्था के विक्षोभ के बाद समय t पर आबद्ध रहता है, इस प्रकार है:
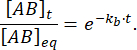
= 50 एमएस पर, केबी≈ 1 एस-1 के साथ प्रतिक्रिया के लिए, अंश बाध्य 0.95, या 95%11,12 है।
मास फोटोमेट्री का उपयोग यहां और पहले5 में किया गया था ताकि IgG मोनोक्लोनल एंटीबॉडी trastuzumab को FcRN के घुलनशील डोमेन में बांधने की जांच की जा सके। दो बाध्यकारी भागीदारों अम्लीय पीएच17 पर nanomolar आत्मीयता के साथ बाँध करने के लिए सूचित किया गया है. मास फोटोमेट्री का उपयोग गुणात्मक रूप से गठित परिसरों की प्रचुरता का आकलन करने के लिए किया गया था, जबकि बाध्यकारी साझेदार पीएच 5.0 पर थे, और नमूनों को एक अतिरिक्त माइक्रोफ्लुइडिक प्रणाली के माध्यम से तेजी से पतला किया गया था। प्रक्रिया पहले से रिपोर्ट किए गए परिणामों के आधार पर विशेष प्रोटीन-प्रोटीन बातचीत के लिए अनुकूलित किया गया था5. एक ही प्रक्रिया अन्य बातचीत का अध्ययन करने के लिए इस्तेमाल किया जा सकता है, बशर्ते उपयोगकर्ताओं को पूर्व ज्ञान है या इस तरह के बफर का उपयोग करने के लिए जो बफर, प्रारंभिक प्रोटीन एकाग्रता, अपेक्षित stoichiometry, और इनक्यूबेशन की राशि के लिए आवश्यक है एक संतुलन तक पहुँचने के लिए बातचीत की अनुमति देने के लिए की जरूरत है.
जब आईजीजी-एफसीआरएन मिश्रण को मैन्युअल रूप से पतला किया गया था, तो आईजीजी-एफसीआरएन परिसरों की उपस्थिति का पता लगाना मुश्किल था, भले ही इन प्रोटीनों को5 बातचीत करने के लिए जाना जाता है। इस पत्र से पता चलता है कि तेजी से कमजोर पड़ने के दृष्टिकोण के परिणामस्वरूप इन परिसरों की उल्लेखनीय रूप से वृद्धि हुई है। एक ही नमूने के लिए, जब तेजी से कमजोर पड़ने का उपयोग किया गया था, 1: 1 FcRn-IgG परिसरों और 2: 1 FcRn-IgG परिसरों दोनों को स्पष्ट रूप से देखा गया था। जटिल गठन में ये अंतर सांद्रता की एक विस्तृत श्रृंखला में बायोमोलेक्यूलर इंटरैक्शन सिस्टम का अध्ययन करने के महत्व को प्रदर्शित करते हैं।
इसके अतिरिक्त, इन परिणामों से यह भी पता चलता है कि कमजोर इंटरैक्शन को पकड़ने के लिए एकल-अणु विश्लेषण के साथ माइक्रोफ्लुइडिक्स का उपयोग करना सीधा है – विधि में एक महत्वपूर्ण अंतर को भरना। बड़े पैमाने पर फोटोमेट्री के साथ तेजी से कमजोर पड़ने वाले माइक्रोफ्लुइडिक्स का संयोजन एक विश्लेषणात्मक तकनीक के रूप में बड़े पैमाने पर फोटोमेट्री के फायदों के कारण आकर्षक लाभ प्रदान करता है। यही है, बड़े पैमाने पर फोटोमेट्री को लेबल की आवश्यकता नहीं होती है, इसमें न्यूनतम नमूना तैयार करना शामिल होता है, और माप समाधान में किया जाता है। इस प्रोटोकॉल के लिए, बड़े पैमाने पर फोटोमेट्री का एक और महत्वपूर्ण लाभ यह है कि सभी प्रजातियों को अलग करने और मात्रा निर्धारित करने की क्षमता है (बशर्ते उनके पास >30 केडीए का एक अलग द्रव्यमान हो)। यह एसपीआर के विपरीत है, उदाहरण के लिए, जो बाध्यकारी और अनबाइंडिंग की दरों को माप सकता है लेकिन आसानी से स्टोइकोमेट्री जानकारी 8 प्रदान नहीं कर सकताहै।
इस प्रोटोकॉल के लिए, साथ ही बड़े पैमाने पर फोटोमेट्री प्रयोगों अधिक आम तौर पर, कई विचार सहायक होते हैं. सबसे पहले, अंतिम प्रोटीन एकाग्रता उस सीमा के भीतर होनी चाहिए जो द्रव्यमान फोटोमेट्री माप सकती है (100 पीएम-100 एनएम)। प्रारंभिक इनक्यूबेशन एकाग्रता भी माइक्रोफ्लुइडिक सिस्टम (90 माइक्रोन तक) की सीमा के भीतर होनी चाहिए और बातचीत10 के वास्तविककेडी से ऊपर होने के लिए सिद्धांतित होना चाहिए। अनुशंसित प्रारंभिक बिंदु माइक्रोन एकाग्रता पर बातचीत करने वाली प्रजातियों के बीच 1: 1 एकाग्रता मिश्रण अनुपात है। अनुपात तब 1: 2, 1: 5, या, इस बातचीत के मामले में, 1:10 के लिए भिन्न हो सकता है। यदि प्रोटीन इंटरैक्शन के बारे में कोई पिछली जानकारी नहीं है, तो उपयोगकर्ता को प्रयोग का अनुकूलन करना होगा, प्रत्येक साथी के लिए उच्च एकाग्रता (अनुशंसित 20 माइक्रोन) से शुरू करके यह निर्धारित करने के लिए कि घटकों की आत्मीयता एकाग्रता सीमा के भीतर है प्रस्तुत विधि द्वारा निरंतर (यानी, परिसरों का गठन किया जाता है)। अनुकूलन भी बातचीत या सही मिश्रण अनुपात निर्धारित करने के लिए बातचीत घटकों में से एक के अनुमापन को बढ़ावा देने के लिए अन्य बफर शर्तों को चुनने शामिल हो सकते हैं. एक बार जब ये निर्धारित हो जाते हैं, तो अध्ययन और विधि के लिए इष्टतम स्थितियों की अनुमति देने के लिए सांद्रता और प्रवाह को अनुकूलित करना संभव है, उदाहरण के लिए, बेहतर शिखर संकल्प की अनुमति देने के लिए सांद्रता को कम करना।
दूसरे, इस प्रयोग को सफलतापूर्वक दोहराने के लिए, अशुद्धियों को कम से कम किया जाना चाहिए। अशुद्धियों के सामान्य स्रोत जो बड़े पैमाने पर फोटोमेट्री माप पर प्रतिकूल प्रभाव डालने के लिए जाने जाते हैं, उनमें अन्य प्रोटीन या सेलुलर मलबे शामिल हैं जो शुद्धिकरण के बाद रहते हैं, अनफ़िल्टर्ड बफ़र्स, मिसेल बनाने वाले डिटर्जेंट (यदि बहुत अधिक एकाग्रता में मौजूद हैं), और नमक, ग्लिसरॉल या अन्य घटकों की उच्च सांद्रता वाले बफ़र। जैसा कि ऊपर प्रोटोकॉल में चर्चा की गई है, माइक्रोफ्लुइडिक्स सिस्टम में बुलबुले को हटा दिया जाना चाहिए। बुलबुले टयूबिंग सिस्टम में बन सकते हैं या यदि नमूनों में उच्च सतह तनाव होता है और फोम गठन के लिए प्रवण होते हैं। बुलबुले भी विसर्जन तेल है, जो फोकस अंगूठी (चित्रा 3) से पता लगाया जा सकता है में फार्म कर सकते हैं. यदि बुलबुले प्रोटोकॉल में वर्णित चरणों का उपयोग कर हटाया नहीं जा सकता है, एक और समाधान एक desiccator और एक वैक्यूम पंप का उपयोग कर नमूना degas कुछ मिनट के लिए कम दबाव के तहत नमूना छोड़ने के लिए है. भंवर या मिलाते हुए अत्यधिक केंद्रित प्रोटीन समाधान इन कार्यों बुलबुला गठन को बढ़ावा देने के रूप में अनुशंसित नहीं है.
जबकि एक विशिष्ट प्रोटीन-प्रोटीन इंटरैक्शन का माप यहां प्रदर्शित किया गया है, उसी प्रोटोकॉल को महत्वपूर्ण संशोधन के बिना अन्य प्रोटीन-प्रोटीन इंटरैक्शन सिस्टम पर लागू किया जा सकता है। इस प्रोटोकॉल का एक और भविष्य दिशा की पहचान परिसरों के लिए कश्मीरडी मूल्यों की गणना करने के लिए माप का उपयोग करने के लिए किया जाएगा, के रूप में बड़े पैमाने पर फोटोमेट्री 5,7 के संदर्भ में कहीं और वर्णित किया गया है. जबकि पूर्व अध्ययनों ने मैनुअल कमजोर पड़ने और मजबूत बातचीत से जुड़े प्रयोगों से डेटा का उपयोग किया था, विश्लेषण सिद्धांत को इस संदर्भ में आसानी से लागू किया जा सकता है – बशर्ते माइक्रोफ्लुइडिक डिवाइस में और सुधार लागू किए गए हों (जैसे प्रवाह संवेदक सटीकता और पंप स्थिरता में वृद्धि)।
प्रोटीन-प्रोटीन इंटरैक्शन से परे, संयुक्त द्रव्यमान फोटोमेट्री और तेजी से कमजोर पड़ने वाले माइक्रोफ्लुइडिक्स दृष्टिकोण के लिए व्यापक अनुप्रयोग होने की संभावना है। मास फोटोमेट्री नमूना शुद्धता, एकत्रीकरण, और18,19 समरूपता का आकलन करने के लिए इस्तेमाल किया जा सकता है; अध्ययन प्रोटीन oligomerization20, macromolecular विधानसभा21 या पोलीमराइजेशन22; और अन्य क्षेत्रों में। मास फोटोमेट्री विश्लेषण भी प्रोटीन से परे फैली हुई है; इसका उपयोग न्यूक्लिक एसिड और प्रोटीन23, वायरल कणों24 और नैनोकणों25 के बीच बातचीत की जांच के लिए किया गया है। इस प्रकार यह प्रोटोकॉल एक संयुक्त द्रव्यमान फोटोमेट्री माइक्रोफ्लुइडिक्स प्रणाली के एक महत्वपूर्ण अनुप्रयोग का वर्णन करता है – यह व्यक्तिगत अणुओं और परिसरों के स्तर पर कमजोर प्रोटीन-प्रोटीन इंटरैक्शन के प्रत्यक्ष माप को सक्षम बनाता है। वर्तमान आवेदन का मूल्य अधिक है, क्योंकि यह सीधे तौर पर उन इंटरैक्शन को चिह्नित करने की संभावना को खोलता है जो आम तौर पर अध्ययन करना मुश्किल है – महत्वपूर्ण चिकित्सीय क्षेत्रों में प्रासंगिकता के साथ। यह संयुक्त दृष्टिकोण दसियों माइक्रोमोलर तक सांद्रता वाले नमूनों के लिए जांच की एक विस्तृत श्रृंखला के आधार के रूप में भी काम कर सकता है।
Declarações
The authors have nothing to disclose.
Acknowledgements
डब्ल्यूएस को यूकेआरआई फ्यूचर लीडर्स फैलोशिप [MR/V02213X/1] द्वारा समर्थित किया जाता है। पांडुलिपि पाठ और ग्राफिक्स रेफेन की वैज्ञानिक संचार टीम (पनागियोटा पगानोपोलौ, न्यूस टोरेस तामारिट और कैथरीन लिचटेन) के सदस्यों के समर्थन से तैयार किए गए थे। हम केमिली हेटेज़, सोफिया फरेरा और मैथियास लैंगहॉर्स्ट से मूल्यवान प्रतिक्रिया भी स्वीकार करते हैं।
Materials
| 2-Propanol (Isopropanol) | VWR International LLC | 20880.320 | |
| Data acquisition software | Refeyn | AcquireMP (v2022 R1) | |
| Data analysis software | Refeyn | DiscoverMP (v2022 R1) | |
| FCRN, His-Tag | Sigma | SRP0624 | |
| Herceptin (IgG) | Cambridge Bioscience | HY-P9907-1mg | |
| Mass photometer | Refeyn | TwoMP | |
| Microfluidics box | Refeyn | MassFluidix HC system | |
| Microfluidics chip | Refeyn | MassFluidix HC chip | |
| Microfluidics control software | Fluigent | OxyGEN | |
| Phosphate Buffered Saline (PBS), 1x Ultra Pure | VWR International LLC | K812 | |
| Sodium Hydroxide (NaOH) | Sigma | S2770 | |
| β-Amylase, from sweet potato | Sigma | A8781 |
Referências
- Arter, W. E., Levin, A., Krainer, G., Knowles, T. P. J. Microfluidic approaches for the analysis of protein-protein interactions in solution. Biophysical Reviews. 12 (2), 575-585 (2020).
- Hellenkamp, B., Thurn, J., Stadlmeier, M., Hugel, T. Kinetics of transient protein complexes determined via diffusion-independent microfluidic mixing and fluorescence stoichiometry. The Journal of Physical Chemistry. B. 122 (49), 11554-11560 (2018).
- Li, Z. Editorial: Methods in structural biology: Cryo-electron microscopy. Frontiers in Molecular Biosciences. 9, 1041386 (2022).
- Herling, T. W., et al. A microfluidic platform for real-time detection and quantification of protein-ligand interactions. Biophysical Journal. 110 (9), 1957-1966 (2016).
- Soltermann, F., et al. Quantifying protein-protein interactions by molecular counting with mass photometry. Angewandte Chemie International Edition. 59 (27), 10774-10779 (2020).
- Wu, D., Piszczek, G. Rapid determination of antibody-antigen affinity by mass photometry. Journal of Visualized Experiments: JoVE. 168, 61784 (2021).
- Wu, D., Piszczek, G. Measuring the affinity of protein-protein interactions on a single-molecule level by mass photometry. Analytical Biochemistry. 592, 113575 (2020).
- Young, G., et al. Quantitative mass imaging of single biological macromolecules. Science. 360 (6387), 423-427 (2018).
- Zijlstra, N., et al. Rapid microfluidic dilution for single-molecule spectroscopy of low-affinity biomolecular complexes. Angewandte Chemie International Edition. 56 (25), 7126-7129 (2017).
- MassFluidix® HC system for rapid dilution via microfluidics. Available from: https://www.refeyn.com/massfluidix-hc-system (2023)
- Pollard, T. D. A guide to simple and informative binding assays. Molecular Biology of the Cell. 21 (23), 4061-4067 (2010).
- Jarmoskaite, I., AlSadhan, I., Vaidyanathan, P. P., Herschlag, D. How to measure and evaluate binding affinities. eLife. 9, e57264 (2020).
- Monnet, C., et al. Selection of IgG variants with increased FcRn binding using random and directed mutagenesis: Impact on effector functions. Frontiers in Immunology. 6, 39 (2015).
- . Refeyn TwoMP: Transforming biomolecular characterisation Available from: https://www.refeyn.com/twomp-mass-photometer (2022)
- Lai, S. -. H., Tamara, S., Heck, A. J. R. Single-particle mass analysis of intact ribosomes by mass photometry and Orbitrap-based charge detection mass spectrometry. iScience. 24 (11), 103211 (2021).
- Wu, D., Piszczek, G. Standard protocol for mass photometry experiments. European Biophysics Journal. 50 (3-4), 403-409 (2021).
- Vaughn, D. E., Bjorkman, P. J. Structural basis of pH-dependent antibody binding by the neonatal Fc receptor. Structure. 6 (1), 63-73 (1998).
- Niebling, S., et al. Biophysical screening pipeline for Cryo-EM grid preparation of membrane proteins. Frontiers in Molecular Biosciences. 9, 882288 (2022).
- Paul, S. S., Lyons, A., Kirchner, R., Woodside, M. T. Quantifying oligomer populations in real time during protein aggregation using single-molecule mass photometry. ACS Nano. 16 (10), 16462-16470 (2022).
- Schulz, L., et al. Evolution of increased complexity and specificity at the dawn of form I Rubiscos. Science. 378 (6616), 155-160 (2022).
- Malay, A. D., et al. An ultra-stable gold-coordinated protein cage displaying reversible assembly. Nature. 569 (7756), 438-442 (2019).
- Hundt, N., Cole, D., Hantke, M. F., Miller, J. J., Struwe, W. B., Kukura, P. Direct observation of the molecular mechanism underlying protein polymerization. Science Advances. 8 (35), eabm7935 (2022).
- Acharya, A., et al. Distinct RPA domains promote recruitment and the helicase-nuclease activities of Dna2. Nature Communications. 12, 6521 (2021).
- Ebberink, E. H. T. M., Ruisinger, A., Nuebel, M., Thomann, M., Heck, A. J. R. Assessing production variability in empty and filled adeno-associated viruses by single molecule mass analyses. Molecular Therapy – Methods & Clinical Development. 27, 491-501 (2022).
- Melo, L., et al. Size distributions of gold nanoparticles in solution measured by single-particle mass photometry. The Journal of Physical Chemistry B. 125 (45), 12466-12475 (2021).

