En termoplasmonisk tilgang til undersøgelse af plasmamembranreparation i levende celler og modelmembraner
Summary
Den termoplasmoniske punkteringsmetode integrerer konfokal mikroskopi, optisk pincet og guldnanopartikler for at studere proteinresponser under plasmamembranreparation i celler og gigantiske unilamellære vesikler. Teknikken muliggør hurtig og lokaliseret membranpunktering, hvilket gør det muligt at identificere nøgleproteiner og deres funktionelle roller i det indviklede plasmamembranreparationsmaskineri.
Abstract
Cellemembranen er afgørende for cellens overlevelse, og det er vigtigt at sikre dens integritet, da cellen oplever skader gennem hele sin livscyklus. For at forhindre beskadigelse af membranen har celler udviklet effektive plasmamembranreparationsmekanismer. Disse reparationsmekanismer kan studeres ved at kombinere konfokal mikroskopi og nanoskala termoplasmonik for at identificere og undersøge rollen som nøgleproteiner, såsom annexiner, involveret i overfladereparation i levende celler og membranmodelsystemer.
Punkteringsmetoden anvender en laser til at inducere meget lokaliseret opvarmning ved nanopartikelbestråling. Brugen af nær-infrarødt lys minimerer fototoksicitet i den biologiske prøve, mens størstedelen af absorptionen finder sted i den nær-infrarøde resonans plasmoniske nanopartikel. Denne termoplasmoniske metode er blevet udnyttet til potentiel fototermisk og biofysisk forskning for at forbedre forståelsen af intracellulære mekanismer og cellulære reaktioner gennem vesikel- og cellefusionsundersøgelser. Tilgangen har vist sig at være komplementær til eksisterende metoder til membranforstyrrelser, såsom mekanisk, kemisk eller optisk induceret skade, og giver et højt niveau af kontrol ved at påføre ekstremt lokaliserede skader. Omfanget af skaden er begrænset til nærheden af den sfæriske nanopartikel, og der opstår ingen skadelig skade langs strålebanen i modsætning til pulserende lasere, der bruger forskellige bølgelængder. På trods af visse begrænsninger, såsom dannelsen af nanobobler, tilbyder den termoplasmoniske metode et unikt værktøj til at undersøge cellulære reaktioner i plasmamembranreparation i et næsten naturligt miljø uden at gå på kompromis med cellelevedygtigheden.
Når den integreres med konfokal mikroskopi, kan punkteringsmetoden give en mekanistisk forståelse af membrandynamikken i modelmembransystemer samt kvantitativ information om proteinresponser på membranskader, herunder proteinrekruttering og deres biofysiske funktion. Samlet set kan anvendelsen af denne metode på reducerede modelsystemer forbedre vores forståelse af de indviklede plasmamembranreparationsmaskiner i levende celler.
Introduction
Cellemembranen, der tjener både som en fysisk barriere og en signalplatform, er afgørende for celleoverlevelse1. Gennem hele sin cellecyklus udsættes plasmamembranen (PM) for skader, såsom mekaniske 2,3,4,5 og kemiske6 stressinducerede skader. For at opretholde membranintegritet og sikre celleoverlevelse har cellen udviklet robuste plasmamembranreparationsmekanismer (PMR). Disse mekanismer afhænger af forskellige strategier, såsom cytoskelet reorganisering, membranfusion og membranudskiftningsstrategier 7,8,9,10,11, som alle er afhængige af rekruttering af specifikke proteiner. Især er medlemmer af annexinproteinfamilien blevet identificeret som nøgleproteiner forbundet med processerne i PMR 1,9,12,13,14,15,16. Efter PM-skade oplever cellen en tilstrømning af calciumioner (Ca2+), som udgør en umiddelbar trussel mod cellens overlevelse17. Som reaktion på Ca2+ tilstrømning binder annexinproteiner, som overvejende er placeret i cytosolen, til den indre folder af den beskadigede plasmamembran som en del af PMR-strategierne18. Annexin A2 (ANXA2) var et af de første medlemmer af annexin-familien, der blev forbundet med PMR i dysferlin-mangelfuld muskeldystrofi og blev foreslået at formidle reparation ved at fusionere intracellulære vesikler til PM nær skadestedet 5,19,20,21. Efterfølgende er flere funktioner blevet tilskrevet annexins22, og deres rolle i PMR har fået øget opmærksomhed i løbet af de sidste 20 år. Imidlertid er bilagenes nøjagtige rolle i PMR stadig ikke fuldt ud forstået 15,18,21,22.
Denne artikel foreslår en metode til at undersøge protein-membraninteraktion og membrandynamik på en kontrolleret og meget lokaliseret måde ved hjælp af en kombination af konfokal mikroskopi, optisk pincet og guldnanopartikler (AuNP’er). Denne metode muliggør kvantitativ undersøgelse af protein-, lipid- og små molekyleinteraktioner som reaktion på membranskader og Ca2+ tilstrømning. På trods af kompleksiteten og mangfoldigheden af komponenter, der er involveret i membranreparationsprocessen, er forenklede membransystemer, der efterligner plasmamembranen, blevet anvendt til at opnå en dybere mekanistisk forståelse af membrandynamik og annexinproteiners respons på membranforstyrrelser16. Gigantiske unilamellære lipidvesikler (GUV’er) blev valgt som modelmembransystem med en specificeret lipidsammensætning. GUV’erne blev genereret ved hjælp af gelassisteret hydreringsmetode, specifikt polyvinylalkoholgelhydrering, som beskrevet af Weinberger et al.23, hvilket muliggjorde effektiv indkapsling af annexiner i GUV’er.
Anvendelsen af nærinfrarød (NIR) laserbestråling på metalliske nanopartikler (NP’er) inducerer betydelig opvarmning af NP, hvilket gør det til en effektiv metode til at etablere en lokal varmekilde, der udnyttes i biomedicinske applikationer24. Metoden blev oprindeligt brugt til direkte at måle temperaturen omkring en enkelt AuNP i både 2D og 3D biomimetiske assays. I disse assays 25,26 blev de plasmoniske nanopartikler bestrålet på et understøttet lipiddobbeltlag eller optisk fanget nær GUV’er, der gennemgik en lokal termisk faseovergang ved lokal opvarmning, hvilket muliggjorde kvantificering og kontrol af den nøjagtige temperaturprofil omkring partiklen. Denne referencetemperaturprofil er blevet anvendt ved undersøgelse eller manipulation af biologiske prøver. Yderligere fremskridt i metoden har lettet induktionen af nanoskopiske porer i membraner27, hvilket muliggør vesikel og cellefusion 28,29. Andre undersøgelser har undersøgt opførsel af perifere membranproteiner i GUV’er29 og transmembranproteiner30 ved at skabe nye hybridvesikler, mens cellespecifik lægemiddellevering også er blevet undersøgt for at kontrollere og studere cellulære reaktioner eller genekspression 28,29,31,32,33. For nylig er metoden blevet brugt til at undersøge proteinresponser på membranskader 32,34,35.
Der findes flere metoder til at forstyrre plasmamembranen for at udforske cellulære reaktioner og membranreparation. Disse omfatter mikronålepunkteringer, mikroperlerystelser og celleskrabning, som alle kan forstyrre cellemembranen mekanisk 14,36,37. Kemisk induceret skade kan opnås ved at tilføje vaskemidler 5,38 eller bakterielle toksiner39,40, der destabiliserer lipiddobbeltlaget og genererer membranporer over plasmamembranen. Desuden er optisk inducerede skader ved kontinuerlige bølge- og pulserende lasere blevet anvendt til at studere PMR-komponenter, såsom annexinproteiner 5,14,21,41, i kombination med plasmoniske nanopartikler 42,43,44,45. På trods af effektiviteten af pulserende lasere med høj effekt kan de forårsage betydelige skader og skader på cellens indre langs strålebanen. Desuden mangler de detaljerede ændringer, der sker i det biologiske stof ved pulserende laserbestråling, og om det skaber en veldefineret pore, at blive undersøgt yderligere. En alternativ metode præsenteres i denne artikel, der anvender termoplasmonik til at inducere nanoskopiske huller i PM på en kontrolleret måde34,35 uden at forårsage væsentlig skade på de interne strukturer. Dette opnås ved at udsætte plasmoniske NP’er for en meget fokuseret NIR-laser, hvilket resulterer i en ekstremt lokaliseret temperaturstigning, der let kan nå temperaturer over 200 ° C, hvilket kan føre til små nanoskopiske eksplosioner 25,46,47. Denne proces kan styres ved at justere laserintensiteten samt størrelsen, formen og sammensætningen af NP’erne48. Ved at anvende denne teknik kan forskere undersøge proteiners rolle i PM-reparation i levende celler, hvilket kan hjælpe med at løse nogle af de ubesvarede spørgsmål vedrørende involvering af annexinproteiner i membranreparation uden at gå på kompromis med cellelevedygtigheden.
Den optiske fangst af plasmoniske nanopartikler er blevet veletableret af tidligere undersøgelser 25,49,50,51,52; yderligere indsigt i nanopartiklernes termoplasmoniske egenskaber 53,54,55 kan dog opnås i de supplerende materialer (supplerende fil 1). Den termoplasmoniske metode kan bruges til at skabe nanoskopiske huller i PM med det formål at studere de cellulære respons- og reparationsmekanismer. Mere præcist kan punkteringen opnås gennem optisk opvarmning af AuNP’er tæt på membranen, som vist i figur 1A og B. Denne lokaliserede punktering muliggør Ca2+ tilstrømning, som blev verificeret af en calciumsensor, hvilket aktiverede PMR-maskineriet. Til levende celleeksperimenter blev AuNP’er med en diameter på 200 nm immobiliseret på overfladen under cellen for at overvåge ANXA2’s rolle i PMR via konfokal mikroskopi. NIR-laseren (figur 1A, B) med en bølgelængde på 1064 nm bestråler AuNP og udnytter dens plasmoniske egenskaber (figur 1C), hvilket resulterer i betydelig lokal opvarmning (figur 1D) i det biologiske gennemsigtighedsvindue49, samtidig med at den forårsager minimal skade på selve cellen. Højtemperaturområdet omkring AuNP falder hurtigt med 30-40% i en afstand svarende til NP’s radius, som vist i figur 1E, hvilket giver mulighed for en ekstremt begrænset skade i alle tre dimensioner.
Supplerende dossier 1. Klik her for at downloade denne fil.
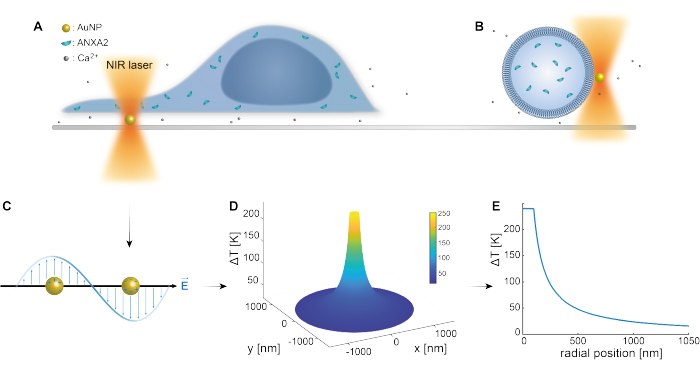
Figur 1: Skematisk oversigt over forsøgsmetoden. (A) ANXA-transfekterede celler er placeret oven på immobiliserede guldnanopartikler (AuNP’er) på overfladen, eller (B) gigantiske unilamellære vesikler (GUV’er) med indkapslet ANXA suspenderes i et medium indeholdende AuNP’er. C) En enkelt AuNP bestråles af den optiske NIR-fælde, hvor vekselvirkningen mellem det indkommende elektromagnetiske felt og ledningselektronerne fører til kollektiv svingning af elektroner i NP. (D) Denne proces resulterer i en meget begrænset, men signifikant temperaturstigning. For at estimere temperaturen på NP-overfladen anvendes Mie-teori, og en (E) temperaturprofil beregnes for en AuNP med en diameter på 200 nm og laserintensitet I = 6,36 x 108 W/cm2. Klik her for at se en større version af denne figur.
For at minimere den termiske effekt på cellemembranen bestråles AuNP’erne kun i ~ 1 sekund. Dette forårsager en forbigående og lokal udbrud af opvarmning, hvilket reducerer skaderne på proteiner, der typisk kræver mere tid at udfolde sig. Ved membranpunktering rekrutteres annexinproteiner i en brøkdel af et sekund, og inden for få sekunder dannes et annexinringlignende stillads omkring skadestedet (figur 2). Denne tilgang er også blevet anvendt til at undersøge involveringen af ANXA5 i både levende celler og modelmembraner16 i et forsøg på at kaste lys over hele reparationsprocessernes plan. Mens det primære fokus har været på den korrelerende rekruttering af forskellige annexinproteiner, er de biofysiske aspekter af reparationsmekanismen endnu ikke belyst.
For fuldt ud at gennemføre den foreslåede metode kræves tre nøglekomponenter: konfokal mikroskopi, optisk pincet og metal nanopartikler. Optisk pincet bruges til at fange AuNP’er, og deres konstruktion kan opnås ved at følge proceduren skitseret af Neuman et al.49. Men hvis opbygning af en optisk pincet viser sig at være for udfordrende, kan en tæt fokuseret NIR-laser bruges til at bestråle AuNP’er, der er immobiliseret under cellerne. Mens sfæriske AuNP’er blev valgt til denne protokol, kunne en række plasmoniske partikler med justerbare absorptionsspektre også anvendes til at opnå en meget lokaliseret temperaturgradient inden for NIR-regionen48.
Fluorescensbilleddannelse er nødvendig for at observere de fluorescerende mærkede proteiners rolle, og derfor kan total intern refleksionsmikroskopi (TIRF)56 betragtes som et alternativ til konfokal billeddannelse. Denne teknik tillader dog kun overfladebilleddannelse og ville ikke være kompatibel med modelmembranvesikeleksperimenterne. Derfor er både den optiske pincet og konfokalmikroskopet afgørende for den præcise lokalisering af nanopartiklen og detaljeret undersøgelse af lokalområdet omkring celleskaden. For effektivt at bestråle nanopartiklen med et diffraktionsbegrænset laserfokus er det nødvendigt at visualisere nanopartiklen. Dette kan opnås optimalt ved refleksionsmikroskopi, som er en standardbilleddannelsesfunktion i Leica konfokale mikroskoper. Men hvis refleksion eller spredningsbilleddannelse ikke er tilgængelig, kan alternative metoder, såsom den mindre effektive fluorescerende AuNP-mærkning, overvejes.
Sammenfattende har den meget kontrollerbare og lokaliserede termoplasmoniske metode, der præsenteres i denne undersøgelse, potentialet til at tjene som en fremragende platform til at undersøge de molekylære komponenter, der er involveret i cellulære reaktioner og PM-reparationsmekanismer i levende celler. Ud over at studere proteinresponset ved PM-skader kan denne tilgang også bruges til lokalt punktering af vesikler, hvilket muliggør en undersøgelse af proteinresponset i både protein-protein og protein-membrandynamik. Desuden giver denne metode mulighed for en kvantitativ analyse af interaktionerne mellem proteiner, lipider og små molekyler, når membraner forstyrres. Samlet set har disse fremskridt potentialet til at kaste lys over nogle af de uløste spørgsmål vedrørende de indviklede og komplekse plasmamembranreparationsmaskiner.
Protocol
Representative Results
Discussion
Undersøgelsen fremhæver den termoplasmoniske tilgang som en lovende teknik til at udforske proteinresponser i levende celler og modelmembraner efter membranforstyrrelser. Denne metode giver ikke kun omfattende information om proteinrekruttering, men også om den biofysiske funktion af proteiner, der er involveret i proteinmembrandynamik. Derfor letter det identifikationen af molekylære komponenter, der er ansvarlige for overfladereparation, og fremmer forståelsen af det komplekse, men vitale maskineri til plasmamembranreparation. Selvom der findes forskellige metoder til at inducere membranforstyrrelser, såsom mekaniske, kemiske og optiske teknikker, lider disse metoder af begrænsninger, såsom at være ikke-specifikke for celler, generere flere skader på cellemembranen eller forårsage betydelig skade på membranen og ablere internt cellulært materiale langs laserbanen, når der anvendes pulserende lasere med høj effekt. Mens integrationen af konfokal mikroskopi og optisk pincet giver den mest omfattende information, kan alternative billeddannelsesmetoder også anvendes. For eksempel, da billeddannelsen af den plasmoniske nanopartikel opnås ved hjælp af refleksionsmikroskopi, kan en indbygget billeddannelsestilstand i Leica-konfokale mikroskoper, yderligere billeddannelsesteknikker, såsom mørkefeltmikroskopi65,66, andre spredningsmetoder som iSCAT67,68 eller fluorescerende mærkning af nanopartiklen, anvendes til AuNP-visualisering, selvom dette kan begrænse metodens anvendelighed.
Den præsenterede metode er desuden i stand til at inducere nanoskopiske huller i modelmembraner, hvilket muliggør undersøgelse af synergieffekterne mellem forskellige annexiner. Dette opnås ved at indkapsle forskelligt mærkede rekombinante annexiner, fx henholdsvis RFP og GFP, efterfulgt af termoplasmonisk punktering. Dette modelsystem giver indsigt i, hvordan annexiner interagerer med membraner i nærheden af frie kanter, som vist i figur 2D. I modsætning til i celler fortsætter hullerne påført GUV’er imidlertid med at ekspandere efterfulgt af destabilisering af vesiklen. Billeddannelse af huludviklingen ved hjælp af konfokalmikroskopi kan være udfordrende på grund af den hurtige udvidelse af huldiameteren, men kan opnås ved at fange flere z-stakke over tid. En alternativ metode ville være at bruge en roterende disk konfokal til hurtigere billeddannelse. Desuden giver den termoplasmoniske tilgang typisk et begrænset antal optimale resultater i timen, når den anvendes på enkeltceller eller GUV-eksperimenter, normalt to til tre, ved prøvetemperaturer mellem 20 °C og 30 °C. For at opnå den mest nøjagtige observation af proteinmembrandynamik anbefales det at opbevare cellerne i en HEPES-holdig buffer og udskifte prøven hver time. Alternativt kan forsøgsvinduet udvides ved at udføre forsøgene i et celleinkubationskammer, dvs. ved en konstant temperatur på 37 °C med 5% CO2. Desuden kan kombinationen af denne tilgang med andre billeddannelsesteknikker, såsom stokastisk optisk rekonstruktionsmikroskopi (STORM), give en dybere forståelse af den biofysiske funktion og interaktion mellem nøgleproteiner, der er involveret i membranreparation på et enkeltmolekyleniveau. Dette kunne give detaljerede oplysninger om skadestedet, herunder sårgeometri og placering af annexinproteiner, samt identificere andre nøgleaktører, der er involveret i reparation af membranoverfladen.
For at opnå maksimal effektivitet og præcision ved inducering af membranskader er det bydende nødvendigt at verificere placeringen af laserfokus før hvert eksperiment og sikre, at laserfokusets aksiale position falder sammen med det konfokale fokus. Denne justering optimerer intensiteten under AuNP-billeddannelse, hvilket fører til en maksimal lokal temperaturstigning og deraf følgende membranskade ved lavere lasereffekt. Denne proces udføres manuelt og er derfor modtagelig for variation i membranbrudeffektivitet, da fokus manuelt oversættes til en position, der falder sammen med partiklens placering. I mikroskoper, der mangler en refleksionstilstand, som i nogle kommercielle systemer, kan co-lokalisering af laserfokus og partikel være udfordrende. I sådanne tilfælde kan alternative billeddannelsestilstande (f.eks. Lyst felt) anvendes, og en langsom rasterscanning kan udføres omkring den forventede partikelposition. Det skal bemærkes, at lav lasereffekt sandsynligvis kun inducerer membranpermeabilisering, mens høj lasereffekt kan generere temperaturer omkring NP, der overstiger vandets kogepunkt, selvom glasoverfladen har en køleeffekt. Det anslås, at dannelsen af nanobobler omkring NP’erne sker mellem 200 °C og 300 °C25,48, hvor den eksplosive varme kan resultere i enten partikelforskydning fra laserfokus eller partikelfragmentering. Derudover udgør dannelsen af nano- eller mikrobobler under opvarmning en udfordring for denne metode. Da luftgrænseflader affugter membraner og kan forårsage proteindestabilisering, hvilket er uønsket, er det bydende nødvendigt at begrænse opvarmningen, når man undersøger membranreparation. Især guldnanoskaller tåler ikke høje temperaturer og nedbrydes under disse forhold, som demonstreret ved mikroskopi med høj opløsning58.
Denne artikel indeholder en detaljeret protokol til brug af termoplasmonik til at udføre stærkt lokaliserede punkteringer i membraner, som gælder for både celler og modelmembraner. For yderligere at reducere omfanget af opvarmning kan mindre nanopartikler, der resonerer med NIR-lys, anvendes, hvilket muliggør intracellulære punkteringer i endosomer, det endoplasmatiske retikulum og den nukleare kuvert. Sådanne nanopartikler, herunder stænger og nanomatryoshkas48, kan bruges til at undersøge reparation af nukleare kuverter ved at målrette endocytoserede guldnanopartikler, der let optages på celleoverfladen og handles mod kernen69. Samlet set muliggør denne teknik identifikation og undersøgelse af centrale molekylære komponenter, der er involveret i PMR, hvilket belyser deres biofysiske funktion og rolle, samtidig med at cellernes levedygtighed bevares.
Declarações
The authors have nothing to disclose.
Acknowledgements
Vi vil gerne takke Jesper Nylandsted for at give os rekombinante annexinproteiner og plasmider, der koder for annexiner. Dette arbejde er støttet økonomisk af Det Frie Forskningsråd, Natural Sciences (DFF-4181-00196), Novo Nordisk Foundation Interdisciplinary Synergy Program 2018 (NNF18OC0034936), Videnskabelig Komité Danish Cancer Society (R90-A5847-14-S2), Lundbeckfonden (R218-2016-534) og Lundbeckfondens grundforskningscenter (Biomembranes in Nanomedicine).
Materials
| 1064 nm trapping laser | Spectra Physics | N/A | Spectra Physics J201-BL-106C, Nd: YVO4 NIR laser |
| 160 nm Gold Nanoshells | NanoComposix | NCXGSIR150 | |
| 200 nm Gold Nanoparticles | BBI Solutions | EM.GC200/7 | |
| 35 mm glass surface MatTex microwell | MATTEK | P35G-1.5-14-C | |
| Amber-glass vials | Supelco Sigma Aldrich | 243438 | |
| Annexin A2 plasmids | N/A | N/A | Received from our collaborator at the Danish Cancer Research Center |
| Annexin A4 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA4 received from our collaborator at the Danish Cancer Research Center |
| Annexin A5 recombinant-protein | N/A | N/A | N-terminal GFP tagged ANXA5 received from our collaborator at the Danish Cancer Research Center |
| beta-casein | Sigma Life Science | C6905-1G | |
| CaCl2 | Suprlco (sigma Aldrich) | 10035-04-8 | |
| Centrifuge 5702 | Eppendorf | 5702 | |
| Chloroform | VWR Chemicals | 67-66-3 | |
| Culture dish (Nunclon Delta Surface) | Thermo scientific | 150460 | |
| DID cell-labelling Solution | Invitrogen | 7757 | |
| Distilled water | Gibco | 15230-089 | |
| DOPC | Avanti Polar Lipids | 850375C | Dissolved in chloroform |
| DOPS | Avanti Polar Lipids | 840035C | Dissolved in chloroform |
| Dulbecco's Modified Eage's Medium | Thermo Fisher Scientific | 11995065 | |
| FIJI ImageJ distribution | ImageJ2 | N/A | |
| GCaMP6s-CAAX | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Gibco Fetal Bovine Serum | Fisher Scientific | 11573397 | 10% of the culture medium |
| Glucose | PROLABO | 24 374.297 | |
| Hamilton syringes | Hamilton Company | N/A | 50 and 500 microliters |
| Harrick Plasma Cleaner PDG-002 | Harrick Plasma | N/A | |
| HEK293T cells | N/A | Received from our collaborator at the Danish Cancer Research Center | |
| Leica Acousto-Optical Beam Splitter (AOBS) | Leica | N/A | |
| Leica PL APO 63x water immersion objective, NA = 1.2 | Leica | N/A | |
| Leica SP5 confocal scanning microscope | Leica | N/A | |
| Lipofectamine | Fisher Scientific | 15338030 | |
| MatLab | The Mathworks, Inc., Natick, Massachusetts, United States | N/A | |
| NaCl | VWR Chemicals | 7647-14-5 | |
| Opti-MEM Reduced-Serum Medium | Thermo Fisher Scientific | 11058021 | |
| Parafilm | Bemis | PM-992 | |
| Penicillin-Streptomycin | Thermo Fisher Scientific | 15140122 | 1% of the culture medium |
| Phosphate Buffered Saline (PBS) | Thermo Fisher Scientific | 10010023 | |
| Piezoelectric stage (PI 731.20) | Physik Instrumente (Germany) | N/A | |
| Poly-L-Lysine | Sigma-Aldrich | P8920-100ML | 0.01-0.1% for coating |
| Polyvinyl alcohol | Sigma-Aldrich | 363065-25G | |
| round glass slide 25 mm Ø | VWR | 631-1584 | |
| Sonicator Brandson 2800 | Brandson | N/A | |
| sucrose | Sigma Life Science | 57-50-1 | |
| T25 tissue culture flask | Falcon | 353108 | Blue Vented cap |
| Tris-HCl | Invitrogen | 15567-027 | |
| TrypLE | Thermo Fisher Scientific | A1285901 | |
| Trypsin-EDTA | Fisher Scientific | 11590626 | |
| VWR Mixer mini vortex 230V EU | VWR | 12620-84 | ECN: 444-2790, SN: 150713022 |
Referências
- Bendix, P. M., et al. Interdisciplinary synergy to reveal mechanisms of annexin-mediated plasma membrane shaping and repair. Cells. 9 (4), 1029 (2020).
- Gajic, O., Lee, J., Doerr, C. H., Berrios, J. C., Myers, J. L., Hubmayr, R. D. Ventilator-induced Cell Wounding and Repair in the Intact Lung. American Journal of Respiratory and Critical Care Medicine. 167, 1057-1063 (2003).
- McNeil, P. L., Khakee, R. Disruptions of muscle fiber plasma membranes. Role in exercise-induced damage. The American Journal of Pathology. 140 (5), 1097-1109 (1992).
- Yu, Q. C., McNeil, P. L. Transient disruptions of aortic endothelial cell plasma membranes. The American Journal of Pathology. 141 (6), 1349-1360 (1992).
- Boye, T. L., et al. Annexin A4 and A6 induce membrane curvature and constriction during cell membrane repair. Nature Communications. 8, 1623 (2017).
- Bischofberger, M., Gonzalez, M. R., van der Goot, F. G. Membrane injury by pore-forming proteins. Current Opinion in Cell Biology. 21, 589-595 (2009).
- Tang, S. K. Y., Marshall, W. F. Self-repairing cells. Science (New York, N.Y.). 356, 1022-1025 (2017).
- Abreu-Blanco, M. T., Verboon, J. M., Parkhurst, S. M. Single cell wound repair: Dealing with life’s little traumas. Bioarchitecture. 1, 114-121 (2011).
- Sønder, S. L., et al. Annexin A7 is required for ESCRT III-mediated plasma membrane repair. Scientific Reports. 9, 6726 (2019).
- Andrews, N. W., Almeida, P. E., Corrotte, M. Damage control: cellular mechanisms of plasma membrane repair. Trends in Cell Biology. 24 (12), 734-742 (2014).
- Idone, V., Tam, C., Goss, J. W., Toomre, D., Pypaert, M., Andrews, N. W. Repair of injured plasma membrane by rapid Ca2+-dependent endocytosis. The Journal of Cell Biology. 180 (5), 905-914 (2008).
- Lauritzen, S. P., Boye, T. L., Nylandsted, J. Annexins are instrumental for efficient plasma membrane repair in cancer cells. Seminars in Cell & Developmental Biology. 45, 32-38 (2015).
- Häger, S. C., Nylandsted, J. Annexins: players of single cell wound healing and regeneration. Communicative & Integrative Biology. 12 (1), 162-165 (2019).
- Jaiswal, J. K., et al. S100A11 is required for efficient plasma membrane repair and survival of invasive cancer cells. Nature Communications. 5, 3795 (2014).
- Draeger, A., Monastyrskaya, K., Babiychuk, E. B. Plasma membrane repair and cellular damage control: The annexin survival kit. Biochemical Pharmacology. 81 (6), 703-712 (2011).
- Moreno-Pescador, G. S., et al. Thermoplasmonic nano-rupture of cells reveals annexin V function in plasma membrane repair. Nanoscale. 14 (21), 7778-7787 (2022).
- Zhivotovsky, B., Orrenius, S. Calcium and cell death mechanisms: A perspective from the cell death community. Cell Calcium. 50 (3), 211-221 (2011).
- Gerke, V., Moss, S. E. Annexins: From structure to function. Physiological Reviews. 82 (2), 331-371 (2002).
- Idone, V., Tam, C., Andrews, N. W. Two-way traffic on the road to plasma membrane repair. Trends in Cell Biology. 18 (11), 552-559 (2008).
- Boye, T. L., et al. Annexins induce curvature on free-edge membranes displaying distinct morphologies. Scientific Reports. 8, 10309 (2018).
- Bouter, A., et al. Annexin-A5 assembled into two-dimensional arrays promotes cell membrane repair. Nature Communications. 2, 270 (2011).
- Boye, T. L., Nylandsted, J. Annexins in plasma membrane repair. Biological Chemistry. 397 (10), 961-969 (2016).
- Weinberger, A., et al. Gel-assisted formation of giant unilamellar vesicles. Biophysical Journal. 105 (1), 154-164 (2013).
- Numata, T., Tatsuta, H., Morita, Y., Otani, Y., Umeda, N. Localized thermal processing with a laser-trapped and heated metal nanoparticle. IEEJ Transactions on Electrical and Electronic Engineering. 2, 398-401 (2007).
- Bendix, P. M., Reihani, S. N. S., Oddershede, L. B. Direct measurements of heating by electromagnetically trapped gold nanoparticles on supported lipid bilayers. ACS Nano. 4 (4), 2256-2262 (2010).
- Kyrsting, A., Bendix, P. M., Stamou, D. G., Oddershede, L. B. Heat profiling of three-dimensionally optically trapped gold nanoparticles using vesicle cargo release. Nano Letters. 11 (2), 888-892 (2011).
- Andersen, T., Kyrsting, A., Bendix, P. M. Local and transient permeation events are associated with local melting of giant liposomes. Soft Matter. 10 (24), 4268-4274 (2014).
- Bahadori, A., Oddershede, L. B., Bendix, P. M. Hot-nanoparticle-mediated fusion of selected cells. Nano Research. 10, 2034-2045 (2017).
- Rørvig-Lund, A., Bahadori, A., Semsey, S., Bendix, P. M., Oddershede, L. B. Vesicle fusion triggered by optically heated gold nanoparticles. Nano Letters. 15 (6), 4183-4188 (2015).
- Moreno-Pescador, G., Arastoo, M. R., Ruhoff, V. T., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic vesicle fusion reveals membrane phase segregation of influenza spike proteins. Nano Letters. 23 (8), 3377-3384 (2023).
- Bahadori, A., Lund, A. R., Semsey, S., Oddershede, L. B., Bendix, P. M. Controlled cellular fusion using optically trapped plasmonic nano-heaters. SPIE Proceedings. SPIE 9922, Optical Trapping and Optical Micromanipulation XIII. 992211, (2016).
- Bahadori, A., Moreno-Pescador, G., Oddershede, L. B., Bendix, P. M. Remotely controlled fusion of selected vesicles and living cells: a key issue review. Reports on Progress in Physics. 81 (3), 32602 (2018).
- Moreno-Pescador, G., Arastoo, M. R., Chiantia, S., Daniels, R., Bendix, P. M. Thermoplasmonic induced vesicle fusion for investigating membrane protein phase affinity. bioRxiv. , (2022).
- Pescador, G. S. M., et al. Investigating plasma-membrane repair employing thermoplasmonics. Biophysical Journal. 120 (3), 45A (2021).
- Moreno-Pescador, G. S., Qoqaj, I., Thusgaard Ruhoff, V., Iversen, J., Nylandsted, J., Bendix, P. M. Effect of local thermoplasmonic heating on biological membranes. SPIE 11083, Optical Trapping and Optical Micromanipulation XVI. 110830M, (2019).
- Bement, W. M., Mandato, C. A., Kirsch, M. N. Wound-induced assembly and closure of an actomyosin purse string in Xenopus oocytes. Current Biology. 9 (11), 579-587 (1999).
- Weisleder, N., et al. Recombinant MG53 protein modulates therapeutic cell membrane repair in treatment of muscular dystrophy. Science Translational Medicine. 4 (139), 139ra85 (2012).
- Sudji, I. R., Subburaj, Y., Frenkel, N., García-Sáez, A. J., Wink, M. Membrane disintegration caused by the steroid saponin digitonin is related to the presence of cholesterol. Molecules. 20 (11), 20146-20160 (2015).
- Babiychuk, E. B., Monastyrskaya, K., Potez, S., Draeger, A. Intracellular Ca2+ operates a switch between repair and lysis of streptolysin O-perforated cells. Cell Death & Differentiation. 16, 1126-1134 (2009).
- Nygård Skalman, L., Holst, M. R., Larsson, E., Lundmark, R. Plasma membrane damage caused by listeriolysin O is not repaired through endocytosis of the membrane pore. Biology Open. 7 (10), bio035287 (2018).
- Swaggart, K. A., et al. Annexin A6 modifies muscular dystrophy by mediating sarcolemmal repair. Proceedings of the National Academy of Sciences of the United States of America. 111, 6004-6009 (2014).
- Yeheskely-Hayon, D., Minai, L., Golan, L., Dann, E. J., Yelin, D. Optically induced cell fusion using bispecific nanoparticles. Small. 9 (22), 3771-3777 (2013).
- Minai, L., Yeheskely-Hayon, D., Golan, L., Bisker, G., Dann, E. J., Yelin, D. Optical nanomanipulations of malignant cells: Controlled cell damage and fusion. Small. 8 (11), 1732-1739 (2012).
- Lukianova-Hleb, E., et al. Plasmonic nanobubbles as transient vapor nanobubbles generated around plasmonic nanoparticles. ACS Nano. 4 (4), 2109-2123 (2010).
- Vogel, A., Noack, J., Hüttman, G., Paltauf, G. Mechanisms of femtosecond laser nanosurgery of cells and tissues. Applied Physics B. 81, 1015-1047 (2005).
- Baffou, G., Polleux, J., Rigneault, H., Monneret, S. Super-heating and micro-bubble generation around plasmonic nanoparticles under cw illumination. Journal of Physical Chemistry C. 118 (9), 4890-4898 (2014).
- Sasikumar, K., Liang, Z., Cahill, D. G., Keblinski, P. Curvature induced phase stability of an intensely heated liquid. Journal of Chemical Physics. 140 (23), 234506 (2014).
- Jauffred, L., Samadi, A., Klingberg, H., Bendix, P. M., Oddershede, L. B. Plasmonic heating of nanostructures. Chemical Reviews. 119 (13), 8087-8130 (2019).
- Neuman, K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nature Methods. 5 (6), 491-505 (2008).
- Bendix, P. M., Jauffred, L., Norregaard, K., Oddershede, L. B. Optical trapping of nanoparticles and quantum dots. IEEE Journal of Selected Topics in Quantum Electronics. 20, 15-26 (2014).
- Samadi, A., Bendix, P. M., Oddershede, L. B. Optical manipulation of individual strongly absorbing platinum nanoparticles. Nanoscale. 46, 18449-18455 (2017).
- Jørgensen, J. T., Norregaard, K., Tian, P., Bendix, P. M., Kjaer, A., Oddershede, L. B. Single particle and PET-based platform for identifying optimal plasmonic nano-heaters for photothermal cancer therapy. Scientific Reports. 6, 30076 (2016).
- Goldenberg, H., Tranter, C. J. Heat flow in an infinite medium heated by a sphere. British Journal of Applied Physics. 3 (9), 296-298 (1952).
- Eustis, S., El-Sayed, M. A. Why gold nanoparticles are more precious than pretty gold: Noble metal surface plasmon resonance and its enhancement of the radiative and nonradiative properties of nanocrystals of different shapes. Chemical Society Reviews. 35, 209-217 (2006).
- Landau, L. D., Lifshitz, E. M. . Fluid Mechanics: Landau and Lifshitz: Course of Theoretical Physics. 6, (2013).
- Niederauer, C., Seynen, M., Zomerdijk, J., Kamp, M., Ganzinger, K. A. The K2: Open-source simultaneous triple-color TIRF microscope for live-cell and single-molecule imaging. HardwareX. 13, e00404 (2023).
- Richardson, A. C., Reihani, N., Oddershede, L. B. Combining confocal microscopy with precise force-scope optical tweezers. SPIE Proceedings:SPIE 6326, Optical Trapping and Optical Micromanipulation III. 632628, (2006).
- Samadi, A., Klingberg, H., Jauffred, L., Kjær, A., Bendix, P. M., Oddershede, L. B. Platinum nanoparticles: a non-toxic, effective and thermally stable alternative plasmonic material for cancer therapy and bioengineering. Nanoscale. 10 (19), 9097-9107 (2018).
- . Available from: https://www.thermofisher.com/order/catalog/product/A7816 (2023)
- Kreibig, U., Vollmer, M. Theoretical considerations. In: Optical Properties of Metal Clusters. 25, (1995).
- Mie, G. Beiträge zur Optik trüber Medien, speziell kolloidaler Metallösungen. Annalen der Physik. 330 (3), 377-445 (1908).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529 (2017).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9, 676-682 (2012).
- Klenow, M. B., Heitmann, A. S. B., Nylandsted, J., Simonsen, A. C. Timescale of hole closure during plasma membrane repair estimated by calcium imaging and numerical modeling. Scientific Reports. 11, 4226 (2021).
- Li, T., Wu, X., Liu, F., Li, N. Analytical methods based on the light-scattering of plasmonic nanoparticles at the single particle level with dark-field microscopy imaging. Analyst. 142 (2), 248-256 (2017).
- Gibbs-Flournoy, E. A., Bromberg, P. A., Hofer, T. P. J., Samet, J. M., Zucker, R. M. Darkfield-Confocal Microscopy detection of nanoscale particle internalization by human lung cells. Particle and Fibre Toxicology. 8 (1), 2 (2011).
- Taylor, R. W., Sandoghdar, V. Interferometric scattering microscopy: Seeing single nanoparticles and molecules via Rayleigh scattering. Nano Letters. 19 (8), 4827-4835 (2019).
- Wu, Y., Ali, M. R. K., Chen, K., Fang, N., El-Sayed, M. A. Gold nanoparticles in biological optical imaging. Nano Today. 24, 120-140 (2019).
- Klingberg, H., Oddershede, L. B., Loeschner, K., Larsen, E. H., Loft, S., Møller, P. Uptake of gold nanoparticles in primary human endothelial cells. Toxicology Research. 4 (3), 566-666 (2015).

