Next Generation Sequencing for påvisning av Actionable mutasjoner i faste og flytende Svulster
Summary
This manuscript describes clinical protocols for two next-generation sequencing panels. One panel interrogates hematologic malignancies while the other panel targets genes commonly mutated in solid tumors. Molecular classification of driver mutations in human malignancies offers valuable prognostic and predictive information.
Abstract
As our understanding of the driver mutations necessary for initiation and progression of cancers improves, we gain critical information on how specific molecular profiles of a tumor may predict responsiveness to therapeutic agents or provide knowledge about prognosis. At our institution a tumor genotyping program was established as part of routine clinical care, screening both hematologic and solid tumors for a wide spectrum of mutations using two next-generation sequencing (NGS) panels: a custom, 33 gene hematological malignancies panel for use with peripheral blood and bone marrow, and a commercially produced solid tumor panel for use with formalin-fixed paraffin-embedded tissue that targets 47 genes commonly mutated in cancer. Our workflow includes a pathologist review of the biopsy to ensure there is adequate amount of tumor for the assay followed by customized DNA extraction is performed on the specimen. Quality control of the specimen includes steps for quantity, quality and integrity and only after the extracted DNA passes these metrics an amplicon library is generated and sequenced. The resulting data is analyzed through an in-house bioinformatics pipeline and the variants are reviewed and interpreted for pathogenicity. Here we provide a snapshot of the utility of each panel using two clinical cases to provide insight into how a well-designed NGS workflow can contribute to optimizing clinical outcomes.
Introduction
Neste generasjons sekvensering (NGS) of Clinical Oncology prøver har blitt mer allment tilgjengelig i løpet av de siste årene som vokser vitenskapelige litteraturen viser til viktigheten av å identifisere målrettbare genetiske endringer og prediktiv / prognostiske molekylære markører. Multi-gen panel analyser og hele exome sekvense studier i både epitelceller 1,2 og hematologisk 3 maligniteter har stivnet begrepet svulst heterogenitet og klonal evolusjon som sykdommen utvikler seg og tilbakefall. I tillegg, i motsetning til konkurrerende teknologier som for eksempel polymerasekjedereaksjon (PCR) eller Sanger-sekvensering, kan NGS oppdage de fleste genomiske forandringer i alle klinisk relevante kreftgener i en enkelt assay 4.
The Center for Tilpassede Diagnostics opprinnelig lansert med to kliniske NGS paneler, et tilpasset Hematologisk Panel (Heme-NGS Panel) og en off-the-sokkel Cancer Panel for FFPE- prøver (Solid-NGS panel) (se <strong> Figur 1). Disse panelene dekker klinisk relevante eller høy rente regioner av utvalgte gener; ikke alle gener eller eksoner er fullt dekket. Amplikonene er generert av probe-hybridisering, etterfulgt av forlengelse og ligering. De målrettede regionene er ytterligere forsterket ved hjelp av PCR med universell dual-indeksert primere, slik at opptil 96 prøver skal være felles for sekvensering.
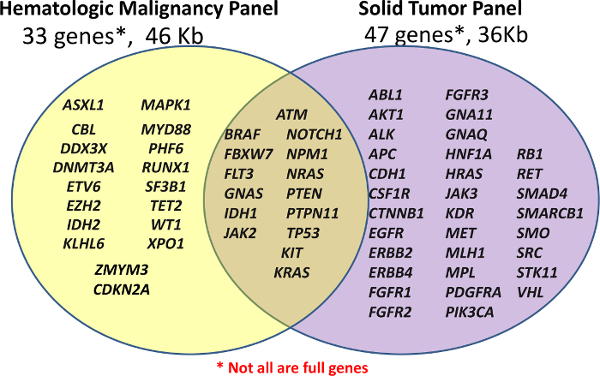
Figur 1:. Liste over Gener som dekkes i Panels Library forberedelser er utført ved hjelp av enten den tilpassede Hematologisk Panel (Heme-NGS Panel) av 33 gener eller off-the-sokkel Amplicon Cancer Panel (Solid-NGS) av 47 gener. Ikke alle gener eller eksoner dekkes i sin helhet, som noen amplikonene kan bare omfatte visse hotspots. Klikk her for å se en større versjon av dette tallet. </ A>
Innholdet til den Heme-NGS Panel ble avledet fra flere kilder, men sentre rundt 16-genene mutert i akutt myeloid leukemi (AML) som tidligere er beskrevet som viser et høyt nivå av klinisk anvendelighet 5. Solid-NGS Panel er kommersielt produsert med den målrettede regioner basert på vanlig muterte gener i kreft som rapportert i Katalog av somatiske mutasjoner i Cancer (COSMIC) database seks.
Flere viktige skritt karakterisere den generelle arbeidsflyten for kliniske NGS. Etter klinikeren beordrer testen, fastslår en patolog tilstrekkelighet av prøven følgende analyse for svulst prosent og prøvevolum. I vår institusjon, krever vi at minst 10% tumor på grunn av bakgrunnssekvensefeilhyppigheten ( "støy") av teknologien og effektiviteten av målrettet tilnærming. Når vevet er tilstrekkelig for testing, er genomisk DNA ekstrahert. Dette DNA blir deretter utsatt for flere kvalitetskontroll (QC) trinn. Dersom DNA passerer QC, er et fragment biblioteket generert og sekvensert. Den resulterende dataene er analysert gjennom en in-house bioinformatikk rørledningen. Etter bioinformatikk analyse, er varianter manuelt gjennomgått og tolket for patogenitet før innlemmelse i en klinisk rapport. Nedenfor beskriver vi to tilfeller som gikk gjennom denne grundige arbeidsflyt og til slutt førte til endringer i klinisk ledelse.
Sak 1 – Akutt myelogen leukemi
En benmargsbiopsi fra pasient A var diagnostisk for AML, uten modning. Cytogenetiske studier ble sendt på benmargen prøven og viste en normal kvinnelig karyotype. Det var 95% som sirkulerer blasts stede, så et perifert blod eksemplar ble sendt for personlig diagnostisk testing på Heme-NGS Panel.
Akutt myelogen leukemi (AML) er en hematologisk malignitet av myeloid avstamning av hvite blodlegemer. deteksjons~~POS=TRUNCav genmutasjoner i AML har blitt stadig viktigere for prognose og behandling, med tilbakevendende genmutasjoner anerkjent som viktig i patogenesen og prognose 7. Mutasjoner i NPM1 og CEBPA har vært forbundet med en gunstig prognostisk risiko, mens interne tandem duplikasjoner (ITDs) i FLT3 har vært forbundet med en mindre gunstig utfall 8. En voksende mengde bevis støtter en patogen rolle for disse og andre mutasjoner i AML 9.
Tilfelle 2 – Lung Adenocarcinoma
En biopsi av en venstre supraclavicular masse fra pasient B vist lunge adenokarsinom. Biopsimateriale fra formalinfiksert parafin-embedded (FFPE) lymfeknute massen ble sendt for genomisk testing (Solid-NGS Panel) som ruller / krøller med mer enn 50% tumor, for å finne ut om en mutasjon var til stede for målrettet terapeutisk intervensjon.
Lung cancer er den ledende årsak til kreft relatert dødelighet i USA og er delt inn i to hovedtyper, ikke-småcellet lungekreft (NSCLC) og småcellet lungekreft (SCLC). NSCLC kan bli ytterligere definert som enten adenokarsinom eller skvamøst cellekarsinom, basert på histologisk av lesjonen. Lunge adenokarsinom er den vanligste undertype av lungekreft, sett i både røykere og ikke-røykere, og er den vanligste formen for lungekreft for ikke-røykere 10. Molekylære studier av lunge adenokarsinomer har identifisert mutasjonen i flere onkogener 11. De vanligste driver mutasjoner identifisert i røykere er mutasjoner i KRAS og BRAF. De vanligste mutasjoner i ikke-røykere er mutasjoner i EGFR og rearrangements involverer gener ALK, RET og ROS1. Lungesvulster har blitt beskrevet med en in-frame ekson 20 innsetting i genet ErbB2 (HER2 / neu). Den vanligste abnormitet i HER 2 / neu er en forsterkning av dette locus i brystkreft hvor en målrettet terapi er tilgjengelig (trastuzumab: et humanisert monoklonalt antistoff mot HER2 / neu). HER2 / neu ekson 20 innsetting som er observert i 2-4% av lunge adenocarcimomas 12 har vist delvis respons på kombinasjonsbehandling med HER2 / neu og mTOR-hemmere (neratinib og temsirolimus, henholdsvis) 13.
Protocol
Representative Results
Discussion
Da de to NGS testene som er beskrevet i dette manuskriptet tilbys klinisk, er det mest viktige praktiske hensyn kvalitetskontroll. Spesielt må nær det tas hensyn til kvaliteten og kvantiteten av ekstrahert DNA. Dette er spesielt viktig for FFPE-prøver som ofte er sterkt degradert med variabel DNA utbytte. En isopropanol utfelling metode ble utviklet for å maksimalisere DNA-utbytte fra FFPE-prøver som kolonne-baserte metoder ble funnet å noen ganger føre til DNA skjær med begrenset elueringsvolumer. Derfor er de fleste av tiden når en prøve gir for lav konsentrasjon eller er for degradert for analysen, er det mest sannsynlig på grunn av vev størrelse, type, eller fiksering og ikke ekstraksjonsprosessen. For blod / benmargsprøver, hvis det er en svikt utvinning, er det vanligvis på grunn av en prøve som hemodilute (dvs. ikke å ha tilstrekkelig antall hvite blod eller tumorceller i den trekningen) eller kjemoterapi ablasjon.
. Nt "> Under validering, bør etableres tidsavgrensninger for aksept av DNA kvalitet og kvantitet Den anbefalte inngang på 100-250 ng er ofte brukt i analysen, men hvis DNA kvaliteten er god, deretter lavere innsatsbeløp kan være vellykket. i tillegg, hvis DNA er av dårlig kvalitet (dvs. mengden av forøkbare DNA er mindre enn 100-250 ng) deretter høyere inngangs mengder kan forbedre kvaliteten av sekvenseringsresultatene (siden mengden av forøkbare DNA vil nå den anbefalte input) . Metrics for DNA kvalitet og kvantitet skal brukes til hver prøve før fremme DNA i biblioteket forberedelse. Disse prøvene i en "gråsone" (se figur 2) skal kjøres på skjønn av laboratorielederen eller en utpekt. Foreløpig best måte å forutsi hvis DNA ikke vil gi gode resultater i løpet av sekvensering er å utføre en qPCR-basert assay som gjør det mulig for kvantifisering og kvalitetsvurdering av inngangs DNA. Denne fremgangsmåten løser bioavailability av forskjellige størrelser fragmenter i prøven, gjennom forsterkning av forskjellige størrelser fragmenter (f.eks, 100 bp, 150 bp, 200 bp og 300 bp) og sammenligning utbytte.For tiden innebærer bibliotek forberedelse et stort antall manuelle trinn hvor en feilsteg på en av flere knutepunkter kan føre til at biblioteket til enten ikke eller for å være av dårlig kvalitet. Den microfluidic gel analyse er den eneste QC skritt å sjekke bibliotek prep problemet før sekvensering. Følgelig, er det flere viktige trinnene hvor ekstra oppmerksomhet kan øke sannsynligheten for en vellykket reaksjon. Det er viktig å sikre korrekt prøven og oligonukleotid bassenget blir brukt for hver prøve. Sikre og riktig opptak at hver prøven inneholder en av 96 unike kombinasjoner av dual-indeksert PCR primerpar reduserer sjansen for et utvalg blanding opp. Dessuten er det viktig å sikre at filterplaten (FPU) drenerer riktig; hvis det ikke renne riktig kan dette føre til at extension-ligering trinn av biblioteket forberedelse til å utføre suboptimalt og føre til dårlig kvalitet sekvenseringsdata. Etter bibliotek QC, er det viktig å sikre at LNB1 perlene er fullstendig resuspendert og at LNB1 / LNA1 oppløsning blandes godt før tilsetning av den til prøvene som konsentrasjonen av denne blandingen blir anvendt for å bestemme molariteten av biblioteket. Til slutt, hvis vulsten elueringstrinn fører til en suboptimal mengde av biblioteket eluering av kulene vil det avta clustering tetthet og muligens føre til biblioteket for å ikke oppnå tilstrekkelig middeldekning. Motsatt vil et overskudd av bibliotek føre til dårligere kvalitet leser. Derfor er det viktig å være konsekvent på perle-baserte normalisering skritt for å sikre optimal samkjøring og clustering av bibliotekene på sequencer.
I tillegg til bibliotek forberedelse, er det avgjørende å validere en bioinformatikk rørledning som vil produsere nøyaktige mutasjon samtaler fra de rå, de-multiplex fastq filer. velge entilpasset løsning kan være tidkrevende som det er mange åpen kildekode og kommersielt tilgjengelige aligners, variant innringere, og NGS programvarepakker som man ville ha til å sile gjennom. Tilpassede algoritmer må være utformet for å trekke ut viktige resultatstatistikk, identifisere unike vendende mutasjoner som unngikk de fleste open source verktøy, og bestemme kopiantall status over hver av de loci. Under valideringsprosessen av en bioinformatikk rørledning, er det viktig å finne de rapporteringstidsavgrensninger for varianter som oppfyller eller overgår både en minimumsdybde på dekning etter kvalitet filtrering (f.eks minimum 250 lesninger) og et minimum allel frekvens (f.eks 4 %). Etter denne en multiplekset amplikon-baserte analysen, er det viktig å bestemme den minste midlere dybde av dekning (f.eks 1,000x) at biblioteket behov for å oppnå å være i stand til å få lavest utfører fragment til den minimumsdybde på lesninger. I tillegg er det multiplekset arten av analysen gjør cause av målet effekter og disse "gjenstander" må bli oppdaget og fullt vetted før lanseringen. En annen viktig begrensning for den angitte analyse er et behov for prøver for å inneholde mer enn 10% tumor for å oppnå den validerte minimum allel frekvens.
Påvisning av lav frekvens, 1%, FLT3 innsett er bevis på at manuell vurdering er fortsatt ønskelig i denne prosessen. Selv med et allel frekvens cut-off på 5%, noen viktige mutasjoner kanskje savnet, og dermed manuell vurdering vil være avgjørende for å fastslå disse variantene. For FLT3-ITDs, er visuell inspeksjon av ekson 14 utføres for alle AML pasienter for å sikre et lavt nivå eller store innsetting / duplisering ikke gå ubemerket hen. I tillegg HER2 ekson 20 innsett som er vanlig ved siden av primer sekvens, trenger manuell inngripen. Til tross for å ha en robust bioinformatikk rørledning, kan noen varianter går oversett noe som er bare natur å ha en hard kuttoff for de fleste statistikken nevnt ovenfor. Bedre bioinformatikk ville være nødvendig for å bidra til å lindre dette problemet, så vil bedre bibliotek forberedelse og / eller sekvensering metoder, fordi det er mer fordelaktig å ha god kvalitet data på enda lavere tidsavgrensninger som inneholder færre gjenstander og falske positiver.
Deteksjon og fortolkning av allel frekvenser kan være vanskelig på grunn av vanskeligheten i tumor prosent bestemmelse og amplifikasjon forspenning av noen regioner av genomet. I tillegg kan allel frekvenser over 50% skal detekteres, som observert i tilfellet 2. Dette tolkes som et tap av heterozygositet (LOH) hendelse, enten på grunn av tap av den normale allelet, som fører til den tilsynelatende økning av mutant leser, en forsterkning av den mutante allel (f.eks, 2-mutant og en normal kopi), eller andre mekanismer. Disse mekanismene kan belyses ved å anvende matrisen komparativ genomisk hybridisering (aCGH 19) og / eller en SNP genotyping array. 20.
De nåværende target berikelse metoder stole på heldags prosedyrer enten ineffektiv hybrid fangst eller multipleksede PCR teknikker som resulterer i behov for mer sekvensering dekning av en enkelt prøve og mer utenfor mål sekvense leser. Tilleggsprogrammer for NGS molekylær onkologi forventes i nær fremtid vil omfatte enklere bibliotek tilberedningsmetoder som kan være fullt automat og være i stand til å behandle prøvene med svært lave mengder innspill DNA (dvs. mindre enn 1 ng) samt prøver med svært degradert DNA. For å møte disse utfordringene, vil de fleste metoder antagelig være PCR baserte, enten som en flertrinns PCR tilnærming eller et massivt-parallell singleplex PCR tilnærming. I tillegg har molekylstrekkoding av de enkelte amplikonene vist seg å dramatisk redusere bakgrunnsstøy sekvensering, og vil muliggjøre testing av prøver med lavere andeler av tumorceller for å oppnå lavere allel frekvenser og bevege seg mot fange circulating tumorceller.
Påvisning av sykdomsassosierte mutasjoner i kreftprøver har vært standard vare i flere tiår. Historisk gener ble ofte testet sekvensielt, ett gen / exon av gangen, med identifikasjon av en mutasjon som fører til den ende av testsekvensen. Ankomsten av NGS har gjort det mulig for en mindre forspent tilnærming til sekvensering av flere gener assosiert med mange kreftformer i parallell som fører til identifisering av flere mutasjoner som er forbundet med neoplasi. Den kliniske nytten av NGS for påvisning av somatiske mutasjoner i kreft er stadig tydeligere. Faktisk NGS-basert analyse av tumorprøver representerer et nytt paradigme som utfordrer tradisjonelle, enkelt gen testing, men den kliniske nytten er veldig klar. Kliniske laboratorier i dag har en spennende mulighet til å gifte seg forsiktig metodevalidering og tolkning av tester med bruk av denne kraftige teknologien.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne ønsker å takke hjelp av Daniel Wild for lesing av manuskriptet og bistand i produksjon.
Materials
| Genomic DNA ScreenTape | Agilent Technology | 5067-5365 | |
| Genomic DNA Reagents | Agilent Technology | 5067-5366 | |
| High Sensitivity D1000 ScreenTape | Agilent Technology | 5067-5584 | |
| High Sensitivity D1000 Reagents | Agilent Technology | 5067-5585 | |
| TapeStation 2200 | Agilent Technology | G2965A | |
| TapeStation Analysis Software | Agilent Technology | A.01.04 or higher | |
| 96-well Tube Storage Racks | Any Vendor | ||
| 15/50 ml Tube Rack | Any Vendor | ||
| 96-well Plate Rack | Any Vendor | ||
| Pipette, single-channel, 0.5–2.5 μL | Any Vendor | ||
| Pipette, single-channel, 1–10 μL | Any Vendor | ||
| Pipette, single-channel, 2–20 μL | Any Vendor | ||
| Pipette, single-channel, 10–100 μL | Any Vendor | ||
| Pipette, single-channel, 20–200 μL | Any Vendor | ||
| Pipette, single-channel, 100–1000 μL | Any Vendor | ||
| Serological Pipettor | Any Vendor | ||
| Vortexer | Any Vendor | ||
| Ice bucket | Any Vendor | ||
| Microcentrifuge (for tubes and strip tubes) | Any Vendor | ||
| Freezer, -20 °C | Any Vendor | ||
| 4 °C Refrigerator | Any Vendor | ||
| Water or Bead Bath | Any Vendor | ||
| Incubator (37 oC) | Any Vendor | ||
| Serological Pipettes, 1 mL | Any Vendor | ||
| Serological Pipettes, 5 mL | Any Vendor | ||
| Serological Pipettes, 10 mL | Any Vendor | ||
| Serological Pipettes, 25 mL | Any Vendor | ||
| Gloves | Any Vendor | ||
| Razor Blades/Scaples | Any Vendor | ||
| KimWipes | Any Vendor | ||
| 15 mL Conical Tube | Any Vendor | ||
| 50 mL Conical Tube | Any Vendor | ||
| Paper Towels | Any Vendor | ||
| 200 proof Ethanol | Any Vendor | Store in Flammable Cabinet | |
| 2-Propanol (Isopropanol) | Any Vendor | Store in Flammable Cabinet | |
| 25ml Reservoirs | Any Vendor | ||
| 10N NaOH | Any Vendor | ||
| Pipette, 8-channel, 1–10 μL | Any Vendor | ||
| Pipette, 8-channel, 10–100 μL | Any Vendor | ||
| Pipette, 8-channel, 20–300 μL | Any Vendor | ||
| Ice Bucket | Any Vendor | ||
| Water Squirt Bottle | Any Vendor | ||
| Alcohol Squirt Bottle | Any Vendor | ||
| Lens Cleaning Paper | Any Vendor | ||
| Plates, 96-well PCR, Semi-Skirted | Any Vendor | ||
| Tube strips, 8-well, 0.2 mL | Any Vendor | ||
| Agencourt AMPure XP Beads | Beckman Coulter | A63881 | |
| BioShake IQ or 3000-T elm | Bulldog Bio/Q.Instruments | 1808-0506/ 1808-0517 | |
| DropPlate96 S – LabChipDS | Caliper | 128876 | |
| DropPlate96 D – LabChipDS | Caliper | 132848 | |
| DropSense96 | Caliper (Trinean) | ||
| DropQuant Software | Caliper (Trinean) | ||
| Plate Sealing Film | Denville | B1212-5S | |
| Aluminum Seal Foil | Denville | B1212-6S | |
| Nuclease-Free, Pure Water System | EMD Millipore | ||
| 5424 centrifuge | Eppendorf | 22621408 | |
| 5804R centrifuge | Eppendorf | 22623508 | Both 15 ml tube and plate rotators, preferably a centrifuge that can go up to 2,500 x g. |
| Safe-Lock Tube 1.5 mL, Natural | Eppendorf | 22431021 | |
| 5 mL Tube, DNA LoBind Tube | Eppendorf | 30108310 | |
| 5430R Centrifuge | Eppendorf | 022620645 | Any plate rotator centrifuge will work |
| Hybex Microsample Incubator | Fisher Scientific | 1057-30-0 | |
| Hybex 0.2 mL Tube Block | Fisher Scientific | 1057-31-0 | |
| TruSeq Amplicon – Cancer Panel | Illumina | FC-130-1008 | 96 reactions |
| TruSeq Custom Amplicon | Illumina | PE-940-1011 | 96 reactions |
| TruSeq Custom Amplicon Index Kit | Illumina | FC-130-1003 | 96 Indices, 384 Samples |
| MiSeq Reagent Kit v3, 500 Cycles | Illumina | MS-102-3003 | |
| MiSeq Reagent Kit v2, 300 Cycles | Illumina | MS-102-2002 | |
| MiSeq Reagent Kit v2, 500 Cycles | Illumina | MS-102-2003 | |
| Experiment Manager | Illumina | 1.3 or higher | |
| MiSeq Reporter | Illumina | 2.0 or higher | |
| Sequencing Analysis Viewer | Illumina | 1.8 or higher | |
| TruSeq Index Plate Fixture and Collar Kit | Illumina | FC-130-1007 | |
| MiSeq v2 | Illumina | SY-410-1003 | |
| TruSeq Custom Amplicon Filter Plate | Illumina | FC-130-1006 | |
| Index Adapter Replacement Caps | Illumina | 11294657 | |
| Qubit 2.0 | Invitrogen | Q32866 | |
| Qubit 0.5 ml Tubes | Invitrogen | Q32856 | |
| Qubit dsDNA Broad Range Assay Kit | Invitrogen | Q32853 | |
| DynaMa6-96 Magnetic Stand, Side Skirted | Invitrogen | 120.27 | |
| GeneAmp PCR System 9700 (gold/silver block) | Life Technologies | N8050200 | |
| Gentra Puregene Blood Kit | Qiagen | 158489 | |
| Deparaffinization Solution (16ml) | Qiagen | 19093 | |
| Buffer ATL (4x50ml) | Qiagen | 939011 | |
| Protein Precipitation Solution (50 ml) | Qiagen | 158910 | |
| DNA Hydration Solution (100ml) | Qiagen | 158914 | |
| Glycogen Solution (500 μl) | Qiagen | 158930 | |
| Qiagen Proteinase K | Qiagen | 19133 | |
| Rnase (5ml) | Qiagen | 158924 | |
| Nuclease-Free Water (10 x 50 ml) | Qiagen | 129114 | |
| Pestles | USA Scientific | 1415-5390 | |
| TipOne RPT 10 ul elongated filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips). | USA Scientific | 1180-3810 | |
| TipOne RPT 100 ul natural, beveled filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1840 | |
| TipOne RPT 200 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-8810 | |
| TipOne RPT 20 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1810 | |
| TipOne RPT 1000 μl natural, graduated XL filter pipet tips in | USA Scientific | 1182-1830 |
References
- Gerlinger, M., et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing. N Engl J Med. 366 (10), 883-892 (2012).
- Campbell, P. J., et al. The patterns and dynamics of genomic instability in metastatic pancreatic cancer. Nature. 467 (7319), 1109-1113 (2010).
- Ding, L., et al. Clonal evolution in relapsed acute myeloid leukaemia revealed by whole-genome sequencing. Nature. 481 (7382), 506-509 (2012).
- Frampton, G. M., et al. Development and validation of a clinical cancer genomic profiling test based on massively parallel DNA sequencing. Nature Biotechnol. 31 (11), 1023-1031 (2013).
- Patel, J. P., et al. Prognostic relevance of integrated genetic profiling in acute myeloid leukemia. N Engl J Med. 366 (12), 1079-1089 (2012).
- Forbes, S. A., et al. COSMIC (the Catalogue of Somatic Mutations in Cancer ): a resource to investigate acquired mutations in human cancer. Nucleic Acids Res. 38 (Database Issue), 652-657 (2010).
- Shih, A. H., Abdel-wahab, O., Patel, J. P., Levine, R. L. The role of mutations in epigenetic regulators in myeloid malignancies. Nat Rev Cancer. 12 (9), 599-612 (2012).
- Liersch, R., Müller-Tidow, C., Berdel, W. E., Krug, U. Prognostic factors for acute myeloid leukaemia in adults – biological significance and clinical use. Br J Haematol. 165 (1), 17-38 (2014).
- Bacher, U., Schnittger, S., Haferlach, T. Molecular genetics in acute myeloid leukemia. Curr Opin Oncol. 22 (6), 646-655 (2010).
- Subramanian, J., Govindan, R. Lung cancer in "Never-smokers": a unique entity. Oncology (Williston Park). 24 (1), 29-35 (2010).
- Sakashita, S., Sakashita, M., Tsao, M. S. Genes and pathology of non-small cell lung carcinoma. Semin Oncol. 41 (1), 28-39 (2014).
- Arcila, M. E., Chaft, J. E., Nafa, K. Prevalence clinicopathologic associations, and molecular spectrum of ERBB2 (HER2) tyrosine kinase mutations in lung adenocarcinomas. Clin Cancer Res. 18 (18), (2012).
- Gandhi, L., et al. Phase I study of neratinib in combination with temsirolimus in patients with human epidermal growth factor receptor 2-dependent and other solid tumors. J Clin Oncol. 32 (2), 68-75 (2014).
- Sheikhha, M. H., Awan, A., Tobal, K., Liu Yin, J. A. Prognostic significance of FLT3 ITD and D835 mutations in AML patients. Hematol J. 4 (1), 41-46 (2003).
- Mazières, J., et al. Lung cancer that harbors an HER2 mutation epidemiologic characteristics and therapeutic perspectives. J Clin Oncol. 31 (16), 1-8 (2014).
- Robinson, J. T., et al. Integrative Genomics Viewer. Nat Biotechnol. 29 (1), 495-500 (2011).
- Forbes, S. A., et al. COSMIC: exploring the world’s knowledge of somatic mutations in human cancer. Nucleic Acids Res. 43 (Database issue), D805-D811 (2014).
- Daber, R., Sukhadia, S., Morrissette, J. J. Understanding the limitations of next generation sequencing informatics, an approach to clinical pipeline validation using artificial data sets. Cancer Genetics. 206 (12), 441-448 (2013).
- Haraksingh, R. R., et al. Genome-Wide Mapping of Copy Number Variation in Humans: Comparative Analysis of High Resolution Array Platforms. PLoS ONE. 6 (11), e27859 (2011).
- de Leeuw, N., et al. SNP Array Analysis in Constitutional and Cancer Genome Diagnostics – Copy Number Variants, Genotyping and Quality Control. Cytogenet Genome Res. 135 (3-4), 212-221 (2011).

