RNAi-medieret Kontrol af aflatoksiner i Peanut: metode til at analysere Mykotoksin Produktion og transgenekspression i Peanut /<em> Aspergillus</em> Pathosystem
Summary
Vi demonstrere en metode til analyse af aflatoksiner og transgen ekspression i peanut frø, der indeholder RNA-interferens signaler til silencing aflatoksin-syntese gener i svampen Aspergillus flavus. RNAi-medieret kontrol af mykotoksiner i planter er ikke blevet rapporteret tidligere.
Abstract
Organisationen af De Forenede Nationers Levnedsmiddel- og Landbrugsorganisation anslår, at 25% af afgrøder i verden er forurenet med aflatoksiner. Det repræsenterer 100 millioner tons fødevarer bliver ødelagt eller omdirigeret til ikke-konsum hvert år. Aflatoksiner er stærke kræftfremkaldende stoffer normalt akkumuleret af svampene Aspergillus flavus og A. parasiticus korn, nødder, rodfrugter og andre landbrugsprodukter. Silencing af fem aflatoxin-syntese gener ved RNA-interferens (RNAi) i jordnøddeplanter blev anvendt til at kontrollere aflatoksin akkumulering efter inokulering med A. flavus. Tidligere fandtes ingen metode til at analysere effektiviteten af RNAi i de enkelte peanut transgene begivenheder, da disse normalt producerer få frø og traditionelle metoder til store markforsøg under aflatoksin-befordrende betingelser var ikke en mulighed. I marken, sandsynligheden for at finde naturligt forurenet frø ofte 1/100 til 1/1,000. Desuden er aflatoksinforureningen ikke jævnt fordelt. Vores metode bruger nogle frø pr transgen begivenhed, med små stykker forarbejdede for real-time PCR (RT-PCR) eller små RNA-sekventering, og for at påvise aflatoksin ophobning af ultra-performance væskekromatografi (UPLC). RNAi-udtrykkende peanut linjer 288-72 og 288-74, viste op til 100% reduktion (p≤0.01) i aflatoksin B 1 og B 2 sammenlignet med kontrollen, der akkumuleret op til 14.000 ng. G -1 af aflatoksin B 1, når inokuleret med aflatoxigenic A. flavus. Som reference, de samlede aflatoksiner tilladte til konsum i USA maksimale er 20 ng. G -1. Denne protokol beskriver anvendelsen af RNAi-medieret styring af aflatoksiner i transgene peanut frø og metoder til evaluering. Vi mener, at dens anvendelse i avl af peanut og andre afgrøder vil bringe hurtige fremskridt på dette vigtige område af videnskab, Medicin og human ernæring, og vil bidrage væsentligt til den internationale indsats for at styre aflatoksiner og potentielt andre mykotoksiner i de store afgrøder.
Introduction
Ca. 4,5 milliarder mennesker er kronisk udsat for aflatoksiner 1, de mest magtfulde kræftfremkaldende stoffer er kendt i naturen 2. Disse mykotoksiner forurener 25% af fødevareafgrøder i verden 3, herunder majs, kassava, ris, nødder, korn og krydderier. 4.. Aflatoksiner årsag forkroebling hos børn 5, svække immunsystemet 6, er til stede i 58% af hepatocellulære-karcinomer i menneskelige biopsier 7,8, og dræbe hundredvis af mennesker i løbet af periodiske udbrud af aflatoksikose 9,10. Aflatoksiner er polyketid-afledte mykotoksiner normalt produceret af Aspergillus flavus og A. parasiticus; aflatoksiner B 1 og B2 fremstilles ved A. flavus, mens A. parasiticus producerer også G 1 og G2. Den kemiske struktur af disse forbindelser og et chromatogram, der viser deres separation ved UPLC er vist i figur 1. </strong>
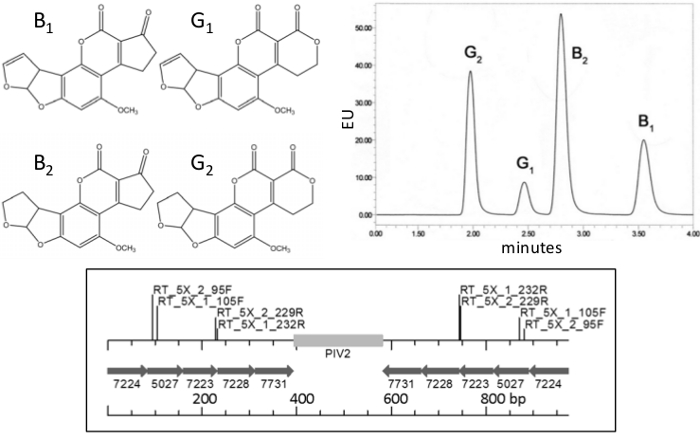
Figur 1. Aflatoksiner og RNAi indsætte Top:. Kemiske struktur (venstre) og eksempel på kromatogram (til højre) af de fire mest almindelige polyketid-afledte aflatoksiner: B 1, B 2, G 1 og G 2, produceret af Aspergillus parasiticus, A . flavus producerer B 1 og B 2 Nederst: Skematisk af genfragmenter i RNAi konstruere p5XCAPD bruges til peanut transformation, tal under pile er gen-fragment accessionsnumre i Aspergillus flavus genomet;. PIV2: kartoffel intron; BP: basepar; RT_5X_1 og RT_5X_2:. Realtids-PCR-primer sites Klik her for at se en større version af dette tal.
Økonomiske tab i eksporten som følge af aflatoksiner i jordnødder alene overstige $ 450 mio dollars, hvis beregnet på grundlag af 4 ng. G -1 grænse for aflatoksin tilladt til konsum i EU 11. Aflatoksiner har været kendt i 60 år 12; Men selvom mange landbrugspraksis blev udviklet for at afbøde deres virkning, herunder anvendelse af andre svampestammer 13,14, findes der ingen ensartet metode til kontrol, og resistente plantesorter er ikke tilgængelige. Test plante kimplasma for resistens over for aflatoksiner er særlig vanskelig, fordi selv under gunstige forhold for patogen invasion, mykotoksin akkumulation er uforudsigelig, og følger ikke en normalfordeling. Således eksperimenter kræver normalt store plantning områder, hundreder af frø og flere prøver af 100-1,700 g for at reducere variation i data 15,16.
RNA-interferens varopdaget i 1998 17; og fordelene ved "tavshed" er ved at blive undersøgt i en række nye applikationer, f.eks., i menneskelige behandlingsformer mod brystkræft 18, levercancer 19, myeloid leukæmi 20, og i plantebeskyttelse mod insekter 21 og nematoder 22 metastatisk. I planter, kan RNA-interferens signalerne celle til celle, med små interfererende RNA (siRNA) og høj molekylvægt RNA er ansvarlig for den systemiske posttranskriptionel gendæmpning 23,24, selv inde svampepatogener, der er i tæt kontakt med plantevært 25. Effektiviteten af RNAi om plante-medieret inaktivering af svampe–patogen gener er blevet beskrevet i få plante pathosystems, for disse, visuel undersøgelse af symptomer i de overjordiske dele af planter (blade) tilladt sygdom kvantificering, dvs. oomycete Bremia i salat 26 , Puccinia i hvede <sup> 27 og Fusarium i banan 28. Meget vanskeligere er at evaluere RNAi effektivitet til at styre mykotoksiner i planter, især aflatoksiner i jordnødder som bladene viser ingen symptomer på infektion, organerne invaderet (frø) er under flere inches af jord, forekomsten af infektion er uforudsigelig, og kun kemisk Analysen kan bestemme tilstedeværelsen af aflatoksiner. Desuden har hver transgen begivenhed i peanut producerer normalt få frø (4-6 per plante); derfor, traditionelle test for en no-aflatoksin ophobning træk i store parceller, varig hele beskæring sæsoner, og bruge hundredvis af frø ikke er mulig. Fremgangsmåde beskrives her at analysere på mindre end en uge, RNAi peanut frø til tilstedeværelsen af transgen og for en ikke-aflatoksin ophobning træk, der kun bruger få frø.
Protocol
Representative Results
Discussion
Plant-host RNAi-medieret inaktivering af gener i svampepatogener er påvist 27,43, men der er ingen publikationer, der viser muligheden for RNAi-medieret kontrol med mycotoxin akkumulering i planter. Én begrænsende faktor for disse undersøgelser i peanut var manglen på en metode til at vurdere en no-aflatoksin ophobning fænotype i de enkelte planter, som blade viser ingen symptomer upon svampeinfektion af underjordiske bælg. Desuden har de ikke-normalfordelt ophobning af aflatoksiner, og behovet for store prøver til kemisk analyse 15,16 hindret kvantificering af potentielle RNAi effekt på en enkelt plante. Metoden præsenteres her består af 72 timer forsøg under anvendelse af fem frø til at udføre tre 24 h-interval prøvetagninger i tre eksemplarer (tabel 1, figur 7). Sammenlignet med den typiske aflatoksinanalyser, der kræver ikke mindre end 100 g frø, vores metode er særligt velegnet til individual transgene begivenheder peanut planter, som oprindeligt producerer ikke mere end to eller tre bælg.
RNA-medieret dæmpning af aflatoksin syntese er blevet påvist ved genetisk transformation af Aspergillus flavus og A. parasiticus. Da aflR er en vigtig regulator af aflatoksin produktion i A. flavus og A. parasiticus 44,45, bliver det et interessant mål for RNA-medieret inaktivering i planter. Imidlertid har genetiske variationer i aflR påvist blandt Aspergillus arter 46 og disse genetiske varianter kunne undslippe silencing hvis der ikke er perfekte sekvens matcher med RNAi signal frembragt i planteværten. Således aflR var et af de mål for tavshed i vektor p5XCAPD, men var ikke den eneste. Inverterede gentagelser af aflR genet indført i A. flavus og A. parasiticus ved omdannelse resulterede i at lukke munden og minimal eller ingen produktion af aflatoksiner 47 (McDonald et al., 2005b). Også silencing AFLD gen forhindret aflatoksin produktion med op til 98% i A. flavus og A. parasiticus i direkte transformation 48. For at øge sandsynligheden for succes i vores system blev peanut transformeret med inverterede gentagne fragmenter af fem gener involveret i aflatoksin produktion i A. flavus. Her er det vist, at brug af p5XCAPD, der er målrettet til at lukke munden på flere gener i aflatoksin syntesevejen, 90% -100% lavere niveauer af aflatoksin B 1 og B 2 blev opnået på linje 288-72, og 60-100% lavere niveauer akkumuleret i line 288-74 sammenlignet med kontrollen, når halvdelen kimbladene blev podet med A. flavus, figur 4, 7. Vigtigst er det, denne metode påvises statistisk signifikante forskelle i aflatoxin ophobning af linjer 288-72, 288-74 vs. kontrol under hele forsøget ved anvendelse af parametrisk statitics, figur 7. I betragtning af den lille stikprøve, er det vigtigt at fremhæve behovet for at bruge en kraftfuld metode til at opdage aflatoksiner, blev disse eksperimenter analyseret af UPLC som har en høj opløsning, fem gange højere ydeevne og tre gange højere følsomhed end HPLC 49.
Ekspression af RNAi insertet i 288-74 blev kun fundet i umodne kimblade (gul) ved 24 timers inkubation. RNAi insert blev ikke detekteret ved RT-PCR på modne kimblade af 288-74 på 24 timer, eller på en årgang på 48 timer, figur 6. Det samme fænomen blev observeret i andre RNAi transgene peanut linjer (Arias, RS, 2015 upubliceret), hvor normalt RNAi udskrifter kun blev fundet på umodne kimblade på 24 timer. RNA-prøver blev behandlet med DNAse inden cDNA-syntese, data blev normaliseret til niveauet af actin ekspression og ingen tegn på DNA-kontaminering blev observeret. Skulle DNA har været til stede i prøverne, bør deter blevet påvist i de 48 timers prøver så godt, men konsekvent det var ikke tilfældet. Ekspression under kontrol af 35S-promotoren er ikke altid ensartet; Det kan blive påvirket af miljøforhold 50, vævstype og udviklingsstadiet 51,52. Samtidig, i vejen for RNA-interferens, kan hastigheden af mRNA forfald og hastigheden af siRNA henfald variere betydeligt 53. Det er muligt, at den hurtige nedbrydning af mRNA ved mekanismen af RNA-interferens kunne have forhindret mRNA detektion ved 48 timers inkubation. Uanset om fravær af udtryk på 48 timer var på grund af lave 35S-promotor drevet transskription eller til hurtig nedbrydning af dsRNA ved Dicer mangler at blive besvaret. Således ville detektering af små RNA'er af high throughput sekventering give et bedre indblik i de processer, der finder sted via RNAi 54 i disse forsøg. Men da RNA nedregulering spreder systemisk, hovedsageligt gennem Phloem fra photosynthader kilder til saccharose dræn (i dette tilfælde peanut frø) 55, undertrykkelse af aflatoxin-syntese kan forekomme i frø uden lokal udtryk for RNAi indsatsen. Megen forskning mangler at blive gjort for at bestemme tærskelværdien af små interfererende RNA (siRNA'er) er nødvendige for at forhindre, at aflatoksin ophobning i frø. Det er vigtigt at understrege, at både mRNA ekspression af RNAi konstruktion (figur 6), og akkumulering af aflatoksiner B 1 og B2 (figur 7) viste forskellige resultater for umodne (gul) vs. moden (brun) kimbladene. Peanut planter har ubestemmelig vækst, det vil sige, de præsenterer ved høst en række løbetider bælg, figur 2. Desuden frø fra forskellige løbetider grupper er forskellige i deres kemiske sammensætning, f.eks., 2,4% saccharose i umodne frø, og 1,9% i modne frø under samme markforhold 56,57. Således at forstå den faktiske efficiency af RNA-medieret kontrol af aflatoksin ophobning, er det vigtigt at analysere modenhed grupper hver for sig.
En naturlig forsvar for peanut frø er produktion af phytoalexiner, som varierer i mangfoldigheden af forbindelser, der produceres og deres relative mængder afhængigt af modenhed af frø og miljøforhold 58-61, og det er særligt højere i embryoner end kimblade 62. Embryoner har også signifikant højere koncentrationer af nukleinsyrer, både DNA og RNA end kimbladene (Arias RS, upublicerede). Som peanut frø modnes, ændringer i deres fysiologi og kemiske sammensætning forekomme 63. Phenoliske antioxidanter i peanut testa danner kondenserede tanniner med fungistatisk aktivitet 64; det er også tydeligt i den mesocarp farve, der afspejler etaper løbetid, gul til sort 35, da dens indhold af tanniner og phenolforbindelser stiger med løbetiden 65. Således tilstedeværelsen af tESTA eller embryoner i forsøget på grund af deres antimikrobielle egenskaber, kunne have begrænset svampevækst og dermed overvurderet effekten af RNAi lyddæmpning derfor blev de fjernet. Også fjernelse af TESTA og embryoner hjælper begrænse kilder til variation i analysen, da den halve cotyledon der bærer embryo vil have flere phytoalexiner og mere RNA indhold.
Ud over analyse ved modenhed grupper og fjernelse af Testa embryo i disse eksperimenter, er det vigtigt at påpege nogle flere observationer: a) selvom resultaterne er vist i op til 96 timers inkubering, anbefales det at anvende ikke mere end 72 hr at opnå ensartede resultater, som frø bliver nedbrudt af 96 timer; og b) henviser til halv kimblade fra samme frø, selvom udvalgt tilfældigt, udgør ikke perfekt uafhængige stikprøver, RT-PCR og aflatoksin ophobning inden transgene begivenheder viste minimale variation mellem frø. Også en nøjagtig fungal spore noget, podevolumens af 2 pi, og anvendelse af sporer på snitfladen af kimbladene undgå dryp på siderne er vigtigt at sørge for de spirede sporer er udsat for plantevævet. Vand / agar på pladerne bør være på 1,5% (w / v), blødere agar forårsager afstrømning af sporer, som vist på det sidste billede i figur 4 (nederst). Skal frø ledighed fra et bestemt transgen begivenhed begrænses, kan prøveudtagningen ske i to eksemplarer i stedet for tredobbelte opnå lignende resultater (dvs. figur 7); dog vil tredobbelte prøver at reducere standardafvigelsen. Den eneste begrænsning ved denne metode er, at det kræver en meget følsomt system (UPLC) for aflatoksin påvisning / kvantificering, men samtidig reducerer dette sandsynligheden for at overvurdere effekten af RNAi bør aflatoksiner ikke påvises ved mindre følsomme metoder.
Afslutningsvis denne metode giver for første gang en pålidelig metode til at undersøgevirkningen af RNAi i kontrollen med aflatoksiner. Reducere den tid til et eksperiment fra en hel beskæring sæson til mindre end en uge, vil denne metode uhyre fremskynde forskningen i RNAi-peanut / Aspergillus pathosystem mod afbødning og / eller eliminering af aflatoksiner.
Disclosures
The authors have nothing to disclose.
Acknowledgements
This work received the financial support of USDA-ARS CRIS project 6604-21000-004-00D, CRIS project 6604-42000-008-00D, and USAID Feed-the-Future program Agreement number 58-0210-3-012. We thank Valerie Orner, LaTanya Johnson, Joseph Powell and Kathy Gray for their technical assistance. Mention of trade names or commercial products in this article is solely for the purpose of providing specific information and does not imply recommendation or endorsement by the US Department of Agriculture.
Materials
| Primers, oligonucleotides | DNA Technologies, Coralville, IA, USA | n/a | |
| Dneasy Plant Mini Kit | Qiagen, Valencia, CA | 69106 | |
| Czapek Dox agar medium | Oxoid, by Thermo Fisher Scientific, Waltham, MA | CM0095 | |
| Agar | Thermo Fisher Scientific, Waltham, MA | BP 1423 | |
| Freezer -80°C | n/a | n/a | |
| Aluminum Oxide, Al2O3 | Fisher Scientific | A941 | |
| SPE Reservoirs 1.5 mL | Grace Davison Discovery Scientific | 210011 | |
| Frits for 1.5 mL SPE reservoir | Grace Davison Discovery Scientific | 211401 | |
| Autosampler vials | Waters Corporation, Milford, MA | 186005221 | |
| Waters Acquity Ultra-Performance Liquid-Chromatography (UPLC) instrument; UPLC-H-Class Quaternary Solvent Manager; UPLC Sample Manager; UPLC Fluorescent detector (FLR); UPLC BEH C18 2.1mmx50mm, 1.7mm column | Waters Corporation, Milford, MA | ||
| Finnigan LCQ Advantage MAX ion trap mass spectrometer, with Xcalibur version 1.4 software | Thermo Electron Corp., San Jose, CA | ||
| Aflatoxin standards, B1, B2, G1 and G2 | Sigma-Aldrich, St. Louis, MO | A6636; A9887; A0138; A0263 | |
| Systat Software 12.2 | SYSTAT Software Inc., Point Richmond, CA | ||
| Trizol reagent | Invitrogen, CA | 15596-018 | |
| SuperScript III First Strand Synthesis Super Mix | Invitrogen, CA | 11752-050 | |
| ABI 7500 Real-Time PCR | Lifetechnologies, Grand Island, NY | 4406984 | |
| Luria Broth-Miller | Fisher Scientific | R453642 | |
| pENTR1A | Invitrogen, CA | A10462 | |
| LR Clonase II enzyme mix | Invitrogen, CA | 11791-020 | |
| T4 DNA Ligase | NEB Biolabs | M0202L | |
| Gelrite | Sigma-Aldrich, St. Louis, MO | G1919 | |
| Acetosyringone | Sigma-Aldrich, St. Louis, MO | D134406 | |
| QIAcube robot workstation | Qiagen, Valencia, CA | 9001292 | |
| Antibiotics: kanamycin, cefotaxime, gentamicin; streptomycin | Goldbio, St. Louis, MO | cef.: C-104-25; kan: K-120-5; gent.: G-400-1; strep.: S-150-50 | |
| Platinum Taq DNA Polymerase High Fidelity | Invitrogen, CA | 11304-029 |
References
- Williams, J. H., et al. Human aflatoxicosis in developing countries: a review of toxicology, exposure, potential health consequences, and interventions. The American Journal of Clinical Nutrition. 80, 1106-1122 (2004).
- American Association for Cancer Research: AACR. An evaluation of chemicals and industrial processes associated with cancer in humans based on human and animal data: IARC Monographs Volumes 1 to 20. Cancer Research. 40, 1-12 (1980).
- Turner, P. C. The molecular epidemiology of chronic aflatoxin driven impaired child growth. Scientifica. , (2013).
- Rasooly, R., Hernlem, B., He, X., Friedman, M. Non-linear relationships between aflatoxin B1 levels and the biological response of monkey kidney vero cells. Toxins (Basel). 5, 1447-1461 (2013).
- Gong, Y. Y., et al. Determinants of aflatoxin exposure in young children from Benin and Togo, West Africa: the critical role of weaning. International Journal of Epidemiology. 32, 556-562 (2003).
- Eaton, D. L., Groopman, J. D. . The toxicology of aflatoxins: human health, veterinary, and agricultural significance. , (1994).
- Murugavel, K. G., et al. Prevalence of aflatoxin B1 in liver biopsies of proven hepatocellular carcinoma in India determined by an in-house immunoperoxidase test. Journal of Medical Microbiology. 56, 1455-1459 (2007).
- Wang, J. S., et al. Hepatocellular carcinoma and aflatoxin exposure in Zhuqing Village, Fusui County, People’s Republic of China. Cancer Epidemiology, Biomarkers & Prevention. 10, 143-146 (2001).
- Azziz-Baumgartner, E., et al. Case-control study of an acute aflatoxicosis outbreak, Kenya, 2004. Environmental Health Perspectives. 113, 1779-1783 (2005).
- Lye, M. S., Ghazali, A. A., Mohan, J., Alwin, N., Nair, R. C. An outbreak of acute hepatic encephalopathy due to severe aflatoxicosis in Malaysia. American Journal of Tropical Medicine and Hygiene. 53, 68-72 (1995).
- Villers, P. Aflatoxins and safe storage. Frontiers in Microbiology. 5, 158 (2014).
- Kensler, T. W., Roebuck, B. D., Wogan, G. N., Groopman, J. D. Aflatoxin: A 50-year odyssey of mechanistic and translational toxicology. Toxicological Sciences. 120, S28-S48 (2011).
- Dorner, J. W., Cole, R. J., Wicklow, D. T. Aflatoxin reduction in corn through field application of competitive fungi. Journal of Food Protection. 62, 650-656 (1999).
- Cotty, P. J., Bhatnagar, D. Variability among atoxigenic Aspergillus flavus strains in ability to prevent aflatoxin contamination and production of aflatoxin biosynthetic-pathway enzymes. Applied and Environmental Microbiology. 60, 2248-2251 (1994).
- Whitaker, T. B. Standardisation of mycotoxin sampling procedures: an urgent necessity. Food Control. 14, 233-237 (2003).
- Whitaker, T. B., Dorner, J. W., Giesbrecht, F. G., Slate, A. B. Variability among aflatoxin test results on runner peanuts harvested from small field plots. Peanut Science. 31, 59-63 (2004).
- Fire, A., et al. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature. 391, 806-811 (1998).
- Rafael, D., et al. EMT blockage strategies: Targeting Akt dependent mechanisms for breast cancer metastatic behaviour modulation. Current Gene Therapy. , (2015).
- Li, G., Chang, H., Zhai, Y. P., Xu, W. Targeted silencing of inhibitors of apoptosis proteins with siRNAs: a potential anti-cancer strategy for hepatocellular carcinoma. Asian Pacific. Journal of Cancer Prevention: APJCP. 14, 4943-4952 (2013).
- Koldehoff, M. Targeting bcr-abl transcripts with siRNAs in an imatinib-resistant chronic myeloid leukemia patient: challenges and future directions. Methods in Molecular Biology. 1218, 277-292 (2015).
- Zhang, J., et al. Pest control. Full crop protection from an insect pest by expression of long double-stranded RNAs in plastids. Science. 347, 991-994 (2015).
- Ajjappala, H., Chung, H. Y., Sim, J. S., Choi, I., Hahn, B. S. Disruption of prefoldin-2 protein synthesis in root-knot nematodes via host-mediated gene silencing efficiently reduces nematode numbers and thus protects plants. Planta. 241, 773-787 (2015).
- Jose, A. M., Hunter, C. P. Transport of sequence-specific RNA interference information between cells. Annual Review of Genetics. 41, 305-330 (2007).
- Vazquez, F., Hohn, T. Biogenesis and biological activity of secondary siRNAs in plants. Scientifica. , (2013).
- Tinoco, M. L. P., Dias, B. B. A., Dall’Astta, R. C., Pamphile, J. A., Aragao, F. J. L. In vivo trans-specific gene silencing in fungal cells by in planta expression of a double-stranded RNA. BMC Biology. 8, (2010).
- Govindarajulu, M., Epstein, L., Wroblewski, T., Michelmore, R. W. Host-induced gene silencing inhibits the biotrophic pathogen causing downy mildew of lettuce. Plant Biotechnology Journal. , (2014).
- Yin, C., Jurgenson, J. E., Hulbert, S. H. Development of a host-induced RNAi system in the wheat stripe rust fungus Puccinia striiformis f. sp. tritici. Molecular Plant-Microbe Interactions. 24, 554-561 (2011).
- Ghag, S. B., Shekhawat, U. K., Ganapathi, T. R. Host-induced post-transcriptional hairpin RNA-mediated gene silencing of vital fungal genes confers efficient resistance against Fusarium. wilt in banana. Plant Biotechnology Journal. 12, 541-553 (2014).
- Filichkin, S. A., et al. Efficiency of gene silencing repeats vs. transitive RNAi in Arabidopsis: direct inverted vectors. Plant Biotechnology Journal. 5, 615-626 (2007).
- Sciaky, D., Montoya, A. L., Chilton, M. D. Fingerprints of Agrobacterium Ti Plasmids. Plasmid. 1, 238-253 (1978).
- Clark, D. J., Maaloe, O. DNA Replication and Division Cycle in Escherichia coli. Journal of Molecular Biology. 23, 99-112 (1967).
- Murashige, T., Skoog, F. A revised medium for rapid growth and bio assays with tobacco tissue cultures. Physiol Plantarum. 15, 473-497 (1962).
- Srinivasan, T., Kumar, K. R. R., Kirti, P. B. Establishment of efficient and rapid regeneration system for some diploid wild species of Arachis. Plant Cell Tissue and Organ Culture. 101, 303-309 (2010).
- Gomes, A. L. V., et al. Single-tube nested PCR using immobilized internal primers for the identification of dengue virus serotypes. Journal of Virology Methods. 145, 76-79 (2007).
- Williams, E. J., Drexler, J. S. A non-destructive method for determining peanut pod maturity. Peanut Science. 8, 134-141 (1981).
- Sobolev, V. S., Dorner, J. W. Cleanup procedure for determination of aflatoxins in major agricultural commodities by liquid chromatography. Journal of AOAC International. 85, 642-645 (2002).
- Biselli, S., Hartig, L., Wegner, H., Hummert, C. Analysis of Fusarium. toxins using LC-MS-MS: Application to various food and feed matrices. LC GC North America. 23, 404-413 (2005).
- Arias, R. S., Sobolev, V. S., Orner, V. A., Dang, P. M., Lamb, M. C. Potential involvement of Aspergillus flavus laccases in peanut invasion at low water potential. Plant Pathology. 63, 353-363 (2014).
- Dang, P. M., Chen, C. Y., Holbrook, C. C. Evaluation of five peanut (Arachis hypogaea) genotypes to identify drought responsive mechanisms utilising candidate-gene approach. Functional Plant Biology. 40, 1323-1333 (2013).
- Schmittgen, T. D., Livak, K. J. Analyzing real-time PCR data by the comparative C-T method. Nature Protocols. 3, 1101-1108 (2008).
- Amaike, S., Keller, N. P. Aspergillus flavus. Annual Review of Phytopathology. 49, 107-133 (2011).
- Nowara, D., et al. HIGS: Host-induced gene silencing in the obligate biotrophic fungal pathogen Blumeria graminis. Plant Cell. 22, 3130-3141 (2010).
- Woloshuk, C. P., et al. Molecular characterization of aflR, a regulatory locus for aflatoxin biosynthesis. Applied and Environmental Microbiology. 60, 2408-2414 (1994).
- Price, M. S., et al. The aflatoxin pathway regulator AflR induces gene transcription inside and outside of the aflatoxin biosynthetic cluster. FEMS Microbiology Letters. 255, 275-279 (2006).
- Ehrlich, K. C., Montalbano, B. G., Cotty, P. J. Sequence comparison of aflR from different Aspergillus. species provides evidence for variability in regulation of aflatoxin production. Fungal Genetics and Biology. 38, 63-74 (2003).
- McDonald, T., Brown, D., Keller, N. P., Hammond, T. M. RNA silencing of mycotoxin production in Aspergillus and Fusarium species. Molecular Plant Microbe Interactions. 18, 539-545 (2005).
- Abdel-Hadi, A. M., Caley, D. P., Carter, D. R., Magan, N. Control of aflatoxin production of Aspergillus flavus. and Aspergillus parasiticus. using RNA silencing technology by targeting aflD. (nor-1) gene. Toxins (Basel). 3, 647-659 (2011).
- Swartz, M. E. Ultra performance liquid chromatography (UPLC): An introduction: Separation Science Redefined. LCGC North America. , 8-14 (2005).
- Maghuly, F., Khan, M. A., Fernandez, E. B., Druart, P., Watillon, B., Laimer, M. Stress regulated expression of the GUS-marker gene (uidA) under the control of plant calmodulin and viral 35S promoters in a model fruit tree rootstock: Prunus incisa x serrula. Journal of Biotechnology. 135, 105-116 (2008).
- de Mesa, M. C., Santiago-Doménech, N., Pliego-Alfaro, F., Quesada, M. A., Mercado, J. A. The CaMV 35S promoter is highly active on floral organs and pollen of transgenic strawberry plants. Plant Cell Reports. 23, 32-38 (2004).
- Sunilkumar, G., Mohr, L., Lopata-Finch, E., Emani, C., Rathore, K. S. Developmental and tissue-specific expression of CaMV 35S promoter in cotton as revealed by GFP. Plant Molecular Biology. 50, 463-474 (2002).
- Groenenboom, M. A. C., Maree, A. F. M., Hogeweg, P. The RNA silencing pathway: The bits and pieces that matter. PLoS Computational Biology. 1, 155-165 (2005).
- Zhao, D., Song, G. Q. High-throughput sequencing as an effective approach in profiling small RNAs derived from a hairpin RNA expression vector in woody plants. Plant Science: an International Journal of Experimental Plant Biology. 228, 39-47 (2014).
- Kamthan, A., Chauduri, A., Kamthan, M., Datta, A. Small RNAs in plants: recent development and application for crop improvement. Frontiers in Plant Science. 6, 208 (2015).
- Manda, A., Bodapati, P. N., Rachaputi, N. C., Wright, G., Fukai, S. . Aflatoxins and their relationship with sugars in peanut (Arachis hypogaea L). , (2004).
- Uppala, S. S. . Factors affecting pre-harvest aflatoxin contamination of peanut (Arachis hypogaea L). , (2011).
- Sobolev, V. S. Localized production of phytoalexins by peanut (Arachis hypogaea) kernels in response to invasion by Aspergillus species. Journal of Agricultural and Food Chemistry. 56, 1949-1954 (2008).
- Sobolev, V. S., Guo, B. Z., Holbrook, C. C., Lynch, R. E. Interrelationship of phytoalexin production and disease resistance in selected peanut genotypes. Journal of Agricultural and Food Chemistry. 55, 2195-2200 (2007).
- Sobolev, V. S., Neff, S. A., Gloer, J. B. New stilbenoids from peanut (Arachis hypogaea) seeds challenged by an Aspergillus caelatus strain. Journal of Agricultural and Food Chemistry. 57, 62-68 (2009).
- Dorner, J. W., Cole, R. J., Sanders, T. H., Blankenship, P. D. Interrelationship of kernel water activity, soil temperature, maturity, and phytoalexin production in preharvest aflatoxin contamination of drought-stressed peanuts. Mycopathologia. 105, 117-128 (1989).
- Sobolev, V. S. Production of phytoalexins in peanut (Arachis hypogaea) seed elicited by selected microorganisms. Journal of Agricultural and Food Chemistry. 61, 1850-1858 (2013).
- Basha, S. M. M., Cherry, J. P., Young, C. T. Changes in free amino acids, carbohydrates, and proteins of maturing seeds from various peanut (Arachis hypogaea L.) cultivars. Cereal Chemistry. 53, 586-596 (1976).
- Lansden, J. A. Aflatoxin inhibition and fungistasis by peanut tannins. Peanut Science. 9, 17-20 (1982).
- Yen, G. C., Duh, P. D., Tsai, C. L. Relationships between antioxidant activity and maturity of peanut hulls. Journal of Agricultural and Food Chemistry. 41, 67-70 (1993).

